浙江新高考加试题备考指导
浙江 方大学
浙江新高考加试题备考指导
浙江 方大学
【编者按】2017年浙江省将进行新高考综合改革后的首次高考。为更好地指导考生备考,本刊特选义乌市教育研修院方大学老师的文章,对2015年10月浙江首次学考选考中的加试题进行深入分析,以期对考生复习有所帮助。
2015年10月,浙江省实施了高中学考和高考选考相结合的首次化学考试。对高考选考化学的考生来说,既要通过必考题(满分70分)考试获得高中学考等级,又要参加加试题(满分30分)的考试,必考题和加试题两项的总分获得高考化学等级和赋分。其中必考题重视基础考查,加试题重视能力考查。据统计,此次考试中三道化学加试题的全省平均分为:30题3.36分,31题5.51分,32题3.51分。今年的高二年级是新高考改革以来的第一届,也是第一次参加10月份的各学科学考、选考,大家对这次化学考试卷的关注程度很高,大家都想知道改革之后的化学试题会有什么特点,什么难度。为科学指导新高考化学复习,学会快速有序解题,本文试将三道加试题做一探讨。
一、三道加试题的题型特点和解题分析
30.【加试题】(10分)由某精矿石(MCO3·ZCO3)可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,取该矿石样品1.84g,高温灼烧至恒重,得到0.96g仅含两种金属氧化物的固体,其中m(M)∶m(Z)=3∶5,请回答:
(1)该矿石的化学式为_____________________。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2∶1)。写出该反应的化学方程式:_____________________________。
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是______________。
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:

其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图1所示。
则ΔH3_______________(填“大于”“小于”或“等于”)ΔH2,理由是___________________。
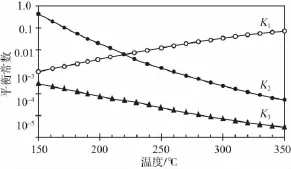
图1
(4)在温度T1时,使体积比为3∶1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。

图2
题型特点:这是一道元素化合物知识与化学反应原理融合的综合题。既需定性的分析推理,又需精确的定量计算才能顺利解答。
解题思路:第(1)问,根据题给数据建立不定方程,金属化合价讨论计算得出,M元素的相对原子质量为20,Z元素的相对原子质量为40,推知矿石化学式为MgCO3· CaCO3。
第(2)问第①题,MgO、CaO、Si三者的反应是一个陌生的化学反应,根据试题告知的生成物为Mg和含氧酸盐,通过元素守恒,电子得失相等很快得出含氧酸盐为Ca2SiO4。第(2)问第②题是考生熟悉的问题,根据电解时阳离子在阴极上放电顺序推知,电解MgCl2溶液得到的是Mg(OH)2,而不是Mg。
第(3)问是对盖斯定律和勒夏特列原理的应用。根据盖斯定律推知ΔH3-ΔH2=ΔH1,根据图1中,升高温度K1增大,推知反应1是吸热反应,即ΔH1>0,故ΔH3>ΔH2。
第(4)问是绘图,考查学生获取信息能力和绘图能力。题给H2与CO2体积比3∶1,暗示化学反应为反应3,根据第(3)题图1可知,K3随温度升高而减小,可推知ΔH3<0,为放热反应。根据勒夏特列原理,其他条件不变,降低温度,平衡向右移动,甲醇的浓度会增大,一段时间后达到新的平衡。作图时应注意,起点与原平衡在t时刻相连,由于试题缺乏作图数据,只能画出曲线变化趋势图。
参考答案:
(1)MgCO3·CaCO3
②电解MgCl2溶液时,阴极上H+比Mg2+容易得电子,电极反应式2H2O+2e-===H2↑+2OH-,所以不能得到Mg单质
(3)小于
由图1可知,随着温度升高,K1增大,则ΔH1>0,根据盖斯定律又得
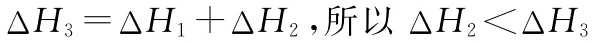
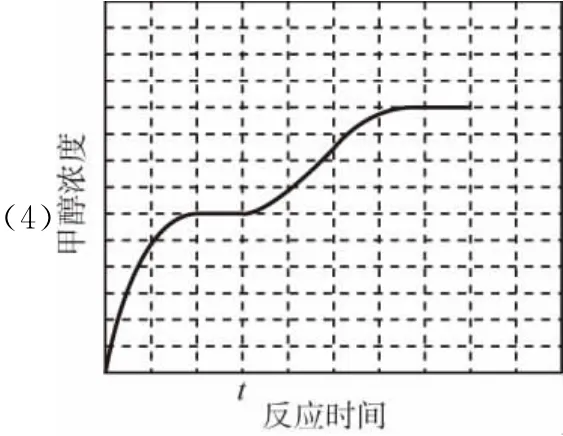
备考策略:复习时要深刻理解热化学、电化学、化学反应速率、盖斯定律和勒夏特列原理等理论,理论联系实际解决相关问题。注意化学原理和化学元素、化学计算的融合。题目的设问、考查的内容较多,思维切换角度大,同学们要加强思维能力的训练。
31.【加试题】(10分)纳米CdSe(硒化镉)可用作光学材料。在一定条件下,由Na2SO3和Se(硒,与S为同族元素)反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒。流程图如下:

注:①CdCl2能与配位剂L形成配合物[Cd(L)n]Cl2

②纳米颗粒通常指平均粒径为1~100nm的粒子
请回答下列问题:
(1)图甲加热回流装置中,仪器a的名称是,进水口为__________(填“1”或“2”)。
(2)①分离CdSe纳米颗粒不宜采用抽滤的方法,理由是___________________________。
②有关抽滤,下列说法正确的是_______________。
A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.图乙抽滤装置中只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸

(3)研究表明,CdSe的生成分两步:①SeSO2-3在碱性条件下生成HSe-;②HSe-与Cd2+反应生成CdSe。
完成第①步反应的离子方程式SeSO2-3+_________===HSe-+__________。
写出第②步反应的离子方程式:___________________。
(4)CdSe纳米颗粒的大小影响其发光性质。某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图丙所示;同时探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图丁所示。
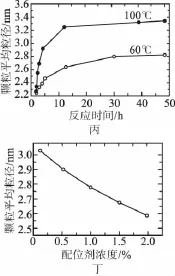
下列说法正确的是______________。
A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒
B.在图丙所示的两种温度下,只有60℃反应条件下可得到2.7nm的CdSe纳米颗粒
C.在其他条件不变时,若要得到较大的CdSe纳米颗粒,可采用降低温度的方法
D.若要在60℃得到3.0nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法
试题特点:这是一道以实验室制取CdSe纳米颗粒流程图为背景的实验综合题。考查知识点涉及仪器的名称,仪器连接方式,物质的分离和提纯方法,离子方程式的书写,利用题给信息图进行化学反应条件的选择。
解题思路:第(1)(2)问,冷凝管的名称和水的进出方向,抽滤的操作方法与步骤,是常用仪器和常做的化学实验,需要考生在理解实验原理的基础上熟记名称、步骤与方法,才能作答。
第(3)问书写离子反应方程式。根据元素守恒、电荷守恒、电子得失守恒,特别要注意碱性条件的提示,才能较好地写出两个离子方程式,有难度。
第(4)问考查考生的识图能力。从图丙可以看出,温度越高,颗粒平均粒径越大,从图丁可以看出,配位剂浓度越大,颗粒平均粒径越大,根据图中曲线变化趋势和图中有关数据综合分析可顺利解答。
参考答案:
(1)冷凝管 2
(2)①抽滤不宜用于过滤胶状沉淀或颗粒大小的沉淀
②AD
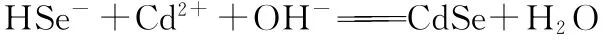
(4)AD
备考策略:复习时以强化实验设计、探究与实验分析能力为主,同时涉及基本操作、基本实验方法、装置与仪器选择、误差分析等知识。关注气体制备、溶液净化与除杂、溶液配制、影响速率因素探究、元素金属性或非金属性强弱(物质氧化性或还原性强弱)、物质成分或性质探究、中和滴定等基本实验的重组或延伸。
解题时要搞清楚实验目的,要把实验目的与装置和操作相联系,找出涉及的化学原理、化学反应或物质的性质等,然后根据问题依次解答即可。
32.【加试题】(10分)乙酰基扁桃酰氯是一种医药中间体。某研究小组以甲苯和乙醇为主要原料,按下列路线合成乙酰基扁桃酰氯。

请回答下列问题:
(1)D的结构简式:_____________________。
(2)下列说法正确的是________________________。
A.化合物A不能发生取代反应
B.化合物B能发生银镜反应
C.化合物C能发生氧化反应
D.从甲苯到化合物C的转化过程中,涉及的反应类型有取代反应、加成反应和氧化反应
(3)E+F→G的化学方程式是_______________。
(4)写出化合物D同时符合下列条件的所有可能的同分异构体的结构简式:________。①红外光谱检测表明分子中含有氰基(—CN);②1H-NMR谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子
(5)设计以乙醇为原料制备F的合成路线(用流程图表示;无机试剂任选)。
题型特点:这是一有机合成路线图为背景的综合题。对题给三条信息中官能团变化的理解是解题的关键。由于路线图中原料与产物的结构简式均已知,故顺推与逆推相结合是解题的重要方法。
解题分析:第(1)(2)问是考查烃的卤代、卤代烃的水解、醇的催化氧化等熟知的反应,结合题给信息中醛的加成反应,可顺利作答。
第(3)问是题给信息的应用,有一定的难度。首先要顺推得出E为羟基酸,F为酰氯,根据题给信息,酰氯与醇羟基发生取代反应生成酯和HCl,据此可完成该化学方程式。()

第(5)问审题很重要,是书写流程图而不是化学方程式。根据题给信息,乙酰氯是由乙酸与SOCl2反应而得,逆推乙酸可由原料乙醇连续氧化而得。
参考答案:
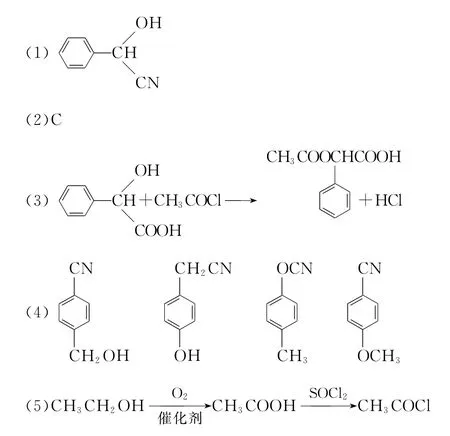
备考策略:学会直接从官能团、前后有机物的结构差异、特殊反应条件、特殊转化关系、不饱和度等角度推断。学会通过化学计算进行推断,一般是先求出相对分子质量,再求分子式,根据性质确定物质。出现情境信息时,要理解信息的本质,采用模仿迁移的方法与所学知识融合在一起使用,采用顺推、逆推、中间向两边推、多法结合推断。
二、三道加试题给我们复习备考的启示
1.高考不是考知识,而是考知识在生产、生活、实验等情境的应用。高考题是将课内学过的知识和新信息结合在一起,设计成生产、生活、实验中实际问题,请考生予以解决。利用信息题全面考查各种能力是命题的重要方向,本卷所给信息很丰富,有流程图(实验、有机合成)2个,新化学反应式8个,平面坐标信息图4幅。
2.只有学会信息的加工处理才能适应新高考。信息处理一般可分三个环节,即阅读、整理和应用。在阅读时,弄清题目给出了哪些信息,所要解决的问题是什么。在整理时,要理解信息之间,信息与问题之间,信息与已学知识之间的联系。在阅读与整理基础上,分析、推理、计算找到解题的正确方法。
3.调控好学考题与加试题的解题时间,是赢得新高考的一个重要方面。由于高中学考和高考选考合卷,故要在仔细做题的前提下,加快必考题的解题速度,使加试题有比较充足的时间去审题解题验题。
(作者单位:浙江省义乌市教育研修院)

