经颈静脉肝内门体分流术误穿肝外门静脉的成功处理(附3例报告)
经颈静脉肝内门体分流术误穿肝外门静脉的成功处理(附3例报告)
梁志会,崔进国,徐树彬,李 亮,陈 静,袁 涛,刘秀芳
目的 探讨经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt, TIPSS)中经肝静脉与肝外门静脉分流的可行性及安全性。方法 回顾性分析TIPSS术中经肝静脉与肝外门静脉分流3例患者的临床资料。结果 3例常规行TIPSS术,造影显示门静脉穿刺点位于肝外,采取先置入覆膜内支架、后球囊扩张的方法经肝静脉(或下腔静脉肝段)与肝外门静脉建立分流道。3例均获成功,分流道通畅,分流量适中,无血管破裂、大出血等并发症发生。随访3个月食道胃底静脉曲张均消失,12个月内无再狭窄发生。结论 对于TIPSS术中门静脉穿刺点位于肝外者,经肝静脉(或肝段下腔静脉)与肝外门静脉建立分流道可作为一种特殊治疗选择。
门体分流术,经颈静脉肝内;手术后并发症;出血

经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt, TIPSS)目前已成为治疗肝硬化门静脉高压合并消化道出血的一种有效方法。一般认为,分流道的门静脉穿刺点应该位于肝内门静脉分叉或左右分支近端,如位于肝外,则容易发生血管破裂、出血等并发症。但是一些特殊患者,如肝硬化严重,肝脏体积重度缩小,或血管走行变异,肝静脉与门静脉的空间关系发生变化,TIPSS操作时很难穿中肝内门静脉,当穿刺点位于肝外时亦可尝试于肝静脉与肝外门静脉间建立分流道。我院2008—2015年共对410例肝硬化门静脉高压合并消化道出血患者行TIPSS术,其中3例门静脉穿刺点位于肝外,我们经肝静脉(或肝段腔静脉)与肝外门静脉成功建立分流道,无并发症发生,现总结经验如下。
1 资料与方法
1.1 一般资料 本组3例,男2例,女1例;平均年龄45.3岁。均有慢性乙型肝炎病史。以突发上消化道出血入院,食道造影或胃镜检查示食道胃底静脉曲张;腹部超声、CT或MRI诊断为重度肝硬化,肝脏体积明显缩小;Child-Pugh分级,B级2例,C级1例。入院后立即给予抑酸、止血、保肝、补充营养等内科保守治疗,当患者出血停止、一般状况稳定后,择期行TIPSS术。
1.2 手术主要器材 5F Cobra导管,0.035 英寸超滑导丝及加硬导丝,Rups-100穿刺套管针,8 mm×4 cm球囊,8 mm×8 cm覆膜内支架(Fluency,美国巴德公司生产)。
1.3 手术操作方法 患者取仰卧位,予心电、血压、脉搏氧监护,常规消毒铺单,局部麻醉后穿刺右侧颈内静脉,置入Rups-100穿刺套管针,在导丝导引下选择肝右静脉,依据肝脏增强CT和经肠系膜上动脉造影所见确定穿刺门静脉的位置和角度。穿刺门静脉成功后注入造影剂,3例均为门静脉主干首先显影,左右分支随后显影,此时应考虑到穿刺点位于肝外门静脉可能,应行多角度造影确定穿刺门静脉的进针点。如穿刺点位于肝外门静脉主干(图1a、1b),不应先行球囊扩张,否则将导致腹腔大出血。首先测量门静脉压力,之后沿导丝、导管将Rups-100硬质导管送入门静脉主干(图1c),然后撤出硬质导管,置入覆膜内支架(直径一般选择8 mm,长度为6或8 cm),一边缓慢回撤长鞘,一边释放支架。支架释放后造影显示2例支架扩张不良,此时可行球囊后扩张使支架完全张开。之后将导管送入脾静脉或肠系膜上静脉,造影证实无造影剂外溢后(图1d),再次测量门静脉压力。最后将导管选择至胃冠状静脉,以不锈钢圈进行栓塞,结束操作。
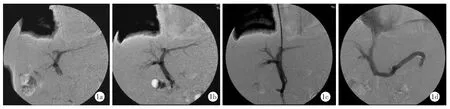
图1 经肝外门静脉建立分流道行经颈静脉肝内门体分流术患者术中所见
1a.穿刺门静脉成功后造影示穿刺点位于肝外;1b.多角度旋转造影确认穿刺点位于肝外;1c.沿导丝、普通导管将硬质导管送入门脉;1d.释放内支架后再次造影示分流道通畅,无造影剂外溢
1.4 术后处理 常规心电、血压、脉搏氧监护1~2 d。给予保肝及抗凝治疗。具体抗凝治疗方案:低分子肝素钠5000 U每12 h 1次皮下注射,连续应用7 d;术后第3日开始给予华法林2.5 mg每日1次口服,根据凝血四项检测结果调整剂量,将凝血酶原时间调整至24~28 s,或国际标准化比值调整至2.0左右。
1.5 观察与随访 术后3、7、14 d复查血常规及肝功能。术后1周复查上消化道造影,了解食道胃底静脉曲张缓解情况。之后每3个月复查上消化道造影及肝脏彩色多普勒超声(彩超)了解分流道通畅情况及血流速度。
2 结果
2.1 手术情况 3例均成功置入覆膜内支架、建立分流道,其中2例行球囊后扩张。3例均栓塞增粗迂曲的胃冠状静脉,成功率100%,无出血、胆汁瘘等并发症发生。术前测门静脉压力为(40.7±12.6)cmH2O,术后即刻测压降至(17.2±3.4)cmH2O。
2.2 随访情况 3例均未再发生消化道出血。术后1周复查消化道造影示食道胃底静脉曲张明显好转,术后3个月恢复正常。术后随访12个月,肝脏彩超示:3例分流道均未发生再狭窄,血流通畅。
3 讨论
TIPSS术自问世以来,已成为治疗肝硬化门静脉高压合并上消化道出血的一线治疗手段[1]。它的常规操作方法是:经右侧颈内静脉穿刺进针,置入Rups-100穿刺套管针,选择肝静脉,造影证实肝静脉无狭窄及阻塞后,根据术前增强CT及经肠系膜上动脉门静脉间接造影结果,穿刺门静脉。穿刺成功后将导管送入脾静脉或肠系膜上静脉,进一步造影确定穿刺点位置、了解胃冠状静脉开口及增粗情况,并测量门静脉压力。首先引入球囊对穿刺道进行扩张,置入内支架,建立分流道并再次测量门静脉压力,后对胃冠状静脉进行选择性栓塞[2]。由此可见,成功穿刺门静脉是本技术的关键,使门静脉穿刺进针点位于肝内,这样在进行球囊扩张及置入内支架后就不会引起腹腔出血等严重并发症。
在严重肝硬化患者中,肝脏体积严重缩小,肝静脉和门静脉空间解剖位置发生变化,因此常规穿刺门静脉难以成功。尤其是在门静脉靠近中线时,需提高穿刺点位置(在右肝静脉开口部或直接经下腔静脉肝段穿刺门静脉)时,难以完全避免穿中肝外门静脉。
为提高门静脉穿刺成功率,减少并发症,很多学者详细研究了门静脉系统解剖和其与肝静脉的空间关系[3-5]。我们的体会是:术前仔细研究影像学资料,了解门静脉系统解剖,尤其是穿刺前首先行经肠系膜上动脉门静脉间接造影,可以显示门静脉与肝静脉的空间关系,有助于避免穿中肝外门静脉。正确的门静脉进针部位应位于门静脉分叉处或门静脉左右分支近端2 cm以内。如果穿刺点位于肝外,行球囊扩张及置入裸支架时,将会导致腹腔大出血等严重并发症发生。覆膜支架的问世有助于打破此禁区。1995年覆膜内支架首次应用于TIPSS术,之后由于它可以明显降低再狭窄率而得到公认[6-8]。覆膜内支架是由金属支架及其表面覆盖的一层生物性聚合物或人造血管移植物构成,不但具有普通支架的支撑作用,而且还通过膜的机械性阻隔和膜表面的特殊物质起到防止血栓形成、胆汁瘘和内膜增生的作用[9]。我们的临床实践表明,通过覆膜内支架的应用,不仅提高了分流道的通畅率,而且使肝静脉与肝外门静脉间建立分流道成为可能。
TIPSS术中如果穿中了肝外门静脉,常规观点是撤出穿刺针,重新穿刺,但是那样势必在肝外门静脉穿刺点上留有血管破口,腹腔内大出血的风险很高。我们经肝外门静脉建立分流道,既能成功完成手术,又能有效规避此风险。本项技术的关键点:①对穿刺门静脉进针点的准确判断非常重要,如穿刺门静脉后注入造影剂见门静脉主干先显影,要行多角度造影以证实穿刺门静脉的进针点是否在肝外门静脉。②当确认穿刺点位于肝外门静脉后,不应拔管,此时应沿导丝、导管将Rups-100硬质导管和长鞘直接跟进,拔出硬质导管后,首先释放覆膜内支架,如支架膨胀不良可行球囊后扩张。释放支架时不可一下将长鞘全部后撤,应一边缓慢后撤,一边缓慢释放支架,这样会降低出血风险。造影确认无造影剂外溢后,再行胃冠状静脉选择性栓塞。
我们的实践证明,随着覆膜内支架临床的广泛应用和TIPSS技术操作的改进,经肝静脉与肝外门静脉建立分流道是可行的、安全的。但风险必然很大,操作稍有不慎就可能造成腹腔大出血。本技术只能在TIPSS术不慎穿入肝外门静脉的特定情况下进行。
[1] Toshikuni N, Takuma Y, Tsutsumi M. Management of gastroesophageal varices in cirrhotic patients: current status and future directions[J].Ann Hepatol, 2016,15(3):314-325.
[2] Wang C M, Li X, Fu J,etal. Construction of Transjugular Intrahepatic Portosystemic Shunt: Bare Metal Stent/Stent-graft Combination versus Single Stent-graft, a Prospective Randomized Controlled Study with Long-term Patency and Clinical Analysis[J].Chin Med J (Engl), 2016,129(11):1261-1267.
[3] 崔进国,张书田,冯艳皎,等.88例门静脉造影解剖分析[J].中华放射学杂志,1996,30(1):28-32.
[4] 梁惠民,冯敢生,杨建勇,等.与TIPSS相关的影像学解剖关系的研究[J].中华放射学杂志,1998,32(4): 243-247.
[5] 金武男,杨香,车成日,等.门静脉的解剖与变异[J].中国临床解剖学杂志,2006,24(2):157-159.
[6] Rossle M, Siegerstetter V, Huber M,etal. The first decade of the transjugular intrahepatic portosystemic shunt (TIPS): state of the art[J].Liver, 1998,18(2):73-89.
[7] Tripathi D, Redhead D. Transjugular intrahepatic portosystemic stent-shunt: technical factors and new developments[J].Eur J Gastroenterol Hepatol, 2006,18(11):1127-1133.
[8] Saad W E, Darwish W M, Davies M G,etal. Stent-grafts for transjugular intrahepatic portosystemic shunt creation: specialized TIPS stent-graft versus generic stent-graft/bare stent combination[J].J Vasc Interv Radiol, 2010,21(10):1512-1520.
[9] 曹广劭,王晓白.覆膜支架防治TIPS分流道再狭窄的研究进展[J].介入放射学杂志,2008,17(9):670-674.
050082 石家庄,解放军白求恩国际和平医院放射科(梁志会、崔进国、徐树彬、李亮、陈静、袁涛); 050000 石家庄,机械化步兵学院门诊部(刘秀芳)
R654.3
B
1002-3429(2017)01-0066-03
10.3969/j.issn.1002-3429.2017.01.023
2016-07-27 修回时间:2016-10-23)

