候选药物T-VA的质谱裂解规律及其在大鼠体内的代谢产物研究
张晨泽,闫萌萌,徐 冰,林宏英,闫文强,刘 帅,陈 静,刘永刚,王鹏龙,雷海民
(1.北京中医药大学中药学院,北京 100102;2.西藏藏医学院教务处,西藏 拉萨 850000)
候选药物T-VA的质谱裂解规律及其在大鼠体内的代谢产物研究
张晨泽1,闫萌萌1,徐 冰1,林宏英1,闫文强1,刘 帅1,
陈 静2,刘永刚1,王鹏龙1,雷海民1
(1.北京中医药大学中药学院,北京 100102;2.西藏藏医学院教务处,西藏 拉萨 850000)
采用液相色谱-线性离子阱-静电场轨道阱高分辨质谱(LC/LTQ-Orbitrap MS)技术研究候选药物T-VA的裂解规律及体内代谢,建立了大鼠体内T-VA及其代谢产物的LC/MSn分析方法,分析讨论了各自的主要碎片离子峰、质谱特征与结构信息,发现了血浆中主要代谢物M1。借鉴药物化学的方法,合成得到了代谢产物实体M1-1,经1HNMR、13CNMR、HRMS确认其结构,根据其色谱、质谱特征进行验证,结果表明,合成得到的M1-1即为血浆主要代谢物M1。借助PC12细胞模型验证了代谢产物M1的神经保护活性,该结果可为进一步研究其生物转化过程与前药修饰提供重要信息。
液相色谱-线性离子阱-静电场轨道阱高分辨质谱(LC/LTQ-Orbitrap MS);候选药物T-VA;裂解规律;代谢产物;化学合成;神经保护活性
从天然产物中寻找先导化合物是新药研发的基本方法之一[1-2]。神经系统疾病,如老年痴呆(AD)、帕金森病(PD)和中风(Stroke)等,在老年人中的发病率居高不下,严重威胁人类的生命健康[3-5]。现代研究证实,这些神经系统疾病均是由神经细胞损伤引起的,因此,开发安全高效的治疗神经细胞损伤的药物仍然是药物研究的重要方向[6]。川芎嗪(TMP)为传统中药伞形科植物川芎根茎中的有效化学成分,已被广泛用于治疗缺血性脑中风[7-8]。现代药理学研究表明,TMP能较快地通过血脑屏障,具有抗氧化、抗自由基、 Ca2+拮抗、抑制血小板聚集、防止血栓形成等作用,有助于神经细胞恢复治疗[9-11]。为了进一步提高TMP的神经保护活性,本课题组借鉴“中药配伍法则·化药拼合原理”研究思路,以TMP和其他具有神经保护效应的中药成分为原料,设计合成了一系列川芎嗪衍生物[12-14]。经实验验证,这些川芎嗪衍生物对损伤的PC12细胞具有保护作用,其中T-VA对CoCl2损伤的PC12细胞保护作用最强(EC50=4.25 μmol/L)[12]。研究还发现,T-VA能够调控核转录因子(NF-κB/p65)和环氧合酶(COX-2)的表达,且能改善中脑动脉栓塞(MCAO)模型大鼠的运动功能[15]。T-VA的分子式为C24H28N4O4,其结构示于图1。

图1 候选药物T-VA的结构Fig.1 Structure of innovative drug T-VA
液相色谱-质谱(LC/MS)联用技术因结合了液相色谱的分离能力和质谱的灵敏度高、专属性强的检测能力,现已成为药物代谢研究的有力工具和代谢物结构分析的重要方法[16-17]。线性离子阱-静电场轨道阱串联质谱(LTQ-Orbitrap MS)的分辨率高达100 000,质量精度高达2×10-6,能够对目标物进行多级质谱分析,因此可在没有标准物质的情况下,通过精确分子质量对未知物进行快速筛查与结构确证[18-19]。
目前,已有一些对川芎中内酯类化合物及川芎嗪衍生物的质谱学研究报道[20-21],但对候选药物T-VA的质谱裂解规律及其在大鼠体内代谢的质谱解析尚无研究。本工作拟采用LC/LTQ-Orbitrap MS技术,通过分析T-VA与其代谢产物的主要碎片离子峰、质谱特征与结构信息,阐明T-VA在大鼠体内的代谢途径。同时还借鉴药物化学的方法,合成得到了代谢产物实体,根据质谱特征验证其与代谢产物结构的一致性,并借助PC12细胞模型验证代谢产物的神经保护活性,希望为进一步研究T-VA的生物转化过程与前药修饰提供重要信息。
1 实验部分
1.1 主要仪器与装置
Accela 600 pump 高效液相色谱-LTQ-Orbitrap XL质谱联用仪:美国Thermo Scientific公司产品,配有电喷雾离子源(ESI)、在线脱气机、自动进样器、高压二元梯度泵和Metworks 2.0数据处理系统;RCT基本型双线恒温加热磁力搅拌器:德国IKA公司产品;BSA224S-CW型分析天平:德国赛多利斯公司产品;AM-500核磁共振仪:瑞士Bruker公司产品;Forma 3111 CO2培养箱,Multiskan GO全波长酶标仪:均为美国Thermo Fisher公司产品。
1.2 材料、试剂与实验动物
化合物T-VA:由本实验室合成[12],经HPLC面积归一化法测定其纯度大于97%;乙腈、甲醇和甲酸:色谱纯,美国Fisher公司产品;对甲苯磺酰氯、香草酸、氯化亚砜、碳酸钾、N,N-二甲基甲酰胺(DMF)、四氢呋喃(THF)和无水甲醇:均为分析纯或化学纯;PC-12细胞:由北京协和细胞资源中心提供;Gibco 1640培养基、胎牛血清、马血清和神经生长因子:美国Thermo Fisher公司产品;四甲基偶氮唑蓝(MTT):美国Sigma公司产品;雄性SD大鼠(质量240~260 g):由北京维通利华实验动物技术有限公司提供。
1.3 实验条件
1.3.1 色谱条件 色谱柱:Agilent Zorbax SB C18柱(250 mm×4.6 mm×5 μm);HPLC流动相:A为0.1%甲酸水溶液,B为甲醇;梯度洗脱程序:0~20 min(70%B~85%B);流速1.0 mL/min;柱温25 ℃;进样量10 μL。
1.3.2 质谱条件 电喷雾离子源(ESI)正离子模式;质量扫描范围m/z50~1 000;喷雾电压3.0 kV;毛细管温度300 ℃;鞘气流速30 L/h;辅助气流速180 L/h。分析时,先采取高分辨傅里叶全扫描采集一级质谱,然后采用二维线性离子阱(LTQ)采集二级和三级质谱,自动选取上一级最强离子峰进行碰撞诱导解离裂解,碰撞能量为30%。
1.4 实验方法
1.4.1 样品制备 雄性SD大鼠给药前12 h禁食,自由饮水,给药组以120 mg/kg的用量灌胃给药,空白对照组灌胃等量0.3% CMC-Na。3 h后,大鼠腹腔注射10%水合氯醛麻醉,腹主动脉取血,注入肝素锂采血管中,以3 000 r/min离心10 min,取上清液;加入3倍量的乙腈,涡旋充分混匀,再以10 000 r/min离心15 min,取上清液,氮气吹干后用甲醇溶解,经 0.45 μm滤头过滤,于-20 ℃保存,备用。
1.4.2 代谢产物M1的合成 将2-羟基-3,5,6-三甲基吡嗪、氢氧化钾置于单口瓶中,加入四氢呋喃混匀,在冰浴下加入对甲苯磺酰氯,于0 ℃搅拌0.5 h,然后缓慢升至室温,继续搅拌15 h。采用薄层色谱(thin layer chromatography, TLC)监测,待原料基本消失,停止反应,向反应液中加水分散,经乙酸乙酯萃取,蒸干,残留物用硅胶减压蒸干拌样,硅胶柱洗脱,得到白色固体。将香草酸置于单口瓶中,加入无水甲醇,待完全溶解后,在冰浴下缓慢滴加氯化亚砜,于0 ℃下搅拌0.5 h,然后缓慢升至室温,继续搅拌15 h。采用TLC监测,待原料基本消失,停止反应,将反应液减压蒸干,得到白色固体。将前两步反应产物与碳酸钾置于单口瓶中,加入N,N-二甲基甲酰胺,在氮气保护下于70 ℃搅拌15 h。采用TLC监测,待原料基本消失,停止反应,加水分散,用二氯甲烷萃取,蒸干,残留物用硅胶减压蒸干拌样,硅胶柱洗脱,得到代谢产物M1。其详细的合成路线示于图2。
1.4.3 代谢产物M1的神经保护活性评价
参考本课题组前期工作[12-14],用85% RPMI 1640细胞培养基、5%胎牛血清、10%马血清,再加入100 U/mL双抗,配制完全培养基。当细胞浓度达到80%时,倒掉原培养基,加入 RPMI 1640,饥饿细胞14 h后,以每孔120 μL接种于多聚赖氨酸包被过的96孔板中,用90% RPMI 1640、10%胎牛血清、100 U/mL双抗配制培养基培育,每孔细胞浓度约为7×103。另加入0.05 mg/L的NGF诱导细胞分化,分化培养48 h。用DMSO溶解化合物,培养基稀释,以浓度分别为3.75、7.50、15、30、60 μmol加药,每一浓度平行4孔,对照组加入等体积培养液,DMSO的终浓度小于0.1%。36 h后,添加终浓度为300 μmol CoCl2损伤细胞。12 h后加20 μL(5 g/L)MTT,培养4 h,去掉上清液,每孔加入100 μL DMSO,振荡5 min,测定490 nm处各孔的吸光度。按式(1)计算细胞增殖率。
[A490(Compd)-A490(CoCl2)]/
[A490(NGF)-A490(CoCl2)]×100%
(1)
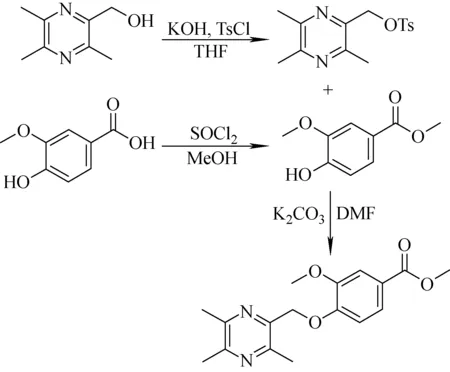
图2 代谢产物M1的合成路线Fig.2 Synthesis route of M1
2 结果与讨论
2.1 T-VA的ESI-MSn分析结果
采用正离子模式对T-VA进行ESI-MSn分析,得到的质谱图示于图3。图3a中可见T-VA的准分子离子峰m/z437 [M+H]+;图3b中可见m/z437 [M+H]+及其裂解碎片m/z285、151;图3c是对m/z285进一步做三级质谱扫描,得到m/z151、123碎片峰。化合物T-VA在上述质谱条件下发生离子化,川芎嗪与香草酸的连接键(酯键和醚键)均存在发生断裂的可能性,不能明确得出其中基团断裂的先后顺序。因此,只能推断化合物T-VA可能的裂解途径,示于图4。
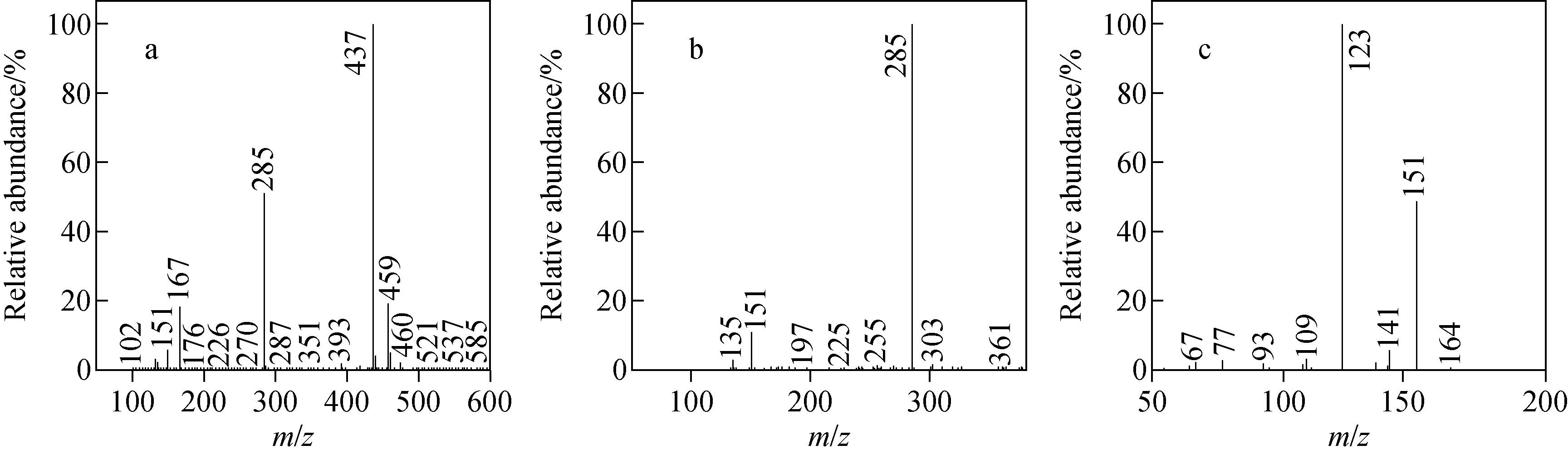
注:a.MS1;b.MS2 of m/z 437;c.MS3 of m/z 285图3 候选药物T-VA的MSn质谱图Fig.3 Mass spectrum of innovative drug T-VA

图4 T-VA可能的裂解途径Fig.4 Possible fragmentation pathway of T-VA
2.2 T-VA大鼠体内代谢产物的鉴定
空白大鼠血浆、给药大鼠血浆、给药大鼠血浆扣除背景后的总离子流图示于图5。与空白组血样比较,对给药大鼠血浆的总离子流图进行背景扣除后,除原型药M0外,在给药大鼠血样中还监测到1种主要代谢产物M1。
在一级全扫描质谱中,M0的准分子离子峰为m/z437[M+H]+,色谱保留时间为6.25 min,裂解碎片为m/z285、151,其他色谱保留时间、准分子离子及碎片离子均与化合物 T-VA相同,故确定M0为母体药物T-VA。
在一级全扫描质谱中,准分子离子m/z317[M+H]+,色谱保留时间为5.09 min,比M0准分子离子(m/z437)少 120 u,推测其为化合物T-VA母核脱去一分子川芎嗪的代谢物。经碰撞诱导解离(CID),该离子产生的二级碎片离子为m/z285、135,与原型药裂解规律类似,推断M1为香草酸甲酸部位在体内代谢发生甲酯化的结果,其结构及可能的裂解途径示于图6。LTQ Orbitrap 高分辨质谱仪可仅通过准确的化合物质量(在除质量外其他条件未知的情况下)推测其分子式,并根据环双键当量值(RDB当量值)确定正确的化合物分子式。采用该方法对M1的分子离子峰(m/z317.148 62)进行分析,得到M1([M+H]+)的分子式为C17H21O4N2(RDB:8.5,delta(ppm):-3.038),与推断结果相符合。

图5 空白大鼠血浆(a)、给药大鼠血浆(b)、给药大鼠血浆扣除背景处理后(c)的总离子流图Fig.5 Total ion chromatogram of control group (a), T-VA group (b), background deduction (c)

图6 代谢产物M1的结构及裂解规律Fig.6 Structure and possible fragmentation pathway of M1
2.3 代谢产物M1的合成及确认
采用药物化学的方法,合成得到推断的代谢产物M1-1,经1H-NMR、1C-NMR确定其结构。M1-1为白色固体,产率52.5%,熔点140.0~140.7 ℃。1H-NMR(CDCl3)(ppm):7.62~7.64(dd,J=1.2,8.4 Hz,1H,Ar—H),7.53(d,J=1.2 Hz,1H,Ar—H),7.06(d,J=8.4 Hz,1H,Ar—H),5.26(s,2H,—CH2),3.88(s,6H,2×—OCH3),2.62(s,3H,—CH3),2.52(s,3H,—CH3),2.51(s,3H,—CH3)。13C-NMR(CDCl3)(ppm):166.95(—COO—),151.99,151.39,150.12,149.30,148.91,145.41,123.41,114.38,112.82,112.51,70.81(—CH2),56.12(—OCH3),52.16(—OCH3),21.70(—CH3),21.51(—CH3),20.67(—CH3)。
M1与M1-1的质谱图示于图7。合成得到M1-1的色谱保留时间为5.11 min,其分子离子峰为m/z317.148 35,二级裂解碎片为m/z285.077 70、134.923 80;而血浆中代谢产物M1的色谱保留时间为5.09 min,分子离子峰为m/z317.148 62,二级裂解碎片为m/z285.078 70、134.947 22。由此可见,合成得到的化合物与血浆中代谢产物的色谱、质谱特征均吻合,据此可以确证M1为香草酸羧基部位在体内代谢发生甲酯化的结果,而合成得到的M1-1即为M1。
2.4 代谢产物M1的神经保护活性评价
前期关于代谢产物M1类化合物的构效关
系研究表明,香草酸与川芎嗪拼合的醚键部分是活性药效基团,而酯键区域可能发挥前药作用,即保护化合物的活性,防止提前被代谢失活。选取CoCl2损伤的PC12细胞模型来验证代谢产物M1与T-VA类似的神经保护活性,详细数据列于表1。

图7 M1(a.MS1,b.MS2)与M1-1(c.MS1,d.MS2)的质谱图Fig.7 Mass spectrum of M1(a.MS1, b.MS2) and M1-1(c.MS1, d.MS2)

化合物Compound细胞增殖率Cellproliferationrate/%60μmol/L30μmol/L15μmol/L7.5μmol/L3.75μmol/LEC50/(μmol/L)M184.8251.7247.4522.6232.1516.01
如表1所示,不同浓度下代谢产物M1对CoCl2损伤的PC12细胞均有一定的保护作用,拟合得EC50值为16.01 μmol/L,活性接近候选药物T-VA。该结果表明,代谢产物M1与T-VA具有类似的神经保护活性,T-VA可能通过体内代谢脱去酯键连接的川芎嗪继续发挥其活性作用。
3 结论
本研究采用LC/LTQ-Orbitrap MS技术对候选药物T-VA的裂解规律及体内代谢进行研究,建立了大鼠体内T-VA及其代谢产物的LC/MSn检测方法, 分析讨论了T-VA及其代谢产物的主要碎片离子峰、质谱特征与结构信息,发现其在大鼠血浆内的主要代谢产物M1为香草酸羧基部位脱吡嗪酯后发生甲酯化的结果。研究还借鉴药物化学的方法,合成得到代谢产物实体,根据其质谱特征对其进行验证,并借助PC12细胞模型验证了代谢产物M1与T-VA具有类似的神经保护活性,该结果可为进一步研究其生物转化过程与前药修饰提供重要信息。
[1] FIALHO A M, DAS GUPTA T K, CHAK-RABARTY A M. Designing promiscuous drugs? Look at what nature made![J]. Letters in Drug Design & Discovery, 2007, 4(1): 40-43.
[2] 刘珂. 源于传统中药的先导化合物筛选与优化[J]. 中国医药技术经济与管理,2007,1(4):62-69.
LIU Ke. Screening and optimization of lead compounds which based traditional Chinese medcine[J]. Chinese Journal of Pharmaceutical Technology Economics and Management, 2007, 1(4): 62-69(in Chinese).
[3] LINDVALL O, KOKAIA Z. Stem cells for the treatment of neurological disorders[J]. Nature, 2006, 441(7 097): 1 094-1 096.
[4] YU L, NING W, ZHANG Y, et al. Neuroprotective effect of muscone on glutamate-induced apoptosis in PC12 cells via antioxidant and Ca2+, antagonism[J]. Neurochemistry International, 2014, 70(1):10-21.
[5] ASSOCIATION A. 2014 Alzheimer’s disease facts and figures[J]. Alzheimers & Dementia the Journal of the Alzheimers Association, 2014, 10(2): 47-92.
[6] TERESHCHENKO J, MADDALENA A, BAHR M, et al. Pharmacologically controlled, discontinuous GDNF gene therapy restores motor function in a rat model of Parkinson’s disease[J]. Neurobiology of Disease, 2014, 65: 35-42.
[7] HAN J Z, SUN J, ZHU Q G, et al. A modified LC-MS/MS method for determination of tetramethylpyrazine in microdialysis samples and calibration of home-made linear probes[J]. Biomedical Chromatography, 2012, 26(10): 1 276-1 281.
[8] TAN F, FU W, CHENG N, et al. Ligustrazine reduces blood-brain barrier permeability in a rat model of focal cerebral ischemia and reperfusion[J]. Experimental and Therapeutic Medicine, 2015, 9(5): 1 757-1 762.
[9] KAO T K, OU Y C, KUO J S, et al. Neuroprotection by tetramethylpyrazine against ischemic brain injury in rats[J]. Neurochemistry International, 2006, 48(3): 166-176.
[10]XIAO X, LIU Y, QI C, et al. Neuroprotection and enhanced neurogenesis by tetramethylpyrazine in adult rat brain after focal ischemia[J]. Neurological Research, 2010, 32(5): 547-555.
[11]ZHANG H, SUN R, LIU X Y, et al. A tetramethylpyrazine piperazine derivate CXC137 prevents cell injury in SH-SY5Y cells and improves memory dysfunction of rats with vascular dementia[J]. Neurochemical Research, 2014, 39(2): 276-286.
[12]WANG P, ZHANG H, CHU F, et al. Synthesis and protective effect of new ligustrazine-benzoic acid derivatives against CoCl2-induced neurotoxicity in differentiated PC12 cells[J]. Molecules, 2013, 18(10): 13 027-13 042.
[13]XU B, GONG Y, XU X, et al. Synthesis and protective effect of new ligustrazine derivatives against CoCl2-induced neurotoxicity in differentiated PC12 cells. Part 2[J]. Medicinal Chemistry Communication, 2015, 6(5): 806-809.
[14]LI G, XU X, XU K, et al. Ligustrazinyl amides: a novel class of ligustrazine-phenolic acid derivatives with neuroprotective effects[J]. Chemistry Central Journal, 2015, 9(1): 9.
[15]LI G, TIAN Y, ZHANG Y, et al. A novel ligustrazine derivative T-VA prevents neurotoxicity in differentiated PC12 cells and protects the brain against ischemia injury in MCAO rats[J]. International Journal of Molecular Sciences, 2015, 16(9): 21 759-21 774.
[16]ALLWOOD J W, GOODACRE R. An introduction to liquid chromatography-mass spectrometry instrumentation applied in plant metabolomic analyses[J]. Phytochemical Analysis, 2010, 21(1): 33-47.
[17]陈学国,赖永权,蔡宗苇. 液相色谱-电喷雾离子阱质谱分析乌头碱及其代谢物[J]. 质谱学报,2012,33(2):65-73.
CHEN Xueguo, LAI Yongquan, CAI Zongwei. Simultaneous analysis of aconitine and its metabolites by liquid chromatography-electrospray ion trap mass spectrometry[J]. Journal of Chinese Mass Spectrometry Society, 2012, 33(2): 65-73(in Chinese).
[18]张加余,蔡伟,李云,等. HPLC/LTQ-Orbitrap MSn结合MDF数据挖掘技术快速鉴定藏白蒿绿原酸类似物[J]. 质谱学报,2015,36(4):321-327.
ZHANG Jiayu, CAI Wei, LI Yun, et al. Rapid characterization of chlorogenic acids analogues in artemisia younghusbandii using HPLC-LTQ-Orbitrap MSncoupled with MDF data mining technology[J]. Journal of Chinese Mass Spectrometry Society, 2015, 36(4): 321-327(in Chinese).
[19]黎永乐,郑彦婕,熊岑,等. 液相色谱/线性离子阱-静电场轨道阱高分辨质谱法快速筛查葡萄酒中的合成色素[J]. 色谱,2013,31(8):729-733.
LI Yongle, ZHENG Yanjie, XIONG Cen, et al. Fast screening of the artificial dyes in wine by liquid chromatography/hybrid linear ion trap-orbitrap mass spectrometry[J]. Chinese Journal of Chromatography, 2013, 31(8): 729-733(in Chinese).
[20]曾志,谢润乾,张涛,等. 川芎中内酯类化合物的质谱学规律[J]. 质谱学报,2011,32(5):293-300.
ZENG Zhi, XIE Runqian, ZHANG Tao, et al. The regular patterns of mass spectrometry of lactones fromLigusticumchuanxiongHort[J]. Journal of Chinese Mass Spectrometry Society, 2011, 32(5): 293-300(in Chinese).
[21]吴吉洋,高方圆,叶晓岚,等. 创新药物川阿格雷及其拼合分子阿魏酸和川芎嗪的质谱裂解规律[J]. 第二军医大学学报,2012,33(7):755-758.
WU Jiyang, GAO Fangyuan, YE Xiaolan, et al. Chuan’a gelei and its flatten structure ferulic acid and ligustrazine: mass fragmentation pathway[J]. Academic Journal of Second Military Medical University, 2012, 33(7): 755-758(in Chinese).
Mass Fragmentation Pathway of a Candidate Drug T-VA and Its Metabolites in Rats
ZHANG Chen-ze1, YAN Meng-meng1, XU Bing1, LIN Hong-ying1, YAN Wen-qiang1, LIU Shuai1, CHEN Jing2, LIU Yong-gang1, WANG Peng-long1, LEI Hai-min1
(1.SchoolofChinesePharmacy,BeijingUniversityofChineseMedicine,Beijing100102,China;2.OfficeofTeachingAffairs,TibetTibetanCollege,Lhasa850000,China)
The candidate drug T-VA (C24H28N4O4) was synthesized using two kind of neuroprotective ingredients from Chinese traditional medicinal herbs, and displayed promising protective effect on the injured PC12 cells. In previous study, this beneficial effect was due to the modulation of nuclear transcription factor-κB/p65 (NF-κB/p65) and cyclooxygenase-2 (COX-2) expressions. T-VA also exhibited neuroprotective effect in a rat model of ischemic stroke with concomitant improvement of motor functions. Understanding drug metabolites contributes to discovering and developing the novel drug from the metabolites possessed the pharmacological activities. The structure profile of the metabolites provides an essential perspective for the synthetic refinement and the candidates among an extensive series of potential structures, resulting in an optimum drug effectiveness and safety. Liquid chromatography with electrospray ionization mass spectrometric detection (LC-ESI-MS) has been extensively utilized for the online analysis and structural characterization of the active ingredients and metabolites. Thus, there is a need to determine the primary metabolites and mass fragmentation pathways of T-VA in order to understand its potential pharmacological applications. It is a pathway via LC/LTQ-Orbitrap MS to investigate the mass fragmentation of a candidate drug T-VA and study its metabolites in rats. As a result, a method of LC/MSnwas established for the analysis of T-VA and its metabolites in rats. The fragmentation pathway of T-VA was explained using the Analyst V4.0 software. By further analysis of main fragment ions (m/z317, 285, 135) and structural information (C17H21O4N2, RDB:8.5, delta ppm:-3.038 ppm), M1 [methyl-3-methoxy-4-((3,5,6-trimethylpyrazin-2-yl)methoxy)benzoate] was discovered as one of the main metabolites. According to the suppositional structure of M1, M1-1 was synthesized via condensation reaction, which was determined by nuclear magnetic resonance spectrum (1H-NMR,13C-NMR) and HRMS. By comparing the mass spectrum characters and chromatographic features of M1-1 and M1, it can confirm the exact structure of M1. Furthermore, the neuroprotective effect of M1 in differentiated PC12 cells were evaluated. As a result, M1 in different concentrations could protect PC12 cells injured by CoCl2(EC50=16.01 μmol/L), which was close to T-VA. The result indicated that both T-VA and its main metabolite have neuroprotective effect, which provides references for further new drug design. In this study, metabolite of candidate drug T-VA was obtained by chemical synthesis and verified by MS technique, which provided a novel idea on the study of drug metabolism. M1 may become a potential neuroprotective agent and further studies are currently underway.
LC/LTQ-Orbitrap MS; candidate drug T-VA; mass fragmentation pathway; metabolite; chemical synthesis; neuroprotective activity
2016-07-11;
2016-10-19
国家自然科学基金面上项目(81173519);北京市中药基础与新药研究重点实验室,北京中医药大学研究生自主课题(2016-JYB-XS117)资助
张晨泽(1992—),男(汉族),陕西人,硕士研究生,中药化学专业。E-mail: zcz920418@163.com
王鹏龙(1985—),男(汉族),河北人,讲师,从事中药先导化合物发现研究。E-mail: wpl581@126.com
雷海民(1968—),男(汉族),陕西人,教授,从事中药先导化合物发现与开发研究。E-mail: leihaimin@126.com
O657.63
A
1004-2997(2017)01-0067-08
10.7538/zpxb.2017.38.01.0067

