替吉奥或卡培他滨联合奥沙利铂一线治疗中晚期胃癌的疗效对比研究
张 伟,谭 睿(.西南交通大学生命学院,四川 成都 6003;2.四川省医学科学院·四川省人民医院胃肠外科,四川 成都 60072)
替吉奥或卡培他滨联合奥沙利铂一线治疗中晚期胃癌的疗效对比研究
张 伟1,2,谭 睿1
(1.西南交通大学生命学院,四川 成都 610031;2.四川省医学科学院·四川省人民医院胃肠外科,四川 成都 610072)
目的 比较替吉奥+奥沙利铂或卡培他滨+奥沙利铂方案治疗中晚期胃癌患者的效果及不良反应。 方法 选取四川省人民医院2014年1月至2015年1月经病理或细胞学确诊为不可手术的胃癌患者111例,利用随机抽样分为A、B两组,A组60例,B组51例,A组给予替吉奥+奥沙利铂,一个治疗周期为21天,替吉奥胶囊40 mg/m2,每日2次,口服,d1~14;奥沙利铂130 mg/m2,d1,口服。B组给予卡培他滨+奥沙利铂,一个治疗周期为21天,卡培他滨片1000 mg/m2,口服,每日2次,d1~14;奥沙利铂130 mg/m2,d1,口服。给药2个周期,用药后及随访期间评价疗效及不良反应。 结果 两组患者的客观有效率(ORR)、疾病控制率(DCR)均无统计学差异(P> 0.05)。两组贫血、乏力、恶心呕吐、肝功能损伤、外周神经炎发生率比较,差异无统计学意义(P> 0.05)。A组腹泻与手足综合征发病率低于B组 (P< 0.05)。 结论 两种治疗方案用于中晚期胃癌患者均有良好的安全性,疗效相当,替吉奥+奥沙利铂组腹泻和手足综合征发病率低于卡培他滨+奥沙利铂组。
替吉奥;卡培他滨;奥沙利铂;胃癌
胃癌是临床常见恶性肿瘤之一,胃癌的发病率在所有恶性肿瘤中居第四位,致死率仅排在肺癌之后,居世界第二位[1~3]。根治性手术仍是治疗胃癌的最有效的方法。然而即使患者接受了根治性手术,仍存在40%~60%的复发转移风险[4~9]。为了克服手术对改善胃癌预后的局限性,围手术期治疗主要包括术前和术后治疗,也已被研究者们广泛接受。常见的胃癌围手术期治疗包括化疗、放疗、生物治疗等,但因各个地区开展的临床研究不同,围手术期治疗方案也不尽相同,尚缺乏全球统一的“金标准”[10,11]。常用的胃癌化疗药物包括5-Fu、替吉奥、卡培他滨、顺销、奥沙利铂、表柔比星、多西他赛、紫杉醇、伊立替康等。替吉奥和卡培他滨是目前临床上常用的口服氟尿嘧啶类药物。口服氟尿嘧啶类药物联合奥沙利铂方案在胃癌治疗中的作用受到了越来越多的关注。本研究比较替吉奥联合奥沙利铂方案以及卡培他滨联合奥沙利铂方案对于中晚期胃癌患者的近期疗效及不良反应等方面的影响,为胃癌的临床治疗提供新思路。
1 资料与方法
1.1 一般资料 选取2014年1月至2015年1月就诊于四川省人民医院胃肠外科的Ⅱ~Ⅳ期胃癌患者共111例,男60例,女51例。年龄为35~65岁,纳入标准为:①年龄>18岁;②未发现其他原发肿瘤;③经病理学证实为不可手术胃癌;④根据RECIST1.1评分标准,患者至少含有1个可测量或可评估的病灶;⑤化疗前ECOG评分为0~2分,KPS评分≥70;⑥所采取的替吉奥或卡培他滨联合奥沙利铂化疗为一线用药方案;若曾行辅助化疗,则与辅助化疗的时间间隔需大于6个月;⑦化疗期间未行放疗或生物治疗;⑧骨髓造血功能、肝肾功能均正常:主要包括中性粒细胞计数≥1.5×109/L,血小板计数≥100 ×109/L,血红蛋白≥9.0 g/dl,AST、ALT≤2.5×正常上限(ULN)(若为肝转移患者则≤5 × ULN),ALP≤2.5 × ULN (若为肝转移患者则≤5 × ULN,若为骨转移患者则≤10 × ULN),总胆红素≤1.5 ×ULN,肌酐清除率≥60 ml/min。排除标准为:①既往曾接受过氟尿嘧啶类或铂类药物姑息化疗者;②患有除胃癌之外的其他原发肿瘤;③因个人体质或其他原因导致化疗不足2周期无法评价疗效的患者。将患者随机抽样法分为A、B两组,其中A组60例,B组51例。两组患者的基线特征比较,差异无统计学意义 (P> 0.05)。
1.2 治疗方法 A组给予替吉奥胶囊(商品名称:艾奕,江苏恒瑞医药股份有限公司))40 mg/m2,每日2次,口服,d1~14;奥沙利铂(商品名称:艾恒,江苏恒瑞医药股份有限公司)130 mg/m2,加入5%葡萄糖溶液500 ml中,持续静脉滴注2小时,d1,均为每21天一个周期。B组:卡培他滨片(商品名称:艾滨,江苏恒瑞医药股份有限公司),1000 mg/m2,每日2次,d1~14;奥沙利铂(商品名称:艾恒,江苏恒瑞医药股份有限公司)130 mg/m2,加入5%葡萄糖溶液500 ml中,持续静脉滴注2小时,d1,均为每21天一个周期。两组患者化疗前均常规使用5-羟色胺受体阻断剂进行止吐治疗,根据患者情况还可同时进行保肝及保护胃黏膜等治疗。化疗过程中给予维生素B1、B6等静脉滴注,以减轻奥沙利铂的神经毒性。化疗前后定期复查血常规及肝肾功等,根据CTCAE4.0评估患者不良反应,必要时给予粒细胞集落刺激因子等进行升白细胞治疗。每2个周期对患者的疗效进行评估,根据患者身体状况调整用药剂量,不良反应严重者终止该方案化疗。随访开始于2015年1月7日,截止于2016年1月31日,每3个月随访一次。
1.3 观察指标 ①以RECIST 1.1为标准进行疗效评价。将患者的疗效分为完全缓解(CR),部分缓解(PR),疾病稳定(SD)和疾病进展(PD)。客观有效率(ORR)= CR+PR,疾病控制率(DCR) =CR+PR+SD。对达到CR、PR和SD的病例于化疗后4周再次进行疗效确认,随访1年。②不良反应:贫血、乏力、腹泻、恶心呕吐、手足综合征、肝功能损伤、外周神经炎等。
1.4 统计学方法 采用SPSS 20.0 统计学软件进行处理。计数资料采用率表示,组间比较采用卡方检验,P< 0.05为差异有统计学意义。
2 结果
2.1 近期疗效比较 所有患者均接受了多于2周期的化疗,无失访患者。两组患者接受治疗的中位周期数分别为6周期和4周期。化疗2周期后,两组患者的ORR、DCR差异均无统计学意义(P> 0.05),见表1。
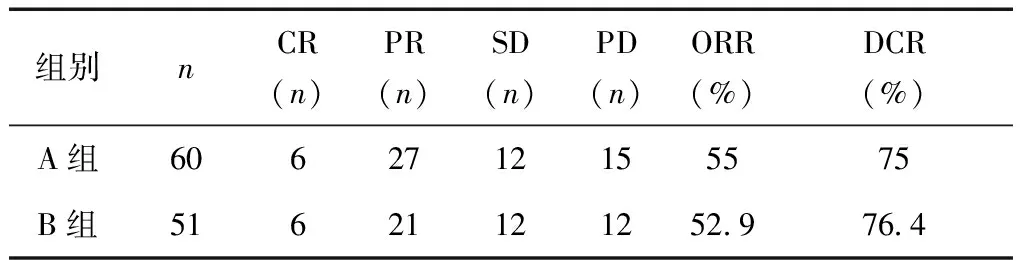
表1 两组患者治疗效果比较
2.2 不良反应比较 两组贫血、乏力、恶性呕吐、肝功能损伤、外周神经炎发生率比较,差异无统计学意义(P> 0.05)。A组腹泻与手足综合征发病率低于B组,差异有统计学意义(P< 0.05),见表2。
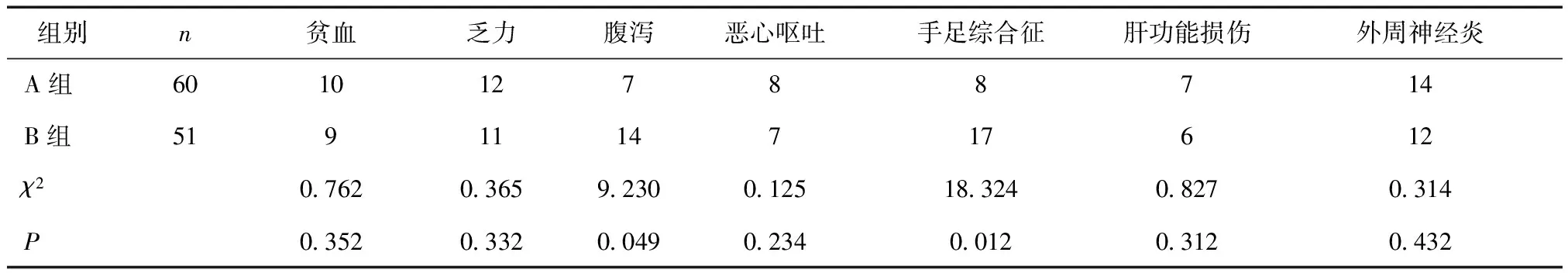
表2 两组患者不良反应发生率比较 (n)
3 讨论
多项临床研究结果显示[12,13],化疗可使晚期胃癌患者的总生存和无进展生存显著延长。对于术后病理分期为IB期伴淋巴结转移或术后病理分期为II期及以上者,推荐进行胃癌术后辅助化疗,化疗方案推荐氟尿嘧啶类药物和铂类药物的双药联合方案。无法手术治疗的晚期胃癌患者,推荐采用姑息化疗,常用方案有单药、双药联合或三药联合。如果患者身体状况较差、年龄较大,采用口服氟尿嘧啶类化疗药物。
本研究对两种口服氟尿嘧啶类药物联合奥沙利铂治疗胃癌方案的疗效及不良反应情况进行了比较。研究发现,经两种一线治疗方案治疗,两组患者的ORR、DCR差异均无统计学意义。几项Ⅱ期非随机对照试验和回顾性病例对照研究显示替吉奥或卡培他滨联合奥沙利铂方案治疗进展期胃癌均获得较好效果,替吉奥+奥沙利铂方案可延长患者总生存期(OS)至7.8~16.5个月,至疾病进展时间(TTP)为4.6~6.5个月,总有效率为53%~59%;卡培他滨联合奥沙利铂方案可使患者OS达到13.3~11.9个月,TTP为5.6~5.8个月,总有效率为42%~63%。2012年Bang等[12]进行了一项I期随机对照临床研究,首次对替吉奥和卡培他滨联合奥沙利铂治疗胃癌的效果进行了比较,结果表明,替吉奥+奥沙利铂组(SOX)的中位无进展生存期PFS为6.2个月,中位OS为12.4个月,卡培他滨+奥沙利铂组(CAPOX)的中位PFS为7.2个月,中位OS为13.3个月,两种方案间疗效差异无统计学意义。
本研究中两个治疗组中常见不良反应为恶心、呕吐、厌食、中性粒细胞减少、白细胞减少、周围神经毒性等,与多个临床研究结论基本一致[14~18],在卡培他滨+奥沙利铂组,腹泻与手足综合征发病率较高,提示在采用卡培他滨+奥沙利铂方案时,应对腹泻、手足综合征等可能不良反应进行关注,对患者做好用药教育。值得注意的是,目前替吉奥+奥沙利铂方案治疗胃癌没有标准推荐剂量[19,20]。且奥沙利铂的常见剂量限制性毒性为神经系统毒性,通常表现为外周感觉神经病变,如遇冷加重的肢体末端感觉障碍、感觉异常、痛性痉挛等。虽然在治疗间歇期症状会有所减轻,但治疗周期的持续增加会使症状不断加重。在该研究中患者接受的奥沙利铂治疗剂量为130 mg/m2,虽然两组患者均未出现严重神经系统毒性,但在临床用药过程中,应考虑到奥沙利铂累积剂量较大给患者带来的危险,监测患者的奥沙利铂累积剂量,并结合病情对用药剂量进行及时调整。在SPIRITS研究[21]中,对298例胃癌晚期患者随机给予替吉奥联合顺铂或替吉奥单药治疗,结果表明,在OS和PFS方面,替吉奥联合顺铂均显著优于替吉奥单药,分别为13个月vs.11个月,6个月vs.4个月。FLAGS试验[22]对晚期胃腺癌或胃食管腺癌一线治疗方案替吉奥联合顺铂(SP)与5-Fu联合顺铂(FP)的疗效进行了比较,结果显示两种方案疗效相似,中位OS为8.6个月,但SP方案具有更好的安全性;亚组分析显示,改善弥漫型胃或胃食管腺癌,结SP方案可使患者获得更长的总生存期。Kang等[23]进行临床试验发现,卡培他滨+顺铂(XP)的中位OS为10.5个月,优于FP方案的9.3个月。与上述3个研究[21~23]中应用SP方案和XP方案化疗的患者相比,替吉奥或卡培他滨联合奥沙利铂方案可使患者得到相似甚至更多的生存获益,总生存期更长,3~4级不良反应的发生率也略低。可认为替吉奥或卡培他滨联合奥沙利铂方案均可作为中晚期胃癌一线治疗方案,并且相比于联合顺铂的方案,更适合用于身体状况较差的患者。
本研究仍存在一些缺陷和不足,主要表现在以下几个方面:①随访时间短:无法了解其长期生存状况;②评估不全面:由于本研究只能根据病历记录及随访评价患者疗效,因此对于某些患者的疗效评估可能不够准确、全面。
综上所述,在中晚期胃癌治疗中,替吉奥+奥沙利铂与卡培他滨+奥沙利铂方案的ORR和DCR的差异均无统计学意义,作为中晚期胃癌一线治疗方案,两者疗效相当。替吉奥+奥沙利铂组腹泻和手足综合征发病率低于卡培他滨+奥沙利铂组,本研究为胃癌的治疗提供新的科学数据。
[1] Ichikawa D,Komatsu S,Kosuga T,et al.Clinicopathological characteristics of clinical early gastric cancer in the upper-third stomach[J].World J Gastroenterol,2015,21(45):12851-12856.
[2] Shimada H,Fukagawa T,Haga Y,et al.Does remnant gastric cancer really differ from primary gastric cancer? A systematic review of the literature by the Task Force of Japanese Gastric Cancer Association[J].Gastric Cancer,2016,19(2):339-349.
[3] Pandi NS,Suganya S,Rajendran S.In silico analysis of stomach lineage specific gene set expression pattern in gastric cancer[J].Biochem Biophys Res Commun,2013,439(4):539-546.
[4] Pizzi M,Saraggi D,Fassan M,et al.Secondary prevention of epidemic gastric cancer in the model of Helicobacter pylori-associated gastritis[J].Dig Dis,2014,32(3):265-274.
[5] Correa P.Gastric cancer:two epidemics[J].Dig Dis Sci,2011,56(5):1585-1586.
[6] Babaei M,Pourfarzi F,Yazdanbod A,et al.Gastric cancer in Ardabil,Iran--a review and update on cancer registry data[J].Asian Pac J Cancer Prev,2010,11(3):595-599.
[7] Wang L,Wang XA,Hao JQ,et al.Long-term outcomes after radical gastrectomy in gastric cancer patients with overt bleeding[J].World J Gastroenterol,2015,21(47):13316-133124.
[8] Gu Q,Zhang J,Hu H,et al.Clinical Significance of MiR-137 Expression in Patients with Gastric Cancer After Radical Gastrectomy[J].PLoS One,2015,10(11):e0142377.
[9] Hess LM,Michael D,Mytelka DS,et al.Chemotherapy treatment patterns,costs,and outcomes of patients with gastric cancer in the United States:a retrospective analysis of electronic medical record (EMR) and administrative claims data[J].Gastric Cancer,2016,19(2):607-615.
[10]Choi AH,Kim J,Chao J.Perioperative chemotherapy for resectable gastric cancer:MAGIC and beyond[J].World J Gastroenterol,2015,21(24):7343-7348.
[11]Siegel R,Naishadham D,Jemal A.Cancer statistics,2013[J].CA Cancer J Clin,2013,63(1):11-30.
[12]Bang YJ,Kim YW,Yang HK,et al.Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC):a phase 3 open-label,randomised controlled trial[J].Lancet,2012,379(9813):315- 321.
[13]Nakajima T,Nashimoto A,Kitamura M,et al.Adjuvant mitomycin and fluorouracil followed by oral uracil plus tegafur in serosa-negative gastric cancer:a randomised trial.Gastric Cancer Surgical Study Group[J].Lancet,1999,354(9175):273-277.
[14]刘福银,孟丽娟,王峻,等.替吉奥联合奥沙利铂与卡培他滨联合奥沙利铂一线治疗老年晚期胃癌的疗效分析[J].中国医药科学,2013,(13):14-17.
[15]Koizumi W,Takiuchi H,Yamada Y,et al.Phase II study of oxaliplatin plus tegafur as first-line treatment for advanced gastric cancer (G-SOX study)[J].Ann Oncol,2010,21(5):1001-1005.
[16]Oh SY,Kwon HC,Jeong SH,et al.A phase II study of tegafur and oxaliplatin (SOx) combination chemotherapy as a first-line therapy for patients with advanced gastric cancer[J].Invest New Drugs,2012,30(1):350-356.
[17]Park I,Lee JL,Ryu MH,et al.Phase I/II and pharmacokinetic study of tegafur and oxaliplatin in previously untreated advanced gastric cancer[J].Cancer Chemother Pharmacol,2010,65(3):473-480.
[18]樊翠珍,初玉平,戴红.卡培他滨联合奥沙利铂与替吉奥联合奥沙利铂治疗进展期胃癌的对比研究[J].临床肿瘤学杂志,2011,16(8):725-727.
[19]Tan BH,Brammer K,Randhawa N,et al.Sarcopenia is associated with toxicity in patients undergoing neo-adjuvant chemotherapy for oesophago-gastric cancer[J].Eur J Surg Oncol,2015,41(3):333-338.
[20]Chen Y,Lian G,Ou G,et al.Inverse association between Bmi-1 and RKIP affecting clinical outcome of gastric cancer and revealing the potential molecular mechanisms underlying tumor metastasis and chemotherapy resistance[J].Gastric Cancer,2016,19(2):392-402.
[21]Koizumi W,Narahara H,Hara T,et al.tegafur plus cisplatin versus tegafur alone for first-line treatment of advanced gastric cancer (SPIRITS trial):a phase III trial[J].Lancet Oncol,2008,9(3):215-221.
[22]Ajani JA,Rodriguez W,Bodoky G,et al.Multicenter phase III comparison of cisplatin/tegafur with cisplatin/infusional fluorouracil in advanced gastric or gastroesophageal adenocarcinoma study:the FLAGS trial[J].J Clin Oncol,2010,28(9):1547-1553.
[23]Kang YK,Kang WK,Shin DB,et al.Capecitabine/cisplatin versus 5-fluorouracil/cisplatin as first-line therapy in patients with advanced gastric cancer:a randomised phase III noninferiority trial[J].Ann Oncol,2009,20(4):666-673.
Comparison of curative effect of tegafur and capecitabine in combination of oxaliplatin as first-line therapy for advanced gastric carcinoma
ZHANGWei1,2,TANRui1
(1.DepartmentofStomatology,SouthwestJiaoTongUniversityofLifeScience,Chengdu610031,China; 2.DepartmentofStomatology,SichuanAcademyofMedicalScience&SichuanProvincialPeople’sHospital,Chengdu610072,China)
TANRui
Objective To compare the curative effect and adverse reaction of tegafur + oxaliplatin and capecitabine + oxaliplatin for patients with advanced gastric cancer (GC).Methods We selected 111 GC patients who were definitely diagnosed by pathological and cytological examination in Sichuan Provincial People’s Hospital between January 2014 and January 2015.They were randomly divided into group A (n= 60) and group B (n= 51).The group A was treated with tegafur plus oxaliplatin with 21 days-treatment cycle.In one cycle,the patients orally took tegafur capsule 40 mg/m2,2 times daily for d1~14 and orally took oxaliplatin 130 mg/m2,d1.The group B
capecitabine plus oxaliplatin with a treatment period of 21 days in which the patients orally took capecitabine tablets 1000 mg/m2,2 times daily for d1~14 and orally took oxaliplatin 130 mg/m2,d1.The efficacy and adverse reactions were evaluated after 2 cycles.Results There was no significant difference in the objective response rate (ORR) and disease control rate (DCR) between the two groups (P> 0.05).There was also no significant difference in the incidence of anemia,fatigue,nausea and vomiting,liver function injury and peripheral neuritis between the two groups (P> 0.05).However,the incidence of diarrhea and hand foot syndrome in the group A was lower than that in the group B (P< 0.05).Conclusion The safety of two types of treatment in patients with advanced gastric cancer is quite good.However,incidence of diarrhea and hand foot syndrome incidence in tegafur + oxaliplatin regimen is lower than that in capecitabine + oxaliplatin regimen.
Tegafur; Capecitabine; Oxaliplatin; Gastric cancer
谭 睿
R735.2;R453
A
1672-6170(2017)03-0031-04
2016-09-20;
2017-03-08)

