局部小肝癌患者的超声造影特征及病理分化程度分析
石颖秋 董瑾 胡洋扬 李咏梅 徐婷婷
·论著·
局部小肝癌患者的超声造影特征及病理分化程度分析
石颖秋 董瑾 胡洋扬 李咏梅 徐婷婷
目的 分析局部小肝癌患者的超声造影特征及病理分化程度。方法 回顾性分析2013年9月至2014年8月在医院得到手术病理证实的小肝癌患者70例。比较不同分化程度小肝癌造影剂开始增强、达峰及消退时间。比较不同分化程度和不同病理类型小肝癌造影剂动脉相、门脉相及延迟相增强模式。结果 不同分化程度小肝癌造影剂开始增强时间、达峰时间比较差异无统计学意义(P>0.05),高分化的造影剂消退时间长于中分化、低分化高分化和中分化、中分化和低分化、高分化和低分化造影剂消退时间,两两比较具有明显差异性(P<0.05)。不同分化程度小肝癌造影剂动脉相增强模式比较差异无统计学意义(P>0.05),而高分化和中分化、中分化和低分化、高分化和低分化小肝癌造影剂的门脉相和延迟相增强模式差异有统计学意义(P<0.05)。不同病理类型小肝癌造影剂动脉相增强模式比较差异无统计学意义(P>0.05),纤维硬化型和实体型、纤维硬化型和假腺管型、纤维硬化型梁索型、实体型和腺管型、实体型和梁索型、假腺管型和梁索型小肝癌造影剂门脉相、延迟相增强模式存在明显差异性(P<0.05)。 结论 对小肝癌患者的超声造影特征做出全面分析,有利于对肿瘤病理分化程度做出初步判断,在临床中制定治疗方案及做出预后判断时,也提供了影像学参考依据。
超声造影;小肝癌;病理分化程度
原发性肝癌在恶性肿瘤中是较为常见的一种,小肝癌是指临近癌结节直径总和<3 cm,或者单个结节直径≤3 cm的肝细胞癌[1]。对小肝癌的病理分化程度尽早做出确诊,有利于临床选择合理有效的临床治疗方法及对预后做出评估。但当前在诊断小肝癌中依然存在局限性,在确定病理分化程度中最为常见的方式有穿刺活检或手术切除,然而常常会因为操作不当致肿瘤转移,费用较高、创伤大等不足之处,其广泛应用性受到限制[2]。近年来,伴随着新一代超声造影剂在临床中得到逐步推广与运用,在实时动态观察微循环灌注及肿瘤血管时相变化中也成为了可能,也给早期确定小肝癌患者病理分化程度提供了新途径,然而依然欠缺循证依据,关于临床价值的争议依然尚存[3,4]。本研究通过回顾性分析小肝癌患者病理分化程度的不同在超声造影中的表现,以分析局部小肝癌患者的超声造影特征及病理分化程度。
1 资料与方法
1.1 一般资料 回顾性分析2013年9月至2014年8月在我院得到手术病理证实的小肝癌患者70例,并拟行超声造影,其中男58例,女12例;年龄34~78岁,平均年龄(52.43±2.44)岁。对70例患者给予超声造影检查,共查出83个病灶,3个病灶的有2例患者,2个病灶的患者有9例,1个病灶的患者有59例。肿瘤直径为12.43~29.54 mm,平均(18.43±2.54)mm。病理检查和超声造影检查的时间间隔<2周。所有患者的肿瘤均进行了手术切除。根据WHO分级标准把小肝癌分为高分化(Ⅰ级)、中分化(Ⅱ级)、低分化(Ⅲ级)三个程度;把小肝癌分为纤维硬化型、实体型、假腺管型、梁索型四种病理类型[5]。在70例小肝癌患者83个病灶中共有42个高分化,31个中分化,10个低分化;病理类型中4个位纤维硬化型,10个是实体型,15个为假腺管型,54个梁索型。
1.2 方法
1.2.1 使用东芝aplio500型多普勒彩色超声诊断仪,探头6C1,频率2~5 MHz,具有对比脉冲序列超声造影成像技术,由意大利Bracco公司提供SonoVue造影剂,在使用前使用0.9%氯化钠溶液5 ml溶解造影剂冻干粉,稀释后使用注射器抽取2.4 ml,并注入至肘静脉内,方式为团注形式。
1.2.2 在超声造影前用二维超声方式观察病灶的内部回声、边界、大小、形态、位置及数目。当机械指数<0.1的造影模式时,对病灶及周围组织时相变化及增强方式作出观察,每个病灶的观察时间保持在5 min。超声造影过程共分为3个时相[6],当注射造影剂5~30 s后属于动脉相,31~120 s属于门脉相,121~360 s属于延迟相,按照周围正常肝组织回声和病灶回声强度对结果进行比较,主要包括低增强、等增强、及高增强,当注射造影剂后,马上启动计时器,对造影剂开始增强的时间、达峰时间及消退时间进行记录。
1.2.3 若患者的病灶有2处时,需选取合适的断面对2处病灶进行同时观察。若难以同时观察,当检查完其中一处病灶10 min后,重新注射造影剂,对另一处病灶进行观察。需要2名具有经验的医师完成整个检查过程。
1.3 观察指标 比较不同分化程度小肝癌造影剂开始增强、达峰及消退时间。比较不同分化程度和不同病理类型小肝癌造影剂动脉相、门脉相及延迟相增强模式。

2 结果
2.1 不同分化程度小肝癌造影剂开始增强、达峰及消退时间比较 不同分化程度小肝癌超声造影剂开始增强时间、达峰时间比较差异无统计学意义(P>0.05),造影剂消退时间比较差异有统计学意义(P<0.05)。见表1。
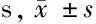

小肝癌分化程度开始增强时间达峰时间消退时间高分化(n=42)14.21±2.0229.21±2.4399.78±9.43中分化(n=31)13.98±2.0129.03±2.4172.43±7.15低分化(n=10)13.25±1.9828.97±2.3942.65±4.36χ2值0.00580.00507.5098P值0.99710.99750.0234
2.2 不同分化程度小肝癌造影剂动脉相、门脉相及延迟相增强模式比较 不同分化程度小肝癌造影剂动脉相增强模式比较差异无统计学意义(P>0.05),而高分化和中分化、中分化和低分化、高分化和低分化小肝癌造影剂的门脉相和延迟相增强模式存在明显的差异性(P<0.05)。见表2。

表2 不同分化程度小肝癌造影剂动脉相、门脉相及延迟相增强模式比较 例(%)
2.3 不同病理类型小肝癌造影剂动脉相、门脉相及延迟相增强模式比较 不同病理类型小肝癌造影剂动脉相增强模式比较无明显差异性(P>0.05),纤维硬化型和实体型、纤维硬化型和假腺管型、纤维硬化型梁索型、实体型和腺管型、实体型和梁索型、假腺管型和梁索型小肝癌造影剂门脉相、延迟相增强模式存在明显差异性(P<0.05)。见表3。
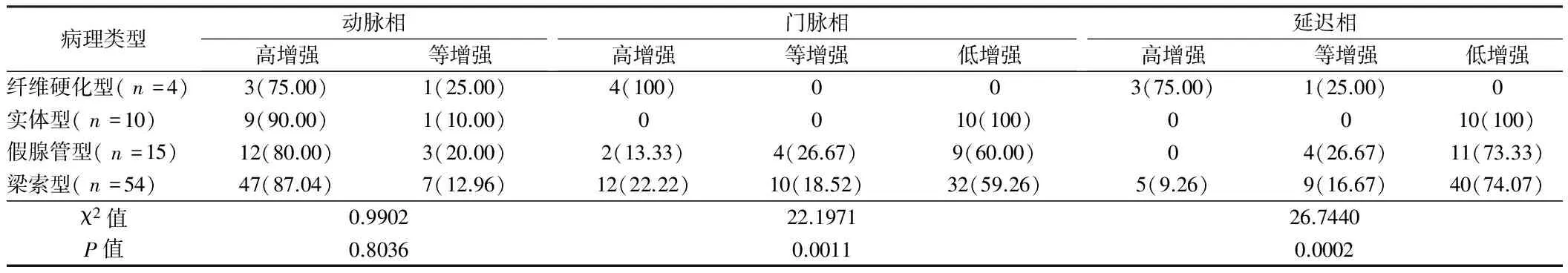
表3 不同病理类型小肝癌造影剂动脉相、门脉相及延迟相增强模式比较 例(%)
2.4 小肝癌梁索型病灶超声造影形式 实体型、假腺管型及梁索型小肝癌病灶造影剂主要表现为“快出”模式,73.33%(11/15)的假腺管型和74.07%(40/54)的梁索型小肝癌病灶主要表现为延迟相与门脉相等增强或者低增强及动脉相高增强的“快进快出”模式。见图1。
2.5 小肝癌纤维硬化型病灶超声造影形式 小肝癌纤维硬化型病灶造影剂表现为“快进慢出”形式。见图2。
3 讨论
肿瘤血液供应类型和超声造影的影像学特征存在着密切的关联性,大部分小肝癌患者的血液供应来自于肝动脉,也有少部分患者是门静脉与肝动脉双重供血或者单独的门静脉供血[7,8]。本研究结果显示,大部分小肝癌病灶在动脉相中呈现为高增强模式,在延迟相及门脉相中表现为等增强或者低增强模式,是一种典型的“高-低-低”或者“高-等-低”模式,其中动脉相中的高增强模式占到了全部病灶的85.54%(71/83),和相关文献[9]报道具有一致性。通过进一步研究得出,造影剂的消退时间随着分化程度的不同具有差异性,高分化肿瘤的造影剂消退时间明显长于低分化肿瘤,即肿瘤分化程度越高,则造影剂的消退时间会相对较长。究其原因主要是因为中、低分化小肝癌患者的供血主要来自肝动脉,造影剂能通过动脉作用快速流入肿瘤;但周围的肝实质供血途径主要来自门静脉,增强时间较晚;一旦肿瘤中的造影剂快速廓清后,正常肝实质强化,和肝组织相比,肿瘤内的回声强度相对较低[10,11]。相关研究显示,在门脉相中表现为等增强或高增强模式相对于低增强模式,病灶分化程度相对较好,在延迟相中表现为等增强模式的相对于低增强,其病灶分化程度相对较好[12]。本研究结果显示,肿瘤分化程度和小肝癌门脉相、延迟相的增强水平存在密切关联性。高分化肿瘤缺乏新生动脉血管、具有门静脉与肝动脉双重供血的病理特征、包膜不完整或未形成,也是导致动脉相回声时间较长增强的主要因素。除此之外,伴随着小肝癌分化程度的降低,延迟相与门脉相造影剂消退时间会缩短,还会减少低增强病灶个数,表明分化程度和小肝癌门静脉血供情况有着密切的关联性[13]。可见,在对造影剂开始增强时间及消退时间做出测量时,也相应地观察延迟相与门脉相回声特征做出观察,有利于判断小肝癌分化程度。
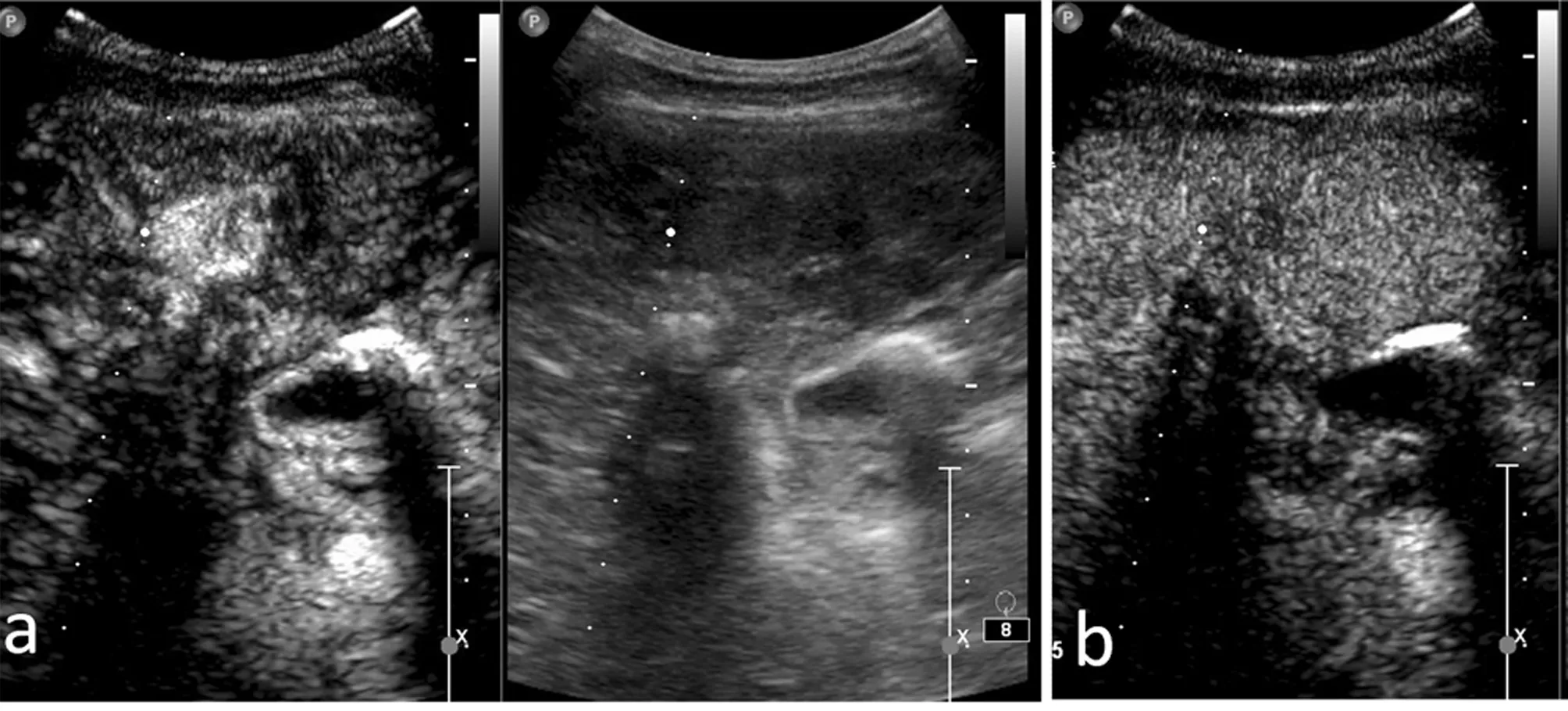

图1 小肝癌梁索型病灶超声造影形式
小肝癌病理类型包括纤维硬化型、实体型、假腺管型、梁索型[14]。小肝癌假腺管型的癌细胞表现为腺管状排列,小肝癌为梁索型的索状结构是根据厚薄不同的癌细胞紧密排列而形成,并且有些小肝癌梁索型为高分化的组织结构和正常肝组织类似[15]。本研究结果显示,小肝癌假腺管型和梁索型在超声造影中表现和高、中分化肿瘤差不多一致,大部分为“快进快出”模式,也有一些病灶动脉相表现为等增强改变,究其原因可能和小肝癌梁索型细胞较为成熟,并未扩张梁索间血窦,未增加血供;但小肝癌假腺管型的腺腔是因为假腺管中心部出现凝固反应而坏死,此部分具有较差的血供能力。小肝癌实体型癌细胞主要表现为紧密排列,低分化为主,为片状或巢状。本次研究中的小肝癌实体型为“高-低-低”造影剂增强模式。
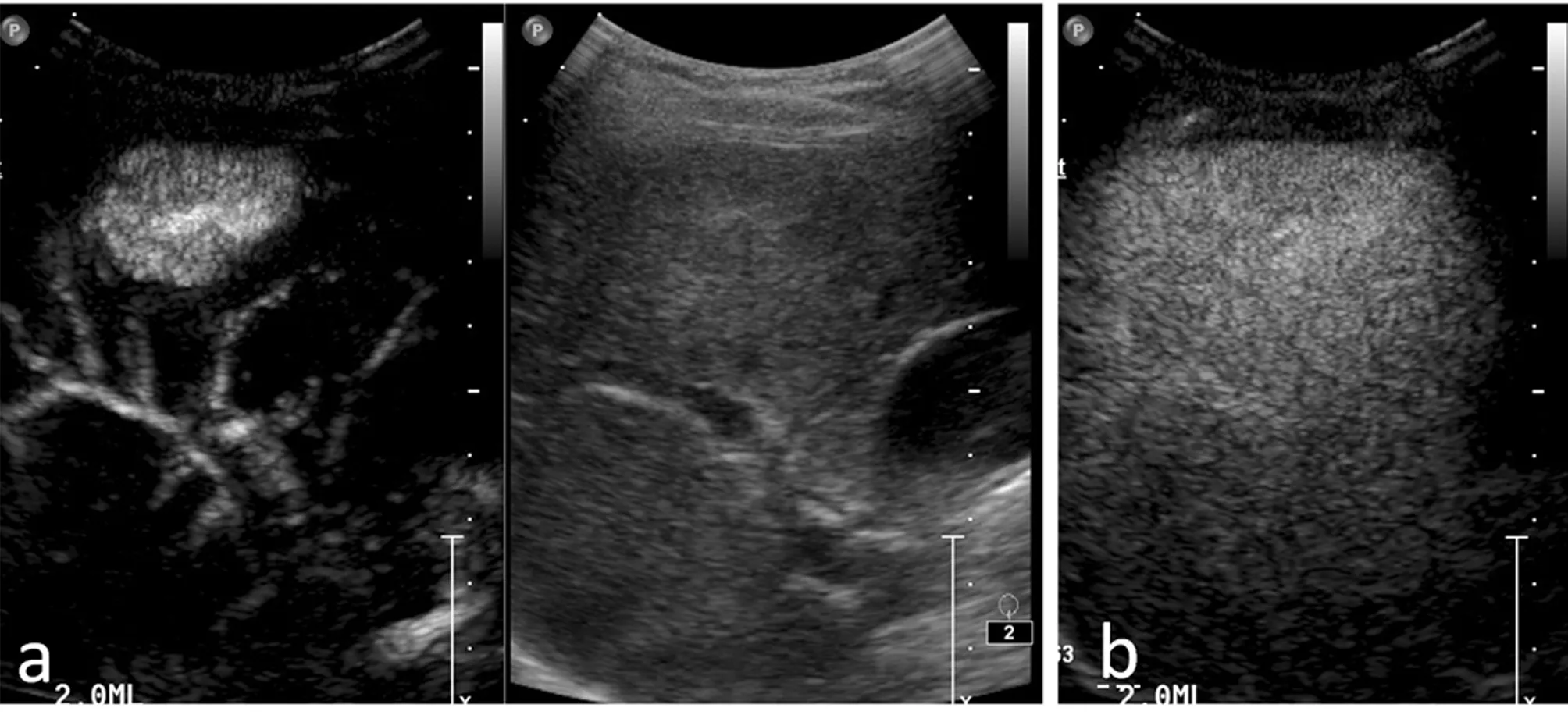
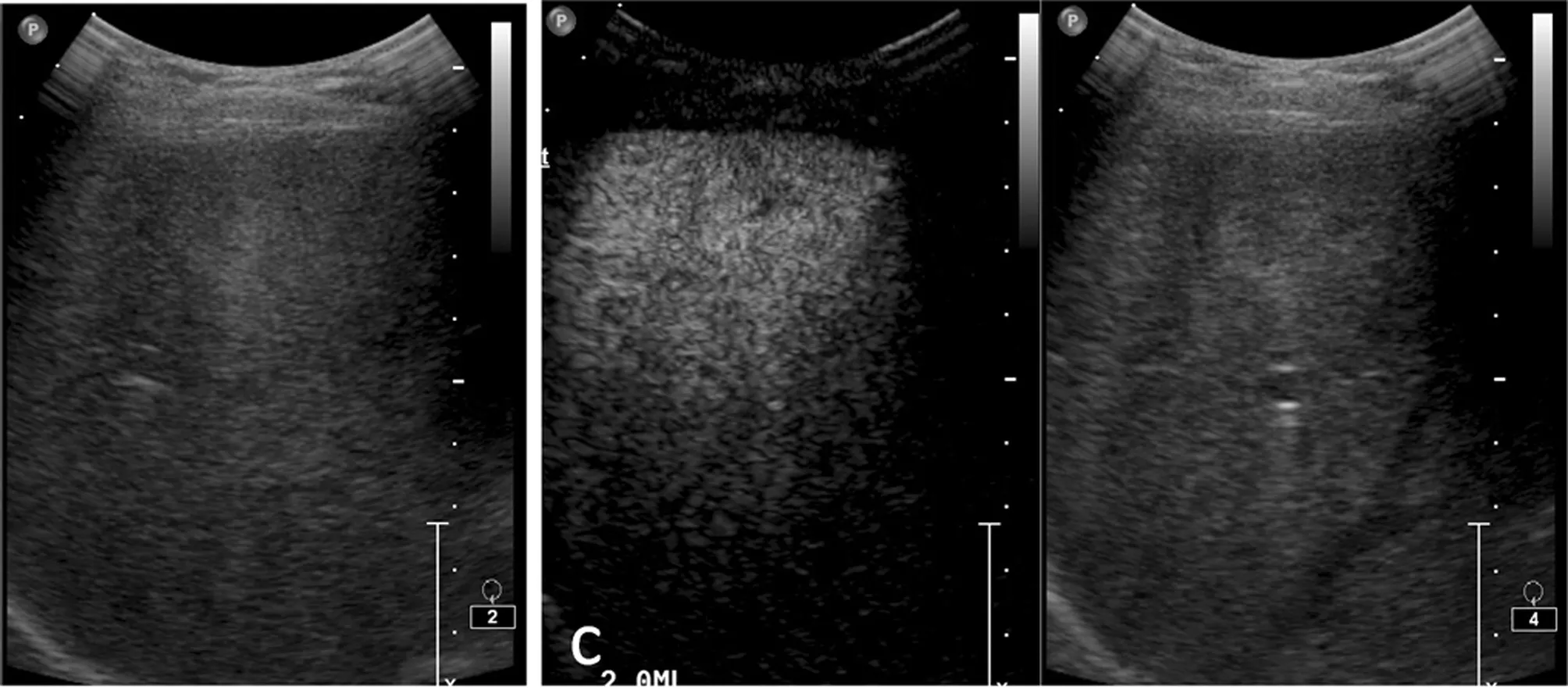
图2 小肝癌纤维硬化型病灶超声造影形式与病理图
综上所述,对小肝癌患者的超声造影特征做出全面分析,有利于对肿瘤病理分化程度做出初步判断,在临床中制定治疗方案及做出预后判断时,也提供了影像学参考依据。
1 郭娟,郭瑞强,陈金玲,等.对比增强超声造影对小肝癌诊断价值的Meta分析.武汉大学学报(医学版),2013,34:196-200.
2 黄婷,董常峰,罗婷婷,等.小肝癌与肝硬化再生结节的超声造影定量分析的临床价值.中国超声医学杂志,2012,41:28733-736.
3 陈红健,张一心,陈钟,等.超声造影配合射频消融与手术治疗原发性小肝癌的疗效比较.江苏医药,2012,38:36-39.
4 韦柳,李智贤,彭涛,等.超声造影鉴别诊断肝硬化背景下的小肝癌与不典型增生结节.中国医学影像技术,2012,28:1140-1143.
5 王凹弟,原发性肝癌超声造影特征与病理对照研究.中华保健医学杂志,2011,13:45-47.
6 朱世能.肝癌的病理与生物学特征∥汤钊猷,余业勤主编.原发性肝癌.上海:上海医科大学出版社,1999.132-154.
7 Palmieri VO,Santovito D,Marano G,et al.Contrast-enhanced ultrasound in the diagnosis of hepatocellular carcinoma.Radiol Med,2015,120:627-633.
8 Minami Y,Kudo M.Ultrasound fusion imaging of hepatocellular carcinoma:a review of current evidence.Dig Dis,2014,32:690-695.
9 Mishima M,Toh U,Iwakuma N,et al.Evaluation of contrast Sonazoid-enhanced ultrasonography for the detection of hepatic metastases in breast cancer.Breast Cancer,2016,23:231-241.
10 苏晓妹,朱亚杰,张涛,等.超声下微波治疗肝功能分级差的小肝癌.介入放射学杂志,2012,21:825-828.
11 Ronot M,Vilgrain V.Hepatocellular carcinoma:diagnostic criteria by imaging techniques.Best Pract Res Clin GastroenteroL,2014,28:795-812.
12 虞梅,梅琪,倪娟,等.肝超声造影监测和早期诊断微小肝癌的应用价值.中国癌症杂志,2014,32:203-207.
13 任卫平,俞明华,徐萍.超声造影判断小肝癌的分化程度和病理类型的价值.世界华人消化杂志,2015,32:907-913.
14 Forner A,Vilana R,Bianchi L,et al.Lack of arterial hypervascularity at contrast-enhanced ultrasound should not define the priority for diagnostic work-up of nodules 2 cm.J Hepatol,2015,62:150-155.
15 伍晓敏,周平,马树花,等.超声引导下激光消融治疗高危部位小肝癌.南方医科大学学报,2016,32:120-125.
10.3969/j.issn.1002-7386.2017.16.020
224001 江苏省盐城市第三人民医院超声诊断科
R 735.7
A
1002-7386(2017)16-2478-04
2017-03-11)

