局部晚期宫颈癌同步放化疗后的手术探讨
葛俊丽,孙季冬,吕小慧,李 佳,荆 如,陈必良*
(1空军军医大学西京医院妇产科,西安 710032;2空军军医大学西京医院神经外科;*通讯作者,E-mail:cblxjh@fmmu.edu.cn)
局部晚期宫颈癌同步放化疗后的手术探讨
葛俊丽1,孙季冬2,吕小慧1,李 佳1,荆 如1,陈必良1*
(1空军军医大学西京医院妇产科,西安 710032;2空军军医大学西京医院神经外科;*通讯作者,E-mail:cblxjh@fmmu.edu.cn)
目的 探讨局部晚期宫颈癌同步放化疗后的手术范围及临床疗效。 方法 回顾性分析2013-01~2016-12收治的444例ⅠB2-ⅡB期宫颈癌患者临床资料,根据术前是否接受同步放化疗分为两组:术前接受同步放化疗264例为术前同步放化疗(CCRT)+手术组,术前未接受任何治疗180例为手术组。分析比较两组患者的手术时间、术中出血量、术后住院天数、术中术后并发症、术后病理资料和术后补充放化疗及复发生存等情况。统计分析CCRT+手术组术前同步放化疗的临床疗效。 结果 两组患者在年龄、BMI和病理类型方面,差异无统计学意义(P>0.05)。两组的手术时间、术中出血量、术后住院时间、术后通气时间和术后尿管留置时间均无明显差异(P<0.05)。术前接受同步放化疗的总有效率(CR+PR)为92.6%,其中CR 9.1%,PR 87.1%。宫颈深间质浸润阳性率,淋巴结转移阳性率、淋巴脉管浸润阳性率,手术组均高于CCRT+手术组,差异均有统计学意义(P<0.05)。CCRT+手术组和手术组术后接受辅助治疗的患者分别为24例和162例,差异有统计学意义(P<0.05)。手术组患者术后辅助放疗后下肢水肿、放射性肠炎、放射性膀胱炎的发生率高于CCRT+手术组,差异均有统计学意义(P<0.05)。CCRT+手术组和手术组患者3年无进展生存率分别为91.7%和90.0%,3年总生存率分别为93.6%和92.8%,差异均无统计学意义(P>0.05)。 结论 局部晚期宫颈癌采用术前同步放化疗联合根治性手术的综合治疗方法可以取得较好的临床疗效,不增加术中及术后并发症的发生率。
术前同步放化疗; 局部晚期宫颈癌; 根治性手术
宫颈癌是严重威胁女性健康的恶性肿瘤,据世界流行病学调查显示,全球78%宫颈癌发生于发展中国家,其中我国约占世界新病例数的30%。宫颈癌在我国女性生殖系统恶性肿瘤中占首位,是妇女因癌症死亡的主要原因。由于缺乏定期妇科检查及宫颈癌筛查的普及率较低,多数患者发现时期别较晚(IB2-ⅡB)。国际妇产科联盟(FIGO)指出,局部晚期宫颈癌(locally advanced cervical cancer,LACC)广义上一般泛指ⅠB2-ⅣA期宫颈癌,而狭义的LACC一般是指ⅠB2-ⅡB期宫颈癌。LACC因肿瘤体积过大,范围较广,边缘部分超出常规宫颈癌有效放射治疗曲线范围,使放射剂量不足,治疗后复发率高,单纯放疗疗效不好,单纯手术疗效亦不理想。有研究表明[1],在后装放疗设备匮乏的国家,术前同步放化疗(concurrent chemoradiotherapy,CCRT)联合根治性子宫切除术与根治性放疗相比,可以提高9%-17%生存获益。2017年NCCN指南指出,对于LACC,CCRT后行根治性子宫切除术或直接根治性手术均可选择。但术前给予辅助治疗后再手术,还是直接手术及手术范围大小,目前尚无一致意见,探讨LACC最佳治疗模式一直是宫颈癌治疗研究中的热点。本研究通过分析术前CCRT联合机器人宫颈癌根治术治疗LACC临床疗效、预后及术后并发症等情况,探讨CCRT后的手术范围、优缺点及其并发症。
1 资料与方法
1.1 研究对象
回顾性分析2013-01~2016-12于第四军医大学西京医院妇产科收治的ⅠB2-ⅡB期宫颈癌患者病例资料。根据术前是否接受过CCRT,将其分为CCRT+手术组和手术组。CCRT+手术组为术前接受过CCRT的ⅠB2-ⅡB期宫颈癌患者;对照组为术前未接受过辅助治疗的ⅠB2-ⅡB期宫颈癌患者。纳入标准:①宫颈癌病理诊断明确,FIGO分期:ⅠB2-ⅡB期;②心肺功能良好,可耐受手术;③无肝肾等重要脏器疾病;④无其他手术禁忌证。排除标准:①有严重内科疾病者;②不能耐受人工气腹或头低臀高位者;③大的腹疝及膈疝;④急性弥漫性腹膜炎。
1.2 治疗
1.2.1 术前同步放化疗 CCRT+手术组:放射治疗采用盆腔外照射(external-beam radiation therapy,EBRT),我院采用三维适形放射治疗(three-dimensional conformal radiation therapy,3-DCRT),照射靶区包括病灶区域及宫旁组织和子宫骶骨韧带、骶前淋巴结及其他可能受累淋巴结和足够的阴道组织(至少在病灶外3 cm)。盆腔放射剂量为45-50 Gy(分割放疗时,常规每天1.8-2.0 Gy),25次;放疗期间同时配合化疗,方案为每周顺铂单药化疗1次(40 mg/m2,共4-6次)。
1.2.2 疗效评定 放化疗期间每周进行疗效评估。由两名副主任或以上医师行妇科检查并结合阴道B超或CT测量的子宫颈病灶大小的变化来评估,进行临床疗效的判定。近期疗效评定标准参照世界卫生组织(WHO)实体瘤治疗评价标准[2]:可见的肿瘤病变完全消失为完全缓解(complete remission,CR);肿瘤病灶的最大直径与最大垂直横径的乘积缩小达50%以上为部分缓解(partial remission,PR);肿瘤病灶的两径乘积缩小不足50%或增大不超过25%为稳定(stable disease,SD),肿瘤病灶的两径乘积增大25%以上或出现新病灶为进展(progressive disease,PD)。临床有效为完全缓解和部分缓解(CR+PR),临床无效为稳定和进展(SD+PD)。CCRT结束后,由两名副高以上妇产科医师进行评估,当患者完全缓解或肿瘤体积缩小时行机器人宫颈癌根治术。手术时间为CCRT后3-4周。
1.2.3 手术及观察指标 两组患者均行机器人腹腔镜下广泛全子宫切除+双附件切除+盆腔淋巴结清扫术±腹主动脉淋巴结切清扫术。术后病理如有任一高危因素如盆腔淋巴结阳性,宫旁浸润,淋巴管间隙浸润,手术切缘阳性或宫颈间质浸润深度≥0.5 cm,术后需进行辅助治疗。观察指标包括:年龄、体质量指数(body mass index, BMI)、临床分期、病理类型,术前CCRT后临床疗效;手术时间,术中出血量,术中是否输血,术中并发症及是否中转开腹;术后住院时间,术后病理结果,胃肠和膀胱功能恢复情况,术后并发症、辅助治疗及复发等随访情况。
1.2.4 术后随访 术后3个月内每月随访1次,随后每隔3个月进行随访1次,随访至1年,1年后每间隔6个月随访1次,如无复发则每年随访1次。随访方式以门诊随访和电话随访为主。随访内容包括:实验室检查(血细胞计数,肝肾功能检查),经阴道超声,腹部超声检查,浅表淋巴结检查,包括胸部CT,盆腔MRI。总生存期始于放疗第一天或手术完成之日至患者死亡或随访截止时间。无进展生存期起始于放疗第一天或手术完成之日到首次发现肿瘤复发时间。随访截止时间为:2017年5月31日。
1.3 统计学方法
采用SPSS17.0统计软件进行数据分析。正态分布的计量资料用均数±标准差表示,组间比较用t检验;非正态分布的计量资料用中位数、最大值和最小值表示,组间比较用Mann WhitneyU检验。计数资料用χ2检验。用Kaplan Meier法计算生存率,用Log rank检验比较两组间生存率。以P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料比较
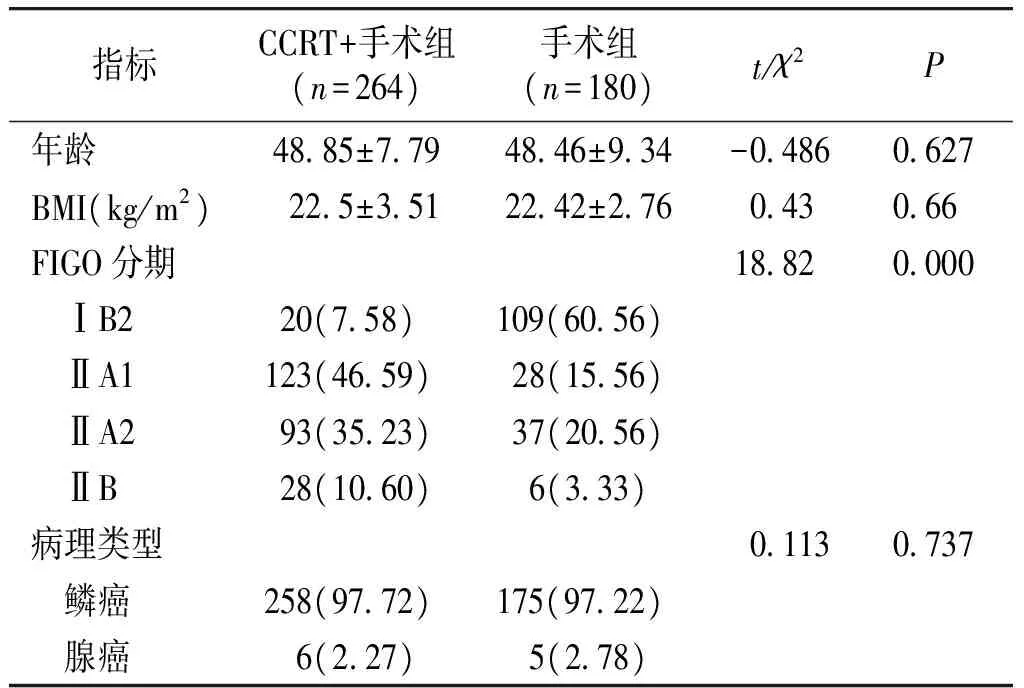
本研究共纳入了FIGO分期为ⅠB2-ⅡB期的宫颈癌患者444例,所有患者均接受了机器人腹腔镜下广泛全子宫切除+盆腔淋巴结清扫术±腹主动脉旁淋巴结清扫术。CCRT+手术组共有264例患者;手术组共有180例患者。两组在年龄、BMI、病理类型方面,差异无统计学意义(P>0.05,见表1)。两组在临床分期上存在差异:CCRT+手术组ⅡA-ⅡB期患者所占比例较手术组明显增加(P<0.001),CCRT+手术组患者临床分期较手术组晚。CCRT+手术组患者术前同步放化疗后24例(9.1%)患者CR,230例(87.1%)患者PR,10例(10.0%)患者SD,无PD患者,总有效率(CR+PR)为92.6%。
表1两组患者一般临床资料比较
Table1Comparisonofclinicaldataofpatientsbetweentwogroups
指标CCRT+手术组(n=264)手术组(n=180)t/χ2P年龄4885±7794846±934-04860627BMI(kg/m2) 225±3512242±276043066FIGO分期18820000 ⅠB220(758) 109(6056) ⅡA1123(4659) 28(1556) ⅡA293(3523)37(2056) ⅡB28(1060)6(333)病理类型01130737 鳞癌258(9772) 175(9722) 腺癌6(227)5(278)
2.2 两组患者术中、术后资料比较
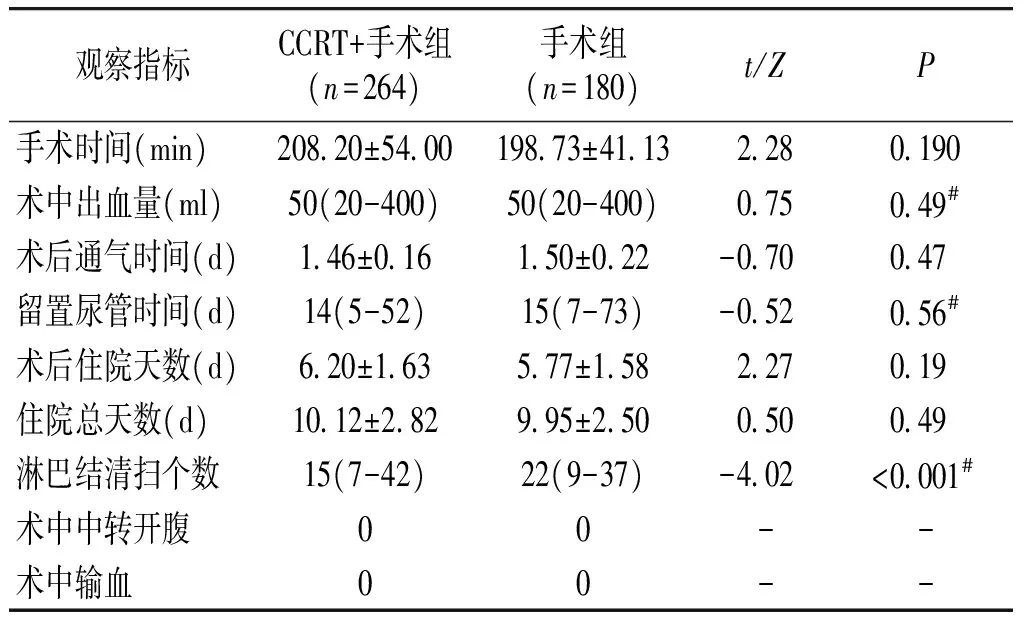
两组患者在手术时间、术中出血量、术后通气时间、留置尿管时间、术后住院天数、住院总天数方面,差异均无统计学意义(P>0.05)。手术组中清扫的淋巴结数多于CCRT+手术组,差异有统计学意义(P<0.05,见表2)。
表2两组患者术中、术后资料比较
Table2Comparisonofinteroperativeandpostoperativeclinicaldatabetweentwogroups
观察指标CCRT+手术组(n=264)手术组(n=180)t/ZP手术时间(min)20820±540019873±41132280190术中出血量(ml)50(20-400)50(20-400)075049#术后通气时间(d)146±016150±022-070047留置尿管时间(d)14(5-52)15(7-73)-052056#术后住院天数(d)620±163577±158227019住院总天数(d)1012±282995±250050049淋巴结清扫个数15(7-42)22(9-37)-402<0001#术中中转开腹00--术中输血00--
Mann-WhitneyU检验
2.3 术后病理检查及淋巴结转移情况
两组患者术后病理结果显示:手术组患者宫颈深间质浸润阳性率、宫旁浸润阳性率、脉管浸润阳性率及盆腔淋巴结阳性率均高于CCRT+手术组,差异均有统计学意义(P<0.05,见表3)。
表3两组患者术后病理资料比较例(%)
Table3Pathologicaldataofpatientsintwogroupscases(%)

因素CCRT+手术组(n=264)手术组(n=180)χ2P宫颈间质浸润深度20858 0000 <05cm227(860) 53(130) ≥05cm37(140)127(870)宫旁浸润25200000 阳性6(23)27(150) 阴性258(977) 153(850)脉管浸润36140000 阳性9(34)39(213) 阴性255(966) 141(787)盆腔淋巴结45430000 阳性30(113)51(283) 阴性234(887) 129(717)癌灶残留0 0 -手术切缘阳性0 0 -
P值为Fisher确切概率法所得
2.4 两组术后并发症及随访结果
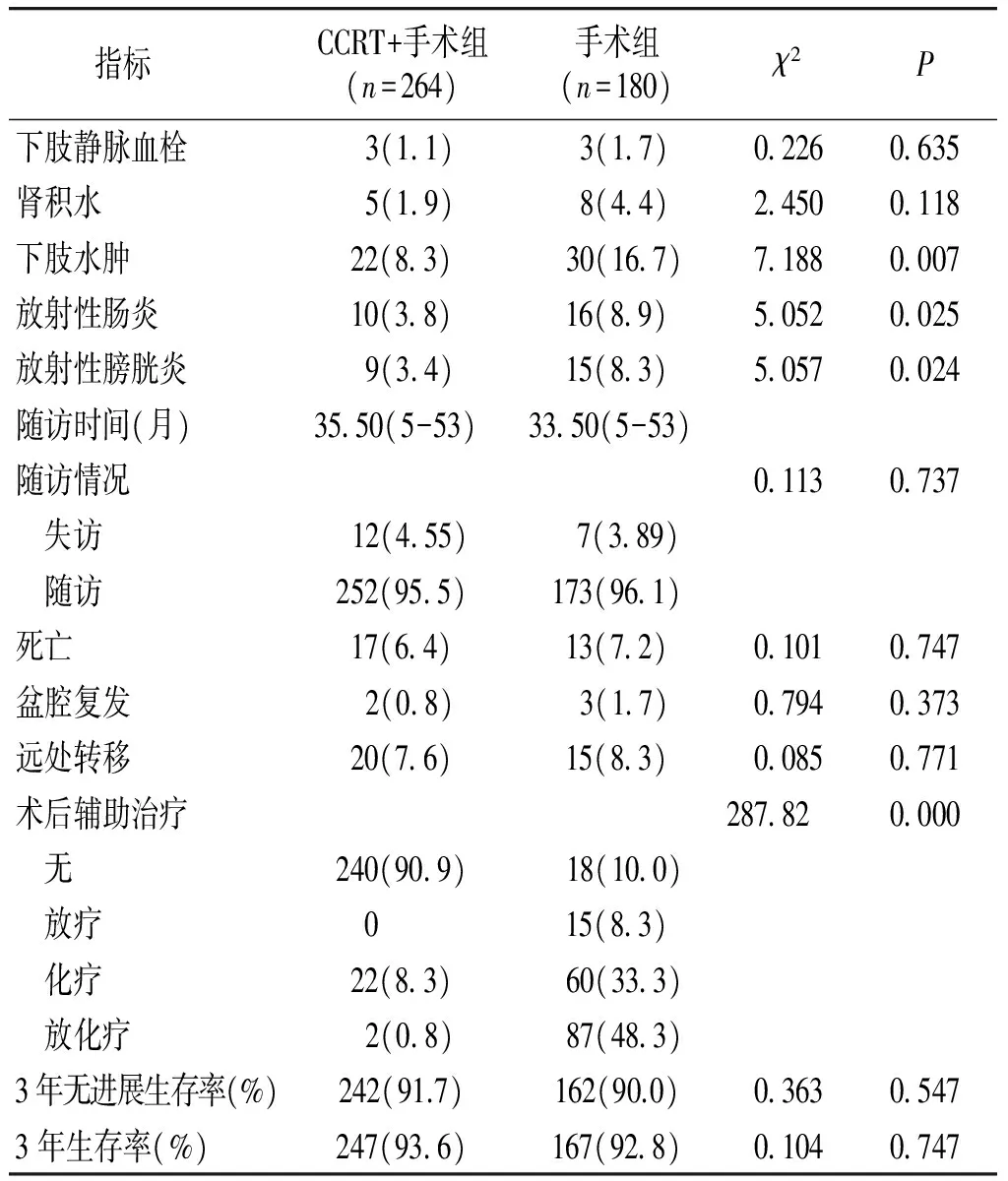
两组患者手术均顺利完成,术中均无临近器官损伤及大出血。手术组患者术后辅助放疗后下肢水肿、放射性肠炎、放射性膀胱炎的发生率高于CCRT+手术组,差异均有统计学意义(P<0.05)。随访两组患者盆腔复发及远处转移的发生率,手术组高于CCRT+手术组,但差异无统计学意义(P>0.05)。两组间术后需要辅助治疗患者所占比例比较,手术组明显高于CCRT+手术组,且差异有统计学意义(P<0.05,见表4)。两组患者3年生存率差异无统计学意义。
表4两组患者术后并发症及随访结果比较例(%)
Table4Comparisonofpostoperativecomplicationsandfollowupresultbetweentwogroupscases(%)
指标 CCRT+手术组(n=264)手术组(n=180)χ2P下肢静脉血栓 3(11) 3(17)02260635肾积水 5(19) 8(44)24500118下肢水肿22(83) 30(167)71880007放射性肠炎10(38)16(89)50520025放射性膀胱炎 9(34)15(83)50570024随访时间(月)3550(5-53) 3350(5-53) 随访情况01130737 失访 12(455) 7(389) 随访252(955)173(961)死亡17(64)13(72)01010747盆腔复发 2(08) 3(17)07940373远处转移20(76)15(83)00850771术后辅助治疗287820000 无240(909) 18(100) 放疗0 15(83) 化疗22(83) 60(333) 放化疗 2(08) 87(483)3年无进展生存率(%)242(91.7)162(90.0)036305473年生存率(%)247(936)167(928)01040747
3 讨论
局部晚期宫颈癌是一组具有高危因素的宫颈癌,因局部肿瘤体积过大,手术难度大,且常伴有肿瘤浸润生长和淋巴结转移,术后容易复发和转移,无瘤生存期短,5年生存率50%-70%,预后较差。同步放化疗是局部晚期宫颈癌的标准治疗方法,2017年NCCN指南指出,对于ⅠB2和ⅡA2期的局部晚期宫颈癌治疗可选择:①盆腔外照射+顺铂同期化疗+阴道近距离放疗,A点剂量≥85 Gy(1级证据)。②广泛性子宫切除术+盆腔淋巴结切除±主动脉旁淋巴结取样(2B级证据)。③盆腔外照射+顺铂同期化疗+近距离放疗,A点剂量75-80 Gy,放疗后行辅助性子宫切除术(3级证据)。以上3种推荐中,首选同期放化疗。对于ⅡB期及以上:在美国大多数晚期患者采用放化疗,通常不采用子宫切除术,但疗效并不十分理想。近年来国内外学者着眼于探索放疗、化疗联合手术治疗的综合治疗用于LACC患者的临床疗效[4]。
3.1 术前同步放化疗后手术范围的探讨
2017年NCCN指南对于ⅠB2和ⅡA2期治疗中指出,第3种选择同期放化疗之后进行辅助性子宫切除术还存在争议。该做法可减少盆腔复发、不改善总生存率,但却增加并发症,故只适用于放疗结束后仍有肿瘤残留,或病灶或子宫已超出近距离放疗所能涉及放疗区域的患者。但在腔内后装设备相对缺乏的中国,近2/3的宫颈癌患者无法接受近距离放射治疗[5]。因此近年来国内学者研究发现,术前CCRT联合根治性子宫切除术(或根治性手术)与根治性放疗相比,可使5年总生存率提高9%-17%[1,6,7]。国外学者Ferrandina等[8]近期探讨了术前CCRT联合宫颈癌根治术治疗LACC(ⅠB2-ⅣA期)的临床疗效,其结果表明术前CCRT后4周,行根治性手术治疗LACC是安全可行的。术后病理结果提示病理完全缓解率44.2%,27.6%患者存在微观残留病灶(≤3 mm),28.2%患者可见肉眼可见病灶,盆腔淋巴结阳性率达12.4%,腹主动脉淋巴结阳性率13.8%,只有13.8%患者需要术后辅助化疗。我们的研究数据表明术前CCRT联合机器人宫颈癌根治术和直接行宫颈癌根治术,两组患者在手术时间、术中出血量、术后通气时间、留置尿管时间、术后住院天数、住院总天数方面,差异均无统计学意义(P>0.05),表明术前CCRT联合根治性手术是安全可行的,这与国内外的研究结果一致[7,8]。CCRT+手术组患者术前同步放化疗后仅9.1%患者完全缓解,两组患者术后病理检查结果表明CCRT+手术组患者宫颈浸润深度、宫旁浸润、脉管浸润及盆腔淋巴结阳性率均低于手术组,且差异均有统计学意义(P<0.05),CCRT+手术组术后病理阳性率仍高达29.5%(78/264),盆腔淋巴结阳性率11.3%(30/264)。因此我们认为术前CCRT后行根治性手术是必要的,可减少盆腔淋巴结的转移,减少术后复发。这一结果与文献报道一致[9]。
3.2 放疗技术及微创技术的进步对手术的影响
放射治疗作为宫颈癌治疗的手段之一,在宫颈癌的治疗中占有重要地位。2017年NCCN指南明确指出EBRT以CT为基础的放疗计划辅以适形挡板是EBRT的标准方案。随着放疗技术不断进步,目前宫颈癌EBRT已由二维时代推向了三维时代(three-dimensional conformal radiotherapy,3DCRT)。调强适形放疗(intensity-modulated radiotherapy,IMRT)比3DCRT更好地解决了适形度、剂量均匀性问题,并且能更好地避开危及器官,因此能更好地杀灭肿瘤细胞、降低肿瘤周围正常组织放疗毒副反应,因此放疗技术的进步为LACC放化疗后行宫颈癌根治术提供了条件。术前CCRT的作用在于:①缩小肿瘤体积,增加手术切除率和减少手术风险及术后并发症;②控制局部病灶,提高放疗敏感性;③减少或消灭微转移,减少不良预后因素,降低复发风险,提高患者的生存率。本研究中264例患者术前接受CCRT,其中24例患者达到完全缓解,230例患者部分缓解,总有效率达(CR+PR)92.6%。结果表明术前CCRT缩小了LACC的病灶体积,降低了其手术期别,为手术创造了条件。同时本研究比较了两组患者术后病理检查结果,术前CCRT可降低手术后病理检查阳性率,减少或消灭微转移,这一结果与国内外研究结果一致[7,10]。
随着微创技术的飞速发展,达芬奇机器人手术系统是新一代的微创智能手术系统。其高清三维立体图像及10倍的放大系数可以更清楚直观地显示患者体腔内精细的解剖结构;其可转腕操作臂更有利于术者在狭小间进行分离解剖操作;其人手除颤系统和人工力学设计可以减少手术操作过程中非技术性失误发生的概率。机器人手术系统的这些优势更有利于手术医生对放化疗后的组织进行手术操作,为明显减少术中及术后并发症的发生创造了条件。
3.3 术前同步放化疗对术中、术后并发症及与预后的影响
国外有研究认为:术前同步放化疗会使宫旁浸润组织细胞水肿坏死,纤维化、盆腔内纤维增生、组织粘连,这不仅增加了手术难度,还有可能会增加治疗相关的并发症[11]。本研究中根治性手术时间选择在CCRT后3-4周,病灶周围组织水肿逐渐消退,纤维化尚未形成的时间段。由表1、2可知虽然术前CCRT+手术组患者临床分期较晚,但两组在手术时间、术中出血量、术中输血率、术后通气时间、术后留置尿管时间、术后住院时间方面均无明显差异(P>0.05)。本研究数据表明,术前CCRT并未增加手术时间、手术相关风险和患者术后恢复时间。两组患者术后并发症比较可知:术前CCRT+手术组下肢水肿,放射性肠炎及放射性膀胱炎的发生率低于手术组(P<0.05)。此外本研究还比较了两组患者术后辅助治疗情况,结果表明CCRT+手术组患者需要接受辅助治疗者24例,而手术组术后需要接受辅助治疗者162例,两组间差异有统计学意义(P<0.05)。因此手术组术后下肢水肿、放射性肠炎及放射性膀胱炎的发生率较高可能与其术后病理阳性率高,术后需要辅助放化疗患者比例较高,且术后淋巴结清扫完毕,血液回流障碍;患者抵抗力相对较差,对术后辅助治疗反应的副作用敏感有关。由以上可知,对于LACC患者,术前CCRT联合机器人宫颈癌根治术可使大部分患者免于接受术后的辅助放化疗,减少相关并发症的发生。
此外,在随访期内,两组患者盆腔肿瘤复发率,远处转移率及死亡率比较,CCRT+手术组略低,但差异无统计学意义(P>0.05)。两组患者无进展生存率及总生存率比较,差异无统计学意义(P>0.05)。考虑到随访时间尚短,该结果仍需大样本随机对照研究进一步来证实。
综上所述,针对我国的后装设备相对缺乏的具体情况,对于局部晚期宫颈癌可采用术前同步放化疗联合根治性手术的综合治疗方法同样可以取得较好的治疗效果,不增加手术及术后并发症的发生率。
[1] Chuang L, Kanis MJ, Miller B,etal. Treating locally advanced cervical cancer with concurrent chemoradiation without brachytherapy in low-resource countries[J].Am J Clin Oncol, 2016,39:92-97.
[2] Therasse P, Arbuck SG, Eisenhauer EA,etal. New guidelines to evaluate the response to treatment in solid tumors. European Organization for Research and Treatment of Cancer, National Cancer Institute of the United States, National Cancer Institute of Canada[J].J Natl Cancer Inst,2000,92(3):205-216.
[3] Cox JD, Stetz J, Pajak TF. Toxicity criteria of the Radiation Therapy Oncology Group(RTOG) and the European Organization for Research and Treatment of Carcinoma(EORTC)[J].Int J Radiat OncolBiol Phys,1995,31:1341-1346.
[4] Kokka F, Bryant A, Brockbank E,etal. Hysterectomy with radiotherapy or chemotherapy or both for women with locally advanced cervical cancer[J]. Cochrane Database Syst Rev, 2015, 4(4):CD010260.
[5] Wang L, Lu J, Yin W,etal. Perspectives on patient access to radiation oncology facilities and services in Mainland China[J].Semin Radiat Oncol,2017,27:164-168.
[6] Wei L, Wang N, Shi M,etal. Outcome observation of preoperative concurrent chemoradiotherapy/radiotherapy alone in 174 Chinese patients with local advanced cervical carcinoma[J].OncoTargets Ther,2013,6:67-74.
[7] Wang N, Li W, Li J,etal. Comparison of concurrent chemoradiotherapy followed by radical surgery and high-dose-rate intracavitary brachytherapy: a retrospective study of 240 patients with FIGO stage ⅡB cervical carcinoma[J].OncoTargets Ther,2014,7: 91-100.
[8] Ferrandina G, Ercoli A, Fagotti A,etal. Completion surgery after concomitant chemoradiation in locally advanced cervical cancer: a comprehensive analysis of pattern of postoperative complications[J].Ann Surg Oncol, 2014,21: 1692.
[9] 马芮,马佳佳,李娜,等.机器人宫颈癌根治术用于放化疗后局部晚期宫颈癌的可行性研究[J].中国妇幼健康研究,2017,28(5):498-501.
[10] Favero G, Pierobon J, Genta ML,etal. Laperoscopic extrafascial hysterectomy(completions surgery) after primary chemoradiation in patients with locally advanced cervical cancer: technical aspects and operative outcomes[J].Int J Gynecol Cancer,2014,24(3):608-614.
[11] Leguevaque P, Motton S, Delannes M,etal. Completion surgery or not after concurrent chemoradiotherapy for locally advanced cervical cancer[J].Eur J Obstet Gynecol Reprod Biol,2011,155(2):188-192.
Surgicaltreatmentoflocallyadvancedcervicalcancerafterconcurrentchemoradiotherapy
GE Junli1,SUN Jidong2,LÜ Xiaohui1,LI Jia1,JING Ru1,CHEN Biliang1*
(1DepartmentofObstetricsandGynecology,XijingHospital,AirForceMilitaryMedicalUniversity,Xi’an710032,China;2DepartmentofNeurosurgery,XijingHospital,AirForceMilitaryMedicalUniversity;*Correspondingauthor,E-mail:cblxjh@fmmu.edu.cn)
ObjectiveTo explore the surgical scope and clinical efficacy of locally advanced cervical cancer(LACC) after concurrent chemoradiotherapy(CCRT).MethodsThe clinical data of 444 LACC patients with stage ⅠB2-Ⅱ B receiving robot-assisted radical surgery from January 2013 to December 2016 were retrospectively analyzed. These patients were divided into two groups according to the treatment of preoperative CCRT. Totally 264 patients with preoperative CCRT were in CCRT+radical surgery group, while 180 patients without receiving any adjuvant therapy before operation were in radical surgery group. The operative time, intraoperative blood loss, postoperative hospital stay, intraoperative and postoperative complications, postoperative pathological data, postoperative adjuvant radiotherapy and chemotherapy, and recurrence were analyzed. The clinical efficacy of preoperative concurrent chemoradiotherapy in CCRT+radical surgery group was analyzed statistically.ResultsThere was no significant difference in age, BMI and pathological type between the two groups(P>0.05). There was no significant difference in operation time, intraoperative blood loss, postoperative hospital stay, postoperative ventilation time and postoperative catheter indwelling time between the two groups(P>0.05). The total effective rate of preoperative CCRT(CR+PR) was 92.6%, including 9.1% for CR and 87.1% for PR. The positive rates of deep cervical stromal invasion, lymph node metastasis and lymphatic vessel invasion were higher in radical surgery group than those in CCRT+radical surgery group(P<0.05).Totally 24 patients
adjuvant therapy in the CCRT+radical surgery group and 162 patients in radical surgery group, and there was statistically significant difference(P<0.05). The incidence of leg edema, radiation enteritis and radioactive cystitis was significantly higher in radical surgery group than that in CCRT+radical surgery group(P<0.05). The 3-year progression-free survival rate was 91.7% in CCRT+radical surgery group and 90.0% in radical surgery group, and there was no significant difference between the two groups(P>0.05).The 3-year overall survival rates were 93.6% and 92.8% in CCRT+radical surgery group and radical surgery group, respectively, and there was no significant difference between the two groups(P>0.05).ConclusionThe preoperative CCRT combined with radical surgery for LACC can achieve better clinical curative effect but not increase in the incidence of intraoperative and postoperative complications.
preoperative concurrent chemoradiotherapy; locally advanced cervical cancer; radical surgery
国家自然科学基金资助项目(81301921);西京医院临床高新技术基金资助项目(XJGX13LZ04)
葛俊丽,女,1984-05生,在读博士,主治医师,E-mail:gejunli1984@foxmail.com
2017-06-26
R737.33
A
1007-6611(2017)11-1177-06
10.13753/j.issn.1007-6611.2017.11.019

