枣仁安神胶囊的制备工艺和质量控制研究
卢海莎
(安顺职业技术学院,安顺,561000)
失眠症状主要因患者入睡或者睡眠时间短,造成机体产生了睡眠障碍、睡眠质量差而直接影响到第二天正常工作的一种主观体验[1],尤其对于老年性失眠症,在临床上较为常见[2]。中医药在治疗失眠症方面具有明显的优势,其中枣仁安神胶囊方剂由酸枣仁、丹参、五味子等中药组成,由镇静催眠、养血安神的作用,可用于失眠、多梦、惊悸等[3]。本次研究据参考文献[4-6]以酸枣仁皂苷A、B作为观察指标,采用正交试验法对提取工艺进行优化,同时采用薄层色谱法进行定性鉴别,以期获得最佳的提取工艺以及对其质量进行有效的控制。现将研究步骤报道如下。
1 仪器与试药
1.1 实验仪器 CS-9700型双波长薄层扫描仪器(由日本生产),微量注射器(北京市玻璃仪器生产厂),微量定量毛细管,高速离心机(美国雅培公司生产),索氏提取器(北京市玻璃仪器厂生产)。
1.2 实验试药 枣仁安神胶囊(市售,某制药公司,批号分别为170601、170602、170603),酸枣仁皂苷A、B对照品(中国药品生物制品检定所),酸枣仁、丹参、五味子(购于药材公司),高效硅胶G板(青岛海洋化工厂),其他试剂均为分析纯。
2 制备工艺优化方法
2.1 正交试验设计 采用正交试验对枣仁安神胶囊处方组成的中药材进行水提工艺优选,以提取次数(A)、加水量(B)和提取时间(C)作为试验因素,以出膏率和酸枣仁皂苷A、B含量作为考察指标,因素水平见表1。
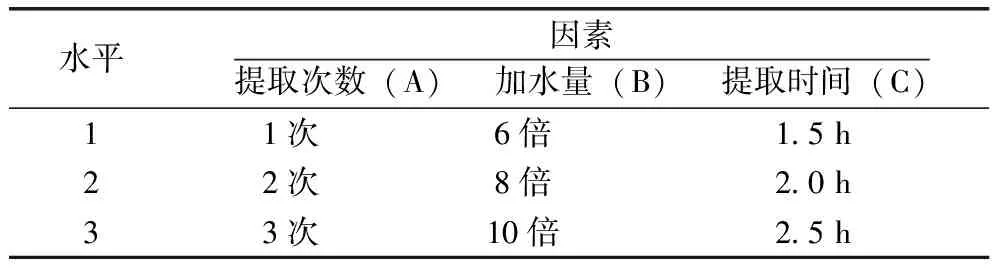
表1 提取因素水平表
2.2 最佳提取工艺的确定 采用L9(34)对正交试验结果进行优化,并进行极差和方差分析,结果见表2,表3。
由表2的结果可知,3个因素的极差大小为A>B>C,提取次数的影响最为显著,其他因素对制备工艺优化的影响较小。由表3的结果可知,因素A对本方的提取具有显著影响,因素B、C的影响性小,因此确定枣仁安神胶囊的最佳提取工艺为A3B2C2,即采用8倍量的水浸泡后提取3次,每次2.0 h时得到的出膏率最高,提取工艺最佳。
3 枣仁安神胶囊质量控制
3.1 薄层色谱鉴别
3.1.1 供试品即对照品溶液制备 取枣仁安神胶囊内容物4.0 g置于索氏提取器中,氯仿适量加热回流提取至颜色为无色,将药渣中的氯仿挥发后加入甲醇溶液提取至无色,滤过,滤液蒸干,残渣加水20 mL溶解后,饱和正丁醇提取3次,每次25 mL,合并正丁醇液,采用氨试液洗涤2次,每次10 mL,取正丁醇液,蒸干,残渣加入甲醇2 mL溶解后作为供试品溶液。另取不含酸枣仁皂苷A、B的阴性样品,按照上述方法提取,制成阴性样品。分别取酸枣仁皂苷A、B对照品,甲醇溶液定容后制备成2.0 mg/mL的对照品溶液。
3.1.2 鉴别 微量定量毛细管吸取酸枣仁皂苷A、B对照液2.0 μL,供试品和阴性样品溶液5.0 μL分别点于同一薄层色谱板上,取正丁醇-冰醋酸-水(15∶5∶20)上层,饱和30 min后,上行展开10 cm,取出薄层板将溶剂挥干后,2.0%香草醛硫酸乙醇溶液喷色后置于100 ℃烘箱中干燥2 min。观察供试品、对照品色谱对应位置出现形状相同的清晰深蓝色斑点,无拖尾,阴性对照色谱中无斑点。
3.2 含量测定
3.2.1 供试品和对照品的制备 取枣仁安神胶囊20粒,将内容物倒出混合后精密称定,置于索氏提取器中按照3.1.1的操作步骤,甲醇溶液定容至2 mL作为供试品溶液。精密称取酸枣仁皂苷A和B对照品适量,甲醇溶液定容制备成含酸枣仁皂苷A 2.30 mg/mL及酸枣仁皂苷B 1.90 mg/mL的对照品混合溶液。
3.2.2 扫描条件 单波长反射法扫描,测定波长选择620 nm。
3.2.3 线性关系考察 精密吸取酸枣仁皂苷A、B对照品溶液0.5、1.0、1.5、2.0、2.5 μL,在同一块薄层板上点样后,按照层析条件及扫描条件操作,测定各个斑点的面积积分值,以点样量X为横坐标,斑点面积积分分值Y为纵坐标,得到酸枣仁皂苷A回归方程:YA=0.958X+0.921×10-4(r=0.999 8),酸枣仁皂苷B的线性回归方程为:YB=0.652X+0.767×10-4(r=0.999 7),皂苷A点样量在2.1~7.1 μg,皂苷B点样量在2.0~6.0 μg范围内线性关系良好。
3.2.4 精密度和稳定性试验 精密吸取酸枣仁皂苷A、B对照品溶液,点于同一硅胶G薄层色谱板上,共6个点,展开,显色,扫描进行测定。结果RSD值分别为2.54%、1.52%。另准确吸取酸枣仁皂苷A、B对照品溶液,点于硅胶G薄层板,共6个点,展开显色后,每隔30 min进行扫描测定。结果表明,薄层色谱板显色后3.0 h内测定结果稳定,RSD值分别为1.52%、1.34%。
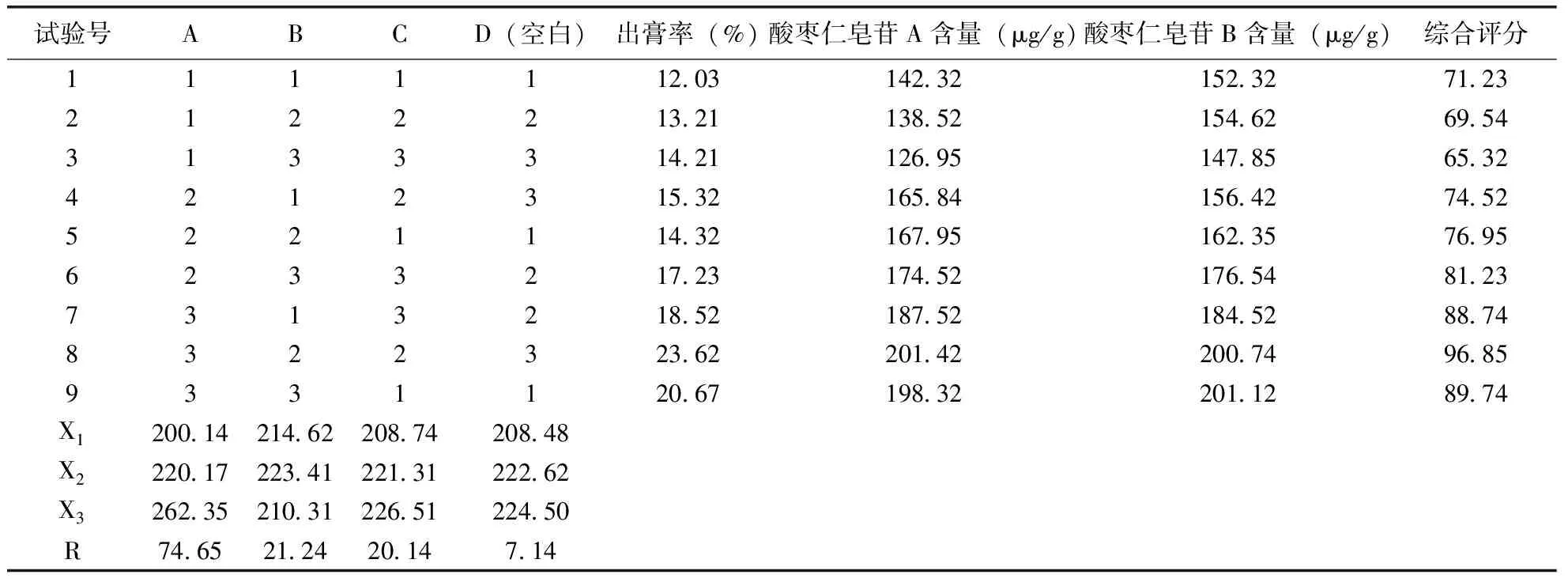
表2 L9(34)正交试验结果

表3 正交试验方差分析
注:F0.05(2,2)=19.0
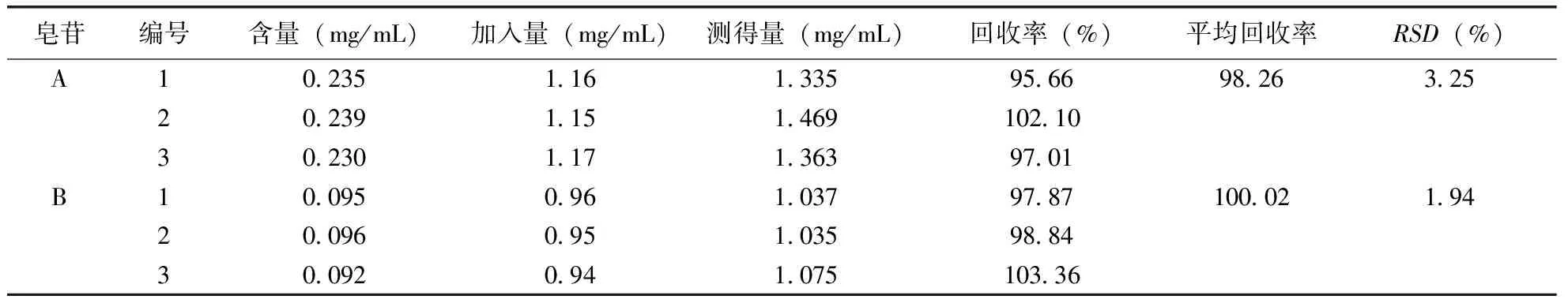
表4 酸枣仁皂苷A、B加样回收率试验(n=3)

表5 酸枣仁皂苷A、B的含量(n=3)
3.2.5 加样回收率测定 取已知含量的样品3份精密称定,加入一定量的酸枣仁皂苷A、B对照品溶液;再取枣仁安神胶囊20粒将内容物取出后混匀,按照供试品溶液的制备方式制备,取一定量的溶液点样,展开,显色,扫描并进行测定,计算加样回收率。见表4。
3.2.6 样品含量测定 精密吸取对照品溶液2.0 μL、3.0 μL,供试品溶液4.0 μL,分别交叉点于同一薄层色谱板上,用外标2点法测定供试品中酸枣仁皂苷A、B的含量。见表5。
4 小结
4.1 酸枣仁为枣仁安神胶囊中的君药,其中酸枣仁皂苷A、酸枣仁皂苷B为酸枣仁镇静催眠的主要有效成分[7],其性质为易溶于水。水煎煮法可以提取出较多的酸枣仁皂苷有效成分,同时也符合中医传统用药的习惯,溶剂价格便宜,容易得到[8],结合实际的生产规模、安全性等因素,实验中确定水为生产工艺的提取溶剂。
4.2 正交试验结果得到的最佳提取工艺为A3B2C2,处方药材重量与水为1∶8,提取3次,每次2.0 h时,浸膏率和酸枣仁皂苷A、B的提取率高,稳定性好,在保证临床治疗疗效的同时节约了提取成本。
4.3 研究过程中采用的正丁醇-冰醋酸-水(15∶5∶20)展开剂,样品分离效果好,显色后斑点清晰,无拖尾,形状完整。
4.4 对样品进行索氏提取时,参考文献资料有关乙醚[9]和氯仿[10]两种提取液方法的报道,优先氯仿作为提取液。结果表明,氯仿可以有效除去样品中的无效杂质和干扰因素;供试液在展开时,酸枣仁皂苷A、B可以彻底分离,能准确测量含量。
本试验对枣仁安神胶囊中的酸枣仁皂苷A、B进行鉴别研究,并对其进行含量控制,可以对枣仁安神胶囊进行有效的质量控制,为进一步的研究及优化提供参考依据。
[1]刘海燕,陈福忠.枣仁安神胶囊治疗老年性失眠症的疗效研究[J].世界最新医学信息文摘,2017,17(2):71-73.
[2]刘彦,许志刚.镇静安神药联合复方枣仁胶囊治疗失眠症的疗效观察[J].临床合理用药杂志,2012,6(1):77.
[3]王浴生,邓文龙.中药药理与应用[M].2版.北京:人民卫生出版社,2000:1208.
[4]张淑玲,沙玟,陆军,等.正交试验法优选和丹舒胶囊提取工艺[J].广东药学院学报,2010,26(1):41-44.
[5]马玲云,吴朝阳.RP-HPLC-ELSD法同时测定中药及保健食品中酸枣仁皂苷A和B含量的方法验证[J].临床合理用药,2012,7(3):37-38.
[6]徐晏.枣仁安神胶囊中丹参酮IIA的含量测定[J].中国医药指南,2013,11(18):100-103.
[7]彦冬华,郑捷,熊志玲,等.咳特灵颗粒提取工艺研究[J].中南药学,2012,3(4):224-226.
[8]王烈群,张欣.蒙药荜茇三味胶囊提取工艺的研究[J].中国民族医药杂志,2011,2(2):37-39.
[9]罗东,代青.速效枣仁安神胶囊中酸枣仁皂苷A、B的TLC鉴别和含量测定[J].华西药学杂志,2006,14(2):397-399.
[10]许英爱,金瑛.薄层扫描法测定逍遥丸中阿魏酸的含量[J].药学实践杂志,2012,19(4):166-167.

