伴微管状κ轻链沉积的增生性肾小球肾炎
梁丹丹 曾彩虹
病例摘要
病史62岁男性患者,因“水肿、发现蛋白尿1月余”于2017-07-04入院。
患者2017年5月无明显诱因出现双下肢凹陷性水肿,外院查尿蛋白+++,隐血+++,血清白蛋白(Alb)28 g/L,血清肌酐(SCr) 143.2 μmol/L,血红蛋白(Hb)84 g/L,予降压、降脂等治疗。6月26日复查SCr升至306.7 μmol/L。7月1日南京总医院国家肾脏疾病临床医学研究中心门诊查尿蛋白14.45 g/24h,尿红细胞计数345.1 个/μl,混合型,Alb 33.40 g/L,球蛋白23.8 g/L,SCr 216.6 μmol/L,Hb 90 g/L,为进一步检查及治疗入院。病程中患者无皮疹、关节痛、腹痛等,目前精神尚可,食欲、睡眠、大便及排尿正常。病程中无发热、骨痛、关节痛等。自起病来精神、体力、食欲、睡眠正常,近2年体重下降10余斤,大便正常,尿量偏少。
既往史高血压病史2年,血压最高220/120 mmHg,长期服用氨氯地平片降压,血压控制在150~160/80~90 mmHg。2017年3月双下肢皮肤散在丘疹,伴瘙痒,当地医院诊断“银屑病”。否认肝炎、结核、疟疾等传染病史。否认手术史、外伤史、输血史、食物、药物过敏史,预防接种史不详。
个人史、婚育史、家族史无特殊。
体格检查体温36.3℃,脉搏77次/min,呼吸16次/min,血压185/90 mmHg,体质量指数25.6 kg/m2;神清,查体合作。四肢皮肤色素沉着,散在红色丘疹、斑块,伴瘙痒。全身浅表淋巴结无肿大。咽不红,扁桃体不大。心、肺、腹部未见明显异常,双下肢无水肿。
实验室检查
血常规 Hb 84 g/L,RBC 2.99×1012/L,平均红细胞容积84.6 fL,平均红细胞血红蛋白量28.1 pg,平均血红蛋白浓度332 g/L,WBC 7.3×109/L,PLT 330×109/L,网织红细胞1.63%,红细胞碎片1%~2%。
尿液 尿蛋白定量9.69 g/24h,尿沉渣红细胞414.4 个/μl,混合型,白细胞计数11.6 个/μl;尿C3 70.17 mg/L(正常值≤2.76 mg/L),α2-巨球蛋白18.90 mg/L(正常值≤2.87 mg/L),RBP 23.4 mg/L(正常值<0.5 mg/L),Lyso<0.5 mg/L,NAG 51.6 U/(g·Cr)[正常值≤16.5 U/(g·Cr)],禁饮13h尿渗量 383.00 mOsm/(kg·H2O),尿本周蛋白阴性。
血生化 Alb 25.2 g/L,球蛋白17.2 g/L,尿素氮 28.20 mmol/L,SCr 183.9 μmol/L,尿酸418 μmol/L,谷丙转氨酶6 U/L,谷草转氨酶14 U/L,总胆固醇2.15 mmol/L,三酰甘油5.13 mmol/L,钠138.6 mmol/L,钾3.81 mmol/L,氯104.8 mmol/L,总二氧化碳23 mmol/L,钙1.83 mmol/L,磷1.39 mmol/L。
其他 IgG 10.3 g/L,IgA 1.34 g/L,IgM 1.14 g/L,IgE>1 000 IU/ml,ASO正常、RF阴性,补体C3 0.662 g/L,补体C4 0.290 g/L。抗中性粒细胞胞浆抗体谱阴性。血免疫固定电泳见κ型Ig G单克隆免疫球蛋白条带。血游离κ轻链165.6 mg/L,游离λ轻链49 mg/L,κ/λ 3.38(正常值0.37~3.1)。HbA1c 6.1%。传染病四项均阴性。直接、间接Coomb’s试验阴性。C3肾炎因子阴性、补体H因子正常,抗H因子抗体阴性。血免疫球蛋白冷沉淀(IgG、IgM)和VEGF 正常。肿瘤标志物基本正常,β2微球蛋白6.63 mg/L。甲状腺功能基本正常,甲状腺相关抗体阴性。
影像学检查双肾B超:左肾118 mm×43 mm×59 mm,右肾126 mm×57 mm×63 mm,双肾皮质回声稍增强。心电图示左心室高电压。心脏超声示左房左室大;左室舒张功能减低;轻度主动脉瓣反流;中度二尖瓣反流;极少量心包积液;室间隔厚度11 mm,左心室内径56 mm,左室后壁厚度11 mm,LVEF:54%。胸部CT:两肺上叶及右肺中叶小纤维硬结灶;右肺中叶小肺大泡,两肺下叶少许机化性炎症;右侧胸膜局限增厚,心包少量积液;主动脉及冠状动脉硬化。腹部CT:升结肠、横结肠肠壁稍增厚、周围渗出,炎性肠病可能;盆腔少量积液。X线: 头颅骨未见明显异常。骨盆未见明显异常。甲状腺:甲状腺右叶囊性结节,TI-RADS超声分级2级。双侧甲状腺低回声团块,TI-RADS超声分级3级,双侧甲状旁腺区声像图未见占位。骨髓穿刺术示浆细胞占3.5%。“右髂后上棘”骨髓活检示骨髓增生减低,伴少许散在浆样细胞。眼底检查示双眼高血压视网膜病变(黄斑区中心凹反光消失、视网膜出血、1级动脉硬化)。
肾活检
光镜 皮质、皮髓质肾组织各1条。34个肾小球中10个球性废弃,6个节段硬化。余肾小球正切体积增大,系膜区重度增宽,较多袢内皮细胞增殖伴单个核细胞、中性粒细胞浸润,部分袢腔堵塞、开放欠佳(图1A),数处袢腔内见“栓子”,节段外周袢与囊壁黏连,囊壁增厚、分层。PASM-Masson:肾小球系膜区、内皮下节段嗜复红物沉积,节段外周袢分层(图1B)。肾小管间质中度急性病变伴轻度慢性病变,多灶性肾小管上皮细胞扁平、刷状缘脱落,灶性肾小管萎缩、基膜增厚,间质灶性增宽、纤维化+,灶性炎细胞浸润,以单个核细胞为主。小叶间动脉内膜增厚,小动脉节段透明变性,偶见小动脉狭窄、闭锁。
免疫荧光 冰冻切片荧光染色示IgG、IgA、IgM、C3、C1q、Fibrin均阴性。石蜡切片复染IgG染色仍阴性。石蜡切片荧光染色κ 轻链局灶、节段分布于外周袢及袢腔。λ轻链阴性(图1C、D)。
电镜 未见肾小球。间质纤维化,散在炎细胞浸润。灶性肾小管萎缩、基膜增厚,未萎缩肾小管基膜外侧缘未见明确电子致密物分布。取石蜡组织重新处理,观察的肾小球见节段基膜内皮下微管状结构,部分呈平行排列,外径14~22 nm,内径4~8 nm(图1E、F)。
免疫组化 肾组织CD68染色示肾小球平均细胞数目为28.9个/球,间质平均细胞数目为264 个/mm2。
其他 肾组织刚果红染色未见阳性。皮肤脂肪组织刚果红染色未见阳性。免疫荧光染色示κ轻链、λ轻链均为阴性。
小结:伴微管状κ轻链沉积的增生性肾小球肾炎。
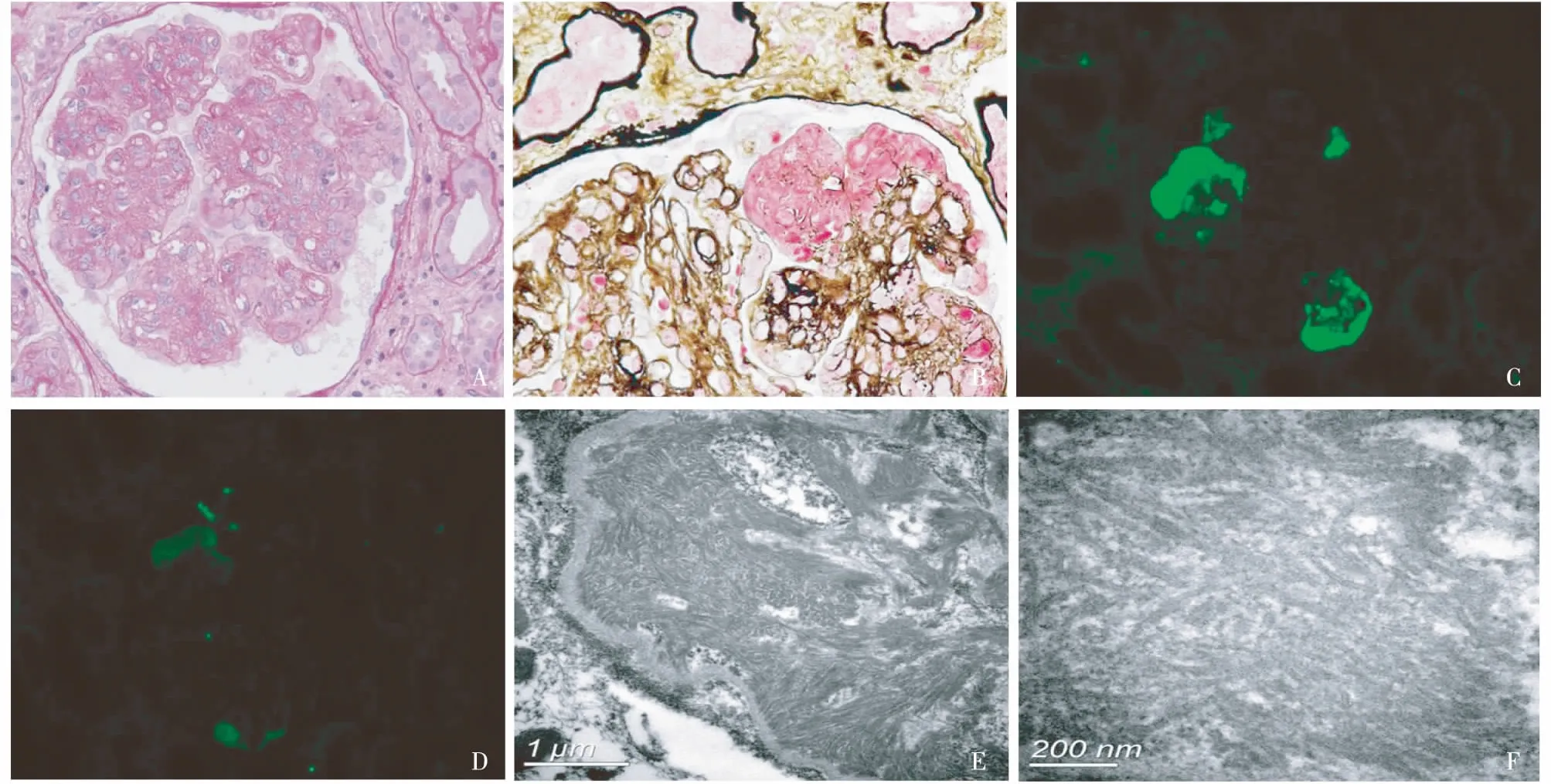
图1 A:肾小球呈膜增生性病变,系膜区中~重度增宽,系膜细胞增生,基质增多,袢腔内内皮细胞增殖伴单个核细胞浸润致袢腔堵塞(PAS,×400);B:肾小球毛细血管袢局灶内皮下、袢腔内见较多嗜复红物沉积,外周袢“双轨”形成(PASM-Masson,×600);C:κ 轻链局灶、节段分布于肾小球血管袢及袢腔,肾小管基膜阴性(IF,×400);D:肾小球、肾小管基膜λ轻链均阴性(IF,×400);E:肾小球毛细血管袢内皮下大量微管状结构,部分呈平行排列(EM);F:高倍镜下观察肾小球内皮下微管外径14~22 nm,内径4~8 nm(EM)
讨 论
该例患者中年男性,水肿起病,肾脏损害表现为大量蛋白尿、镜下血尿,伴低蛋白血症、急性肾损伤、高血压等,肾外表现有贫血、体重下降。血免疫固定电泳示κ型IgG单克隆免疫球蛋白条带。肾活检病理光镜示肾小球膜增生性病变,免疫荧光示肾小球κ 轻链局灶阳性,电镜下见肾小球毛细血管袢基膜内皮下微管状超微结构,部分呈平行排列,外径约14~22 nm,内径4~8 nm。
综合该患者临床和肾活检病理表现,血免疫固定电泳及肾组织染色均显示出单克隆免疫球蛋白特征,需重点考虑“具有肾脏意义的单克隆丙种球蛋白病(MGRS)”。MGRS是2012年由国际肾脏和单克隆免疫球蛋白血症研究组提出[1],是指由于单克隆免疫球蛋白或其片段直接或间接损伤肾脏而导致的一系列疾病,同时需除外多发性骨髓瘤、B细胞恶性增殖性疾病等,包括淀粉样变性、单克隆免疫球蛋白沉积病、Ⅰ型冷球蛋白血症肾损害、伴单克隆免疫球蛋白沉积的增生性肾小球肾炎等。同时该例患者血中存在M蛋白,尚需鉴别POEMS综合征,而从临床来看该患者无多发性周围神经病、脏器肿大、内分泌功能障碍和皮肤病变等,从病理来说,POEMS综合征肾脏损害主要表现为肾小球系膜溶解性病变,该患者不符,因此该病可排除。此外,该患者刚果红染色阴性可排除肾淀粉样变性,故需主要鉴别以下几种疾病。
单克隆免疫球蛋白沉积病该类疾病包括轻链沉积病、重链沉积病及轻重链沉积病,光镜常表现为肾小球结节样病变,肾小管基膜、包囊壁增厚及动脉管壁沉积物,电镜见泥沙状电子致密物沿肾小球基膜内侧缘、包囊壁外侧缘及肾小管基膜外侧缘分布,而该患者仅仅肾小球受累,且未见典型的电镜表现,因此不考虑此病。
冷球蛋白血症肾损害该病光镜亦可表现为肾小球膜增生性病变,通常伴袢腔内大量单核细胞浸润以及PAS阳性“栓子”。电镜可见电子致密物分布于肾小球毛细血管袢基膜内皮下及袢腔内,半数以上病例可见特殊超微结构,如微管、纤维丝、指纹样结构等,而该患者临床查血冷球蛋白阴性,不符合该诊断。
结晶贮积性组织细胞病此病是由单克隆免疫球蛋白导致的一种相对罕见的并发症。肾活检病理光镜表现为间质组织细胞胞质内含嗜伊红的轻链结晶包涵体,类似病变亦可同时出现在近端小管上皮细胞和足细胞[2-3]。此外,亦有文献报道仅肾小球受累的组织细胞病,即袢腔内较多CD68阳性细胞,其胞质内见轻链结晶或含轻链的吞噬性溶酶体[4-6]。该患者肾小球内虽见大量CD68阳性的组织细胞,且部分细胞胞质内亦见嗜复红颗粒,但电镜下观察这些沉积物主要分布于肾小球内皮下及袢腔内,与该病不符。
免疫管状肾小球病和纤维性肾小球肾炎这两种疾病光镜可表现为肾小球膜增生性病变,通常肾小管间质和血管无受累,免疫荧光示免疫球蛋白沉积,部分病例为单克隆免疫球蛋白,电镜下观察时高倍镜下可见特殊超微结构,纤维性肾小球肾炎表现为无分枝、无序排列的纤维丝结构,直径10~30 nm,与该病例不符;而免疫管状肾小球病则表现为直径30~60 nm的中空微管状结构,少数病例微管小至20 nm。目前尚无肾组织单一轻链致免疫管状病的报道,仅见1例单一κ轻链所致的免疫管状胃病的文献报道,HE染色显示胃黏膜固有层内大量无定形的嗜伊红物质沉积,电镜下观察为直径41~87 nm的微管状结构[7]。因此,与常见的免疫管状肾小球病有所不同,该例患者仅见单一轻链沉积,而非完整的免疫球蛋白,同时微管状结构直径略小,但该例是否为免疫管状肾小球病的少见类型尚需更多病例去进一步证实。
伴单克隆免疫球蛋白沉积的增生性肾小球肾炎该病光镜多表现为肾小球膜增生性病变或毛细血管内增生性病变,少数表现为肾小球系膜增生性病变或膜性病变[8-10]。免疫荧光染色常见肾小球单克隆免疫球蛋白沉积,其中重链以γ3最多见。电镜见肾小球毛细血管袢基膜内皮下、系膜区沉积物,伴或不伴上皮侧沉积物,多数情况下电子致密物无特殊超微结构,但亦有文献报道该类疾病可见特殊超微结构[11-12]。此外,亦有单克隆IgA或IgM相关的增生性肾小球肾炎的报道[13-14]。仅轻链沉积的增生性肾小球肾炎报道并不多,且均为个案报道。Yun等[15]报道1例46岁女性临床表现为肾病综合征伴SCr升高,肾活检光镜示肾小球毛细血管内增生性病变,免疫荧光示λ轻链2+,电镜示肾小球系膜区、内皮下散在电子致密物沉积,该患者临床给予硼替佐米联合地塞米松化疗3个周期,但治疗效果差,很快进展至终末期肾功能衰竭。Komatsuda等[16]报道1例39岁男性患者临床表现为尿检异常伴SCr升高,肾活检光镜示肾小球系膜增生性病变伴单克隆λ轻链沉积,电镜示肾小球系膜区颗粒状电子致密物沉积,未见特殊超微结构及特殊沉积方式,该患者临床给予血管紧张素Ⅱ受体拮抗剂治疗1年后随访肾功能稳定。Kurita等[17]报道1例55岁多发性骨髓瘤患者临床表现为少尿型急性肾功能不全,血免疫固定电泳见κ轻链单克隆条带,血冷球蛋白阴性,肾活检光镜提示轻链型管型肾病,同时肾小球袢腔内见大量κ轻链阳性的“栓子”,肾小球基膜内皮下亦见少量κ轻链沉积,该患者接受化疗和肾脏替代治疗2月后死亡。
该例患者肾脏病理表现为肾小球膜增生性病变伴κ轻链沉积,同时电镜下尚见沉积物为大量微管状结构,最终诊断为伴微管状κ轻链沉积的增生性肾小球肾炎。这些微管状结构是否确实由κ轻链所形成,可行免疫电镜进一步证实,遗憾的是该患者并未预留免疫电镜组织。本中心曾报道1例增生性肾小球肾炎伴单克隆IgA λ沉积,其沉积物亦呈微管状[18]。此外,目前已有单克隆免疫球蛋白血症相关的血栓性微血管病(TMA)病例报道[19],而TMA慢性期可表现为肾小球膜增生样改变,该患者实验室检查示外周血红细胞碎片阳性,这点支持TMA的可能性;但亦存在诸多疑问,比如尽管临床存在贫血,而网织红细胞水平并不高,并非溶血性贫血的典型表现,肾活检亦存在不能由TMA解释的病变,比如肾小球内大量增殖浸润的细胞及内皮下沉积物,因此该例不能简单归因为TMA。该患者光镜未见动脉TMA病变,电镜留取的组织未取到肾小球,未能全面观察是否存在肾小球内皮细胞病变,尚不能完全排除合并存在TMA可能。本例患者后续给予沙利度胺联合地塞米松化疗,随访8个月时复查SCr已降至89.3 μmol/L。
小结:仅轻链沉积的增生性肾小球肾炎相对罕见,光镜可表现为肾小球系膜增生性病变、毛细血管内增生性病变及膜增生性病变,电镜下可见颗粒状电子致密物,亦可见轻链形成微管状结构。单纯轻链与单克隆免疫球蛋白所致的增生性肾小球肾炎相比,其临床特征及预后是否存在差别尚待进一步研究。

