青皮药材的HPLC指纹图谱建立及聚类分析和主成分分析Δ
靳贝贝,裴香萍,梁惠珍
(山西中医药大学中药学院,山西 晋中 030619)
青皮,亦称青桔皮或青柑皮,为芸香科植物橘(Citrus reticulataBlanco)及其栽培变种的干燥幼果或未成熟果实的果皮[1]。除用橘类的未成熟果实的果皮外,其同属植物甜橙(C.sinensisOsbeck)、香橼(C.wilsoniiTanaka)以及茶枝柑(C.chachiensisHort)等柑类未成熟果实的果皮在有的地区亦作青皮使用。青皮为常用中药,味苦、辛,性微温,具有破气行痰、消痞除满、理气健脾、燥湿化痰等功效。现代药理研究表明,青皮具有较好的升高血压、抗休克等作用[2],具有抗病毒、抗肿瘤及抗氧化等活性[3],还可用于松弛胃肠和子宫平滑肌、促进消化液分泌、利胆、祛痰平喘[4-6]等。挥发油类、黄酮类等是青皮的主要活性成分[7-8]。目前,2015年版《中国药典》(一部)采用单一成分橙皮苷来控制青皮药材的质量[1]。本研究通过检测10批青皮药材样品,建立其高效液相色谱(HPLC)指纹图谱,并结合聚类分析、主成分分析对其质量进行评价,旨在为青皮药材的质量控制提供参考。
1 材料
1.1 仪器
e2695型HPLC仪,包括四元泵洗脱系统、自动进样系统、柱温箱及光电二极管矩阵检测器(美国Waters公司);SX-120DT型超声波清洗机(上海圣训仪器有限公司);AB-135型十万分之一电子天平(瑞士Mettler-Toledo公司);FA/JA1004型万分之一电子天平(上海精密科学仪器有限公司);HH-2型数显恒温水浴锅(金坛市杰瑞尔电器有限公司);FW100型高速万能粉碎机(北京市永光明医疗仪器有限公司)。
1.2 试剂
橙皮苷对照品(中国食品药品检定研究院,批号:110721-201617,纯度:96.1%);甲醇、乙腈为色谱纯,其他试剂均为分析纯,水为娃哈哈纯净水。
1.3 药材
共收集青皮药材样品10批,经山西中医药大学中药学院裴香萍副教授鉴定为芸香科植物橘(C.reticulataBlanco)的干燥幼果或未成熟果实的果皮。青皮药材样品来源见表1。
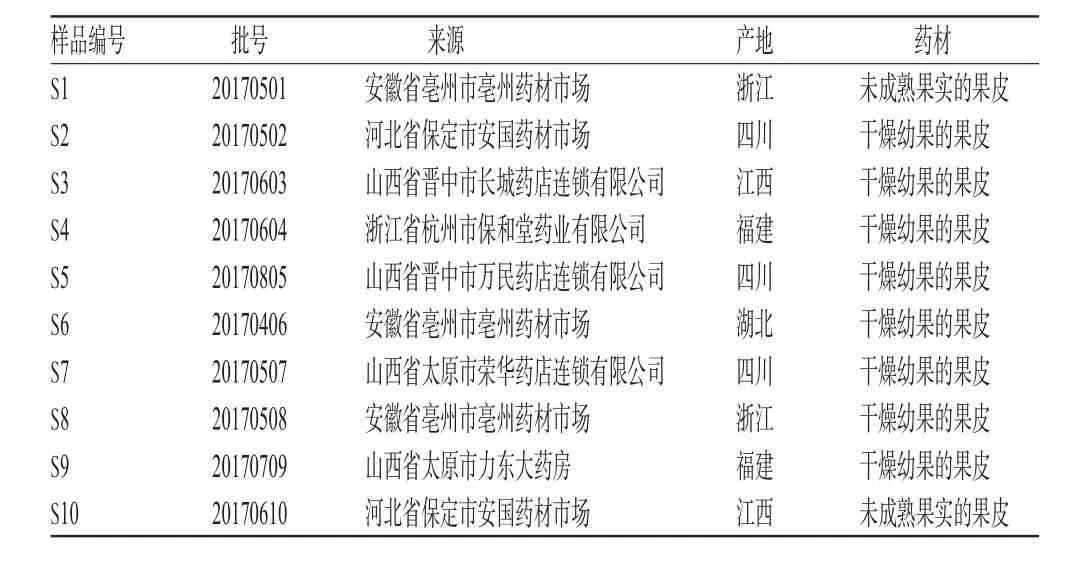
表1 青皮药材样品来源Tab 1 Origins of C.reticulata
2 方法与结果
2.1 色谱条件
色谱柱:XSelect®HSS T3-C18(150 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.5%醋酸溶液(B),梯度洗脱(洗脱程序见表2);流速:1.0 mL/min;检测波长:360 nm;柱温:25 ℃;进样量:10 μL。

表2 梯度洗脱程序Tab 2 Gradient elution procedure
2.2 溶液的制备
2.2.1 对照品溶液 精密称取橙皮苷对照品5.50 mg,置于50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,得质量浓度为0.11 mg/mL的对照品溶液。
2.2.2 供试品溶液 精密称取药材样品粉末约0.2 g,置于50 mL量瓶中,加甲醇30 mL,超声(功率:250 W,频率:33 kHz)处理30 min,放冷,加甲醇稀释至刻度,摇匀,滤过;取续滤液2 mL,置于5 mL量瓶中,加甲醇稀释至刻度,摇匀;精密量取1 mL,置于10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.3 方法学考察
2.3.1 精密度试验 取“2.2.2”项下供试品溶液(批号:20170508)适量,按“2.1”项下色谱条件连续进样测定6次,以橙皮苷峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对保留时间的RSD均小于0.08%,相对峰面积的RSD均小于1.22%(n=6),表明本方法精密度良好。
2.3.2 稳定性试验 取“2.2.2”项下供试品溶液(批号:20170508)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,以橙皮苷峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对保留时间的RSD均小于0.50%,相对峰面积的RSD均小于0.79%(n=6),表明供试品溶液于室温下放置24 h内基本稳定。
2.3.3 重复性试验 取药材样品粉末(批号:20170508)0.2 g,共6份,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,以橙皮苷峰的保留时间和峰面积为参照,记录各共有峰的相对保留时间和相对峰面积。结果,11个共有峰相对保留时间的RSD均小于0.50%,相对峰面积的RSD均小于2.97%(n=6),表明本方法重复性良好。
2.4 HPLC指纹图谱的生成与相似度评价、共有峰相关分析
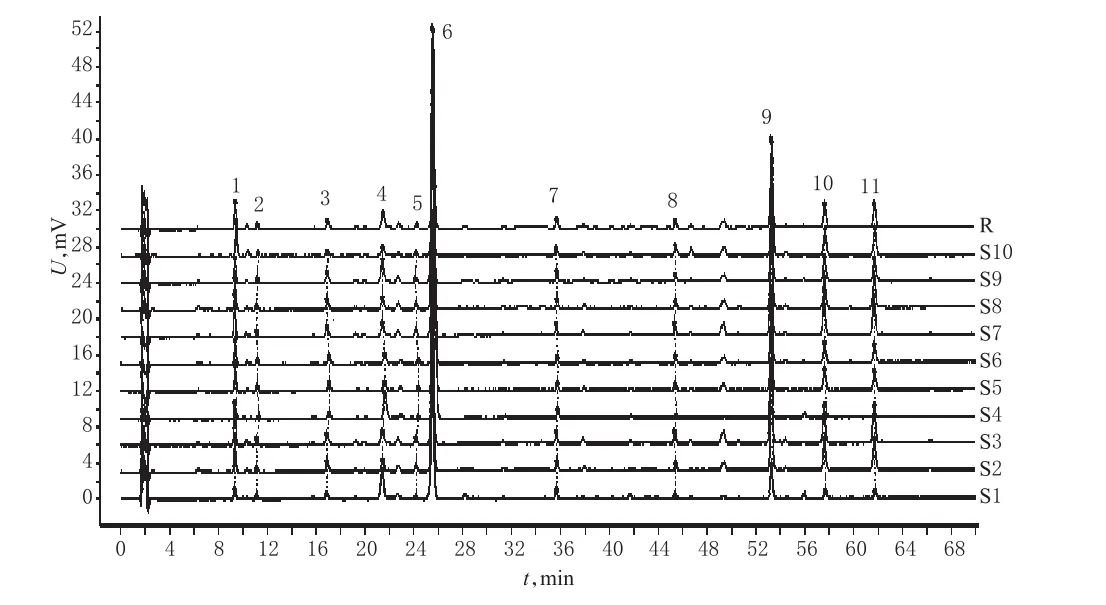
图1 10批药材样品的HPLC叠加指纹图谱Fig 1 HPLC superimposed fingerprint of 10 batches of medicinal materials
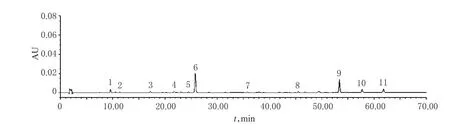
图2 药材样品的HPLC对照指纹图谱Fig 2 HPLC control fingerprint of medicinal materials
2.4.1 HPLC指纹图谱的生成 分别取10批药材样品粉末0.2 g,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,采用《中药色谱指纹图谱相似度评价系统(2012版)》对10批药材样品的HPLC图谱进行分析,得HPLC指纹图谱,详见图1、图2。
2.4.2 相似度评价 采用《中药色谱指纹图谱相似度评价系统(2012版)》,以药材样品的HPLC对照指纹图谱为对照,进行整体相似度评价。结果显示,10批药材样品的相似度为0.919~1.000,表明各批药材样品的化学成分一致性较好,均含有11个成分,但各成分含量存在差异,详见表3。

表3 10批药材样品相似度Tab 3 Similarity of 10 batches of medicinal materials
2.4.3 共有峰的指认及相关分析 10批药材样品有11个共有峰,通过与对照品HPLC图谱(详见图3)比对,指认保留时间为25.588 min的6号峰为橙皮苷峰。其分离度良好,保留时间合适,故以其为参照峰,计算其他峰相对于该峰的相对保留时间和相对峰面积,详见表4、表5。

图3 对照品HPLC图谱Fig 3 HPLC chromatogram of substance control
2.5 聚类分析
以10批药材样品的11个共有峰的相对峰面积为原始数据,采用SPSS 17.0软件,以系统聚类法结合欧氏距离(d)为测度进行分析,结果见图4。由图4可知,d=20时,10批药材样品可聚为2类,S4为一类,其余聚为一类;d=5时,后一类又可聚为2类,S1、S10聚为一类,S2、S3、S5~S9聚为一类。
2.6 主成分分析
2.6.1 主成分因子特征值、方差贡献率分析 采用SPSS 17.0软件进行主成分因子分析,其特征值和方差贡献率见表6。由表6可知,以特征值>1为标准,得到前2个主成分因子的特征值分别为8.237、1.935,方差贡献率分别为75.206%、17.591%,累积方差贡献率为92.797%>85%。故采用前2个主成分因子为指标对10批药材样品进行评价,详见表7。由表7可知,主成分因子1可反映成分1、2、3、5、6、8、9、10、11的信息,主成分因子2可反映成分4、6、7的信息。
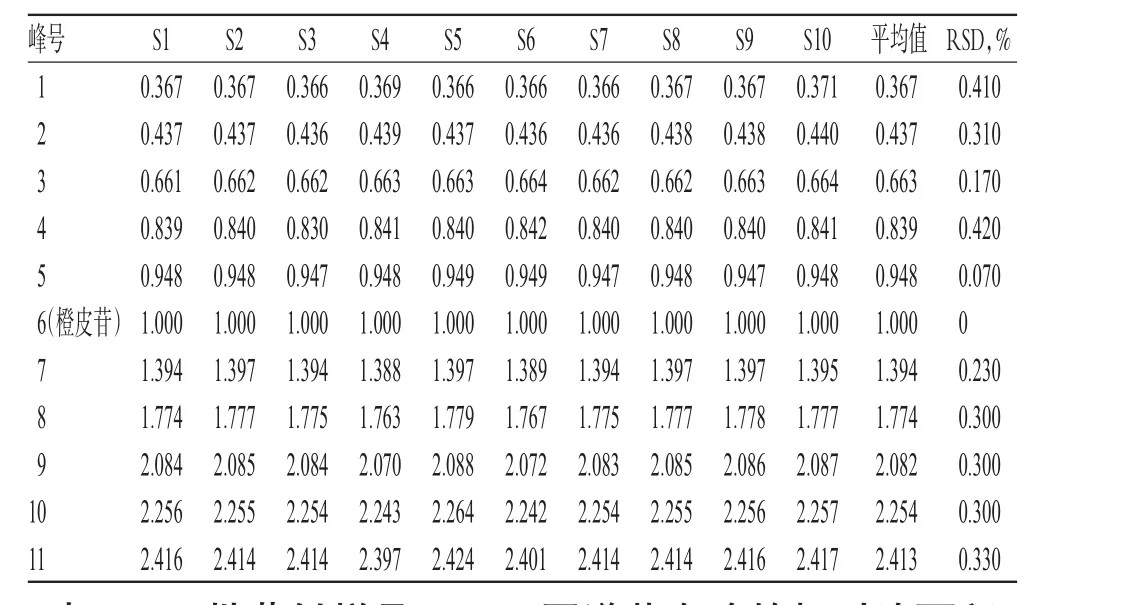
表4 10批药材样品HPLC图谱共有峰的相对保留时间Tab 4 Relative retention time of common peaks for 10 batches of medicinal materials

表5 10批药材样品HPLC图谱共有峰的相对峰面积Tab 5 Relative peak areas of common peaks for 10 batches of medicinal materials

图4 10批药材样品聚类分析树状图Fig 4 Cluster dendrogram for 10 batches of medicinal materials
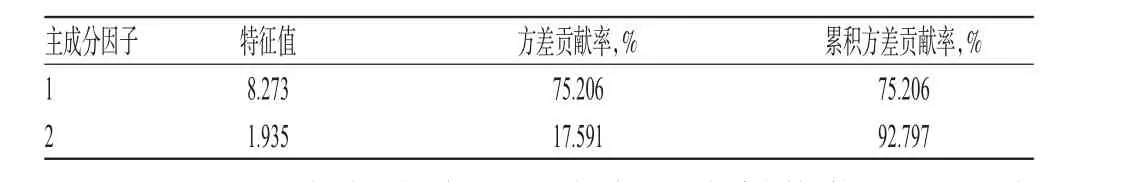
表6 2个主成分因子的特征值和方差贡献率Tab 6 Eigenvalue and variance contribution rate of two main component factors
以上述2个主成分因子为变量绘制载荷图和得分图,详见图5。由图5可知,载荷图结果与初始因子载荷矩阵结果相同,距离原点较远的点为主成分因子1和主成分因子2中权重值较大的成分;由得分图可知,10批药材样品分散在不同区域,表明药材样品质量与地域分布有关。
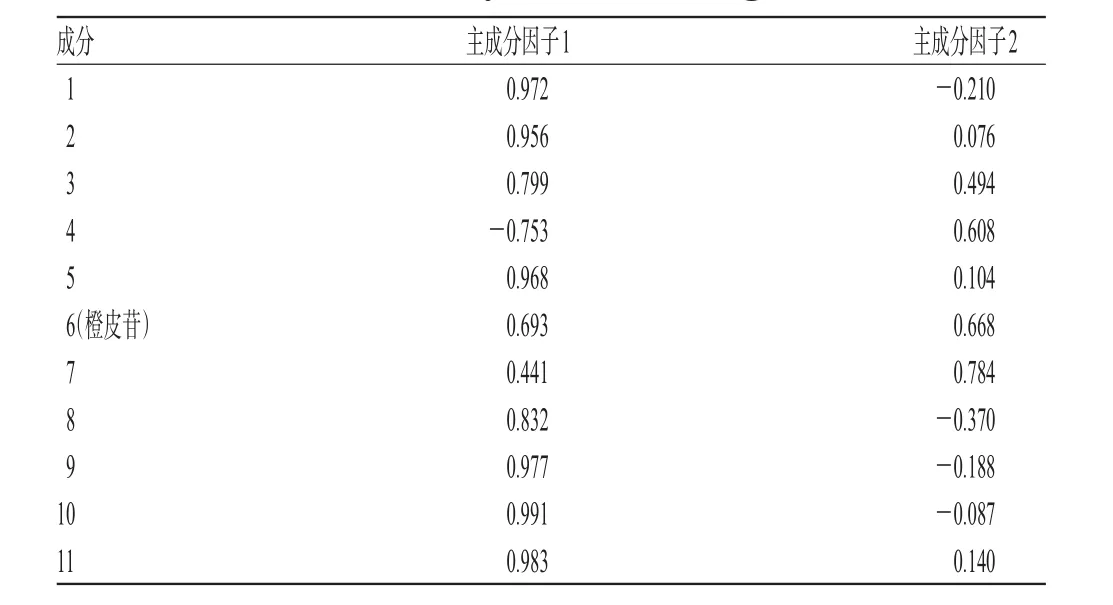
表7 初始因子载荷矩阵Tab 7 Primary factor loading matrix

图5 10批药材样品的载荷图和得分图Fig 5 Loading diagram and score chart of 10 batches of medicinal materials
2.6.2 综合质量评分 以上述2个主成分因子对10批药材样品质量进行综合评分,结果见表8。由表8可知,S7药材样品主成分因子综合得分最高,该批样品中成分1、2、5、6、9、10、11的含量相对较高,整体质量相对较好综合得分越高表示药材样品整体质量越好[9])。
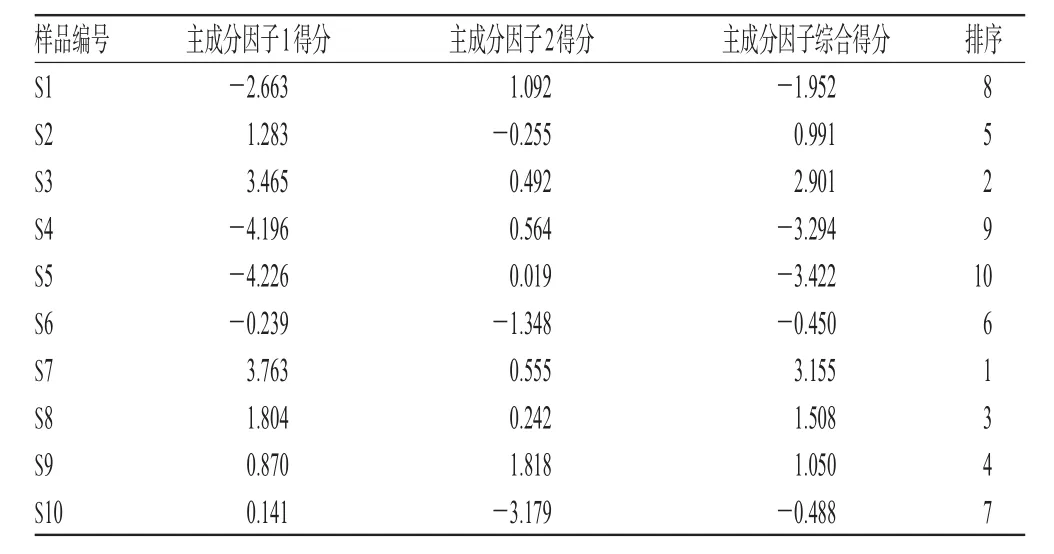
表8 10批药材样品主成分因子得分及排序Tab 8 Main component factor score and ranking of 10 batches of medicinal materials
3 讨论
当前,随着人们对中药需求量的增大以及用药安全意识的加强,中药质量控制越显重要。指纹图谱作为一种有效的中药质量控制模式,以其科学的理论依据获得了国际上的一致认可[10]。指纹图谱在色谱峰未明确为何种成分的情况下,仍能给出充分、可靠的信息,用以控制中药材质量[11]。
本研究在建立青皮药材的HPLC指纹图谱的过程中曾分别考察了乙腈-0.5%醋酸溶液、乙腈-0.2%醋酸溶液、乙腈-水、甲醇-0.5%醋酸溶液、甲醇-0.2%醋酸溶液、甲醇-水为流动相时色谱峰的分离效果。结果,以乙腈-0.5%醋酸溶液为流动相时分离效果最佳,色谱峰的分离度及峰形均良好,且保留时间合适,故最终选择乙腈-0.5%醋酸溶液为流动相进行梯度洗脱。本研究还分别考察了在284、300、360 nm不同检测波长下的出峰情况。结果,检测波长为360 nm时的出峰数较多,故最终选择360 nm为检测波长。
本研究所建立的青皮药材的HPLC指纹图谱,可反映药材样品的特异性和整体性信息。在11个共有峰中,通过与对照品HPLC图谱比对指认出了橙皮苷峰。10批药材样品的相似度评价结果表明,各批药材样品间质量存在差异。各共有峰相对保留时间的RSD差异小,但相对峰面积的RSD相差较大,提示不同产地药材样品的成分虽一致,但含量差异较大,这可能与药材的生长环境、采收季节、加工炮制等因素有关。
综上所述,本研究所建HPLC指纹图谱及聚类分析和主成分分析结果可为青皮药材的质量控制提供参考。

