四川省亨廷顿病家系临床特点、基因诊断与家系分析☆
李彬 罗永杰○☆ 罗芸 汪溯
亨廷顿病(Huntington disease,HD)是一种常染色体显性遗传的变性疾病,通常发病年龄在30~50岁。典型症状包括进行性加重的舞蹈样症状、认知和精神障碍。致病基因IT15位于染色体4p16.3中,其外显子1上的CAG重复次数与发病密切相关[1]。国外研究发现(CAG)n≥40时患者必然会患病;(CAG)n为 36~39时仍可发病,但外显率降低,患者症状可能较轻;(CAG)n为 27~35时不发病,但其后代出现扩增突变的风险增加;(CAG)n<27次为正常范围[2]。最近一个荟萃分析显示中国/日本HD患病率为0.40/10万,而欧洲/北美以及大洋洲患病率为5.7/10万[3]。本研究中,我们收集了来自四川的4个亨廷顿病家系,采用DNA直接测序方法检测IT15基因,并分析家系及临床特点,为HD家系成员提供遗传咨询。
1 资料与方法
1.1研究对象连续收集2016年3月至2018年3月至四川省人民医院就诊的亨廷顿病患者及部分家系成员的详细临床资料。根据中华医学会亨廷顿病的诊断与治疗指南[4],结合阳性家族史、特征性的运动、认知和精神症状作出临床诊断,如无阳性家族史,或症状不典型可通过基因测试而确诊。本研究纳入的4个HD家系均来自四川地区,共有24例参加IT15基因测序,其中男14例,女10例,年龄分布在 7~76 岁,平均年龄为(32.75±17.62)岁。本研究获得所有受试者的同意并通过了四川省人民医院伦理委员会的审核。
1.2资料收集亨廷顿病患者及家系成员进行详细病史资料采集,包括基本信息采集,病史采集,体格检查,认知功能评估(MMSE、MoCA),焦虑抑郁评估(HAMA、HAMD),日常生活能力评估(ADL)等,并绘制系谱图。
1.3基因检测
1.3.1基因组 DNA提取 采集外周静脉血5 mL,采用天根®血液/组织/细胞基因组提取试剂盒(DP304)提取基因组DNA。提取试剂盒购于天根生化科技(北京)有限公司。
1.3.2引物设计与合成 根据IT5基因序列设计荧光修饰引物,上游引物序列(HTT-F):GCCTCCG GGGACTGCCGT;下游引物序列(HTT-R):GTGG CGGCTGTTGCTGCT,荧光修饰引物标记类型为FAM。荧光修饰引物由成都擎科梓熙生物技术有限公司合成。
1.3.3PCR 扩增 ①采用 TSINGKE®2×T5 Super PCR Mix对样本DNA进行PCR扩增。②反应体系为 T5 Mix 15 μL, HTT-F(10P) 0.5 μL,HTT-R(10P)0.5 μL,gDNA 1 μL,ddH2O 13 μL。 ③应用 9700 型自动扩增仪进行扩增反应,反应条件为预变性98℃,3 min,(98℃,10 s;57℃,15 s;72℃,10 s)为1个循环,共 35个循环,最后 72℃,延伸 5 min,4℃保存。
1.3.4定量稀释 将 PCR扩增产物取 2 μL进行1%琼脂糖电泳,150 V、100 mA 20 min电泳观察,根据条带亮度定量稀释PCR产物。
1.3.5上机检测 稀释后的PCR产物与内标500 LIZ混合后上ABI 3730XL DNA测序仪进行毛细管电泳检测。
1.4统计学方法应用SPSS 22.0对符合正态分布的双变量进行Pearson直线相关分析,不符合正态分布的双变量进行Spearman秩相关分析,检验水准 α=0.05。
2 结果
2.1人口学资料与基因检测通过基因检测,确诊8例HD患者,其中男6例,女2例,发病年龄在23~57岁,病程1~31年,CAG长链重复次数41~54次。发现症状前患者7例,其中男5例,女2例,年龄7~47岁,CAG长链重复次数43~58次。详见表1。
2.2部分成员PCR扩增家系A先证者Ⅲa10的IT15基因出现异常扩增,正常等位基因对应扩增片段长度为149 bp,异常等位基因对应扩增片段长度为239 bp(图1A);先证者的儿子Ⅳa9同样出现了异常扩增,其对应扩增片段长度为269 bp(图1B)。家系C中先证者Ⅲc5异常等位基因对应扩增片段长度为257 bp(图1C)。Ⅲa18未出现扩增,两条等位基因对应扩增片段长度分别为146 bp、155 bp(图 1D)。
2.3家系系谱分析家系A有5代,共有患者7例,其中男5例,女2例。4例现症患者,均为男性;发现6例症状前患者,男5例,女1例。在家系传代过程中,第一代发病年龄为50岁,第二代平均起病年龄40岁左右,第三代平均起病年龄36岁左右。家系B有5代,共有患者7例,其中男4例,女3例。2例现症患者,1例育龄期症状前患者。家系C有4代,共4例患者,男1例,女3例。家系C中第一代起病年龄为40岁,第二代平均起病年龄33岁左右,第三代起病年龄23岁。家系D无家族病史,先证者父母于60岁左右死于恶性肿瘤,其余家系成员目前尚未出现舞蹈样症状。上述家系A和C在传代过程中均出现遗传早现现象。

表1家系成员基本资料
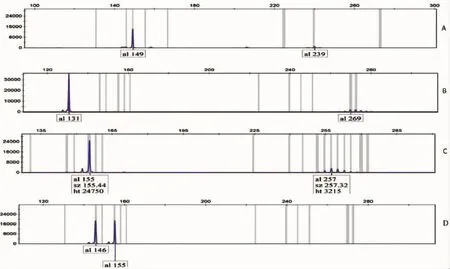
图1部分人员PCR扩增产物毛细管电泳结果
2.4现症HD患者临床特点家系A中先证者(Ⅲa10)44岁,男,36岁时出现双上肢及面部不自主运动,伴有耸肩动作,吐词欠清,并有焦虑、失眠等;其弟弟(Ⅲa14)症状较轻微,但小舅(Ⅱa14)、大舅(Ⅱa1)病程较长,舞蹈样症状更严重、认知功能下降更明显。家系B中先证者(Ⅲb2)52岁,女,44岁出现双下肢不自主运动,后逐渐发展至全身,有明显认知障碍,家属诉及患者早期有性格改变,易激惹。家系C中先证者(Ⅲc5)23岁,男,22岁时出现肢体不自主运动,以手指拨动及肩部不自主运动为主,目前症状较轻,其三姨(Ⅱc5)有明显舞蹈样症状及认知功能下降。家系D中先证者(Ⅱd1)59岁,男,57岁时以行走不稳起病,逐渐出现舞蹈样不自主运动及言语含糊,进行性加重。直线相关分析显示:CAG重复次数与发病年龄成负相关 (r=-0.967,P<0.01)。 秩相关分析显示:ADL评分与病程(r=0.842,P<0.01)呈正相关,与MMSE评分 (r=-0.930,P<0.01)、MoCA 评分 (r=-0.932,P<0.01)呈负相关。
2.5影像学家系A中先证者(Ⅲa10)44岁,头颅CT可见弥漫大脑皮层萎缩,外侧裂池增宽,特征性双侧尾状核萎缩(图3a)。家系C中先证者(Ⅲc5)24岁,病程仅1年,头颅MRI尚未出现明显的异常(图 3b,T2WI)。 家系 D 中先证者(Ⅱd1),59岁,头颅MRI表现为明显的侧脑室增宽、大脑皮层萎缩(图 3c、d,T2WI),亦可见双侧尾状核及壳核的萎缩(图 3c,T2WI)。
3 讨论

图2 4个HD家系系谱图(右上角标*为本次参加基因检测的成员)

表2 HD患者及部分症状前HD患者的临床特点
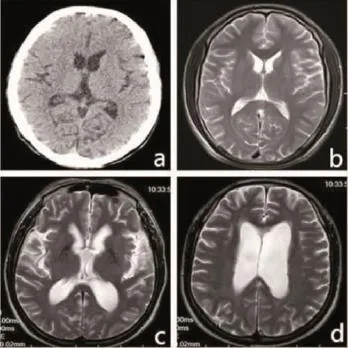
图3 部分先证者的头颅影像学表现
本研究发现发病年龄与CAG重复次数呈负相关(r=-0.967,P<0.01),与 KEUM、LEE 等[5-6]的发现一致,由此我们可以推测家系A中Ⅳa9、Ⅳa12、Ⅳa13的发病年龄可能较早。虽然CAG重复数对发病年龄起主导作用,但仍受修饰基因或环境因素影响[6]。家系A中先证者及其弟弟、表弟(Ⅲa10、Ⅲa14、Ⅲa16)的 CAG 重复次数分别为 48、48、50 次,他们各自子女(Ⅳa9、Ⅳa12、Ⅳa13)的CAG重复数分别为58、58、52次,都出现了扩增的情况,与WHEELER等[7]发现后代从父系遗传的CAG拷贝数更倾向于扩增这一研究一致。但家系B中先证者(Ⅲb2)到女儿(Ⅳb3)的母系遗传过程中也出现了2个拷贝数的扩增。目前所研究的家系的传代过程中尚未发现CAG缩减情况。
经过相关分析发现,ADL评分与病程 (r=0.842,P<0.01)呈正相关,与 MMSE 评分(r=-0.930,P<0.01)、MoCA 评分 (r=-0.932,P<0.01) 呈负相关。这与亨廷顿病疾病进展是一致的,晚期病人临床症状较重,认知功能也明显下降,日常生活能力进一步下降。如家系A中Ⅱa1、Ⅱa14及家系B中的Ⅲb2病程较长,目前生活均无法自理。HD患者认知功能障碍可早于运动障碍数年出现,主要出现执行功能、注意力、记忆、学习、处理速度、自知力等方面的认知功能下降[8]。MMSE常用来评估HD患者认知功能,但MICKES等[9]发现MoCA在HD相关的认知功能障碍检测较MMSE更敏感,这与我们的发现一致。家系A中Ⅲa2、Ⅲa10的MMSE评分正常,但MoCA评分提示认知功能是下降的。
目前报道的HD患者及症状前患者中有10%~80%的不同程度抑郁的风险[10-11],焦虑的患病率在13%~71%的范围[10,12-14]。我们发现参与者中焦虑抑郁发生率均较高。焦虑抑郁可出现在HD病程中的任何阶段,在病程进展与焦虑抑郁的关系研究中,目前尚无一致结论[14-17]。部分人在接受基因测试时的焦虑抑郁水平最高[18-19],如Ⅳa9、Ⅳb3有较严重的焦虑抑郁,可能是因为患病家庭中的年轻一代必须面对遗传风险、婚育、家庭负担及社会歧视等方面的问题[20]。
家系D中先证者(Ⅱd1)57岁起病,发病较晚,与LIPE[21]的研究中晚发型HD很类似。患者头颅MRI(图3c、图3d)及核素脑池显像提示交通性脑积水,既往多篇报道[22-24]的晚发型亨廷顿病被误诊为正常压力脑积水,后经基因检测才被确诊。该家系无家族史,先证者父母均于60多岁时死于恶性肿瘤,不排除其死亡时尚未出现运动症状的情况,但也可能父母其中一人的CAG重复数在27~35的范围[25],在传代的过程中导致CAG扩增。建议先证者儿子及其他直系亲属进一步行基因检测。
目前没有任何药物可以阻止、减缓或逆转疾病的进展。家系A、B、D中先证者曾予以盐酸硫必利、氟哌啶醇改善舞蹈症状,余患者均未接受对症治疗。本研究中有1例HD患者和3例症状前患者近期有生育需要,但其有50%的风险将致病基因传给下一代,所以遗传咨询及产前诊断是非常必要的。随着技术的不断进步,无创的产前诊断[26]或许能为亨廷顿病家系带来福音,从根源上避免患儿的出生。
综上,IT15基因的检测对于亨廷顿病的确诊及症状前诊断具有重要的意义,特别是对家族史阴性及发病晚的症状不典型的患者。CAG重复次数在一定程度上能够预测发病年龄的早晚,本研究中的家系均来自四川地区,与JIANG等[27]研究中国人的CAG重复次数以及与发病年龄的相关性上的发现是一致的。家系传代过程中存在CAG重复次数的扩增,且有遗传早现现象。目前尚无特异的治疗方法,所以遗传咨询及产前诊断是非常必要的。

