Li2CO3-Y3+共掺杂TiO2纳米材料的制备及光催化性能的研究
王 月,李 雪,王春杰
(1.渤海大学新能源学院,锦州 121013;2.渤海大学工学院,锦州 121013)
1 引 言
TiO2凭借其催化活性高且无毒、价格低廉等优势,迅速取代其他催化剂,在污水处理、杀菌消毒以及空气净化等诸多领域得到了广泛研究和应用[1-3]。但是,纯TiO2的能带宽度为3.2 eV,导致其在太阳光下光能利用率极低(约为5%),从而限制了其应用领域。如果能充分利用太阳光对TiO2进行光催化降解定会大大提升其光催化效率[4-5]。目前大部分的研究都集中于对TiO2的改性方面,对纯TiO2改性研究的主要途径是掺杂,但是一些掺杂剂常常会降低光生电子和空穴的复合几率,进而影响光催化活性[6-10]。因此,选择一种合适的掺杂剂对于提高材料的光催化活性是至关重要的。
本研究以经典的溶胶-凝胶法制备TiO2纳米材料,以六水合硝酸钇作为钇源,通过溶胶-凝胶法制备了Y3+掺杂的TiO2。研究了锐钛矿下Y3+-TiO2晶形对光催化的影响。通过对亚甲基蓝降解的时长,研究了掺杂对Y3+-TiO2催化剂光催化效率的影响。此外,通过共掺杂碳酸锂进一步提高了Y3+-TiO2的光催化效率,并对相关机理进行了讨论。
2 实 验
2.1 试剂与仪器
钛酸四丁酯(上海麦克林生化科技有限公司,分析纯),冰乙酸(天津风船化学试剂科技有限公司,分析纯),无水乙醇(天津风船化学试剂科技有限公司,分析纯),六水合硝酸钇(国药集团化学试剂有限公司,分析纯),硝酸(天津风船化学试剂科技有限公司,分析纯)。
真空管式炉GSL-1400(合肥科晶技术有限公司),X-射线衍射仪Rigaku Ultima IV(日本理学),场发射扫描电镜S-4800(日本日立),荧光分光光谱仪Fluoromax-4NIR(法国HORIBA公司)。
2.2 Y掺杂TiO2及Li2CO3,Y3+共掺TiO2样品的制备
取13 mL的无水乙醇,剧烈搅拌下依次加入10 mL的钛酸四丁酯和1.7 mL的冰乙酸,搅拌30 min,得到溶液A;取13 mL的无水乙醇,加入2.2 mL的水,取一定量的六水合硝酸钇(与钛酸四丁酯的摩尔比为0.03∶1)加入到上述溶液中,滴加0.2 mL硝酸,搅拌20 min后得到溶液B;将溶液B滴入到溶液A中继续搅拌10 min,在室温下陈化后得到凝胶,将凝胶放于烘箱中,80 ℃烘干后研磨成粉,500 ℃下煅烧2 h,得到Y3+掺杂的TiO2,标记为0.03Y3+。以相同的方法制备了Li2CO3-Y3+共掺杂的TiO2纳米材料样品(摩尔比为(Li2CO3)∶(Y3+)∶(Ti)=0.03∶0.03∶1),标记为0.03Li2CO3-Y3+。
3 结果与讨论
3.1 Y3+掺杂TiO2光催化研究
3.1.1 物相表征

图1 (a)TiO2标准卡以及TiO2和TiO2∶0.03Y3+的XRD图谱;(b) TiO2和TiO2∶0.03Y3+在24°~26°XRD偏移图谱Fig.1 (a)TiO2 standard card and XRD patterns of TiO2 and TiO2∶0.03Y3+; (b) TiO2 and TiO2∶0.03Y3+ at 24°~26° XRD offset map
首先对材料进行物相分析,图1(a)为通过溶胶-凝胶法制备并在500 ℃退火后得到的TiO2样品以及相同条件制备的TiO2∶0.03Y3+样品的X-射线衍射图谱。由图可知,两组样品的XRD谱图与PDF#71-1166 的TiO2标准卡片对应完好,没有其余杂质峰出现。说明本研究采用的制备方法可以制得纯相锐钛矿TiO2。图1(b)则是2θ在24°至26°范围内的XRD放大图谱,可以明显看出Y3+掺杂合成TiO2的XRD图谱出现明显蓝移。这主要是因为六配位Ti4+半径为0.061 nm,Y3+半径为0.090 nm(如表1)[11],Y3+替换Ti4+使得晶胞整体出现轻微膨胀现象,根据布拉格衍射方程:
2dsinθ=nλ
(1)
晶面间距d变大,2θ变小。因此24°到26°范围内放大图谱出现轻微蓝移,证实了Y3+的掺杂成功[12]。

表1 不同配位数(CN)的Ti4+和Y3+离子的离子半径Table 1 Ion radii of Ti4+ and Y3+ ions with different coordination numbers (CN)
3.1.2 形貌表征

图2 (a)TiO2的SEM图片;(b) TiO2∶0.03Y3+的SEM图片Fig.2 (a)SEM image of TiO2;(b)SEM image of TiO2∶0.03Y3+
图2a和2b分别是TiO2和TiO2∶0.03Y3+的SEM图片。从图中可以看出,TiO2样品尺寸较大,形貌为不规则大块。而经过掺杂后的TiO2∶0.03Y3+样品的尺寸相比于掺杂前要小很多。由于样品形貌为团聚较为严重的块材,无法从SEM图片上得到直观的颗粒尺寸。因此,我们通过谢勒公式,基于XRD数据对样品的颗粒尺寸进行了计算。TiO2样品的平均粒径尺寸约为20.35 nm,而掺杂后样品的尺寸约为13.88 nm。光催化反应是在催化剂材料的表面进行的,而催化剂材料的晶粒尺寸将直接影响到催化剂的催化性能。催化剂的粒径越小,其比表面积越大,这样就会有更多的物质被附着在催化剂的表面,光子利用率也会随之提升,从而改善催化剂的催化性能。此外,催化剂粒径小,电子和空穴迁移至催化剂表面的时间变短,复合的几率变小,并且电荷的传递速率变高,这些因素都有利于改善催化剂的光催化活性[13-14]。
3.1.3 光催化性能研究

图3 (a)和(c)分别为亚甲基蓝溶液在纯TiO2和TiO2∶0.03Y3+光催化作用下在不同光照时间的UV-vis谱;图(b)和(d)分别为纯TiO2和TiO2∶0.03Y3+光降解效率图Fig.3 (a) and (c) UV-vis spectra of methylene blue solution under photocatalysis of pure TiO2 and TiO2∶0.03Y3+ at different illumination time, and Fig.3(b) and (d) photodegradation efficiency diagrams of pure TiO2 and TiO2∶0.03Y3+
图3(a)和3(c)分别为亚甲基蓝溶液在纯TiO2和TiO2∶0.03Y3+光催化作用下在不同光照时间的UV-vis图谱。可以明显看出两个图谱都呈现出下降趋势,TiO2∶0.03Y3+相比于纯TiO2图谱下降更快,当光催化时长达到120 min时,接近于初始强度的1/4,而纯TiO2则是接近初始强度的1/2。在亚甲基蓝的最大吸收波长处测定亚甲基蓝的吸光度。根据公式计算亚甲基蓝降解率:
η=(A0-A)/A0×100%
(2)
式中,A0为亚甲基蓝光降解前的吸光度值;A为亚甲基光降解后的吸光度值[13]。计算后得到纯TiO2和TiO2∶0.03Y3+光降解率的数值绘制成图3(b)和3(d)。图3(b)和3(d)中可以明显看出当光催化时长为120 min时,纯TiO2光降解率达到45.24%,而TiO2∶0.03Y3+光降解率达到73.92%。这是因为掺杂浓度为0.03 Y3+的样品中形成了掺杂能级,使得掺杂能级上电子-空穴对能够更好的分离,降低了电子和空穴的复合率,从而提高了光催化效率[15]。
3.2 Li2CO3、Y3+共掺TiO2光催化研究
3.2.1 物相表征

图4 TiO2∶0.03Y3+和0.03Li2CO3-Y3+共掺TiO2 XRD图谱Fig.4 XRD patterns of TiO2: 0.03Y3+ and 0.03Li2CO3-Y3+ co-doped TiO2
图4是在相同条件下制备的TiO2∶0.03Y3+和0.03Li2CO3-Y3+共掺TiO2复合光催化剂的X-射线衍射图谱。由图可知,0.03Li2CO3-Y3+共掺TiO2的X-射线衍射图谱与TiO2∶0.03Y3+X-射线衍射图谱吻合较好,没有杂质峰出现,也没有出现峰值的偏移。因此,共掺杂并没有引起材料物相变化。
3.2.2 漫反射分析
从图5(a)中可以看出,0.03Li2CO3-Y3+共掺TiO2漫反射图谱相比较于TiO2∶0.03Y3+漫反射图谱发生了明显变化,漫反射率明显提高。根据带隙经验公式可以计算TiO2∶0.03Y3+和0.03Li2CO3-Y3+共掺TiO2带隙[16]:
(αhv)m=A(hv-Eg)
(3)
式中,α为吸收系数;ν为入射光频率;h为普朗克常数;Eg为带隙;A为吸光度。由于TiO2是一种典型的间接跃迁半导体,m一般取1/2而不取2[17],(αhν)1/2与hν成正比,Eg可由曲线(αhν)1/2-hν的切线与x轴相交的截距获得。
经计算,TiO2∶0.03Y3+带隙(如图5(b))和0.03Li2CO3-Y3+共掺TiO2带隙(如图5(c))分别为3.04 eV和3.01 eV,二者数值差距不大,近似可忽略不计,这说明0.03Li2CO3-Y3+共掺TiO2并不会影响到样品带隙的变化,这与XRD图谱结果是相吻合的。没有新的杂质能级的产生,但是0.03Li2CO3-Y3+共掺TiO2却会引起漫反射率的提升,这说明了0.03Li2CO3-Y3+共掺TiO2的样品可以更有效的提高材料的光催化效率,下面我们将会利用光催化的结果进行具体讨论。
3.2.3 光催化性能研究
从上图可以明显看出当光催化时长达到120 min时,0.03Li2CO3-Y3+共掺TiO2光降解率为88.12%,而TiO2∶0.03Y3+在120 min时光降解率为73.92%,光催化结果与漫反射结果相吻合。张文保等[18]曾提出TiO2掺杂可以形成捕获中心,价态高于Ti4+的金属离子捕获电子,低于Ti4+的金属离子捕获空穴,抑制e-和h-。在本文中Y为正三价,低于Ti的正四价,因此Y3+掺杂需要捕获更多的空穴,所以Li2CO3在本文中起到的是空穴补偿剂的作用,而不是传统的电荷补偿剂。一般金属离子掺杂形成的杂质能级靠近于TiO2导带位置,Li2CO3中电子与空穴分离后,电子受到激发,到达导带,随着光生载流子流走,从而在杂质能级留下更多的空穴,进而提高了光催化效率。
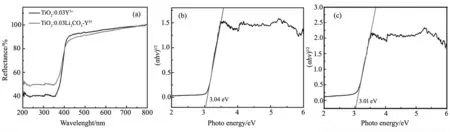
图5 (a)TiO2∶0.03Y3+和0.03Li2CO3-Y3+共掺TiO2漫反射图谱;(b)和(c)分别为TiO2∶0.03Y3+和0.03Li2CO3-Y3+共掺TiO2带隙Fig.5 (a)Diffuse reflectance spectra of TiO2: 0.03Y3+ and 0.03Li2CO3-Y3+ co-doped TiO2 ; (b) and (c)bandgaps of TiO2: 0.03Y3+ and 0.03Li2CO3-Y3+ co-doped TiO2

图6 (a)为亚甲基蓝溶液0.03Li2CO3-Y3+共掺TiO2光催化作用下在不同光照时间的UV-vis谱;(b) 0.03Li2CO3-Y3+共掺TiO2光降解率图Fig.6 (a) UV-vis spectra of methylene blue solution with 0.03Li2CO3-Y3+ co-doped TiO2 under different illumination time; (b)photodegradation rate of 0.03Li2CO3-Y3+ codoped TiO2
4 结 论
通过溶胶-凝胶法制备了纯TiO2、Y3+掺杂的TiO2以及0.03Li2CO3-Y3+共掺TiO2纳米材料,再通过500 ℃煅烧后得到样品。研究了Y3+掺杂锐钛矿TiO2对其光催化性能的影响。Y3+掺杂的TiO2相比于纯TiO2具有更小的颗粒尺寸和更高的光催化效率。同时还对TiO2∶0.03Y3+进行了Li2CO3共掺改良,结果证明Li2CO3共掺可以带来更多的空穴,从而对TiO2∶0.03Y3+光催化效率有了进一步的提升。TiO2∶0.03Y3+进行了Li2CO3共掺后,在光催化120 min时,其光降解率为88.12%,这远远大于相同条件下光降解率为45.24%的纯TiO2,强于光降解率为73.92%的TiO2∶0.03Y3+。

