早产儿动脉导管未闭的危险因素分析
韦冰梅,张艳明,黎瑞珊,韦巧珍
(1.广西医科大学第二附属医院,广西 南宁 530007;2.广西医科大学第一附属医院,广西 南宁 530007)
动脉导管未闭(PDA)是早产儿最常见的先天性心脏病,其发病率高,且通常发病率与胎龄的增长成反比。PDA使体循环进入肺循环,可导致全身器官灌注减少导致肺过度循环和呼吸困难。PDA的存在也可通过改变的脑血流模式导致脑功能下降。此外,PDA可以影响大脑皮质电活动并且与室内出血、脑室周围白质软化和脑瘫的风险增加有关[1]。新生儿PDA常见的临床危险因素为胎龄、败血症、呼吸窘迫综合征、宫内生长受限、遗传易感因素等[2]。本研究以2013年3月-2018年3月广西医科大学第一、第二附属医院收治的PDA患儿进行临床分析,探讨早产儿PDA发生的危险因素,为临床早期发现和诊断PDA提供依据。
1 资料与方法
1.1 病例选择与诊断标准 选择广西医科大学第一、第二附属医院2013年3月-2018年3月收治的46例PDA早产儿为病例组。随机选取同期住院的50例非PDA早产儿为对照组。病例组症状性PDA(sPDA)的诊断标准[3]:①临床及胸片指标:呼吸状况恶化;胸骨左缘上方闻及连续性或收缩期杂音:水冲脉或心前区搏动明显;血压难以维持正常水平;胸片示肺充血或心脏扩大(心胸比>60%);②超声指标:舒张期动脉导管存在左向右分流;动脉导管直径大小>1.5 mm及左房内径/主动脉内径>1.3。符合临床及胸片指标两条及以上并符合超声指标者可诊断。有血流动力学意义的PDA(hsPDA)心脏超声诊断标准:生后48 h-96 h内符合以下任意一项条件[4]:动脉导管直径>1.5 mm;左心房内径/主动脉内径>1.3;舒张末期主动脉反流或不仅有PDA的临床症状且合并心功能不全表现。新生儿并发症诊断标准参照《实用新生儿学》第4版诊断标准[5]。排除标准:伴有其他心脏疾病的患儿。
1.2 方法 所有研究对象记录新生儿年龄、性别、胎次、孕母年龄、分娩方式、羊水、脐带、胎盘、有无围生期窒息、阿氏评分、妊娠期高血压疾病(HDCP)、妊娠期糖尿病(GDM)、妊娠早期感染性疾病、贫血等。新生儿生后早期并发症败血症、新生儿呼吸窘迫综合征(RDS)、肺炎、脑室内出血(IVH)、低血糖、新生儿坏死性小肠结肠炎(NEC)等。记录出现发绀、气促、血氧饱和度下降+心脏杂音的时间,治疗后上述症状消失的时间。病理组根据有无临床症状和超声心动图记录hsPDA和无血流动力学意义的动脉导管未闭(nhsPDA)。根据统计结果对危险因素进行单因素分析和多因素分析。
1.3 统计学分析 采用SPSS 19.0统计软件进行分析。计数资料、单因素分析采用χ2检验;计量资料描述采用均数±标准差(Mean±SD);组间比较采用t检验;多因素分析采用Logistic回归分析。P<0.05 为差异有统计学意义。
2 结果
2.1 一般情况 病例组46例,男29例,女17例,胎龄(32.5±2.8)周,出生体质量(1,752.63±551)g。对照组50例,男32例,女18例,胎龄(33.8±2.5)周,出生体质量(1,887±783)g。两组患儿在胎龄上差异无统计学意义(P>0.05)。病例组胎龄小于34周共35例(76%),胎龄小于30周共18例(39.1%),其中胎龄<28周共8例(17.3%);hsPDA 32例,nhsPDA 14例;外科手术治疗2例,口服布洛芬治疗22例,治愈好转24例,随访观察22例。
2.2 危险因素及常见并发症分析 两组新生儿肺炎、新生儿败血症、IVH、母孕早期感染差异有统计学意义(P<0.05)。
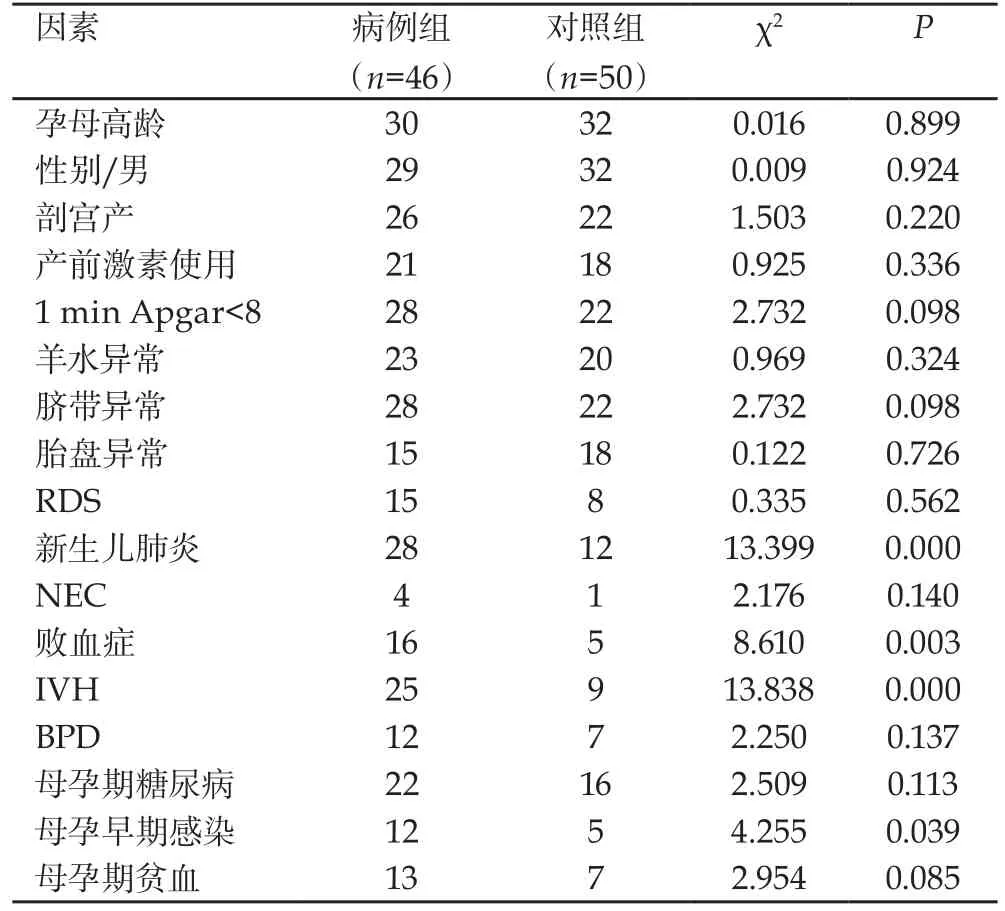
表1 PDA危险因素及常见并发症的比较
2.3 多因素分析 多因素分析结果显示:新生儿肺炎、新生儿败血症、母孕早期感染是PDA的危险因素(P<0.05)。
3 讨论
新生儿出生是一个独特的生理事件,其变化过程影响多个系统器官,尤其是呼吸系统和心血管系统[6]。在胎儿期主要是低氧和前列腺素维持动脉导管的开放,前列腺素由胎盘和动脉导管平滑肌细胞产生,在肺内灭活。出生后随着自主呼吸的建立和脐血管的阻断,肺循环压力下降,体循环阻力升高,动脉导管内氧分压升高,同时前列腺素的胎盘来源阻断,肺内灭活增加,促使动脉导管收缩并于生后24 h内形成功能上关闭[7]。动脉导管收缩引起导管壁缺氧,细胞死亡,并产生生长因子最终导致导管结构重建,形成解剖上的关闭。本研究发现,病理组胎龄小于34周早产儿的PDA发病构成比达76%。早产儿由于其动脉导管平滑肌发育不成熟,对高氧的敏感性低,而对前列腺素敏感性高,在生后早期仍保持开放状态。有研究明,胎龄为30周-37周的早产儿PDA发生率为10%,而胎龄为25周-29周的早产儿PDA发生率高达80%[8]。50%-70%的PDA有血液动力学改变,与发病率和死亡率增加有关[9]。
本研究发现新生儿肺炎、新生儿败血症、母孕早期感染是PDA的危险因素。新生儿感染主要包括宫内感染及生后患感染性疾病。感染导致PDA开放的机制可能为病原体被相应受体识别后激活免疫系统,产生的炎性细胞因子使前列腺素酶的合成及活性增强,同时刺激胎盘滋养细胞促肾上腺皮质激素释放激素的合成及分泌,因而促进前列腺素的合成,导致动脉导管持续开放[10]。有研究认为可能导致动脉导管自发关闭失败的影响因素为炎症介质的增加,如肿瘤坏死因子α、前列腺素和氧自由基[6]。因此减少和避免宫内感染及防治出生后感染对于降低PDA的发生率有重要意义。
据报道,早产儿的PDA是几个短期并发症导致死亡率增加的主要疾病之一。研究证明PDA与急性肺部疾病、机械通气时间延长、慢性肺病(CLD)、脑室内出血(IVH)和坏死性小肠结肠炎(NEC)的死亡率增加相关。本研究发现病例组新生儿IVH是PDA常见的并发症。一项前瞻性生理学研究发现,在极早早产儿中,心脏第一次心输出量低影响出生早期12 h内的心室功能和脑血流量,随后的发展导致IVH[11];另一项回顾性研究发现,早期筛查和针对性地治疗PDA能使IVH的发生率降低[12]。PDA的分流导致脑灌注不足的相对状态,特别是如果它超过婴儿的脑自动调节容量,由于左心室适应负荷的变化条件,它通过增加其输出来调节[13]。由于脑血管床是导管前的,它暴露于突然的恢复/增加血流量,出现缺血再灌注的病理生理学改变,其可能促成IVH的发生;而持续增加肺血管床中的体积易导致CLD,内脏循环的减少易产生NEC。
近年来,遗传变异性的潜在高度相关性研究发现仍在不断更新。本研究发现男性PDA患儿29例(63%),占比超过总数一半。有研究发现男性是hsPDA发展的危险因素[14];兄弟姐妹的发生风险是5%;同卵双胞胎之间发生的相关性更大于异卵双胞胎。对于双胞胎的PDA研究发现,76%的PDA发生与遗传因素以及其共享的环境相关[15]。
由于早产儿PDA发病率和并发症的不良结局对早产儿的生存质量有一定的影响,临床医生需在体循环和肺循环的平衡之间进行权衡以决定是否进行干预。近年来有越来越多的学者开始对早产儿常规治疗PDA的合理性提出质疑[1]。为了减少和避免PDA带来的严重并发症,需要临床医生在了解PDA的危险因素基础上加强围产期母婴管理,对预防与治疗上作出个体化的、针对性的方案。

表2 PDA危险因素多因素分析

