我国基层医院颈动脉狭窄手术治疗现状
吴 潇, 郑月宏
(1.中国医学科学院北京协和医学院,北京 100005;2.中国医学科学院北京协和医院血管外科,北京 100730)
随着人口老龄化的进展和不健康生活方式的流行,我国卒中的发病率和死亡率日益升高。在一项来自全球疾病负担研究 (global burden of disease,GBD)的全球卒中终身风险报告中,我国男性以41.1%的卒中终身风险高居世界首位,并呈现巨大的性别差异(女性为36.7%)[1]。高居不下的卒中风险给我国居民带来极大的疾病负担。我国卒中发病率持续增长,已成为成年人死亡的首位原因[2]。据GBD数据显示,2017年我国卒中发病率为301.44/10万,远高于156.16/10万的全球卒中发病率[3]。我国正面临着严峻的卒中形势。更遗憾的是,卒中在低收入群体中呈现快速增长的趋势[2]。卒中防治报告指出,我国农村地区的卒中患病率及死亡率增长较快。至2013年,农村地区的卒中患病率和死亡率已超过城市地区[4],且这种差距可能随着时间的推移继续拉大[5]。
在2017年全球所有卒中病例中,缺血性约占65%。我国2017年卒中发病率为301.44/10万,缺血性卒中发病率为207.86/10万,占所有卒中的69%[3]。25%~30%的缺血性卒中与颈动脉狭窄密切相关[6]。因此,加强颈动脉狭窄的治疗与管理,对预防卒中、改善居民生活质量的意义深远。
国际指南对颈动脉狭窄治疗的观点
为了认识颈动脉狭窄不同治疗方法的获益,多项著名的随机临床试验,如North American SymptomaticCarotidEndarterectomy Trial(NASCET)、European Carotid Surgery Trial (ECST)、Asymptomatic Carotid Atherosclerosis Study (ACAS)、Asymptomatic Carotid Surgery Trial(ACST)、Carotid Revascularization Endarterectomy versus Stenting Trial(CREST)和 International Carotid Stenting Study(ICSS)等相继开展。基于这些临床试验的结果,学界发布了颈动脉狭窄疾病的管理指南。根据近6个月内是否发生非致残的缺血性卒中、半球缺血事件或黑曚,可将颈动脉狭窄的病人分为症状性颈动脉狭窄和无症状性颈动脉狭窄。颈动脉内膜切除术(carotid endarterectomy,CEA)是预防卒中和治疗颈动脉狭窄的最经典术式。对于症状性颈动脉狭窄病人,当无创检查提示颈内动脉狭窄程度≥70%,或血管造影提示狭窄程度≥50%,推荐手术风险低于平均水平的病人行CEA。当此类病人介入治疗风险低于平均水平时,颈动脉支架置入术(carotid artery stenting,CAS)可作为CEA的替代治疗,由能将症状性病人的围术期卒中及死亡率控制在6%以下的中心开展[7-8]。选择CAS和CEA时,应考虑病人的年龄因素。对年龄较大(>70岁)的病人,尤其是动脉解剖条件不适合介入治疗时,CEA比CAS具有更好的临床结局。对于相对年轻的病人,CAS与CEA的围术期并发症风险(如卒中、心肌梗死、死亡等)和长期的同侧卒中风险相同。不推荐对颈动脉狭窄程度<50%、慢性闭塞、致残性卒中的病人进行血管重建。
对于无症状性颈动脉狭窄病人,首先应改变生活方式,接受规范的内科治疗。当无创检查发现颈动脉狭窄≥70%或血管造影发现狭窄≥60%,且病人的围术期卒中、心肌梗死、死亡风险较低(<3%)时,建议行CEA或CAS。当病人年龄较大,或动脉的病理解剖不适合介入治疗时,应选择CEA而非CAS。当颈部解剖结构不适合进行手术时,如颈部放疗史、CEA术后再狭窄、对侧喉返神经麻痹、严重的颈椎关节炎、颈内动脉狭窄位置过高难以显露、锁骨平面以下的颈总动脉狭窄[7],应选择CAS。当无症状病人的CEA和CAS均有潜在并发症高风险时,血管重建相对于单纯内科治疗的疗效比较尚无定论。遗憾的是,目前的研究还不能确立手术和介入高风险的具体标准。
与美国指南相比,欧洲指南对于症状性病人的血管重建更积极,对于无症状性病人则倾向于内科治疗。对于症状性病人,推荐颈动脉狭窄程度50%~69%作为CEA或CAS的相对指征。对于无症状性病人,预防性CEA及CAS的相对手术指征则扩大到狭窄程度60%~99%。但需满足以下条件:影像学检查证实颈动脉斑块不稳定状态、治疗中心能将围术期卒中和死亡率控制在3%以下,以及病人预期寿命>5 年[9]。
我国颈动脉狭窄治疗指南特点
关于我国的颈动脉狭窄治疗指南,2017年中华医学会外科学分会血管外科学组发布《颈动脉狭窄诊治指南》[10]。与美国及欧洲指南相似,但在其基础上,放宽了无症状性颈动脉狭窄的血管重建指征,将无创检查狭窄度≥70%及无创检查狭窄度<70%但病变处于不稳定状态的无症状性颈动脉狭窄均列为手术相对指征。这也与我国居民居高不下的卒中风险相关。若治疗中心CAS可满足术后30 d内卒中和死亡发生率≤3%,致残性卒中和死亡发生率≤1%,则可作为CEA高危病人的备选治疗方案。CEA髙危病人包括:心脏射血分数<30%,未治疗或控制不良的心律失常、心功能不全、近期心肌梗死病史、不稳定心绞痛、严重慢性阻塞性肺气肿、对侧颈动脉闭塞、颈动脉夹层等。
此外,国内指南将颈动脉斑块是否稳定作为选择CEA或CAS的条件之一,不稳定斑块病人倾向于行CEA手术。稳定性斑块者,则CAS与CEA均可选择。但这一原则来源于医师临床经验,缺少相应的循证医学证据支持。
我国基层医院颈动脉狭窄手术发展现状
CEA是颈动脉狭窄治疗的最经典术式,其治疗效果已在多项随机临床试验中得到充分证明。CAS优势在于创伤小、恢复快、脑神经损伤少、切口并发症发生少、颈部血肿发生率低,但其介入相关的并发症发生率高[9]。哪种治疗策略是最佳方案一直有争议。虽已有多项随机临床试验对两者比较,但临床试验往往在大型医疗中心展开,无法代表CAS和CEA在实际应用中的优劣。为了解我国颈动脉狭窄手术治疗概况,尤其是基层医院手术治疗现状,笔者联合北京中卫云医疗数据分析与应用技术研究院,通过大数据平台及手段,整理国内颈动脉狭窄手术诊疗数据,从地域分布、适合年龄、病人合并症、围术期卒中及死亡率等方面分析我国基层医院手术效果及指南依从性。数据来自2015年至2017年所有出院病人病案,总量为5 099.15万份,共采集住院病人CEA 2 698例、CAS 6 908例。数据分析人员本着可行、可及原则,对各项数据进行甄选、优化,希望为了解我国颈动脉狭窄手术情况及医疗服务能力评估提供借鉴。受现阶段病案填写质量限制,数据难免存在瑕疵。
一、地区分布特点
2 698例CEA共来自24个省区132家医院。开展手术量居前5位的医院手术例数占总手术量的35.03%。6 908例CAS来自28个省市自治区206家医院。开展手术量居前5位的医院手术例数占总手术量的22.70%。图1展示各省市自治区CEA和CAS开展医院比例直方图。从分析结果看,CAS的数量及分布范围均远高于CEA。开展CEA医院的比例普遍低于开展CAS医院,反映CEA准入门槛高、学习曲线长,以至于出现CAS超适应证的广泛应用。CEA和CAS开展医院比例直方图显示,CAS和CEA均存在地区发展不均衡的特点,其中CEA尤甚。
二、性别、年龄特征
2 698例实施CEA的病人中,男2 193例(81%),女505例。6 908例实施CAS的病人中,男5 481例(79.34%),女 1 424例,未注明性别者 3例。男性的颈动脉重建手术数量显著高于女性,这也与我国卒中及颈动脉狭窄发病率与死亡率的性别特点一致[5]。表1显示实施CEA和CAS病人的年龄构成。CEA及CAS均以61~70岁年龄段比例最高。70岁以上年龄段中,CAS的构成比高于CEA。CEA的平均年龄63.52岁,中位年龄64岁,CAS病人平均年龄64.50岁,中位年龄65岁。CAS病人的平均年龄和中位年龄均高于CEA,年龄结构更老龄化,与指南推荐的高龄病人倾向于选择CEA术式相矛盾。
三、合并症情况
糖尿病与冠心病为实施颈动脉血管重建术病人常见的合并症(见表2)。与CAS组相比,CEA组各项合并症病人占比均较低。此表说明我国基层医院倾向于为伴有合并症病人选择CAS,考虑可能与合并症病人耐受全身麻醉手术的能力较差、CEA术后心肌梗死发生率较CAS稍高有关。据指南及临床试验结果[11],CEA围术期后心肌梗死的发生率显著高于CAS。因此冠心病、房颤、肺心病、心肌病病人的推荐倾向于CAS。但对于慢性肾功能衰竭病人,造影剂可能对肾功能造成再次损伤,应综合病人情况谨慎选择。
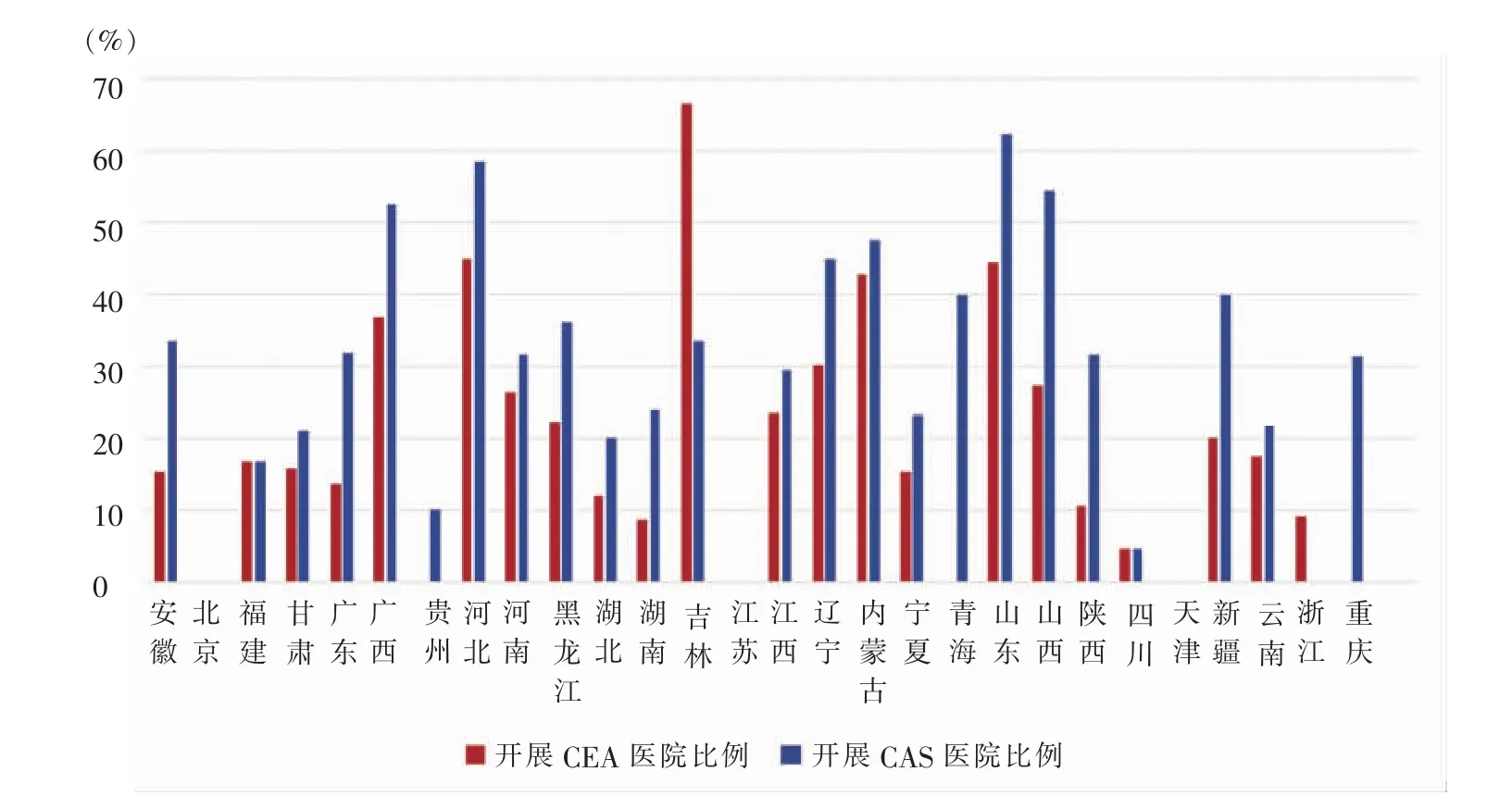
图1 我国28个省市自治区CEA/CAS开展医院比例直方图
四、围术期并发症发生情况
2 698例实施CEA的病人中,填写标准离院方式的有效数据为2 137例。其中死亡8例,死亡率0.37%。6 908例实施CAS的病人中,填写标准离院方式的有效数据为5 843例。其中死亡33例,死亡率0.56%。CAS的围术期死亡率略高于CEA,但<1%。CEA病人卒中12例,发生率0.44%(12/2 698)。CAS病人卒中 82例,发生率 1.19%(82/6 908)。CAS的围术期卒中发生率略高于CEA。CAS和CEA的围术期死亡与卒中发生率均低于指南规定的 3%(见表 3)。
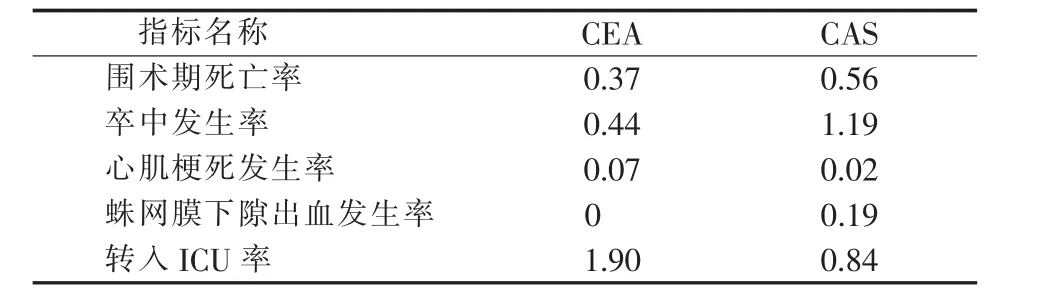
表3 CEA和CAS围术期并发症发生率(%)
2例CEA病人于住院期间发生急性心肌梗死,CEA围术期心肌梗死的发生率为0.07%(2/2 698)。CAS术后1例发生急性心肌梗死,围术期心肌梗死发生率0.02%。CEA围术期心肌梗死发生率略高于CAS,与美国Mayo的CREST结果相似[11]。
CEA病人术后转入ICU为1.90%,CAS病人术后转入ICU为0.84%。反映CEA手术难度较大,围术期病情危险度高。CEA组无一例出现蛛网膜下隙出血,CAS组蛛网膜下隙出血12例,发生率0.19%。
五、住院时间和住院费用
CEA病人平均住院时间为19.29 d,术后住院时间>7 d的病人占62.42%(见表4)。CAS病人平均住院时间为15.87 d,术后住院时间>7 d的病人占24.43%。CEA病人的住院时间显著长于CAS。与CEA相比,CAS具有术后恢复时间短的优点,有效减轻病人痛苦,尽快恢复体能和自理能力。

表4 两种颈动脉手术住院费用和时间
由于我国农村地区发病率、患病率增长迅速,经济因素不得不成为我国居民选择手术方式的重要考量。CEA手术病人的总住院费用、手术及麻醉费用均低于CAS,主要与CAS昂贵的支架费用相关(见表 4)。
总 结
对我国基层医院行颈动脉重建术病人的数据资料进行初步分析,发现我国基层医院现阶段CEA和CAS的手术死亡率和常见并发症之间差异无统计学意义。无论是CEA还是CAS,各医院的围术期死亡和卒中发生率均能控制在3%以内,基本符合指南要求。但也存在CEA发展不均衡、CAS应用范围过广、病人筛选不严格的问题。尤其对于伴有合并症的病人和高龄病人而言,选择CEA、CAS或内科综合治疗,还需综合考虑病人卒中、心肌梗死、肾功能衰竭的潜在风险,进行更谨慎的风险评估。从成本-效益的角度来看,CEA手术费用低,但术后恢复时间长。当两种术式均可作为备选方案时,可结合病人的实际情况提供个性化治疗方案。

