参麦袋泡茶的质量标准研究*
★ 向云亚 蓝荣 徐晶晶*
(厦门医学院/福建省中药精加工与健康产品开发研究室 福建 361023)
参麦袋泡茶由北沙参、麦冬、桔梗、菊花、西洋参、甘草6 味中药组成,具有养阴清肺,生津利咽的功效,适用于缓解咽干音哑和口干舌燥等症。为了有效控制制剂质量且保证临床疗效,本试验对该制剂的质量标准进行了研究,建立了袋泡茶中西洋参、菊花定性的薄层色谱鉴别方法,同时建立高效液相色谱法对袋泡茶中人参皂苷Re、人参皂苷Rb1的含量进行测定。
1 仪器与试药
1.1 仪器 Waters2695 型高效液相色谱仪(美国Waters 公司),XPE105 型1/10 万电子天平(梅特勒-托利多仪器有限公司),QEZ-100 高速粉碎机(浙江屹立工贸有限公司),WD-9403C 型紫外仪(北京市六一仪器厂),TH-II 型薄层加热器(上海科哲生化科技有限公司)。
1.2 试药 聚酰胺薄膜(浙江省台州市路桥四甲生化塑料厂),硅胶G 薄层板(青岛海洋化工有限公司),西洋参对照药材(批号:010-67095219)、菊花对照药材(批号:010-67095219)均购自中国食品药品检定研究院,拟人参皂苷F11 对照品(批号:wkp17081103)、人参皂苷Rb1 对照品(批号:wkp18020808)、人参皂苷Re 对照品(批号:wkp17091811)、人参皂苷Rg1 对照品(批号:wkp17111503)、绿原酸对照品(批号:wkp17112007)均购自四川省维克奇生物科技有限公司,参麦袋泡茶(自制,批号180510、180511、180512),乙腈为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 薄层色谱鉴别
2.1.1 西洋参 本品1 袋,取内容物,加甲醇25mL,加热回流30min,滤过,滤液蒸干,加水20ml 使残渣溶解,用水饱和的正丁醇振摇提取2 次,每次25mL,合并正丁醇提取液,用水饱和的正丁醇洗涤2 次,每次10mL,取正丁醇液,蒸干,残渣用甲醇2mL 使其溶解,作为供试品溶液[1-2]。按参麦袋泡茶处方,除去西洋参,模拟工艺同法制成阴性对照溶液。另取西洋参对照药材1g,按照上述同样的方法制成对照药材溶液。再取拟人参皂苷F11 对照品、人参皂苷Rb1、Re、Rg1 对照品适量,加甲醇制成各含2mg·mL-1的溶液,作为混合对照品溶液,待用。按照薄层色谱法(中国药典2015 年版通则0502),吸取供试品、阴性对照、对照药材以及混合对照品四种溶液各6µL,分别点于同一硅胶G 薄层板上,以在5℃~10℃放置12h 的三氯甲烷- 乙酸乙酯- 甲醇- 水(15∶40∶22∶10)的下层溶液为展开剂,展开后取出并晾干,喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,分别置于日光和紫外灯(365nm)下检视。从薄层色谱图可以看出:样品色谱在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点或荧光斑点,而阴性对照色谱在相应位置上无干扰(图1)。
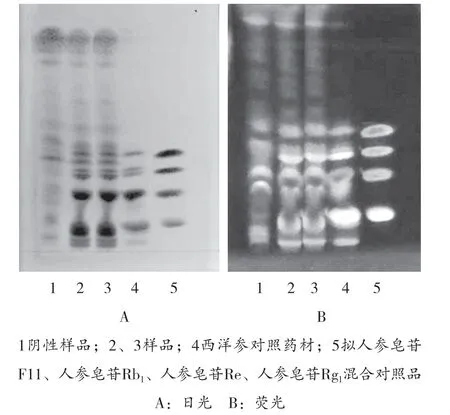
图1 西洋参薄层色谱图
2.1.2 菊花 本品1 袋,取内容物,加石油醚20 mL,超声处理10min,弃去石油醚,药挥干,加稀盐酸、乙酸乙酯1mL 和50mL,超声30min,滤过,滤液蒸干,残渣用甲醇1mL 使其溶解,作为供试品溶液[1]。按参麦袋泡茶处方,除去菊花,模拟工艺同法制备阴性对照溶液。另取菊花对照药材1 g,按照上述同样的方法制备对照药材溶液。取绿原酸对照品适量,用乙醇配制成每0.5mg·mL-1的对照品溶液。按照薄层色谱法(中国药典2015 年版通则0502),分别吸取供试品、阴性对照、对照药材以及混合对照品四种溶液各1µL,点于同一聚酰胺薄膜上,以甲苯- 乙酸乙酯-甲酸-冰醋酸-水(1∶15∶1∶1∶2)的上层溶液为展开剂,展开后取出并晾干,置紫外灯(365nm)下检视[3]。从薄层色谱图中可以看出:样品色谱与对照药材和对照品色谱相应的位置上,显示相同颜色的荧光斑点,而阴性对照色谱在相应位置上无干扰(图2)。

图2 菊花薄层色谱图
2.2 人参皂苷Re、人参皂苷Rb1含量测定
2.2.1 溶液的配制
2.2.1.1 对照品溶液的制备 精密称取人参皂苷Re、人参皂苷Rb1对照品各4.00、10.18mg,用甲醇定容到10mL 的容量瓶中,作为混合对照品溶液,放冰箱冷藏备用。
2.2.1.2 供试品溶液的制备 取制剂(批号:180510)1 袋,精密称定,置具塞三角瓶中,精密加入水饱和的正丁醇50mL,密塞,摇匀,称重,置水浴中加热回流提取1.5h,静置冷却,补足失重,摇匀,滤过。精密量取续滤液25mL,蒸干,用甲醇适量使残渣溶解后转移并定容到10mL 容量瓶中,摇匀,滤过,取续滤液,作为供试品溶液。
2.2.1.3 阴性样品溶液的制备 按处方量比例称取除西洋参外的其他药材制备阴性样品,并按照供试品溶液的制备方法制成阴性样品溶液。
2.2.2 色 谱 条 件 Kromasil C18色 谱 柱(4.6mm×250mm,5μm),流 动 相 为 乙 腈- 水,按表1 的流动相梯度洗脱,柱温30 ℃,流速1.0mL·min-1,检测波长为203nm[4-6],进样量10μL。分别吸取对照品溶液、供试品溶液、阴性样品溶液进行含量测定,供试品溶液与对照品溶液相应峰保留时间一致且各组分相邻成分之间分离度较好,阴性样品无干扰,见图3。

表1 人参皂苷Re、Rb1含量测定的流动相梯度
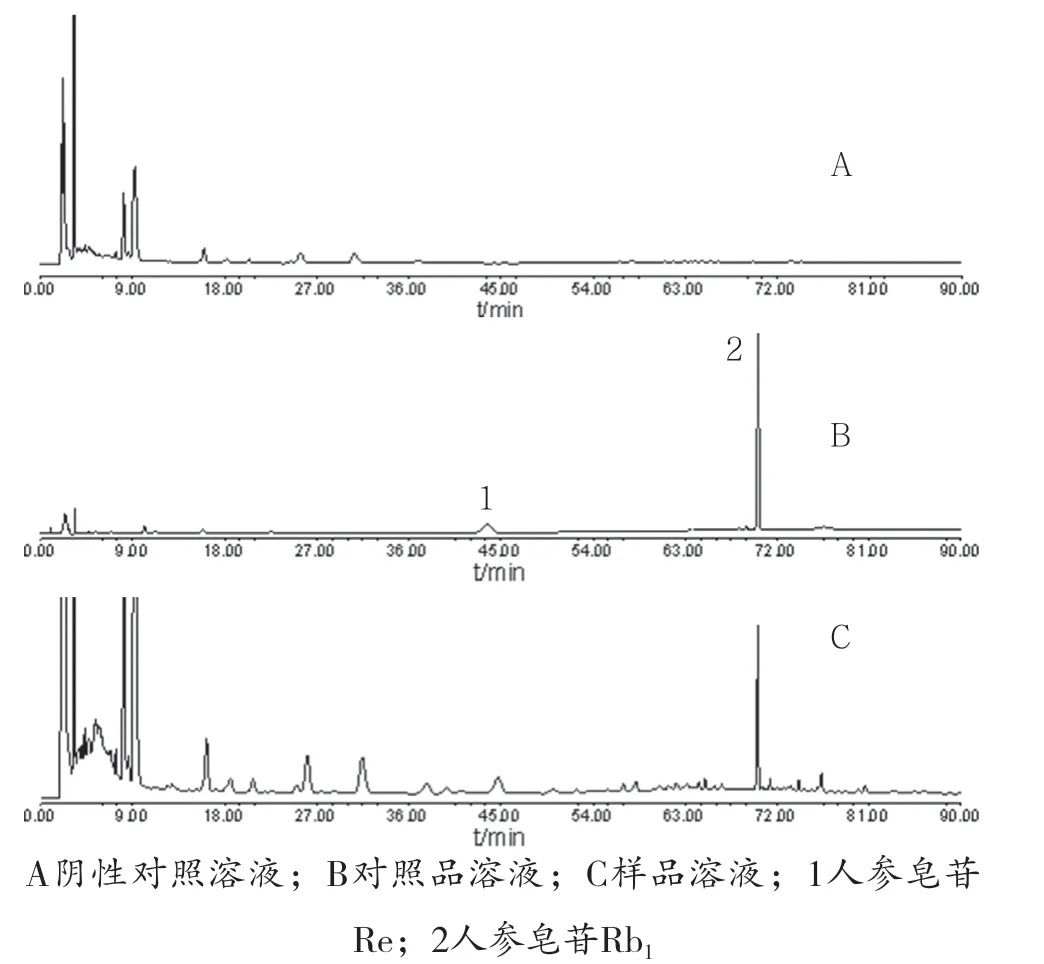
图3 三种溶液的高效液相色谱图
2.2.3 线性关系考察 分别精密吸取混合对照品溶液2、5、10、15、20、25µL 注入液相色谱仪进行含量测定,以质量为横坐标X,峰面积为纵坐标Y,求得人参皂苷Re 和人参皂苷Rb1的回归方程分别为:Y=236519X+7039.6(r=0.9999),Y=221521X-139554(r=0.9999),线性范围分别为0.800~10.000,2.216~25.450µg。
2.2.4 精密度实验 取混合对照品溶液重复进样6 次,记录峰面积。求得人参皂苷Re 和人参皂苷Rb1峰面积的RSD 分别为0.73%、0.36%,说明仪器精密度良好。
2.2.5 重复性实验 取供试品(批号:180510)共6 份,按供试品溶液制备方法制备,进行含量测定,求得人参皂苷Re 和人参皂苷Rb1含量的RSD 分别为1.60%、1.01%,表明该方法重复性良好。
2.2.6 稳定性实验 精密吸取供试品溶液10μL,分别于0、2、4、6、12、24h 进行测定,记录峰面积。测得人参皂苷Re 和人参皂苷Rb1峰面积的RSD 分别为1.34%、1.17%,表明供试品溶液在24h 内稳定性良好。
2.2.7 加样回收率实验 精密称取已知含量(批号:180510)的样品约0.5g,共6 份,分别置于具塞锥形瓶中,精密加入混合对照品溶液1mL,按照供试品溶液制备方法制备即得。过滤后取10μL 按“2.2.2”项下色谱条件进样,测定含量,计算平均加样回收率。求得人参皂苷Re 和人参皂苷Rb1的平均回收率分别为99.73%、102.37%;RSD 分别为1.32%、1.68%。见表2。
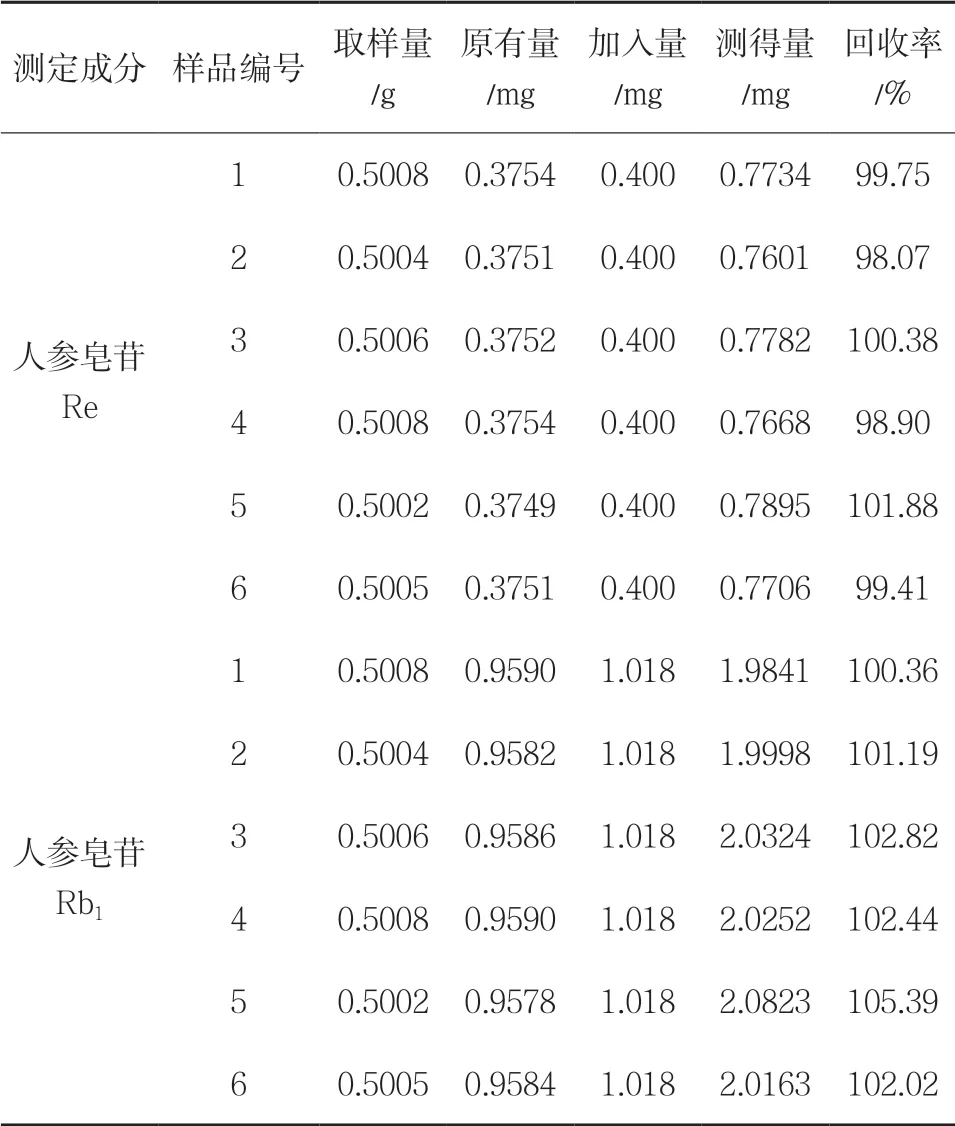
表2 人参皂苷Re和人参皂苷Rb1加样回收率实验
2.2.8 样品含量测定 取3 批(批号:180510、180511、180512)参麦袋泡茶制剂,按“2.2.1.2”项下方法制备供试品溶液,按“2.2.2”项下色谱条件进行含量测定。结果见表3。

表3 3批次参麦袋泡茶中人参皂苷Re、Rb1含量
3 讨论
3.1 薄层鉴别药材的选择 本制剂由北沙参、麦冬、桔梗、菊花、西洋参、甘草6 味中药组成,在对处方中的药材进行薄层鉴别过程中,除了西洋参和菊花外,其他药材未能出现达到符合要求的结果,故只将西洋参和菊花列入定性鉴别中。实验证明,西洋参和菊花的薄层鉴别斑点清晰,阴性无干扰,重复性良好。
3.2 含量测定指标性成分的选择 本研究最初选用人参皂苷Re、人参皂苷Rb1及人参皂苷Rg13 种成分作为制剂含量测定的指标性成分,在优化色谱条件过程中,发现其它成分对人参皂苷Rg1干扰较大,无法获得好的分离效果。人参皂苷Re、人参皂苷Rb1作为西洋参主要的指标性成分,在方法学考察中均符合要求,故重新选取人参皂苷Re、人参皂苷Rb1作为参麦袋泡茶的含量测定指标性成分。

