微孔钛网应用于犬牙槽骨增量术中的实验研究
蒋 斯 匙 莹 李 晔 陈玮璨 周 彪
牙槽骨缺损是在牙周组织出现病变时牙槽骨遭到破坏的结果,牙周组织呈慢性进行性病变,发展到后期可导致牙槽骨丧失,牙齿脱落[1]。牙周组织的丧失直接导致后期义齿修复困难。植骨术是一种能直接增加骨量的方法,临床多应用引导骨组织再生(guided bone regeneration,GBR)技术[2]。术中生物膜屏障选择十分重要,稳定性会影响成骨质量[3]。常用的生物膜屏障包括不可吸收膜与可吸收膜。可吸收膜操作简单,并在体内自然降解,在临床上较为常用。但其降解后的产物对骨再生的影响尚不完全明确。本实验通过建立牙槽骨缺损动物模型,选用可吸收的海奥口腔修复膜作为对照组,观察不可吸收的微孔钛网应用于GBR 术中的骨增量作用效果。
资料和方法
1.实验对象
选择6 只成年健康雄性杂种犬,体重16~20kg。饲养环境为:温度22℃左右,自然光照,单笼饲养,自由饮食水,饲养1 周。
2.实验方法
制备牙槽骨缺损模型:肌注速眠新Ⅱ(0.1ml/kg)麻醉,犬处于仰卧位,消毒铺巾,拔除每只犬左右侧下颌第四前臼齿并去除部分牙槽骨,建立1cm×1cm 的牙槽骨缺损模型。术后肌注青霉素40 万U/次,2 次/日,连续三天。禁食24h,术后1 周内喂流质食物。注意犬术区恢复情况,避免出现术区感染。
自体骨取骨:建立牙槽骨缺损模型4 周后,拔除每只犬左右侧上颌第四前臼齿并去除拔牙窝内牙槽间隔及部分牙槽骨,将取出的牙槽骨剪碎,加入生理盐水润湿、备用。
植骨:将每只犬的左侧下颌牙槽骨缺损区域作为第Ⅰ组,右侧作为第Ⅱ组。两组均给予GBR+自体骨移植术,并由同一手术医师操作。第Ⅰ组采用微孔钛网,第Ⅱ组采用海奥口腔修复膜。第Ⅰ组植骨手术具体方法:首先暴露牙槽骨缺损区域,在皮质骨上钻6 个小孔 ,紧密植入自体骨,微孔钛网覆盖。每只犬使用的微孔钛网均是根据制备后的牙槽骨缺损区形态定制塑形,钛钉固定,黏膜无张力缝合。第Ⅱ组与第Ⅰ组手术方法相同,将微孔钛网替换为海奥口腔修复膜。术后处理同前。
术后6 只犬均存活,术区正常愈合,无感染。将6 只犬分为 3 批,每批 2 只。分别于术后 4、8、12 周处死。最后一批犬被处死的前10d、前3d 分别通过静脉滴注给予茜素红、钙黄绿素与2%生理盐水以20:1 混合的2 种溶液,进行荧光标记,以观察骨矿化过程。这一方法的原理是骨矿化是以骨钙沉积为主要表现,与钙能结合的荧光标记物能直接反映骨钙沉积过程。手术解剖分离每只犬的下颌骨,固定于10%甲醛溶液中。每批处死的犬,首先进行大体标本观察牙槽骨缺损修复的情况,再将正常牙槽骨组织及植骨后牙槽骨部分硬组织制备成石蜡切片,采用Masson 染色法观察每只犬牙槽骨组织成骨情况:新生骨质红染少,成熟骨内红染多,即骨质越成熟,红染越多[4]。术后12 周处死的犬在切片染色前使用荧光显微镜观察骨矿化情况,计算骨矿化率,并增加HE 染色,以观察骨小梁新生情况。
3.观察指标
①两组植骨术后4 周、8 周、12 周大体标本观察结果,并测量每组牙槽嵴高度;②两组植骨术后4周、8 周、12 周硬组织 Masson 染色结果;③两组植骨术后12 周HE 染色骨小梁新生情况;④两组植骨术后12 周骨矿化率;⑤两组植骨术后12 周骨小梁数量、骨小梁厚度、骨体积。采用CT 三维重建方法,在制备切片前对12 周时处死的犬下颌牙槽骨缺损部位进行三维重建,并通过三维形态学定量测定牙槽骨缺损部位骨微结构参数,即骨小梁数量、骨小梁厚度、骨体积。
4.统计学方法
通过SPSS23.0 软件进行数据分析,计量资料组间比较采用独立样本t检验。以P<0.05 表示比较差异具有统计学意义。
结 果
1.两组植骨术后 4 周、8 周、12 周大体标本观察结果
下颌骨大体标本观察:术后4 周:第Ⅰ组微孔钛网固定良好,植骨区表面略有粗糙触感,移植骨与原骨未融合;第Ⅱ组胶原膜未分解,覆盖良好,植骨区表面触感光滑,移植骨与原骨未发生融合。术后8周:第Ⅰ组微孔钛网固定良好,植骨区表面形成新生软组织,移植骨与原骨之间表现出小部分融合;第Ⅱ组部分胶原膜被分解吸收,植骨区表面有新生软组织形成,移植骨与原骨之间界限与之前比略模糊。术后12 周:第I 组微孔钛网固定良好,植骨区表面明显新生软骨组织,移植骨与原骨之间大部分融合,无明显界限;第Ⅱ组大部分胶原膜被分解吸收,植骨区表面也形成明显新生软骨组织,移植骨与原骨之间界限模糊。
大体标本肉眼观察:术后12 周第Ⅰ组新生成骨面积略大于第Ⅱ组,新生成骨形态略优于第Ⅱ组,其它方面差异不明显。两组牙槽嵴高度比较,第Ⅰ组略高于第Ⅱ组,但无显著差异(P>0.05),见表1。
2.两组植骨术后 4 周、8 周、12 周硬组织切片染色结果比较(图1)。
3.两组植骨术后12 周HE 染色后骨小梁新生情况(图2)。
4.两组植骨术后12 周骨矿化率比较、荧光染色情况(表2、图 3)。
术后12 周第Ⅰ组骨矿化率略高于第Ⅱ组,但两组骨矿化率比较无显著差异(P>0.05)。
5.两组植骨术后12 周骨小梁数量、骨小梁厚度、骨体积比较。
两组骨小梁数量、骨小梁厚度、骨体积比较均无显著差异(P>0.05),见表3。
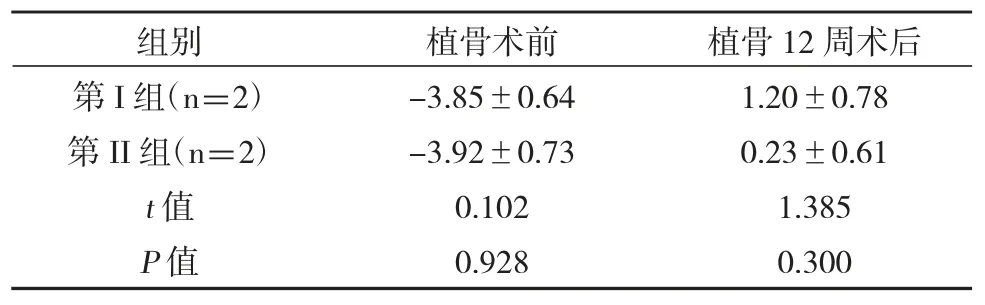
表1 两组植骨前与植骨后12 周牙槽嵴高度比较(mm)
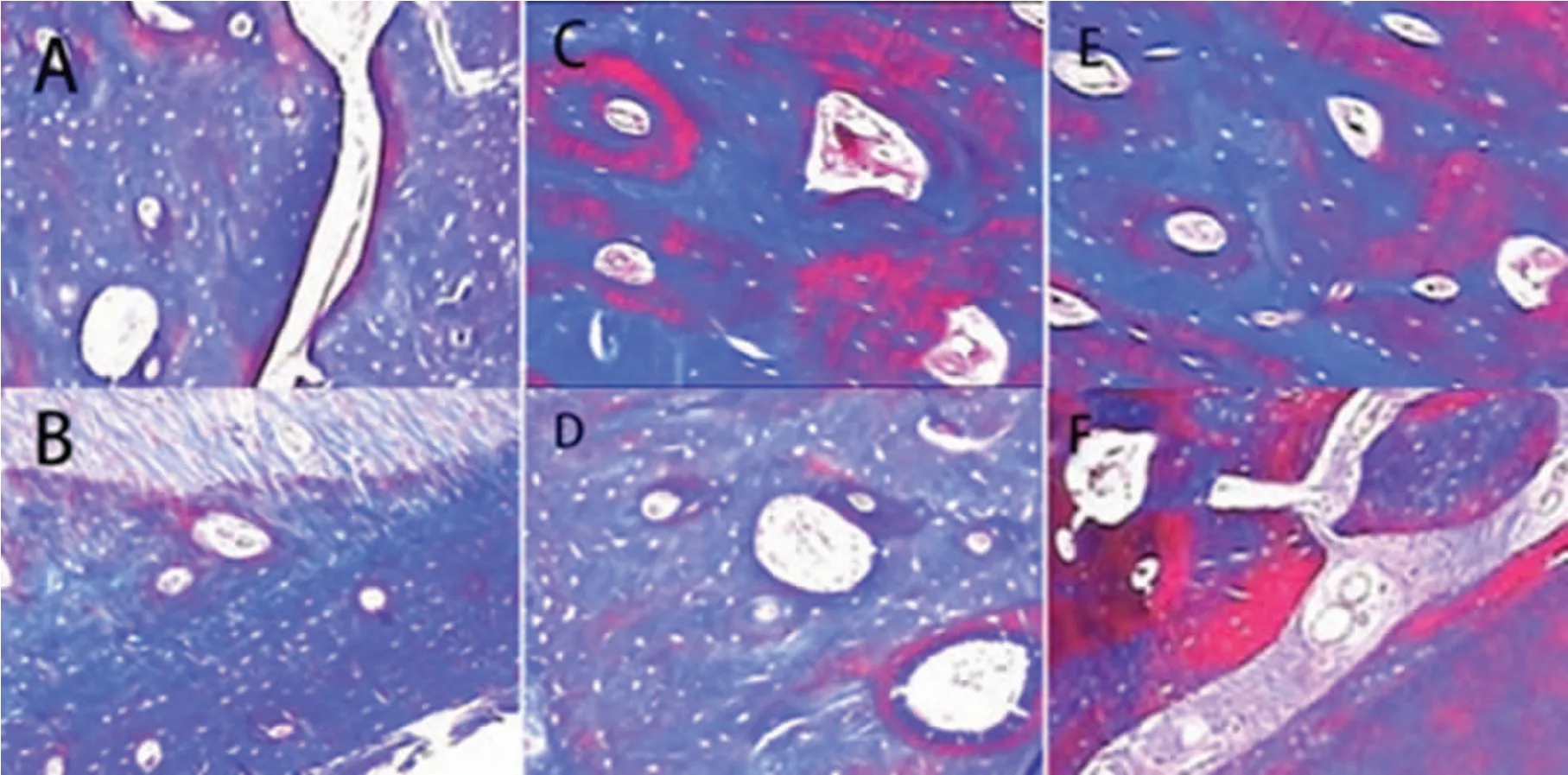
图1 两组Masson 染色结果差异不明显(Masson 染色 ×100)

图2 HE 染色×100
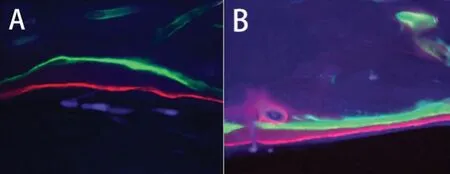
图3 荧光染色
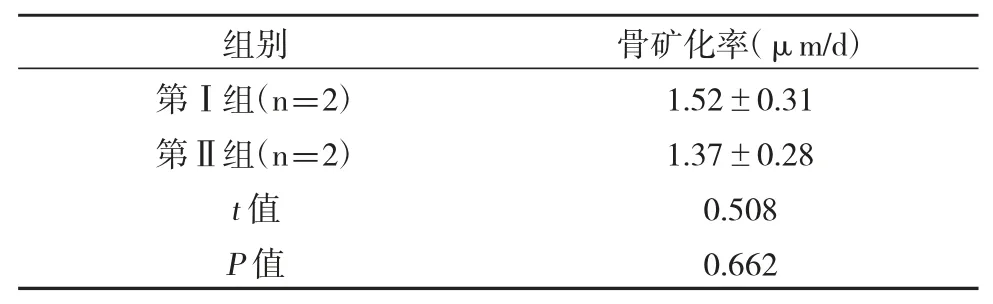
表2 两组植骨术后12 周骨矿化率比较

表3 两组植骨术后12 周骨小梁数量、骨小梁厚度、骨体积比较
讨 论
目前GBR 技术已广泛用于口腔种植手术中,此技术利用膜屏障,在骨缺损区域使植入的骨与原骨长时间保持一个独立的空间,阻止周围增殖速度快的成纤维细胞等快速侵入,给生长较慢的成骨细胞提供一个良好的生长环境,以促进骨再生[5]。因此生物膜屏障材料决定了GBR 手术后再生骨的质量。
理想的GBR 生物膜屏障必须具有较好的组织相容性、骨诱导性、骨传导性、可降解性,并可与其它生长因子复合作用以诱导新骨生成[6]。在长期的骨缺损治疗研究中,临床将生物膜屏障分为不可吸收与可吸收两类,可吸收膜是指可在体内自然降解被吸收,无需二次手术取出。不可吸收膜需二次手术取出[7]。可吸收膜目前常见的材料包括胶原膜、聚乳酸膜等,这些膜都属于高分子材料。虽然可吸收膜具有被吸收的特性,但其降解后的产物对再生骨是否有影响、降解速度是否满足骨再生条件等问题目前尚无得到明确的研究结论[8]。同时胶原膜还缺乏刚度,其对生长速度快的成纤维细胞可能不具有更好的阻挡作用。不可吸收膜虽然不可在体内被吸收,但其本身不会对骨再生产生影响,且具有可定制的优点[9]。实验中应用的微孔钛网有良好的生物相容性、三维立体多孔结构、完全可塑性和稳定的机械强度等特点[10,11]:可根据骨缺损区域大小及形状,进行个性化塑形;钛纤维三维空间结构,可诱导骨原细胞向成骨细胞分化。但其的缺点也很明显,需要二次手术取出增加患者痛苦、精神及经济负担,手术难度大,术后有伤口裂开甚至感染的风险。
本实验建立犬的双侧下颌牙槽骨缺损模型,采用不同GBR 膜分别对左右侧缺损牙槽骨行GBR+自体骨植骨术。发现在植骨术后4 周、8 周的大体标本观察结果差异不明显。术后12 周观察到两组均有新生骨形成,使用微孔钛网的第I 组新生成骨面积略大于第Ⅱ组,新生成骨形态略优于第Ⅱ组,两组牙槽嵴高度比较无显著差异。这可能是由于微孔钛网的网孔支架有利于新生软组织的附着,网孔便于血液通过,为新生组织提供血供,促进新骨生成。同时微孔钛网较可吸收胶原膜具有更好的刚性,能有效阻止成纤维细胞侵入,利于成骨细胞生长。通过术后 4 周、8 周、12 周的犬硬组织 Masson 染色,发现两组新生骨组织均随着时间推移而增多。术后12周HE 染色发现两组骨小梁大量生成,排列成网状,进一步证明在GBR 植骨术中覆盖微孔钛网或可吸收胶原膜均可获得良好修复效果。术后12 周两组骨矿化沉积率比较无显著差异,骨微结构中的骨小梁数量、骨小梁厚度、骨体积比较差异也不明显,表示两种膜在骨钙沉积、骨再生过程中的作用具有一致性。仅在新生骨面积及形态上,微孔钛网稍有优势,这与可吸收胶原膜材料本身刚性小、质地软,而微孔钛网本身弹性好、可塑性强、刚性好有关。
综上所述,微孔钛网与可吸收胶原膜在植骨手术中均可发挥有效促进骨再生作用,且各具优点。微孔钛网对新生骨的形态把控较好,能长时间维持新生骨形态及稳定,但需二次手术取出,增加患者负担。临床应根据患者骨缺损具体情况,合理选择可吸收与不可吸收膜,以保证术后能达到最佳的成骨效果。

