碳化法制备球霰石碳酸钙微球及形成机理
赵 历,卓民权,龚福忠,王 俊,阮 恒,李开成,李艳琳
(1.广西大学化学化工学院,广西南宁530004;2.广西化工研究院有限公司;3.广西新晶科技有限公司)
碳酸钙是自然界中最丰富的非硅质矿物,有3 种常见晶型:球霰石(vaterite)、文石(aragonite)、方解石(calcite)。球霰石型碳酸钙具有生物相容性好、孔状结构、比表面积大、密度小等特点,是一种理想的生物医学材料,近年来受到国内外研究者的广泛关注[1-4]。目前,球霰石型碳酸钙的制备主要采用溶液法(或称复分解法)和碳化法,两种方法基本都是以CaCl2为原料,其中溶液法是在CaCl2-MCO3反应体系中加入少量晶型控制剂(无机/有机物)制备球霰石型碳酸钙[3-16],而碳化法则是将CO2气体通入碱性CaCl2溶液中(用NH3·H2O 调节pH 或添加有机物)制备球霰石型碳酸钙[3,11-18]。碳化法具有操作简单、成本低以及产品收率高、纯度高等优点,是目前工业上采用的最经济的方法,在工业上得到了广泛应用[1,3,15,19]。球霰石的缺点是其热力学不稳定性,在含水介质中容易自发转变为方解石[3-5],因此球霰石型碳酸钙的控制合成是其规模化生产的关键。
合成的球霰石型碳酸钙通常为球形,也有圆盘形、薄片形、六角形、透镜形等,其中球形的球霰石型碳酸钙最有应用前景[4,10-11,14,16]。根据文献报道,实验室研究中采用溶液法制备单分散球霰石型碳酸钙较多,因为溶液法操作简单、工艺条件容易控制[4,15,20];采用碳化法制备分散球霰石型碳酸钙很少,因为碳化法的工艺条件不容易控制、 所得到的球霰石型碳酸钙要么纯度不够(为球霰石和方解石的混合物),要么颗粒大小不均匀[11-18,21],因此制备形貌规整、粒度均匀的单分散纯球霰石型碳酸钙仍然是一个值得研究的问题。影响生成球霰石型碳酸钙的因素很多,如料液浓度、溶液pH、CO2气体流速、反应温度、反应时间、搅拌方式等,但归结起来主要是两个方面:一方面是CO2过饱和度;另一方面是碳酸钙晶粒的界面能。高CO2过饱和度和低碳酸钙晶粒界面能有利于球霰石型碳酸钙的生成[22-26]。提高CO2过饱和度可以通过提高溶液初始pH、增大通入CO2气体压力(提高CO2气体流速)来实现,但是pH 过高会促进方解石碳酸钙的形成。通过添加外加剂(无机/有机物)可以降低碳酸钙晶粒界面能,但是会增加生产成本、增加操作程序(多次洗涤)、产物中带来杂质等[21-23]。
普通碳化法制备球霰石型碳酸钙是以CaCl2-NH3-CO2为反应体系,将CO2气体以直接鼓泡方式通入反应溶液中,CO2气泡大小不均匀、溶液中CO2过饱和度不高、反应时间较长,难以得到单分散纯球霰石型碳酸钙。为克服普通碳化法不足,笔者采用分散鼓泡方式,即将CO2气体先经过孔径大小均匀的多孔分散器分散形成大量的小气泡再进入反应溶液中,通过增大气-液接触面积来提高溶液中CO2过饱和度,制备了颗粒大小均匀、形貌规整的纯球霰石型碳酸钙微球,考察了反应初始和终止pH、反应初始温度、CO2气体流速等对碳酸钙晶型、形貌和粒径的影响,并提出了球霰石微球形成机理。
1 实验部分
1.1 试剂
氯化钙(CaCl2·2H2O,AR),浓氨水(AR,质量分数为25%~28%),盐酸(AR),CO2气体(工业级),气盘石(市售,直径为80 mm,孔径为150~200 μm),纯净水(实验室自制)。
1.2 制备方法
实验装置见图1。将500 mL 0.1 mol/L 的CaCl2溶液加入碳化柱中,加入一定量浓氨水,用盐酸调节pH 至设定值。打开CO2气瓶,使CO2以一定流速通入反应体系中,当体系pH 降低至指定值时停止通气,将浆料过滤,水洗3 次,将滤饼置于80 ℃烘箱中干燥24 h。已有研究表明,当溶液初始pH 为12 以上时,因生成的碳酸钙晶核小、溶解度大,碳酸钙晶核经溶解再重结晶易转变成方解石晶型[23-24,27],因此实验溶液初始pH 控制为不高于11,同时为忽略氨水浓度的影响将浓氨水加入量固定为6.0 mL。
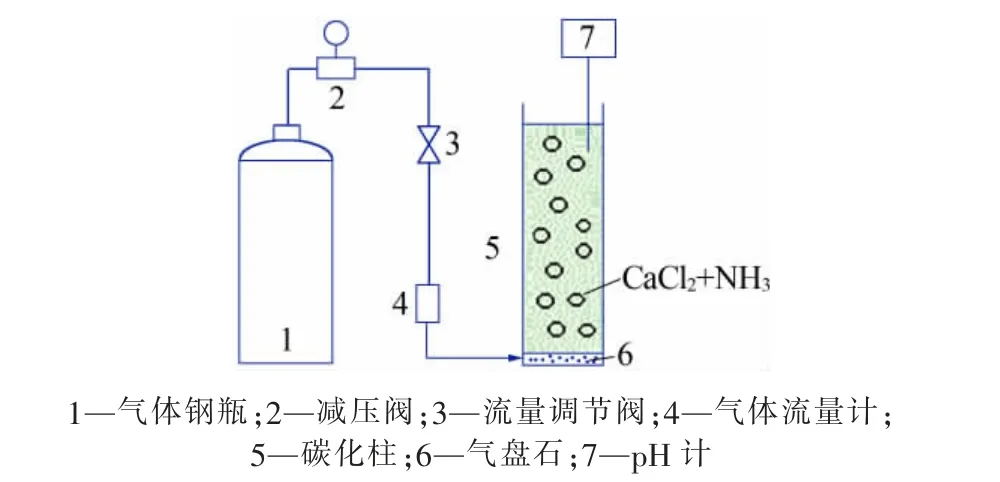
图1 制备中空碳酸钙微球的实验装置
1.3 主要仪器设备
SU8000 型场发射扫描电子显微镜(FE-SEM);S3400N 型扫描电子显微镜(SEM);Ultima Ⅳ型X 射线衍射仪;Nexus470 型傅里叶变换红外分光光度计;LS603 型激光粒度分析仪;DELTA320 型pH 计。
2 结果与讨论
2.1 不同鼓泡方式制备碳酸钙微球形貌和大小比较
图2a、b 分别为直接、分散鼓泡碳化法制备球霰石型碳酸钙SEM 照片。反应条件:反应初始pH 为10.0,反应终止pH 为8.0,CO2气体流速为1 L/min,反应初始温度为25 ℃。由图2 看出,直接鼓泡碳化法制备的碳酸钙颗粒大小不均匀,粒径为1~10 μm,形貌不够规整; 分散鼓泡碳化法制备的碳酸钙颗粒大小比较均匀,大部分颗粒粒径为5~6 μm,形貌更为规整。这是由于,与直接鼓泡碳化法相比,分散鼓泡碳化法产生的CO2气泡数量多且大小比较均匀,气液接触面积大,使CO2气体在溶液中的溶解度和过饱和度更高,另外对溶液的搅拌作用得到加强,因此更有利于形成大小均匀的球霰石型碳酸钙微球。

图2 直接鼓泡碳化法(a)和分散鼓泡碳化法(b)制备碳酸钙微球SEM 照片
2.2 反应初始pH 对碳酸钙颗粒形貌和大小的影响
图3 为不同反应初始pH 制备球霰石型碳酸钙SEM 照片。其他条件:反应终止pH 为7.0,CO2气体流速为1 L/min,反应初始温度为25 ℃。从图3 看出,反应初始pH 为11.0 时,碳酸钙颗粒为球状但大小不均匀,有少量团聚;反应初始pH 为10.5 时,碳酸钙颗粒变为比较规则的球状,分散性较好,基本无团聚;反应初始pH 为10.0 和9.5 时,碳酸钙颗粒变为更加规则的球状,无团聚,基本上为单分散颗粒,大小比较均匀,粒径为5~6 μm。

图3 不同反应初始pH 制备碳酸钙SEM 照片
2.3 反应终止pH 对碳酸钙晶型和颗粒大小的影响
图4 为不同反应终止pH 制备球霰石型碳酸钙SEM 照片。其他条件:反应初始pH 为10.0,CO2气体流速为1 L/min,反应初始温度为25 ℃。由图4 可知,反应终止pH 为8.5~6.0 时都可得到大小比较均匀的球形碳酸钙。反应终止pH 为8.5 和8.0 时颗粒粒径相对较小,平均为3~4 μm;反应终止pH 降低至7.0 时颗粒变大,平均粒径为5~6 μm; 反应终止pH继续降至6.0 时颗粒又略有减小,可能是碳酸钙有微量溶解生成Ca(HCO3)2所致,同时可看到有微量方解石颗粒。图5 为不同反应终止pH 制备碳酸钙XRD 谱图。反应终止pH 为8.5~7.0 时产物各衍射峰均与球霰石型碳酸钙标准谱图PDF#33-0268相一致,反应终止pH 为6.0 时在2θ 为29.4°处出现方解石C(104)衍射峰[8,25,27-29],其余均为球霰石衍射峰。样品XRD 结果与SEM 结果相吻合。

图4 不同反应终止pH 制备碳酸钙SEM 照片
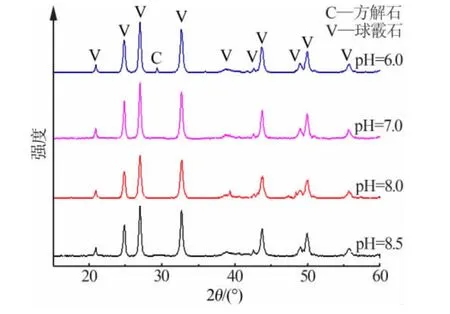
图5 不同反应终止pH 制备碳酸钙XRD 谱图
2.4 CO2气体流速对碳酸钙颗粒形貌和大小的影响

图6 不同CO2 气体流速制备碳酸钙SEM 照片
图6 为不同CO2气体流速制备球霰石型碳酸钙SEM 照片。其他条件:反应初始pH 为10.0,反应终止pH 为7.0,反应初始温度为25 ℃。从图6 可知,当CO2气体流速为0.6 L/min 和1 L/min 时可得到大小比较均匀的球霰石型碳酸钙微球,而当CO2气体流速为0.2 L/min 时得到的碳酸钙一部分为球形、一部分为咖啡豆形、一部分为花瓣球形,说明CO2气体流速大有利于得到大小和形貌均匀的球霰石型碳酸钙微球,这与文献[23,30]的结论一致。这是由于,CO2气体流速小时CO2气体溶解度小,溶液中CO32-浓度低,会促进球霰石的溶解并再重结晶向方解石转变[28]。但是本文中即使在0.2 L/min 的低CO2流速下也未看到方解石出现(图6a),这主要是采用了分散鼓泡方式使CO2气体溶解度增大。CO2气体流速增大后,CO2气体在溶液中的过饱和度随之增大,因此 越 容 易 形 成 规 整 的 球 形 颗 粒[17,31-32];同 时 溶 液 内部传质过程得到强化,使溶液中各部分的和Ca2+浓度均匀,CaCO3晶核的成长速率也大致相同,这也有助于形成大小均匀的球霰石型碳酸钙颗粒。
2.5 反应初始温度对碳酸钙颗粒形貌和大小的影响
在CaCl2-NH3·H2O-CO2体 系 中 生 成CaCO3的反应过程是放热反应,因此只能考察反应初始温度对碳酸钙颗粒形貌和大小的影响(反应初始pH 为10.0,反应终止pH 为7.0,CO2气体流速为1 L/min)。图7a~e 为反应初始温度为10~30 ℃制备碳酸钙的SEM 照片。由图7 可知,当反应初始温度为5~20 ℃时制备的碳酸钙为纯球霰石微球,反应初始温度为25 ℃时制备的碳酸钙有少量方解石出现,反应初始温度为30 ℃时制备的碳酸钙方解石数量有所增加。说明反应初始温度升高促进了球霰石向方解石的转化,反应温度低有利于球霰石的生成与稳定,这一结果与文献[27,33]的结论基本一致,不同的是本文考察的是反应起始温度的影响。由于碳酸钙生成反应是放热反应,初始温度越高CO2气体溶解度减小,不利于球霰石的生成,同时反应过程中体系温度也进一步升高导致球霰石的溶解度增大,溶解的球霰石再结晶就形成了方解石。

图7 不同反应初始温度制备碳酸钙SEM 照片
2.6 球霰石型碳酸钙微球的精细结构
图8a、b、c 分别为球霰石型碳酸钙微球的SEM、TEM 和FE-SEM 照片。由图8a 破碎的半微球可以看出球霰石型碳酸钙微球内部具有一定的小体积空间,直径约为1.2 μm、壁厚约为1 μm,表明合成的球霰石型碳酸钙微球形成了中空结构,但内部空间体积较小,这也可以从图8b 的TEM 照片得到证实。图8c 表明碳酸钙微球表面由鳞片状颗粒聚集而成,与文献[3,34]报道结果一致。

图8 球霰石型碳酸钙微球SEM、TEM 和FE-SEM 照片
2.7 红外光谱(FT-IR)表征
图9 为碳酸钙微球的红外光谱(FT-IR)图。从图9 看出,在1471.03、1088.49、744.63、875.51 cm-1处的特征峰分别对应CO32-的反对称伸缩、 对称伸缩、面外弯曲、面内弯曲。这些特征峰与文献的结果一致,未出现710、713 cm-1的文石和方解石特征峰[10,17,21,31,34-35],表明合成的产品为纯球霰石型碳酸钙。

图9 碳酸钙微球的FT-IR 图
2.8 反应机理探讨
在CaCl2-CO2-NH3·H2O 体系中存在如下化学反应[25]:

上述碳化反应中CO2气体溶解是控制步骤。CO2气体溶解速率(rA)与溶液pH 关系见式(5)[25,35]:
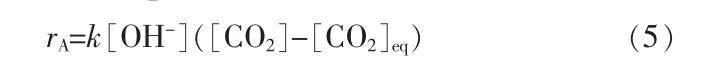
式中:[OH-]为溶液中OH-的浓度;[CO2]为未达到平衡时CO2的浓度;[CO2]eq为平衡时CO2的浓度;k为速率常数。
根据经典成核理论,成核速率与过饱和度的关系可用Gibbs-Thomson[18,28]表示:
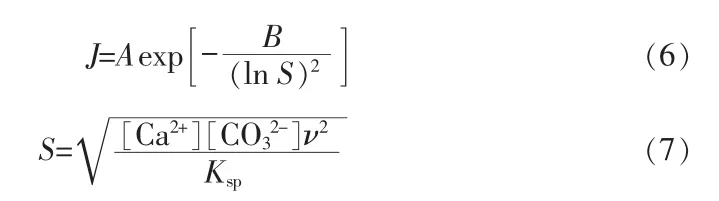
式 中:J 为 成 核 速 率;S 为CO2的 过 饱 和 度;Ksp为CaCO3的溶度积;ν 为二价离子的活度系数;A 为常数;B 表示形成临界大小晶核的热力学能垒,可用式(8)表示:

式中:γ 为界面自由能;ρ 为晶核密度;κ 为Boltzmann常数;T 为绝对温度。
式(5)没有考虑通入的CO2气体的气泡大小对溶解速率的影响。很显然通入的CO2气体产生的气泡越小,气-液接触面积越大,CO2的溶解速率越快。因此式(5)应修正为:
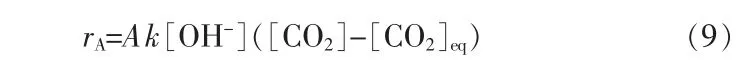
式中:A 为与CO2气泡/液体接触面积有关的参数。采用分散鼓泡方式时A 值显著增大,CO2气体的溶解速率和CO2的过饱和度S 也显著增大,因此更有利于球霰石型碳酸钙的生成。当氨水过量时,CO2和NH3可发生如下反应[20]:
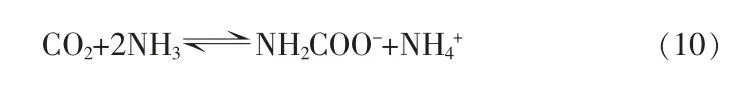
生成的氨基甲酸根(NH2COO-)吸附在新生成的碳酸钙晶核表面并降低形成球霰石型碳酸钙晶核的热力学能垒(B)。根据“奥斯特瓦尔德一步规则(Ostwald step rule)”,在高过饱和状态下同质多形体之间的界面能之差是主要支配作用,这种支配作用促进了亚稳态球霰石型碳酸钙的形成,同时也抑制或延缓方解石的形成[24]。可见过量的NH3和高CO2过饱和度是形成球霰石型碳酸钙的必要条件。
对于初始pH 的影响,由式(5)和(6)可知,溶液pH 越高CO2气体溶解速率越快、CO2过饱和度S 越大、 成核速率J 也越快,因此生成的晶核数量就越多,但同时其粒径也越小。这与实验观察到的现象是一致的,即通入CO2气体的初始阶段溶液中没有观察到明显的白色碳酸钙沉淀。由于新生成的CaCO3晶核为界面能高的无定形碳酸钙(ACC),ACC 会很快转变成球霰石型碳酸钙并通过形成联系紧密的气-液-固3 相状态而稳定存在,这种3 相状态将力图维持球状以使表面积和界面自由能最小[36]。另外进一步通入CO2气体后,随着反应的进行溶液pH进一步降低,碳酸钙晶核的ξ 电位也逐渐减小(pH=11.2 时ξ≈-28 mV,pH=8.5 时ξ≈-12 mV,等电点为pH≈7.5[37]),晶核间相互排斥作用力减小,因此新生成的ACC 晶核在转变为球霰石的同时又不断在气-液-固3 相状态的球状微粒表面聚沉而成长为微米级大颗粒,此时会看到大量的白色碳酸钙沉淀,而且碳酸钙颗粒内部形成一个小的空腔,见图8a 的SEM 照片。球霰石型碳酸钙的形成机理一般有两种,一种是纳米颗粒聚集机理,一种是晶体生长机理。聚集机理适用于核-壳微球和中空球霰石微球[3]。根据以上分析讨论,本文制备的单分散球霰石碳酸钙微球的形成符合聚集机理并可用图10 表示。
3 结论
1)以CaCl2-NH3-CO2为反应体系,采用分散鼓泡碳化法成功制备了单分散的形貌规整的纯球霰石型碳酸钙微球。该方法无需添加剂,保留了传统碳化法设备简单、易于操作、成本低、纯度高等特点。2)在反应初始pH=9.5~11.0 范围内,pH 越高碳酸钙微球越不均匀,相反pH 越低碳酸钙微球越均匀,而且粒径也越大。当反应初始pH=10.0、反应终止pH=8.5~7.0 时,反应终止pH 越高碳酸钙微球粒径越小,反应终止pH=7.0 时碳酸钙微球粒径最大。3)采用分散鼓泡方式和增加CO2气体流量均有利于提高CO2气体的溶解度和溶液过饱和度,并强化溶液传质过程,避免局部浓度不均现象,有利于形成形貌规则、大小均匀的球霰石型碳酸钙微球。4) 对于CaCl2-NH3-CO2反应体系,采用分散鼓泡法制备球霰石型碳酸钙微球的最佳工艺条件:反应初始pH=10.0,反应终止pH=7.0,CO2流速为1 L/min。

