氧化铜/二氧化硅催化苯直接胺化生成苯胺的性能
余天华,覃敏,何杰芳,许婷婷
(贵州师范大学生命科学学院,贵州 贵阳 550001)
有机胺类化合物是一类重要的工业原料[1]。苯胺是典型的芳胺类化合物,是重要化工产品中间体[2-3]。随着科学技术发展,传统工业中以铁粉还原硝基苯制备苯胺的方法正逐步被氢化还硝基苯中的硝基、氨基取代卤苯和苯酚中的卤原子及羟基等方法取代,且在降低能耗、减少污染和节约成本等方面获得显著的进步,但仍存在步骤复杂、条件苛刻、原子利用率低和对环境不友好等缺点[3-6]。
1917年,Wibant报道了以Ni/NiO为催化剂,苯与氨气直接反应合成苯胺的方法[7]。尽管反应条件苛刻,且受热力学平衡的限制,苯的转化率非常低,但其简单的反应步骤和高的原子利用率,获得广大学者的关注[8]。迄今为止,一系列有利于反应向生成苯胺方向移动的物理和化学方法相继被报道,但仍限于实验研究[9,10]。羟胺是一种理想的胺化剂,随着近年羟胺制备方法的突破[11],其已被应用于胺化等相关领域。在偏钒酸钠[12]、Cu-amine-MCM-41[13]等的催化下,苯与羟胺能直接反应生成苯胺,且具有较高的收率和选择性。但偏钒酸钠等为催化剂的均相反应体系,催化剂与产物的分离和回收困难;而MCM-41为载体的多相反应体系,催化剂制备复杂,反应中剧烈的物理搅拌、液固界面和溶剂等作用,导致无定型的孔壁易破碎,活性组分流失严重,难重复使用[14]。
前期工作发现,以溶胶-凝胶法合成的具有介孔和MFI结构的SiO2(MS-1)用做载体时,有利于活性组分Cu在其表面的分散,液相反应中稳定性强,对芳环C—H有良好的活化性能[15]。本研究以MS-1,实验室合成的介孔SiO2(M-1)和购买的介孔SiO2(M-2)为载体,通过浸渍法,制备系列Cu基催化剂,运用X射线衍射(XRD)、透射电子显微镜(TEM)和傅里叶红外光谱(FT-IR)等方法对样品结构和表面Cu的物种进行分析;结合其对羟胺直接胺化苯合成苯胺的催化性能,探究催化剂中的主要活性物种,载体结构、催化剂稳定性和活性之间的相互关系;为获得对芳环中C-H活化效果好、稳定性强、制备简单和易分离的新催化剂和绿色的、可持续合成伯胺类化合物的新方法提供理论依据。
1 实验部分
1.1 原料与仪器
四丙基氢氧化铵(TPAOH),分析纯,上海达瑞化工试剂厂;十六烷基三甲基溴化铵(CTAB),异丙醇(IPA),正硅酸乙酯(TEOS),Cu(NO3)3·6H2O,乙酸,盐酸羟胺,苯和苯胺,均为分析纯,成都科龙化工试剂厂;M-2,分析纯,青岛鑫昶来硅胶有限公司,用前在823 K下焙烧 4 h。
LTD DX-1000 CSC型X射线衍射仪,丹东方圆仪器有限公司;FEI company Tecnai G220 Stwin型透射电子显微镜,美国FEI公司;Micromeritics Trisar3020型比表面积和孔径分析仪(BET),美国Micromeritics公司;IRIS Advantage ER/S型等离子原子发射光谱仪(ICP),美国Thermo公司;TU1901型紫外光谱仪(DR UV-vis),北京普析通用仪器有限责任公司;Nicolet Nexus 670型傅里叶红外光谱仪(FT-IR),美国Nicolet公司;AXIS Ultra DLD(KRATOS)型X射线电子能谱(XPS),日本岛津公司。
1.2 样品的制备[15]
室温、搅拌且保持溶液透明条件下,在48.0 mL TEOS中依次滴加25.0 mL IPA和160.0 mL质量分数为10%的TPAOH溶液,加热至77 ℃,维持溶液体积不变下水解8 h,冷却,强搅拌下加入10.0 mL CTAB的 IPA溶液,继续搅拌8 h后,转移至高压反应釜,N2保护和175 ℃下晶化168 h,过滤、洗涤、烘干后的固体,以5 ℃/min的升温速率升至550 ℃并焙烧 10 h,获得白色的MS-1。
室温搅拌下,在135.0 mL质量分数为1%的NaOH溶液中依次加入4.50 g CTAB和28.0 mL TEOS,保持溶液pH=11下搅拌2 h,转移至高压反应釜,N2保护和110 ℃下水解120 h。后续处理同上,获得白色的M-1。
取载体置于支口试管,抽至压力为2.7 kPa,保持0.5 h,加入等体积所需浓度的Cu(NO3)2溶液,静置24 h,真空干燥。后续处理同上,获得系列Cu基催化剂(未标注Cu含量的样品,w(Cu)=2.5%)。
1.3 样品的表征
采用XRD和TEM对样品的形貌和物相进行分析;采用BET和ICP对样品表面积、孔结构及Cu含量进行分析;采用DR UV-vis、FT-IR和XPS对样品中的Cu物种进行分析。
1.4 胺化反应
在50 mL圆底烧瓶,依次加入一定量的催化剂,溶剂和盐酸羟胺,常温下搅拌5 min,加1 mmol苯,回流条件下,加热到设定温度反应完成后,冷却,用NaOH溶液中和并过滤,以乙腈溶解有机相后定容。采用乙腈和水为流动相,用配有C-18和紫外检测器的Waters1525P 型HPLC对产物进行分析。
2 结果与讨论
2.1 样品表征
2.1.1 形貌及物相分析
图1为w(Cu)=2.5%的样品及其使用后的XRD谱。
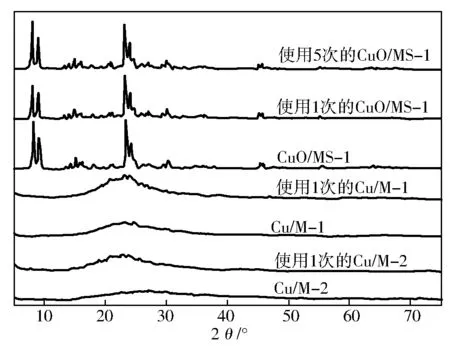
图1 样品的XRD谱
由图1可知,未使用、使用1和5次的CuO/MS-1,在2θ为7° ~9°,23° ~25°和45°均有MFI结构的特征衍射峰,且强度基本相同,表明具有高晶化度的CuO/MS-1在胺化反应体系中稳定性强。CuO/M-1和CuO/M-2在2θ为22.5°时有一弱的宽峰,使用1次后,峰强度明显增加,表明其为无定形结构,胺化反应中,Cu物种的流失严重[16]。所有样品,在2θ为43.2°、50.4°和74.1°处,均无衍射峰,说明制备过程中Cu的分散度高,反应中也没发生Cu的聚集[15]。

图2 样品的TEM照片
图2为w(Cu)=2.5%的样品及其使用后的TEM照片。CuO/MS-1(a)照片中,可观察到样品中MFI结构典型的单斜晶纹理和规则的孔道。CuO/M-1(b)和CuO/M-2(c)照片中,样品呈现蠕虫状孔道和海绵状无定型结构。使用后CuO/MS-1(d)的结构基本不变,而CuO/M-1(e)和CuO/M-2(f)结构发生显著变化[17]。特别是使用后的CuO/M-1,其结构几乎完全被破坏。从TEM照片可知,反应中样品的稳定性依次为:CuO/MS-1>CuO/M-2>CuO/M-1。
2.1.2 样品比表面积、孔结构及w(Cu)的分析
表1为应用N2的等温吸附-脱附和ICP分析获得的样品及其使用后的数据。由表1和辅助材料中图S1可知,所有样品均具有介孔结构,使用后样品的比表面积和w(Cu)均降低。其中,CuO/MS-1使用1次后,w(Cu)、比表面积、孔体积和孔径的变化最小,继续使用5次,各参数基本不变。CuO/M-1和CuO/M-2使用1次后,除孔径外,其他参数的变化明显。特别是CuO/M-1,其w(Cu)、比表面积和孔体积分别从2.5%、500和0.445减小到1.3%、241和0.390。结果说明,无定型孔壁的CuO/M-1和CuO/M-2稳定性差,在物理搅拌、固液界面和溶剂作用的液相反应中,结构易毁坏,导致Cu流失严重,而具有高晶化的MFI结构的CuO/MS-1稳定性强[18]。结果与TEM一致。
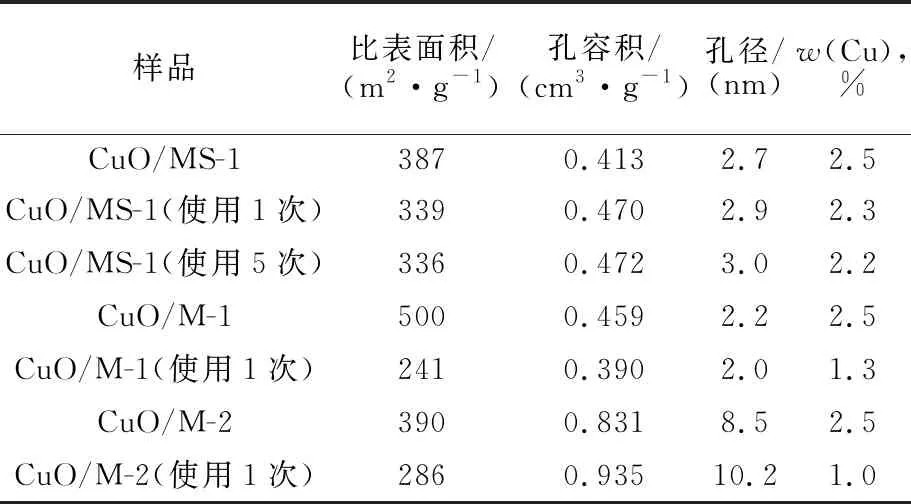
表1 样品表面积、孔结构及Cu含量
2.1.3 样品中Cu物种的分析
图3为载体及w(Cu)=2.5%的样品的FT IR(3A)和DR UV-vis(3B)谱。由图3A可知,所有样品均存在物理吸附H2O的O—H伸缩和弯曲振动吸收峰(3 430~3 450和1 630~1 640 cm-1),Si-O-Si不对称、对称伸缩振动(1 190~1 115和800~816 cm-1)和弯曲振动吸收峰(470 cm-1)。另外,MS-1还存在MFI结构的伸缩震动吸收峰(550 cm-1)[19]。引入Cu后的样品中,960 cm-1处出现了1个弱的吸收峰,说明催化剂制备过程中,Cu与载体相互作用,形成了Cu-O-Si物种[20]。在550 cm-1处,CuO/MS-1吸收峰强度与MS-1相似,表明Cu的引入,没有影响原有MFI结构,与XRD结果相符。
样品DR UV-vis(3B)谱图中,3种载体均未出现明显的吸收峰。引入Cu后,生成了的新的吸收峰。模拟分峰后发现,CuO/M-2含有Cu-O-Si(230 nm)、Cu-O-Cu(440 nm)和高分散CuO(600~800 nm),而CuO/M-1和CuO/MS-1仅含有Cu-O-Si和高分散CuO[21]。根据峰面积比,样品中Cu-O-Si相对含量为CuO/M-1>CuO/MS-1>CuO/M-2。对于CuO/MS-1,当w(Cu)为0.5~4%时,样品中含有Cu-O-Si和高分散CuO,随Cu含量增加Cu-O-Si和高分散CuO的峰面积的比值先增加后减少。w(Cu)=2.5%时,峰面积的比值最大(1.0∶1.2)。w(Cu)>5.5%后,样品中出现Cu-O-Cu,且其含量随w(Cu)迅速增加。随Cu-O-Cu出现及相对含量的增加,Cu-O-Si物种的含量明显减小。
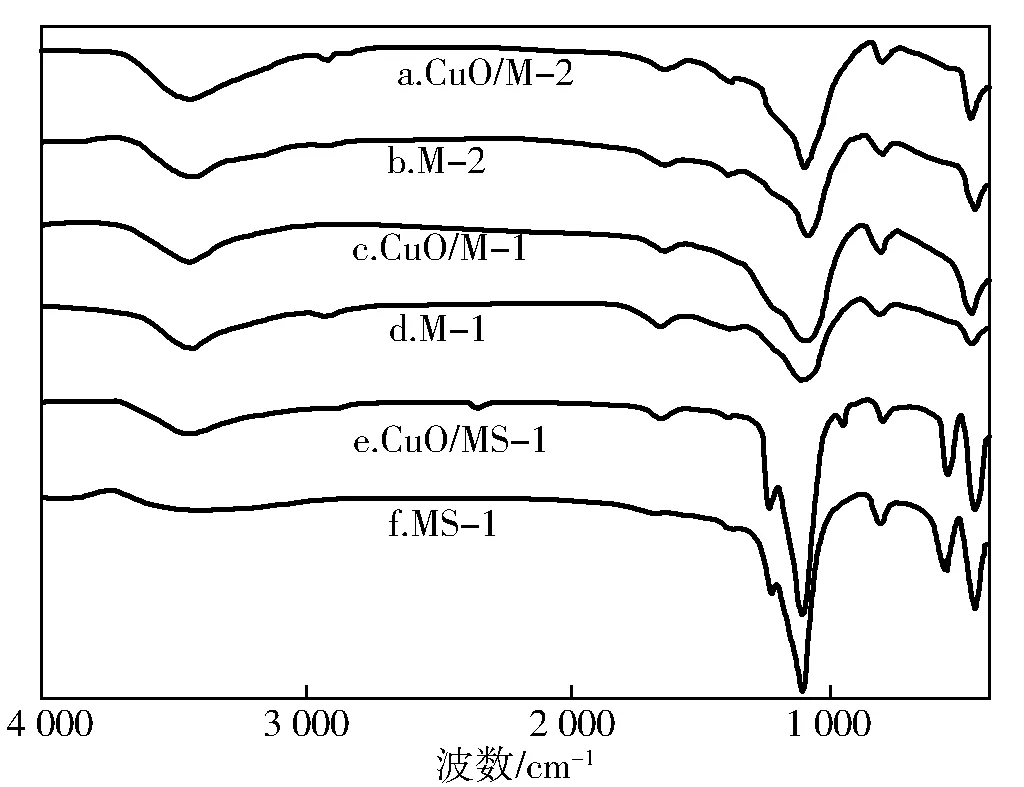
图3 样品的FT IR(A)和DR UV-vis(3B)谱
图4为w(Cu)=2.5%样品的XPS谱图。从图4可知,所有样品的Cu 2p在结合能约为934.0 eV和942.0~944.0 eV时分别存在与文献报道一致的负载于氧化物载体上的CuO的特征峰和d9电子态的特征峰,证明样品中Cu物种是Cu2+。对样品的Cu 2p谱图进行拟合,样品在932.8~935.6 eV之间出现了2个峰,933.0 eV是分散在SiO2表面的CuO结合能,大于934.5 eV是Cu2+和SiO2中的氧之间电子转移(即Cu-O-Si)的结合能,表明存在2种不同形式的Cu2+[22,23]。对于CuO/MS-1,w(Cu)增加,样品中Cu物种仍以Cu2+存在,但934.5 eV处的峰移向电子结合能变大,说明部分Cu聚集形成了Cu-O-Cu,且随着w(Cu)的增加,聚集加重[24]。结果与XRD、DR UV-vis结果一致。
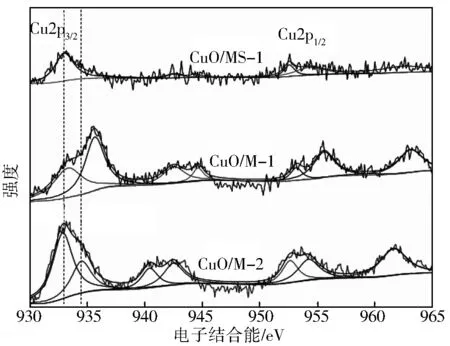
图4 样品的XPS谱
2.2 胺化反应条件的考察
2.2.1 溶剂浓度对胺化反应的影响


图5 溶剂浓度对胺化反应的影响
2.2.2 反应温度对胺化反应的影响
温度对苯的胺化反应影响如图6所示。由图6可知,胺化反应需在40 ℃以上才能进行,苯的转化率、苯胺的收率和选择性随温度升高先增加,后减小。温度是活化苯中C—H关键因素。温度低于40 ℃,不能有效活化苯的C—H,从而反应不能进行。温度高于70 ℃,羟胺将按不利于目标反应的方向分解。当温度超过苯的沸点后,苯被汽化,从而导致反应效率极低。温度为70 ℃时,能有效活化C—H,有利于苯胺的生成,苯的转化率(57.4%)、苯胺的收率(56.8%)和选择性(99%)均最佳。
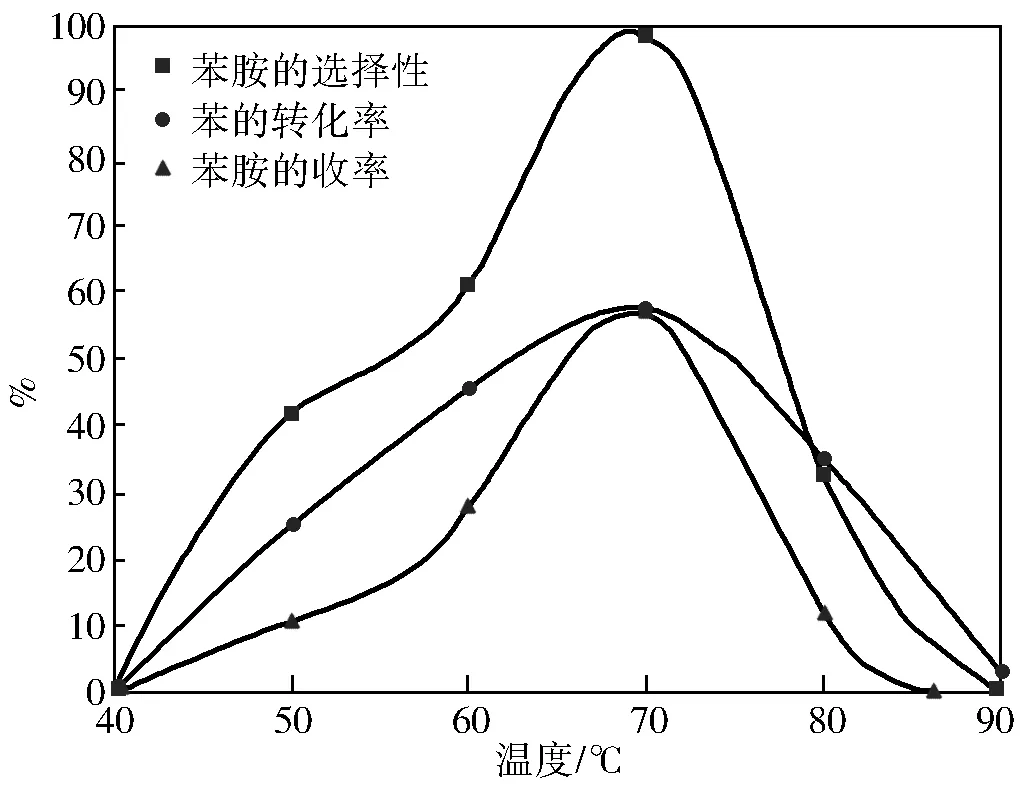
图6 反应温度对胺化反应的影响
2.2.3 催化剂中w(Cu)对胺化反应的影响
催化剂中w(Cu)的变化对苯的胺化反应结果如图7所示。

图7 w(Cu)对胺化反应的影响
MS-1存在下,生成痕量的苯胺。引入Cu后,苯的转化率和苯胺的收率明显升高,说明Cu物种是反应的活性物种。随w(Cu)增加,苯胺的收率和选择性均先增加,后减小,而苯的转化率一直增加。w(Cu)=2.5%时,苯胺的收率(64.7%)和选择性(99%)最大。DR UV-vis和XPS对不同w(Cu)的CuO/MS-1研究中发现,w(Cu)<4.0%的CuO/MS-1中,存在Cu-O-Si和高分散CuO。而w(Cu)=2.5%时,CuO/MS-1中Cu-O-Si的相对含量最大。当w(Cu)>5.5%后,CuO/MS-1中出现Cu-O-Cu,其相对含量随w(Cu)增加而增大,而Cu-O-Si物种的含量明显减小。由此可推测,Cu-O-Si对苯的胺化具有良好的催化活性,是胺化反应的活性物种,而高分散的CuO和Cu-O-Cu物种则更有利于副反应的发生。
2.2.4 盐酸羟胺用量对胺化反应的影响
盐酸羟胺的用量对苯的胺化反应影响如图8所示。
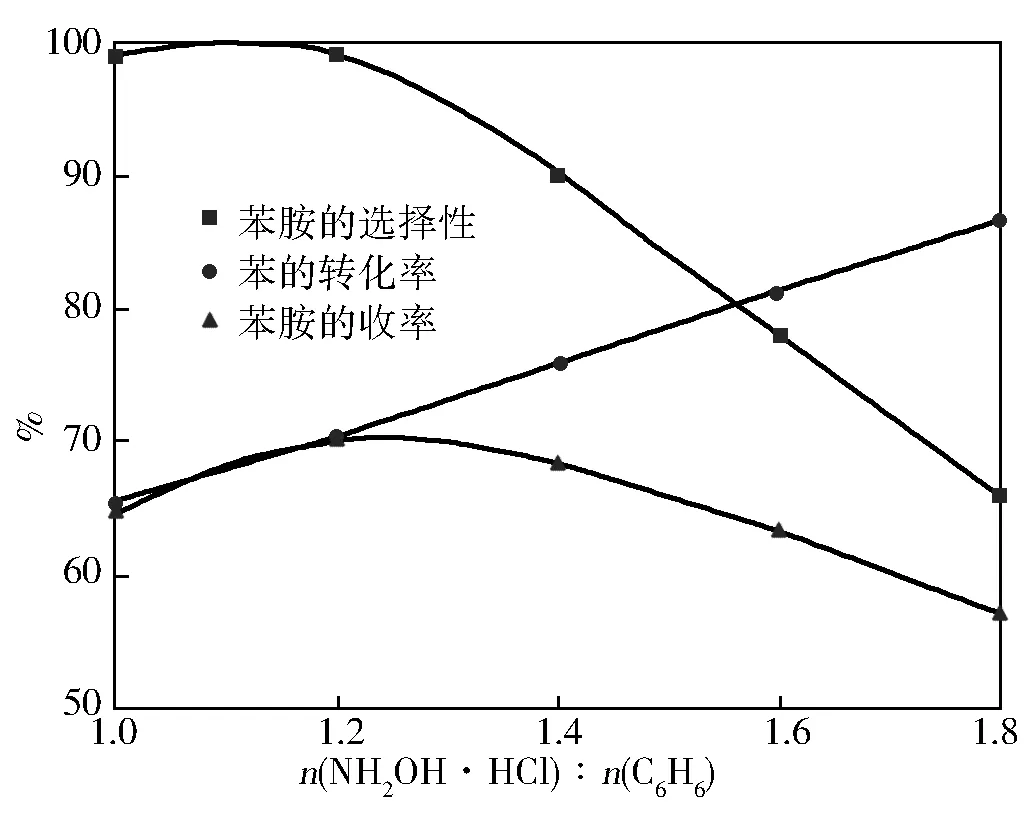
图8 盐酸羟胺用量对胺化反应的影响
随盐酸羟胺用量的增加,苯的转化率持续增加,苯胺的收率先增后降,而苯胺的选择性先保持不变,后迅速减少。当n(NH2OH·HCl)∶n(C6H6)=1.2时,苯胺的收率(70.0%)和选择性(99%)最高。n(NH2OH·HCl)∶n(C6H6)>1.2后,苯胺选择性迅速降低,产物中出现了苯酚,二苯酚及氯苯等副产物。说明盐酸羟胺浓度稍高于苯,有利于反应的进行,但浓度过高,则对副反应更有利。
2.2.5 反应时间对胺化反应的影响
反应时间对苯的胺化反应影响如图9所示。
刚开始反应时,苯的转化率和苯胺的收率随反应时间增长而增加,苯胺的选择性基本不变。反应3.5 h后,苯的转化率增加缓慢,而苯胺的收率和选择性略有下降。说明反应3.5 h后,胺化反应基本达到平衡,随时间增加,副反应增加,甚至生成的苯胺将进一步被氧化。

图9 反应时间对胺化反应的影响
2.2.6 催化剂用量对胺化反应影响
理论上,催化活性中心与催化剂用量成正比,但催化剂用量太大,催化剂的吸附等现象,将导致低反应物浓度降,副反应增加,催化剂用量对苯的胺化反应影响结果如图10所示。当目标反应不存在催化剂时,反应不发生。加入催化剂后,有苯胺生成,催化剂用量为0.1 g时,苯胺的收率和选择性均达到最高。催化剂用量大于0.1 g后,苯的转化率略有增加,但苯胺的收率和选择性均明显减少,即副反应增加。

图10 催化剂用量对胺化反应的影响
2.2.7 不同结构催化剂对胺化反应的影响和催化剂的稳定性考察
2.5% CuO/MS-1为催化剂,在上述最佳反应条件下,苯的转化率,苯胺的收率和选择性分别达到76.2%、75.6%和99%。相同条件下,考察了以w(Cu)=2.5%的CuO/M-1和CuO/M-2对目标反应的催化性能,结果如表2。由表2可知,CuO/M-1和CuO/M-2均具有催化活性,但低于CuO/MS-1。从催化剂中w(Cu)对胺化反应结果可知,催化剂中的主要活性物种为Cu-O-Si,结合BET、TEM、FT-IR、XRD、DR UV-vis及XPS分析及活性结果,上述3种催化剂均具有Cu-O-Si和介孔结构,理论上保障了反应物分子在孔道内外顺利扩散到反应活性中心进行反应。催化剂中Cu-O-Si的相对含量高低的顺序为:CuO/M-1>CuO/MS-1>CuO/M-2,新鲜催化活性高低的顺序为:CuO/MS-1>CuO/M-1>CuO/M-2,使用1次后催化活性高低的顺序为:CuO/MS-1>CuO/M-2>CuO/M-1。这是由于CuO/M-1和CuO/M-2的无定型结构,在剧烈物理搅拌,酸性溶液和液固相界面的作用下,催化剂结构被破坏(特别是CuO/M-1),阻碍反应物分子在载体孔道中的扩散,同时,结构破坏使催化剂内表面变为外表面,使活性物种易流失(CuO/M-1和CuO/M-2中,w(Cu)从2.5%分别减小到1.3%和1.0%),导致催化活性降低(重复1次的CuO/M-1和CuO/M-2做催化剂,苯胺的收率从52.4%和44.8%分别减小到12.4%和30.6%),副产物增多。相比于CuO/M-1和CuO/M-2的无定型结构,具有MFI结构、晶化度高的CuO/MS-1在胺化反应中稳定性更强,保障了活性物种及反应物分子在孔道内外的扩散。使用5次后,CuO/仍保持完整的结构,其w(Cu)从2.5%变为2.2%,表现出更优秀的催化活性和可重复使用性,苯胺的收率和选择性仍高达70.8%和97%。

表2 不同结构催化剂的催化性能
3 结 论
XRD,TEM和BET等系列表征和活性研究发现,以盐酸羟胺直接胺化苯的反应,主要活性物种为Cu-O-Si。由于CuO/MS-1具有高晶化度的孔壁结构,反应中稳定性强,保持相对数量较多的Cu-O-Si,从而表现出优越的活性。在0.1 g 2.5% CuO/MS-1存在下,8 mL乙酸和2 mL水的溶剂中,1 mmol苯和与1.2 mmol的盐酸羟胺在70 ℃下反应3.5 h,苯的转化率,苯胺的收率和选择性分别达到76.2%、75.6%和99%,且催化剂可重复使用。研究为简化催化剂和目标产物合成步骤,提高原子利用率,发展温和条件下活化芳环中的C—H,直接胺化芳烃制备芳胺类化合物的绿色化和可持续化方法提供理论依据。

