颞叶外节细胞胶质瘤继发癫痫的手术治疗研究
谭红平,郭强,华刚,陈俊喜,唐晓伟,李少春,陈淼彬,张伟,王艮波,朱丹
颅内神经节细胞胶质瘤(gangliogliomas,GG)是一种相对罕见的混合性神经元-胶质细胞肿瘤,2016年世界卫生组织(WHO)中枢神经系统肿瘤分类将其归为WHO Ⅰ级肿瘤[1]。GG好发于青少年,常以癫痫发作为主要首发症状[2]。GG继发癫痫常见于肿瘤位于颞叶者,手术切除能获得良好的效果[3]。国内外对于颞叶GG继发癫痫的研究报道比较多,但对于颞叶外GG继发癫痫的研究报道相对较少。为此,本研究对广东三九脑科医院2014年11月—2019年2月,手术治疗的20例颞叶外GG继发癫痫患者的临床资料进行回顾性分析;以探讨颞叶外GG继发癫痫的临床特点、手术方式和疗效,以及影响预后的因素。
1 资料与方法
1.1 一般资料 本组患者中男10例,女10例;年龄5~51岁,平均24.0岁;癫痫发病起始年龄5~39岁,平均16.25岁;病程1个月~30年,平均7.62年;术后病理学检查均确诊为颞叶外节细胞胶质瘤(WHO Ⅰ级)。
1.2 临床表现 均为反复癫痫发作;发作类型主要为简单部分性发作(伴意识保留的局灶性发作)、复杂部分性发作(伴意识障碍的局灶性发作)和(或)继发性全面性强直阵挛发作(局灶进展到双侧的强直阵挛发作)。查体均未见明显异常体征。
1.3 术前评估 所有患者均经过详细和严谨的术前评估,包括病史询问、发作症状学演变、病因、头皮视频脑电图、MRI薄层扫描、功能MRI、神经认知功能检查(韦氏智力、记忆力量表测试等),必要时行头颅PET-CT检查。
1.4 影像学与脑电图检查 MRI薄层扫描检查示,病变位于额叶2例(1例累及中央前回)、顶叶7例(1例累及中央后回)、枕叶5例、颞枕交界处6例,肿瘤为囊性5例、囊实性6例、实性9例;MRI增强扫描示12例患者病变有强化,其中5例患者病变周围水肿。CT检查显示病变钙化者4例(图1)。13例患者行发作间期PET-CT检查,所有的患者均显示病灶区域低代谢,其中9例患者低代谢区域大于MRI显示的病灶范围,4例患者出现除病变周围外远隔部位的低代谢区(图2)。所有患者术前均行长程视频脑电图监测,记录发作间期和(或)发作期脑电图及症状学。其中头皮EEG发作间歇期放电和病灶侧别相一致的患者15例,而不一致或不能定侧的患者2例;间歇期脑电图正常者3例。发作症状学中简单部分性发作(伴意识保留的局灶性发作)患者4例,复杂部分性发作(伴意识障碍的局灶性发作)患者5例,继发性全面性强直阵挛发作(局灶进展到双侧的强直阵挛发作)患者11例,其中3例患者有先兆(预感)。发作期脑电演变显示与病灶侧一致者11例,而不能定侧定位的患者9例。
1.5 手术治疗 根据术前MRI分型和表现特点、头皮视频脑电图结果、发作症状学、PET-CT结果及功能MRI结果拟定初步手术切除方案。并根据导航和三维影像后处理系统设计手术切口与手术入路;术中同时结合皮层脑电图结果确定最终切除范围。对于病变位于功能区的2例患者采用了术中唤醒技术。1例患者采用一期SEEG置入精确定位致痫灶,二期手术切除(图3)。
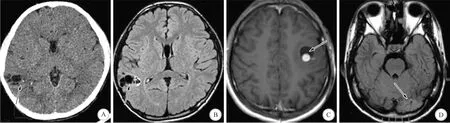
A:头颅CT示右侧颞枕囊性GG伴钙化; B:头颅MRI T2压水示右侧颞枕囊性GG不伴水肿; C:头颅MRI增强示左额中央区囊实性GG伴增强结节及水肿; D:头颅MRI T2压水示左枕实性GG(箭头所指)

A:脑部低代谢范围与病变范围相同; B:低代谢范围大于病变范围; C:低代谢范围大于病变范围,且远隔部位岛叶出现低代谢区(红色箭头所指)

A:MRI示左侧颞枕囊性病变伴周围高信号; B:PET显示左侧颞枕病变及周围低代谢,远隔部位左侧颞岛出现低代谢区; C:SEEG置入电极方案及致痫灶切除范围(红色箭头所指)
1.6 术后随访与预后评定 所有患者术后均服用与术前相同的抗癫痫药物治疗。术后3个月时第1次随访复查,之后每年随访1次。随访时了解癫痫发作情况,进行头皮视频脑电图和头颅MRI复查。术后随访1~3年,以末次随访结果为准,根据改良Engel分级评定患者的预后,将术后癫痫完全无发作(Engel Ⅰ级)定为预后良好,仍有发作(Engel Ⅱ级、Ⅲ级)定为预后不良。

2 结 果
2.1 手术效果及术后并发症 本组患者中肿瘤次全切除者2例,全切除者15例,扩大切除者3例;所有患者术后均未行放化疗治疗。1例左额中央区GG患者术后出现短暂右下肢偏瘫,2例枕叶GG患者术后出现视野缺损。
2.2 病理检查结果 患者的术后病理学检查结果均为GG,WHO Ⅰ级;其中2例患者合并脑皮质发育不良(focal cortical dysplasia,FCD)(图4)。
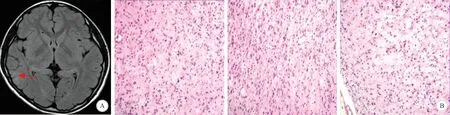
A:术前MRI检查示右侧颞枕实性病变(红色箭头所指); B:术后病理学检查示,GG伴周围FCD Ⅰb(HE染色,×100)
2.3 预后及其影响因素 患者术后随访1~3年,最后1次随访复查MRI显示,与术前比较均无病变复发或病变加重。术后癫痫控制为Engel Ⅰ级者17例(85.0%),Engel Ⅱ级者2例(10.0%),Engel Ⅲ级者1例(5.0%);预后良好患者为17例,预后不良患者为3例。预后与相关临床指标的分析显示,肿瘤切除程度和是否完整切除与预后有关;肿瘤全切除和完整切除患者的预后良好率,明显高于肿瘤次全切除和未完整切除的患者,差异均有统计学意义(P<0.005,P<0.05)。见表1。

表1 预后良好组与预后不良组患者的相关临床指标比较(例)
3 讨 论
颅内GG是一种相对罕见的混合性神经元-胶质细胞肿瘤,好发于青少年,常以癫痫、头痛等症状为主要首发症状,其中以癫痫发作最为多见;GG常位于颞叶,位于颞叶外脑区的相对少见[4]。本院同期经手术病理检查证实的165例GG患者中,颞叶外GG患者仅20例,其中男女各占10例,平均年龄为24.0岁,癫痫发病起始平均年龄为16.25岁,平均病程7.62年。本组颞叶外GG患者的发病年龄和病程与文献报道的颞叶GG患者大致相同[5]。
GG的术前诊断主要依靠头颅MRI和CT检查,但需要与脑软化灶、脑皮质发育不良、胚胎发育不良性神经上皮肿瘤及其他低级别肿瘤相鉴别;而确诊仍须依靠病理学诊断。根据GG的MRI表现可以将其大致分为囊性、囊实性及实性3种类型;MRI增强扫描大多为点状或片状轻度强化,也有部分患者可表现为中度强化或结节性强化;绝大部分患者的瘤周水肿不明显,但也有少数患者可以有瘤周水肿表现。MRI表现为囊性或囊实性肿瘤患者,在头颅CT上表现为低密度病变,少数患者在囊变周围可有点状钙化,呈现点状高密度影;而MRI表现实性肿瘤患者,在CT上表现为等密度病变[6]。本组颞叶外GG患者也有类似的影像学特点。GG的影像学特点与胚胎发育不良性神经上皮肿瘤(dysembryoplastic neuroepithelial tumor,DNET)及神经节细胞瘤相似。但DNET多呈类圆形或三角形囊性或多囊性病变,瘤内分隔多见,无瘤周水肿及占位效应,增强扫描一般不强化,少见钙化;而节细胞瘤主要由神经节细胞组成,不含肿瘤性胶质细胞,通常无浸润性生长表现,少见囊变及钙化[7]。
GG继发癫痫可表现为简单部分性发作(伴意识保留的局灶性发作)、复杂部分性发作(伴意识障碍的局灶性发作)和/或继发性全面性强直阵挛发作(局灶进展到双侧的强直阵挛发作)。颞叶GG继发癫痫常以复杂部分性发作(伴意识障碍的局灶性发作)为主[5]。本组患者的癫痫发作主要为继发性全面性强直阵挛发作(局灶进展到双侧的强直阵挛发作)(11/20例),部分枕叶GG患者发作前有视觉先兆(预感)。发作间歇期脑电图的癫痫样放电区域常与病变区域相一致,但枕叶GG也可因为致痫网络传导而表现前头部放电为主[8]。
GG继发癫痫均为药物难治性癫痫,手术切除病变可以获得良好的预后;有文献报道颞叶GG患者术后的癫痫完全无发作率可达90%[9]。本研究患者的术后随访显示,癫痫完全无发作(Engel Ⅰ级)者17例(85.0%),Engel Ⅱ级者2例(10.0%),Engel Ⅲ级者1例(5.0%)。但本组患者中仍有15.0%的患者术后预后不良,未达到完全无发作;这与致痫灶切除不彻底有关。预后相关临床因素分析也表明,肿瘤切除程度和是否完整切除与预后有关;肿瘤全切除和完整切除患者的预后良好率明显高于次全切除及未完整切除的患者,差异有统计学意义(P<0.005,P<0.05)。本组患者中2例肿瘤次全切除患者,均是病变位于功能区而行术中唤醒的患者。1例患者的病变位于左侧额中央区,病变后界电刺激存在运动功能导致切除不全;另1例患者的病变位于左侧顶叶邻近中央后回及语言区,术中唤醒不理想而导致切除不彻底。PET低代谢常被认为与致痫灶或致痫灶相关的区域有关,也可能代表功能缺失区[10]。本组患者术前的PET检查显示病变区域均为低代谢,部分患者的低代谢区域大于病变范围,甚至可能因致痫网络出现相邻脑叶或远隔部位的低代谢。这表明对有些患者,单纯切除病变并不等于完全切除了致痫灶,致痫灶的范围可能远大于病变的范围,故甚至需要行脑叶或相邻多脑叶切除,而不能仅做裁剪式病灶切除。本组3例患者采用了病变扩大切除术;主要依据是,一方面术前PET检查显示低代谢区域远大于病变范围,另一方面术中皮层电生理监测也提示病变周围仍存在癫痫样放电,或SEEG监测提示致痫区范围大于病灶范围,而且病变周围不存在重要功能区,扩大切除对功能无明显影响。术后随访显示这3例患者均获得癫痫完全无发作。病理学检查显示低级别肿瘤,尤其是GG,有合并FCD或海马硬化等双重病理改变的可能[11]。部分文献甚至报道GG患者合并FCD的比率高达68.4%~74.5%,尤其是颞叶GG[12-13]。本组20例颞叶外GG患者中合并FCD者为2例(10.0%),合并FCD的比例远低于颞叶GG,可能与病例数较少有关。这些合并的双重病理改变同样有极高的致痫性[14]。所以对于颞叶外GG患者,应在术前结合临床症状学、MRI和间歇期脑电图表现及PET低代谢区域等特点综合设计手术切除方案,术中再结合电生理监测,在保护神经功能的情况下,尽可能将肿瘤及其周围的致痫灶一并切除。对于术前评估病变和致痫区不一致的患者,可先行SEEG电极置入监测,明确病变、致痫区和功能这三者之间的关系,二期再选择合适的手术方案行精确致痫区切除。
2000年WHO中枢神经系统肿瘤分类中,GG为Ⅰ-Ⅱ 级,间变性GG为Ⅲ级;而2007年和2016年版WHO中枢神经系统肿瘤分类中,则取消了GG的中间级别Ⅱ级,只分为Ⅰ级和Ⅲ级[15-16]。虽然GG为WHO Ⅰ级,为良性肿瘤,术后不需要行放化疗,但仍有复发或恶变的可能;尤其对于术前MRI示病变强化及周围水肿明显,术后病理检查示细胞增生活跃,却因无血管内皮增生及坏死而不足以诊断WHO Ⅲ级的间变性GG患者,须警惕术后复发、恶变的可能[17]。故对于GG术后患者,一方面需要加强定期随访意识;另一面对癫痫多年未发作而近期突然发作或出现头痛及其他症状的患者,一定要及时复查薄层MRI和增强扫描排除GG残留、复发、恶变的可能。
综上所述,颞叶外GG继发癫痫多为药物难治性癫痫,手术切除可取得良好效果;术前须综合评估病变部位和临床症状、影像学、脑电图特点等资料制定手术策略,术中应尽可能行肿瘤加致痫皮层全切除,以提高手术效果,改善患者的预后。必要时可考虑先行SEEG电极植入明确致痫区后,二期再行致痫灶精准切除术。

