基于机器学习的多种分类模型在新型冠状病毒肺炎与社区获得性肺炎鉴别诊断中的效能
田斌, 余晖, 任基刚, 汪汉林, 徐井旭, 黄陈翠
目前新型冠状病毒肺炎(corona virus disease 2019,COVID-19)仍在全球广泛传播,COVID-19的筛查和确诊主要依靠核酸检测,胸部CT作为一种重要的诊断手段不容忽视,已成为筛选、诊断和评估新型冠状病毒肺炎严重程度的重要工具[1]。因为COVID-19患者首次聚合酶链式反应(reverse transcription poly-merase chain reaction,RT-PCR)检查的平均时间为(30±13)h[2],因此,胸部CT检查不仅对COVID-19的诊断起到预警作用[3,4],还可以在等待RT-PCR结果时将可疑患者分流、隔离,为疫情的防控争取时间。
因此,COVID-19患者的诊断与鉴别诊断非常重要,其早期诊断可避免在等待核酸检测结果的过程中造成进一步的蔓延和播散。由于传统的人工阅片方法鉴别诊断COVID-19与社区获得性肺炎(community acquired pneumonia,CAP)具有局限性,所以将人工智能(artificial intelligence,AI)技术用于COVID-19与CAP的鉴别诊断成为当下研究的热点。部分学者运用线性支持向量机模型(linearSVM)鉴别诊断COVID-19与CAP,结果表明linearSVM模型可以有效鉴别COVID-19与CAP[5]。然而,机器学习的分类模型种类繁多,给应用的选择带来一定困难。此外,目前并不清楚其它分类模型是否也能有效鉴别COVID-19与CAP。因此,本研究通过应用14种常用的机器学习分类模型鉴别COVID-19和CAP,旨在探讨鉴别COVID-19与CAP效能最高的机器学习分类模型,为临床医师的早期干预提供更充分的影像学依据。
材料与方法
1.病例资料
搜集经临床确诊的COVID-19患者86例和CAP患者100例,包括其胸部CT图像及临床资料。
COVID-19患者纳入标准:①至少两次核酸检测阳性的新型冠状病毒肺炎患者;②患病期间有至少一次胸部CT扫描,图像含有薄层图像(层厚≤3 mm),且肺部有炎性CT表现。CAP患者纳入标准:①至少两次核酸检测为阴性的肺炎患者;②患病期间至少有一次胸部CT检查,图像含有薄层图像(层厚≤3 mm),且肺部有炎性CT表现。排除标准:①胸部CT图像中有运动伪影致病灶显示不清;②CT图像中病灶太小不能识别或肺部无炎性CT征象;③胸部CT无薄层图像(层厚≤3 mm);④临床资料、核酸检测资料丢失者。
2.研究方法
研究的机器分类学习流程包括回顾性数据采集、图像预处理、肺部病变分割、特征提取、特征选择和特征构建、性能评价,流程见图1。对患者进行胸部CT检查,按照胸部CT标准的成像方案进行扫描及重建。
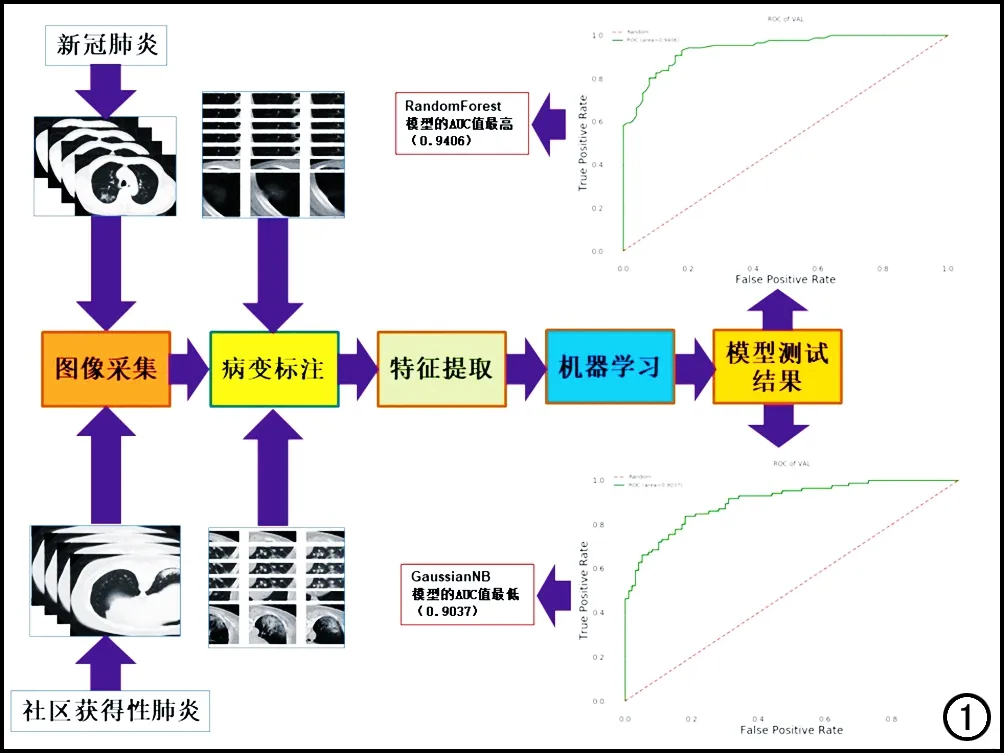
图1 利用14种机器学习模型对COVID-19与CAP的鉴别诊断流程。
3.图像的分割及预处理
将所有病例的胸部CT图像以DICOM格式导入深睿科研平台(https://research.deepwise.com)进行自动分割,分别由两位经验丰富的放射科医生对自动分割的病灶进行修改、确认后提交,以避开血管及肋骨等非病灶区域(图2~7)。
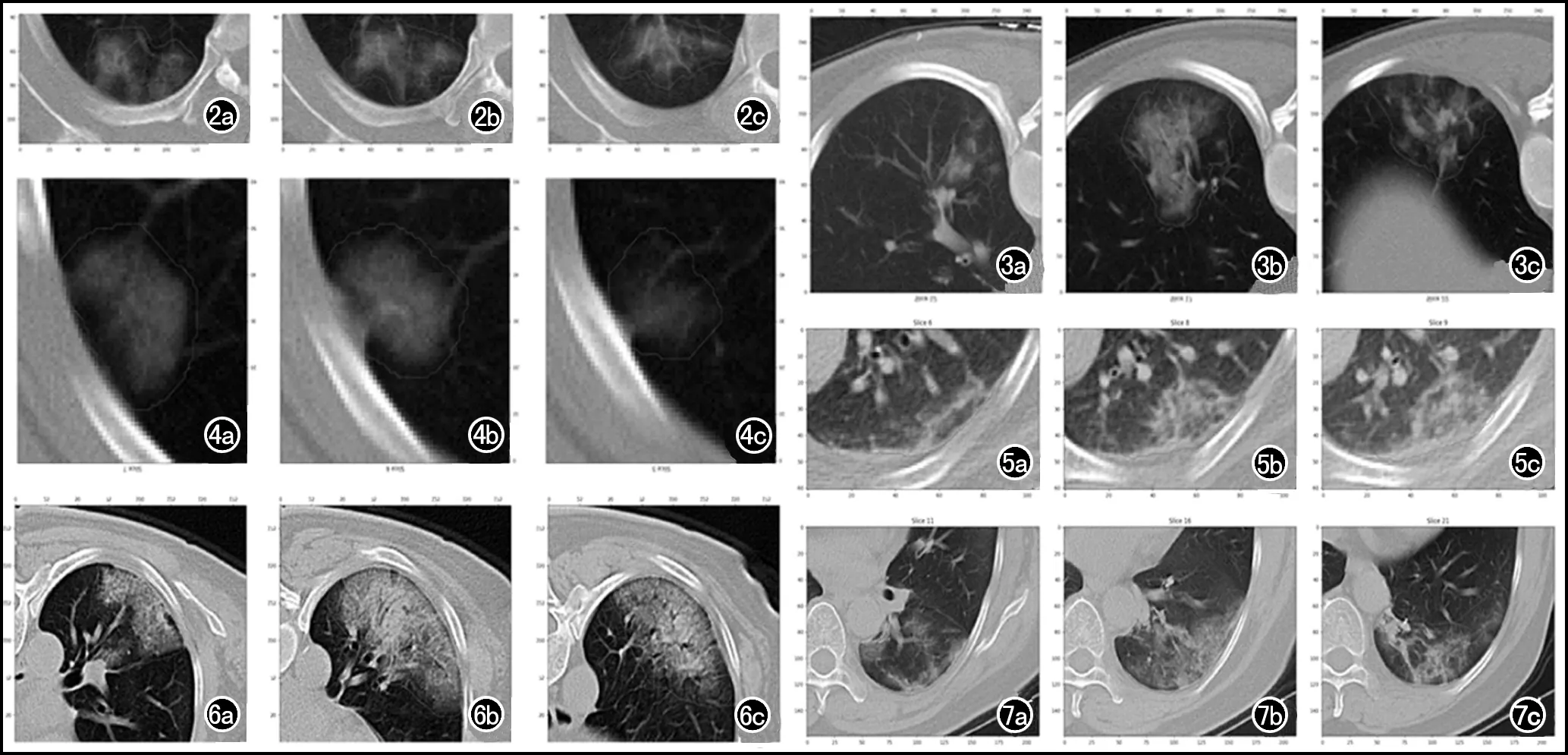
图2 经临床确诊的COVID-19病例,蓝色线条表示边界。a~c) 病灶被准确分割,避开了肋骨。 图3 经临床确诊的COVID-19病例,蓝色线条表示边界。a~c) 密度不均匀的层面被准确分割。 图4 经临床确诊的COVID-19病例,蓝色线条表示边界。a~c) 密度浅淡的层面被准确分割。 图5 经临床确诊的CAP病例,蓝色线条表示边界。a~c) 病灶被准确分割,避开了肋骨和胸膜。 图6 经临床确诊的CAP病例,蓝色线条表示边界。a~c) 病灶被准确分割,避开了血管及支气管。 图7 经临床确诊的CAP病例,蓝色线条表示边界。a~c) 密度不均匀的层面被准确分割,并避开了降主动脉。
14种分类模型采用同样的图像预处理方式。在本研究中,采用了B样条插值采样技术(B-spline interpolation resampling techniques)进行图像预处理,即将原始薄层图像重新采样到1 mm×1 mm×1 mm的分辨率,应用高通或低通小波滤波器(wavelet filter)和拉普拉斯高斯滤波器(laplacian of gaussian filter)对原始图像进行预处理及图像变换。
4.特征提取和筛选
提取原始图像和预处理后图像的影像组学特征,包括基于原始图像或预处理后图像像素值的一阶特征、描述肿瘤形态的形态特征及描述肿瘤内部和表面纹理的灰度共生矩阵(gray level co-occurrence matrix,GLCM)、灰度游程矩阵(gray level run length matrix,GLRLM)、灰度区域大小矩阵(gray level size zone matrix,GLSZM)和灰度相依矩阵(gray level dependence matrix,GLDM)纹理特征。为了消除病变标注所带来的影响,对组间进行一致性分析,删除一致性小于0.75的特征,然后对特征进行相关性分析,随机剔除相关性大于0.9的特征,最后采用Lasso算法用于特征降维和筛选,找出系数不为零的最重要特征用于建模,提升模型表现。
5.建立放射组学特征
利用线性支持向量机(linear SVM)分类器[6]、增强学习分类器(Ada Boost)[7]、逻辑回归分类器(logistic Regression)[7-10]、线性支持向量分类器(LinearSVC)[11]、决策树分类分类器(Decision Tree)[12]、随机森林分类器(Random Forest)[9,13]、梯度推进分类器(Gradient Boosting)[14,15]、极端梯度增加算法分类器(XGBoost)[16]、伯努利贝叶斯分类器(BernoulliNB)[17]、高斯贝叶斯分类器(GaussianNB)[18]、最临近规则分类器(K Nearest Neighbors)[19,20]、线性判别分析分类器(LinearDiscriminant Analysis)[9,21]、随机梯度下降分类器(stochastic gradient descent,SGD)[22]、多层感知机分类器(Multilayer Perceptron)[23]等14种分类器分别建立模型,以上模型均采用5折交叉验证训练方法,即将所有数据分为5部分,其中4部分用于模型训练,1部分用于评估模型的有效性,最后将所有数据用于训练集和验证集。完成所有的训练和验证之后,用5个测试的平均值来评价模型的性能。为了评估预测模型在训练集和验证集中的性能,绘制了受试者工作特征(receiver operating characteristic curve,ROC)曲线,并计算出曲线下面积(area under curve,AUC),以评估分类模型的性能,并将AUC作为评价模型性能的指标。
6.统计学分析
采用SPSS 16.0软件分析样本的人口统计学数据,运用秩和检验和χ2检验分别评估COVID-19与CAP患者之间的年龄、性别差异。利用Scikit学习软件包(0.20.3版)建立分类模型,采用Matplotlib(版本3.1.0)绘制ROC曲线。采用SPSS 16.0软件对一般数据进行统计学分析,对于分类数据,采用χ2检验比较组间差异;对于定量数据,采用独立样本t检验比较组间差异。为了评价预测模型在训练集和验证集上的性能,绘制ROC曲线,在训练集和验证集上显示分类性能。以P<0.05为差异有统计学意义。
结 果
本研究共纳入86例COVID-19患者,其中男34例,女52例,平均年龄(中位数±四分位间距)为(49.00±27.00)岁;同时纳入100例CAP患者,其中男52例,女48例,平均年龄(中位数±四分位间距)为(38.00±31.75)岁。COVID-19与CAP两组患者的性别差异无统计学意义(χ2=2.89,P=0.089),COVID-19组患者的平均年龄大于CAP组(Z=-3.546,P=0.000)。
本研究使用14种机器学习分类模型,所有模型的AUC均大于0.9(表1),Random Forest模型的AUC最高(0.9406,图8a),GaussianNB模型的AUC最低(0.9037,图8b)。
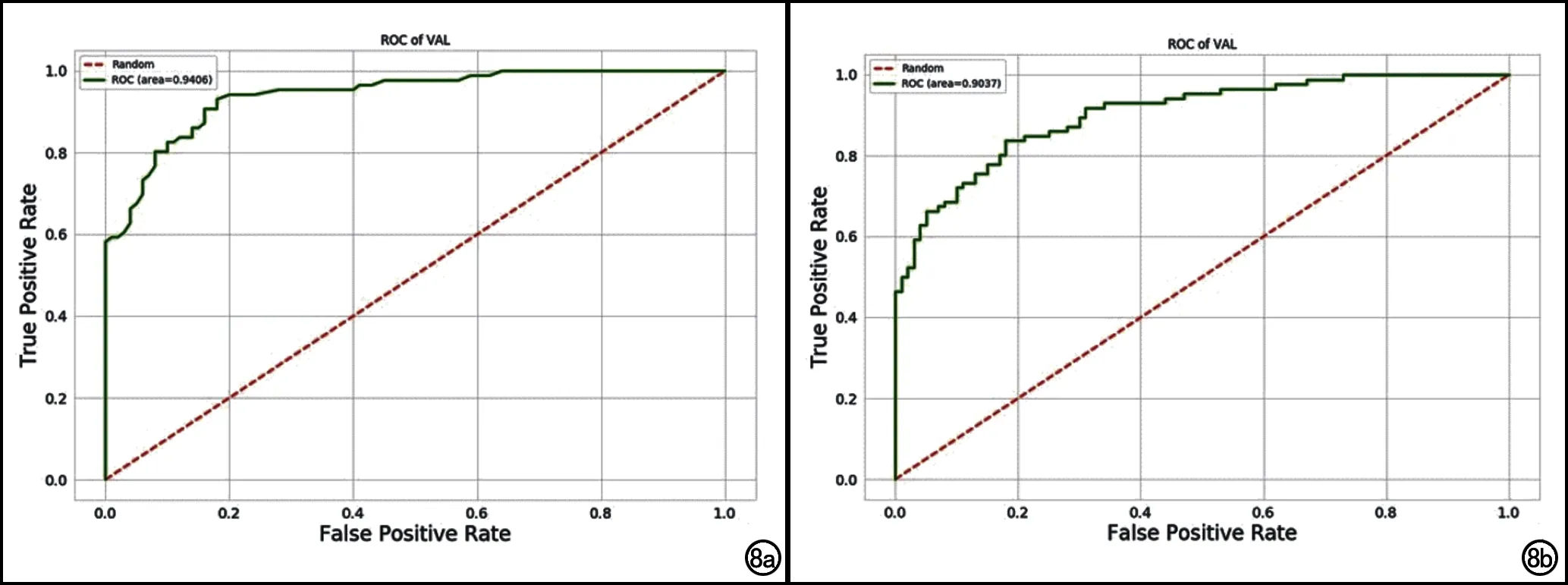
图8 机器学习分类模型的诊断效能。a) Random Forest模型的ROC曲线,其AUC最高(0.9406); b) GaussianNB模型的ROC曲线,其AUC最低(0.9037)。
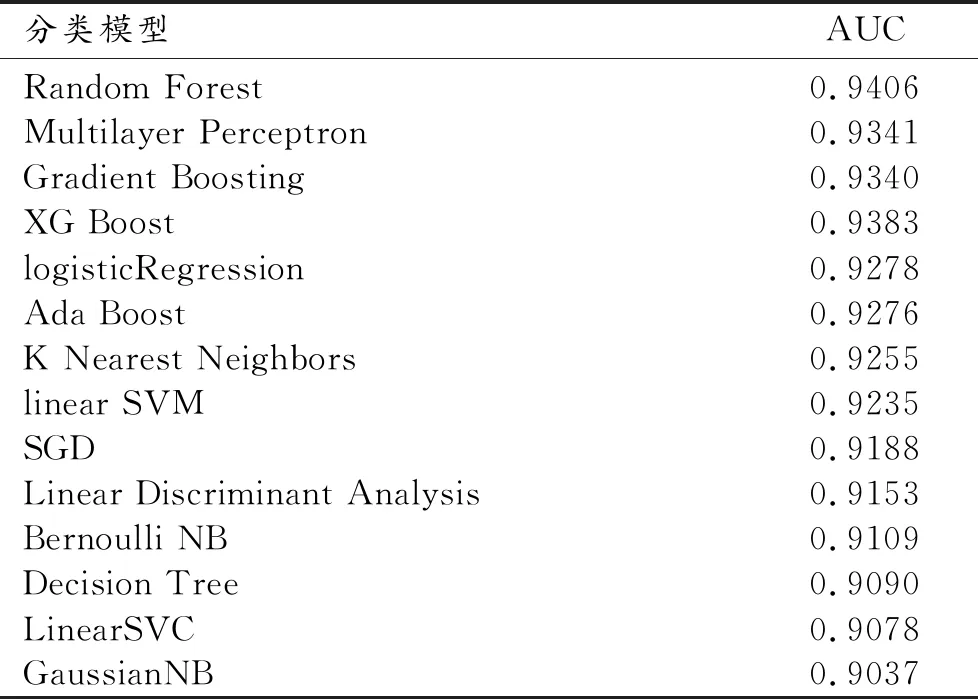
表1 经科研平台计算出的14种机器学习模型的AUC
讨 论
核酸检测是诊断新冠肺炎的金标准[24],但肺部炎症不明显的轻症患者,核酸检测往往呈阴性[25,26]。胸部CT作为诊断COVID-19的一种重要补充检测手段,其可靠性得到广泛认可[27-31]。由于各种病毒性肺炎的CT表现具有相似性,为了鉴别诊断COVID-19与CAP,国内外学者提出了许多可供鉴别的征象,如磨玻璃影、肺内实变、光晕征、气泡征、小叶间隔增厚、支气管充气征、胸膜下线、条索影、血管增粗、胸腔积液等[25,32-35]。然而有学者研究发现,甲型(H1N1)流感病毒感染引起的肺炎表现类似于COVID-19的胸部CT表现,如外周分布、磨玻璃影、实变、胸膜下线、支气管充气征等征象在两种病变间差异无统计学意义[36]。另外有报道指出,单纯的肺部CT筛查可能导致COVID-19误诊为柯萨奇病毒肺炎[37]。传统的人工阅片方式受阅片者工作经验和工作年限等因素的影响,不可避免地带有阅片者的主观性。相关文献报道,4位美国放射科医生鉴别诊断219例COVID-19与205例CAP的敏感度分别为93%、83%、73%和73%,3位中国放射科医生鉴别诊断219例COVID-19与205例CAP的敏感度分别为72%、72%和94%,特异度分别为94%、88%、24%[38],这说明传统的人工阅片方法具有局限性。
因此,有学者使用人工智能(AI)的方法鉴别诊断COVID-19与CAP,结果表明AI可有效鉴别COVID-19与CAP[39,40]。还有学者使用COVNet模型(一种深度学习模型)鉴别诊断COVID-19与CAP[3],结果表明深度学习技术可有效鉴别COVID-19与CAP,但深度学习需要大量的样本数据来进行模型训练,大量的数据不容易获得,而且比较费时。所以本研究采用对数据量要求较小的传统机器学习方法,以胸部CT图像的影像组学信息为特征的分类模型来识别和鉴别COVID-19与CAP。目前,基于机器学习的肺部CT作为鉴别COVID-19与CAP的一种可靠方法和工具,已得到许多学者的研究证实[3,4,41]。
然而,以往研究多使用LinearSVM或单一的分类模型来鉴别COVID-19与CAP,虽然表现出了优越的效能[25],但没有提出效能最优的分类模型。因为机器学习的分类模型有许多种,因此本研究基于传统的机器学习方法,利用14种机器学习分类模型鉴别COVID-19与CAP,通过AUC来评估分类模型的诊断效能,并取得了很好的结果(AUC均大于0.9)。通过对14种机器学习分类模型的横向对比研究发现,在鉴别诊断COVID-19与CAP方面,Random Forest分类模型的性能最优(AUC=0.9406)。研究表明,组合分类器比单一分类器的分类效果更好,Random Forest是一种利用多个分类树对数据进行判别与分类的组合分类方法,该分类模型可用于判断特征的重要程度以及他们之间是否会相互影响,适用于数据集较多的情况,相对于其他算法有较大的优势。Random Forest还具有数据的随机性和特征选取的随机性,使得随机森林不容易陷入过度拟合,同时也使得随机森林具有很好的抗噪声能力[42],这可能是该模型在本研究中表现出优越效能的原因。
本研究中COVID-19组患者的年龄大于CAP组,两组之间差异有统计学意义,这可能是因为COVID-19好发于中老年人,尤其是患有慢性病的老年人[43,44]。
本研究存在以下局限性:①手动修改科研平台自动分割的病灶,存在一定的不稳定因素,但本研究通过组间一致性分析剔除了不稳定的特征,尽量避免了不稳定特征对结果的影响;②本研究仅使用14种分类模型,而其他机器学习分类模型是否能够有效鉴别COVID-19与CAP,有待进一步研究与开发。因此需要更多大样本、多中心的研究为鉴别诊断COVID-19与CAP提供依据。
综上所述,14种机器学习分类模型均可有效鉴别COVID-19与CAP,具有较高的鉴别诊断效能(AUC值均>0.9),效能最高的模型是Random Forest(AUC=0.9406),能够在早期诊断COVID-19方面发挥优势。

