基于改进C-V模型超声颈动脉图像内-中膜厚度的测量
王晓桐 丁海波 辽宁省医疗器械检验检测院 (辽宁 沈阳 110179)
内容提要:颈总动脉内-中膜厚度是心脑血管疾病早期筛查和诊断的主要标准之一。文章提出了一种基于超声图像的颈动脉内-中膜厚度半自动测量方法。最初在相关的颈动脉超声图像中选择感兴趣的区域,然后采用改进的C-V主动轮廓模型算法,在公式中加入局部强度信息,从而实现了图像局部结构的分割。该算法分为两步,第一步利用改进的C-V方法从超声图像中分割腔-内膜边界。在得到腔-内膜边界后,第二步使用类似的方法检测中-外膜边界。成功分割出腔-内膜和中-外膜边界后,可方便地计算内-中膜厚度。实验结果表明该方法可以在较少的人工输入并且不需要任何预处理步骤的条件下准确地测量内-中膜厚度。
心血管疾病是威胁人类健康的主要疾病之一,动脉粥样硬化是心肌梗死等血管闭塞性疾病的主要病因之一。动脉粥样硬化的早期发现对心血管疾病的预防和治疗非常重要。动脉血管结构和功能的损害是冠心病的病理基础。因此,可以通过动脉血管结构和功能的改变来评估血管的病变情况。颈总动脉较其他动脉血管更容易测量,能较好地反映冠状动脉及其他动脉的变化。所以,医生通常通过颈总动脉来评估血管疾病。在心血管疾病的指标中,如斑块的体积、血管狭窄程度、血管直径等,是影响冠心病的关键因素。因此可以通过血管结构和功能的改变来评估血管疾病,其中颈动脉内-中膜厚度指标应用最为广泛。
与其他成像设备相比,超声设备成本低,操作简单,并且图像的内-中膜厚度测量对人体的危害相对较小,从而得知该方法可用于调查研究。现阶段颈总动脉内-中膜厚度通常手动测量完成,由经过培训的操作员进行分割和测量。但人工操作存在一定的弊端,不可控,并且耗时长,不适合大型图像数据库,降低试验的可重复性。因此,本文提出的半自动分割方法,该方法可以有效避免上述缺点。
1.方法介绍
1.1 颈总动脉内-中膜厚度概念
通常颈动脉超声图像显示,可见三层回声:内膜(回声强而光滑,呈连续光滑的光带),中膜(主要由平滑肌和结缔组织组成,条带呈暗色),外膜(即外膜层的外表面,由疏松结缔组织的外表面组成,其回声带较内膜清晰明亮)。从外膜开始,超声波光束折射两条回波线,第一个边界为腔-内膜界面,第二个边界为中-外膜界面。两个边界之间的距离是内-中膜厚度。在动脉粥样硬化过程中,内膜是最先受影响的部位。颈动脉内-中膜不同节段存在生物学差异。分叉处的内-中膜厚度通常是最厚的,然后是颈动脉的内-中膜厚度。颈动脉内-中膜厚度的分布与颈动脉斑块的分布相对应。因此内-中膜厚度可作为颈动脉粥样硬化的早期标志物。
为了获得相对准确的结果,在本文中选择了颈动脉末端不含斑块的部位。之所以选择这个部分,是因为这个部分在大多数颈动脉超声图像中都很容易发现,这部分血管与超声束垂直,取这部分可以获得较高的图像分辨率,选择终端部分可以避免增益问题。为了测量内-中膜厚度,在采集图像数据时,使用超声需要选用高频传感器,通常是7~12MHz。
1.2 关于颈总动脉内-中膜厚度测量算法介绍
本文提出的半自动颈总动脉内-中膜厚度测量方法,流程图如图1所示。首先,需要选择一个包含颈总动脉末端部分的感兴趣区域。其次,采用改进的C-V方法对腔-内膜边界进行分割。在此分割基础上,选择第二个感兴趣区域,与前两步一样对中-外膜边界进行分割。最后通过测量两边界之间的距离得到内-中膜厚度。
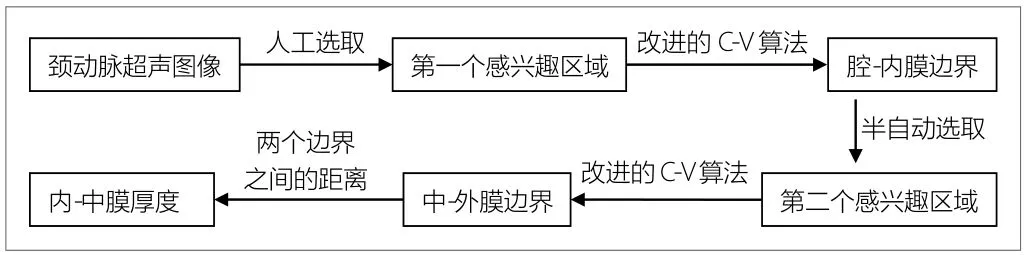
图1.半自动测量方法流程图
1.3 C-V主动轮廓模型介绍
Mumford-Shah模型是Mumford和Shah提出的一种理想的图像处理模型。该模型通过最小化广义能量函数,解决了图像分割、去噪和图像重建的问题。但能量函数不仅包含面积项,而且还包含加长项,求解这个方程要花费很长时间。因此,又提出了简单的Mumford-Shah模型。Chan-Vese方法是一种简单的Mumford-Shah模型,它省略了面积部分而保留了长度方程。假设图像为I(x,y),域集为Ω,演化曲线C由零水平集函数定义C(t)={(x,y)|φ(x,y,t)=0},原始图像为I(x,y),原始图像I(x,y)被划分为内部(insigde(C))和外部(outsigde(C))两个同质区域。能量方程见公式(1)。
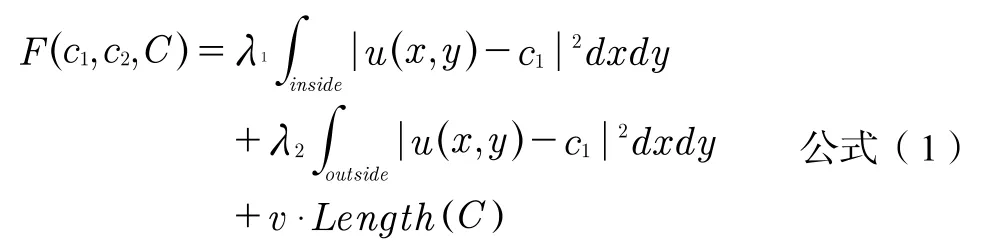
c1,c2是常量,它们分别表示内部区域和外部区域的平均灰度值,因此该模型使用了全局信息。根据水平集方法,将Heaviside函数和Dirac函数定义为公式(2)、公式(3)。
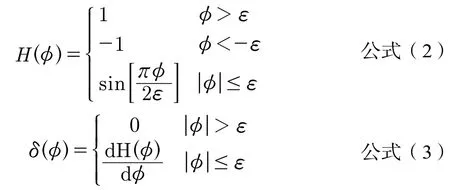
该方法采用Heaviside函数划分演化区域,Dirac函数限定零水平集函数的取值范围。因此,Mumford-Shah模型的能量函数定义为公式(4)。
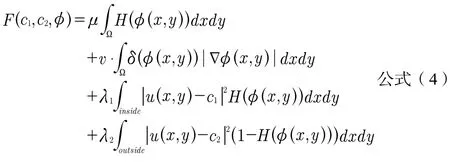
1.4 改进的C-V方法介绍
本文根据超声图像和Chan-Vese模型算法特点,将瑞利分布模型和局部信息增加到Chan-Vese能量函数的分割方法中。
通常不同的成像设备得到的图像噪声的概率分布是不同的。例如,核磁图像的噪声分布为高斯分布,PET为泊松分布,而超声图像的噪声分布为瑞利分布。原有的C-V方法假设噪声分布为分段常数分布,因此不能得到满意的超声图像结果。本文将改变能量函数的噪声分布,使其对应瑞利函数。
瑞利概率分布表示见公式(5):

为了便于计算,将p(u)修改为公式(6):
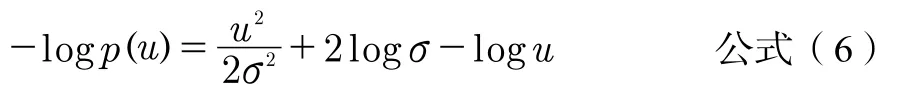
因此,噪声对应于瑞利式函数的C-V模型能量函数修改为公式(7):
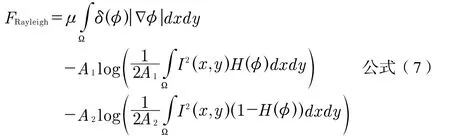
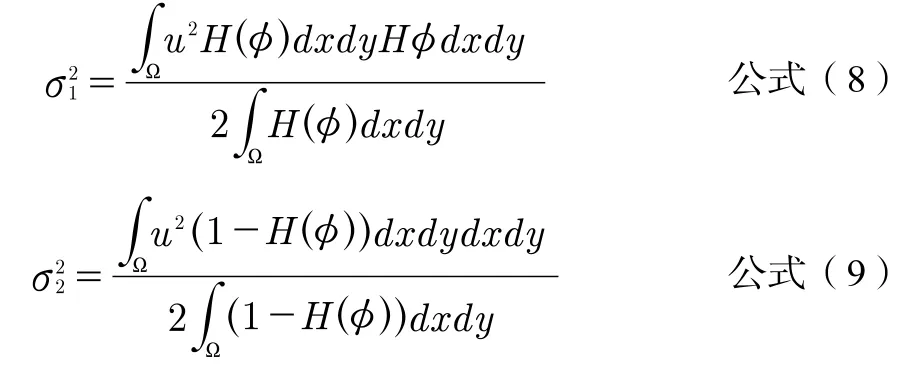
因此,可以得到欧拉-拉格朗日函数见公式(10):
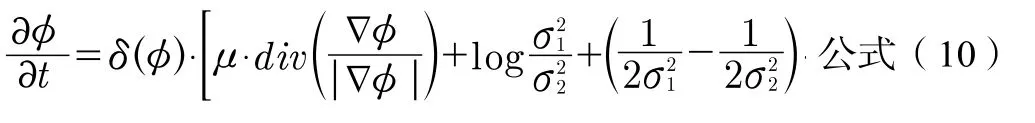
函数(8)、(9)、(10)构成了噪声分布为瑞利式函数的新Chan-Vese模型。
Chan-Vese模型假设图像由目标和背景两个均匀区域组成。但是大多数图像都不能满足这个要求。用于测量颈动脉内-中膜厚度的超声图像中含有大量的散斑噪声,这种现象尤为明显。为了解决这个问题,将局部信息添加到能量泛函中。
在Chan-Vese模型中,分别给出目标区域和背景区域的平均灰度值。本文引入高斯结构因子:。高斯函数G(·)是高斯结构因子见公式(11):
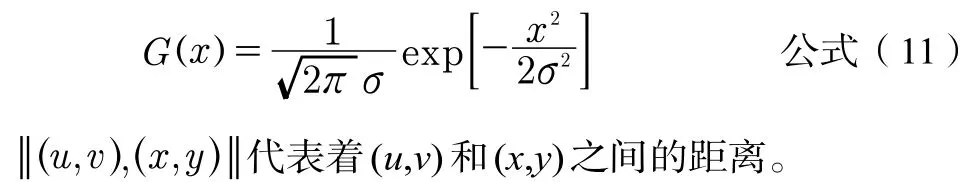
随着(u,v)和(x,y)之间的距离增加,降为0,也就是说只有与(x,y)相邻的点才有意义。考虑到迭代的时间仅在上面的模型中增加局部信息,将能量函数修改为公式(12):
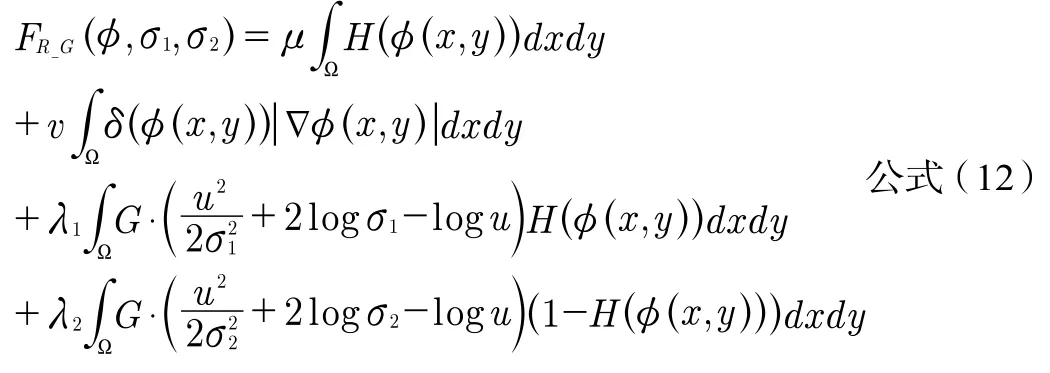
方程(12)是最终演化的Chan-Vese能量方程。
2.试验结果
实验通过测量100张颈动脉超声图像来验证本文提出的方法。在本次实验中,采用改进C-V法进行图像分割得到相应的边界,参数设置为v=0.001×255×255,λ1=λ2=1,Δt=0.1,ε=h=1,σ=3。图像分割过程如图1所示,图1中1a第一幅为原始颈动脉超声图像,试验中人工选取颈动脉末端不含斑块的部位作为第一个感兴趣区域,在此基础上采用改进的C-V算法进行图像分割。第二幅图像所示的白线为分割后得到的腔-内膜界线。
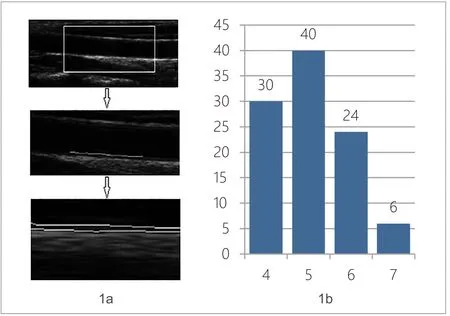
图1.1a图像分割过程,1b内中膜厚度的分布图
第二个感兴趣区域在腔-内膜界线处选取,利用与第一次分割方法相同的改进C-V算法再次进行图像分割,得到中-外膜之间的界线,如第三幅图像显示。在得到腔-内膜界线和中-外膜之间界线后,通过计算得到两个边界之间的像素距离为内-中膜厚度。图1中1b显示100张颈动脉超声图像内-中膜厚度的柱形分布图。本文实验中,选取的100张颈动脉超声图像测量颈动脉末端不含斑块部位的内-中膜厚度,得到最大内-中膜厚度为7个像素值,最小内-中膜厚度为4个像素值,平均内-中膜厚度为5.02个像素值,内-中膜厚度方差为0.4436。
3.小结
在本文中,提出了一种半自动测量颈动脉超声图像内中膜厚度的方法。实验中所要做的唯一人工操作是在颈动脉远端壁周围选择一个感兴趣的区域。根据超声波的噪声分布瑞利分布,推导出了符合瑞利分布的欧拉-拉格朗日函数。对于C-V模型假设图像由目标和背景两个均匀区域组成,在能量函数中加入局部信息,提出改进的C-V模型能较好地分割腔-内膜以及中-外膜边界,从而实现颈动脉超声图像内-中膜厚度的测量。

