LC-MS/MS法测定骨肉瘤患者血清中甲氨蝶呤及其代谢产物7-羟基甲氨蝶呤的浓度*
周 青,张晏洁,薛 源,芮建中,周国华
东部战区总医院 临床药学科,南京210002
骨肉瘤是临床常见的原发性骨恶性肿瘤,好发于儿童与青少年,具有病情进展快、肺转移早、病死率高等特点。目前临床对骨肉瘤的治疗,多以外科治疗为主、化疗或其他治疗为辅[1]。近年来,国内外发布的最新的骨肉瘤诊疗相关指南均推荐甲氨蝶呤(methotrexate,MTX)作为骨肉瘤的一线化疗药物,而大剂量甲氨蝶呤(HD-MTX)联合亚叶酸钙(CF)解救疗法已成为治疗骨肉瘤的重要手段,该方案可显著提高患者的生存率[2]。但由于给药剂量大,MTX 在体内的血药浓度往往较高,在提高疗效的同时也导致毒副反应发生率相应增加,且MTX 在体内代谢具有显著的个体差异,需密切监测患者血药浓度,在确保疗效的同时也减少不良反应的发生。此外,越来越多的研究表明,MTX 体内主要代谢产物7-羟基甲氨蝶呤(7-OH MTX)的血药浓度与MTX 不良反应具有相关性[3]。因此,同时监测MTX 及7-OH MTX 的血药浓度可更为精准、灵敏地预判HD-MTX 临床不良反应的发生,这对于临床合理用药具有重要意义[4]。
本研究建立了一种快速、准确、灵敏的LC-MS/MS 定量分析方法,能够同时测定人血清中MTX 和7-OH MTX 的药物浓度,并应用于临床治疗药物监测(TDM),同时为MTX 人体药动学研究及个体化用药实践提供方法学参考。
1 仪器与药品、试剂
1.1 仪器
Agilent 1260 高效液相色谱仪(美国Agilent 公司);API 4000 三重四级杆质谱仪(美国AB 公司);涡旋混合仪(美国Scientific Industries 公司);高速冷冻离心机(美国Beckman 公司);十万分之一电子天平(瑞士Mettler Toledo 公司)。
1.2 药品与试剂
甲氨蝶呤对照品(纯度99.8%,批号100138-201606,中国食品药品检定研究院);7-羟基甲氨喋呤(7-OH MTX)对照品(纯度97%,批号4-JSH-16-2,Toronto Research Chemicals);内标氨基蝶呤(IS)对照品(纯度≥97%,批号039M4021V,Sigma)。甲醇、乙腈、甲酸为色谱纯;超纯水。
人血清(批号20200508,北京鑫泉永硕科技有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent Zorbax Eclipse Plus C18(2.1 mm×100 mm,3.5 μm);柱温:35 ℃;流动相:含0.1%甲酸的水溶液(A 相)和含0.1%甲酸的乙腈溶液(B 相)(梯度洗脱:0~0.5 min,95%A;0.5~1.2 min,95%~20%A;1.2~3.5 min,20%A;3.5~3.6 min,20%~95%A;3.6~6.5 min,95%A);流速:0.4 mL·min-1;进样量:2 μL。
2.2 质谱条件
离子源:电喷雾源(ESI);正离子模式;离子源电压(IS):5500 V;离子源温度(TEM):550 ℃;碰撞气体(CAD)压力9 psi;气帘气(CUR)压力:25 psi;雾化气(GS1,N2)压力55 psi,辅助气(GS2,N2)压力55 psi。多反应监测(MRM)离子对,MTX、7-OH MTX和内标氨基蝶呤(IS)的监测离子对、去簇电压(DP)、入口电压(EP)、碰撞能量(CE)、碰撞室出口电压(CXP)等见表1。
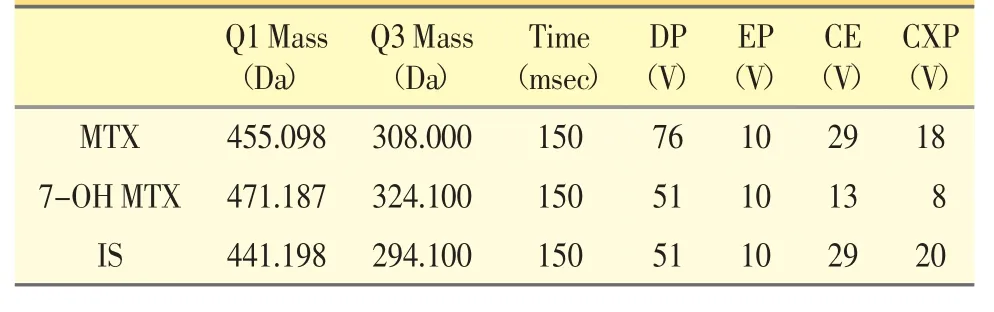
表1 质谱条件
2.3 对照品和内标溶液的配置
分别精密称取MTX、7-OH MTX 对照品各5.0mg,分别置于10mL 量瓶中,用甲醇(含0.1N NaOH)溶解并定容至刻度,配制浓度均为500μg·mL-1储备液,于冰箱-80 ℃避光保存。使用时以甲醇-水(50/50)进一步稀释成所需浓度的MTX 和7-OH MTX 标准曲线工作液(浓度分别为MTX:20、50、100、200、500、1000、2000、5000、10 000 ng·mL-1;7-OH MTX:200、500、1000、2000、5000、10 000、20 000、50 000、100 000 ng·mL-1)。
精密称取氨基蝶呤对照品5.0 mg,置于10 mL量瓶中,用甲醇溶解并定容至刻度,配制浓度为500 μg·mL-1储备液,于冰箱-80 ℃避光保存。最后用甲醇稀释至浓度为20 ng·mL-1的内标工作液。
2.4 样品处理
精密吸取血清40 μL,置1.5 mL EP 管中,再加入含氨基蝶呤的内标工作液(20 ng·mL-1)160 μL,涡旋混匀1 min,12 500 r·min-1离心10 min;取上清液至进样瓶,作LC-MS/MS 分析。
2.5 专属性考察
在“2.1 和2.2”项检测条件下,取空白人血清、空白人血清+MTX+7-OH MTX、骨肉瘤患者MTX 化疗后血清,分别按“2.4”项下方法处理样品后,进样分析。结果表明,MTX、7-OH MTX 和内标IS 的色谱峰形良好,其保留时间分别为2.71、2.73 和2.68 min,而空白血清中未发现有内源性物质干扰待测物和内标的测定,表明该方法专属性良好。见图1。
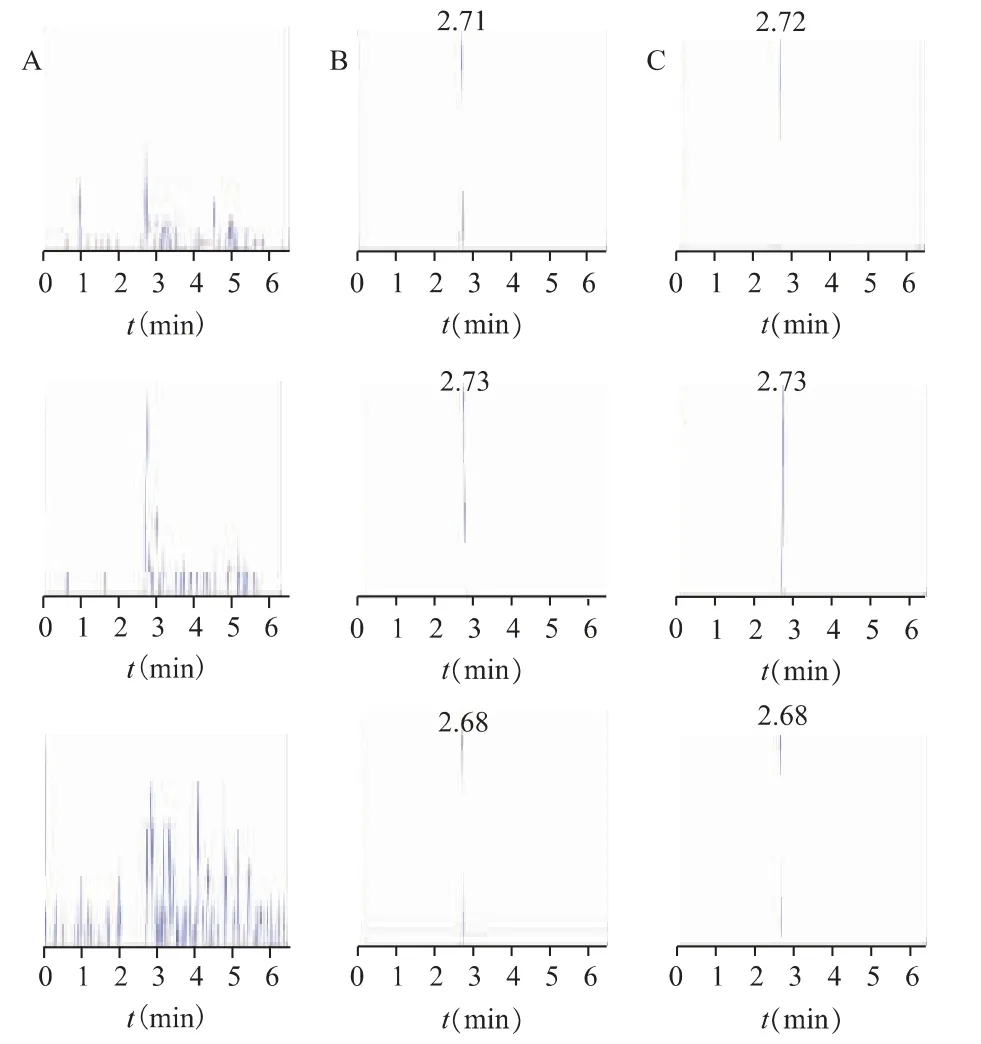
图1 血清中MTX、7-OH MTX 和IS 的MRM 色谱图
2.6 标准曲线的绘制
取空白血清90 μL,分别加入10 μL 不同浓度的系列标准曲线工作液,配制成含MTX 浓度为2、5、10、20、50、100、200、500、1000 ng·mL-1及含7-OH MTX浓度为20、50、100、200、500、1000、2000、5000、10 000 ng·mL-1系列血清标准曲线样品,并按“2.4”项下方法处理,进样2 μL。经LC-MS/MS 分析,以样品峰面积与IS 峰面积之比(Y)为纵坐标,以血清样品浓度(X)为横坐标,作线性回归,经“1/X2”权重得MTX 和7-OHMTX 的回归方程;分别为:Y=0.0638X-0.0754(r=0.998 5),Y=0.005 3X+0.0452(r=0.998 4)。结果表明,MTX 及7-OH MTX 分别在2~1000 ng·mL-1及20~10000 ng·mL-1线性关系良好。
2.7 精密度与准确度试验
分别配制MTX 浓度为2、4、80、800 ng·mL-1,7-OH MTX 浓度为20、40、800、8000 ng·mL-1的血清样品。按“2.4”项下方法处理血清样品,每个浓度日内平行测定6 份,连续测定3 天,根据当天的标准曲线,计算待测物峰面积与内标峰面积比值,代入相应标准曲线得到实测浓度,计算日内、日间精密度和准确度。结果见表2。
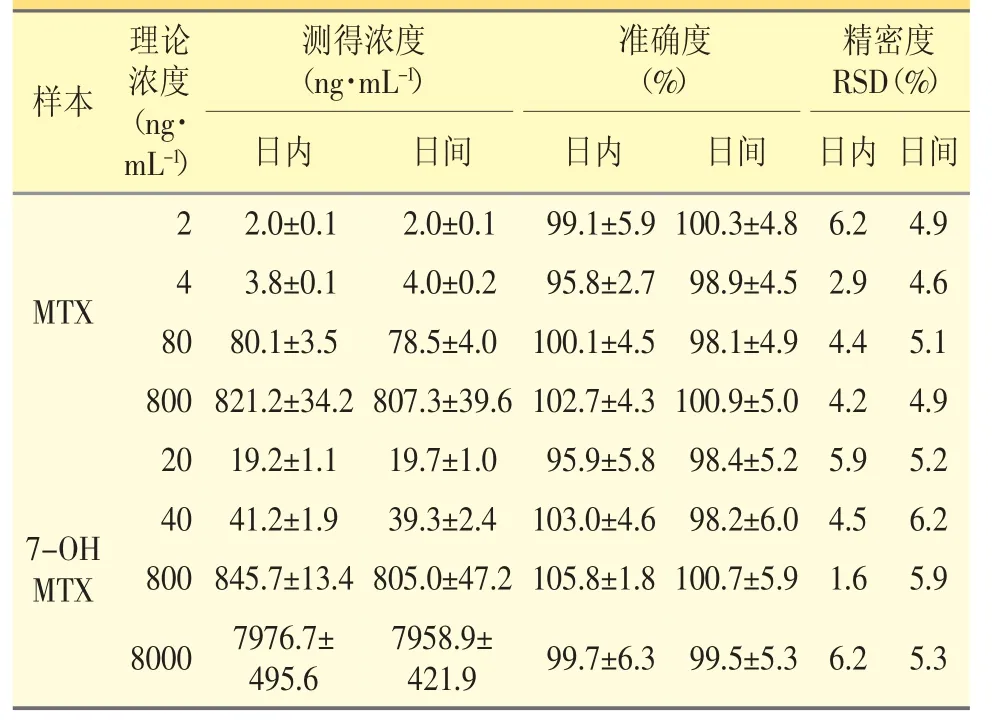
表2 血清中MTX 及7-OH MTX 浓度测定的精密度与准确度(n=6)
2.8 稳定性试验
分别配制MTX 浓度为80、800 ng·mL-1,7-OH MTX 浓度为800、8000 ng·mL-1的血清质控样品。按“2.4”项下方法处理血清样品,分别考察血清样本室温下放置8 h、4 ℃中放置24 h、反复冻融3 次和-20 ℃冷冻放置7 d 后MTX 和7-OH MTX 的稳定性。每个浓度平行测定5 份。结果表明,两个浓度质控样品在4 种储存条件下稳定,结果见表3。
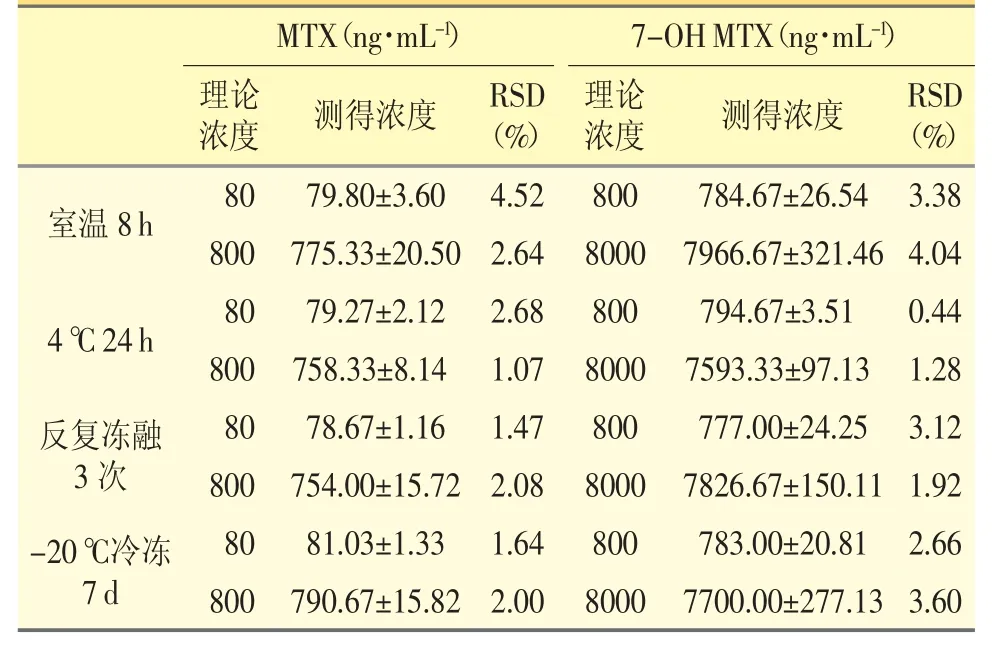
表3 血清中MTX 及7-OH MTX 浓度测定的稳定性(n=5)
2.9 基质效应与提取回收率
分别配制MTX 浓度为2、4、80、800 ng·mL-1,7-OH MTX 浓度为20、40、800、8000 ng·mL-1的血清样品,按“2.4”项下方法处理血清样品,每个浓度平行测定5 份,进样获得相应峰面积A;另取空白血清,按“2.4”项下方法处理空白血清(其中,内标工作液换成纯甲醇),再用提取的上清液分别配制MTX浓度为2、4、80、800 ng·mL-1,7-OH MTX 浓度为20、40、800、8000 ng·mL-1的样品,按“2.4”项下方法处理样品,每个浓度平行测定5 份,进样获得相应峰面积B;以流动相分别配制MTX 浓度为2、4、80、800 ng·mL-1、7-OH MTX 浓度为20、40、800、8000 ng·mL-1的样品。按“2.4”项下方法处理样品,每个浓度平行测定5 份,进样获得相应峰面积C。计算MTX、7-OH MTX 及IS 的基质效应和提取回收率,公式为:基质效应=(B/C)×100%;提取回收率=(A/B)×100%。结果见表4。

表4 血清中MTX、7-OH MTX 及IS 浓度测定的基质效应与提取回收率(n=5)
2.10 临床应用
临床骨肉瘤患者2 例,均为男性,年龄分别为17、19 岁,MTX 化疗剂量分别为5.38、6.00 g·m-2。给药后于不同时间点(~4 h、~8 h、~24 h、~48h、~72 h)测定血清中MTX 及7-OH MTX 的浓度,其中,第1、2、3 个时间点(~4 h、~8 h、~24 h)的血清,在按照“2.4”项下方法处理样品前,分别用空白血清稀释1000、200、10 倍。结果见表5、表6。
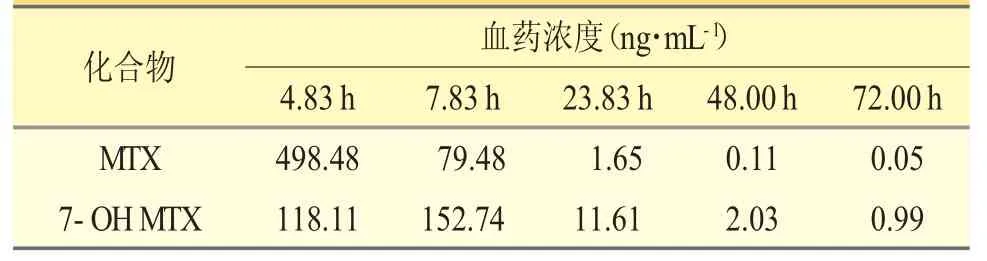
表5 骨肉瘤患者1 的血药浓度监测结果
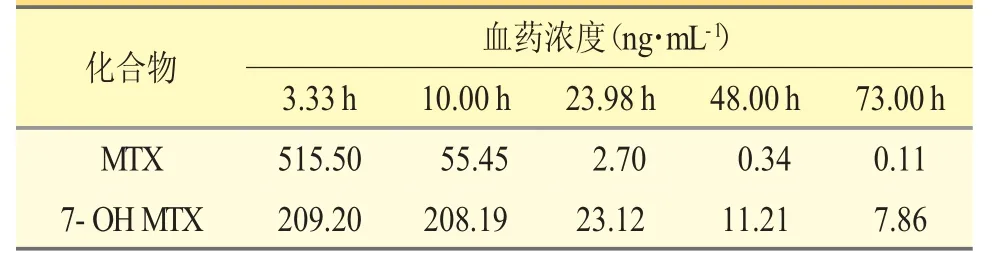
表6 骨肉瘤患者2 的血药浓度监测结果
3 讨论
MTX 是一种抗叶酸类抗肿瘤药物,能够竞争性地抑制细胞中二氢叶酸还原酶的活性,阻止二氢叶酸还原为四氢叶酸,使得嘌呤、嘧啶核苷酸的合成受阻,从而抑制DNA 的生物合成,最终抑制肿瘤细胞的生长与繁殖。大剂量甲氨蝶呤(HD-MTX)联合亚叶酸钙(CF)解救是治疗骨肉瘤重要方案之一。
MTX 细胞毒作用具有非特异性,在杀伤肿瘤细胞的同时对快速分裂的正常细胞(骨髓细胞、肝细胞等)也会造成一定的细胞毒作用,而大剂量使用甲氨蝶呤则意味着毒性加剧。临床上常采用CF 进行解救,但CF 解救HD-MTX 引起的不良反应的同时也会拮抗MTX 的药理作用,减弱MTX 对肿瘤细胞的毒性作用,从而影响治疗效果;并且使MTX 药代动力学特征存在较大的个体差异。因此,HD-MTX化疗后,需进行MTX 血药浓度监测,适时、适量地给予CF 解救,在保证HD-MTX 治疗效果的同时,还能防止严重不良反应的发生。有研究表明,MTX体内主要代谢产物7-OH MTX 的血药浓度与MTX给药后的不良反应(肾毒性、肝毒性等)相关。因此,本研究选择同时测定MTX 和7-OH MTX 的血药浓度,为实行个体化用药提供科学的指导依据。
目前,临床常用的治疗药物监测方法有化学发光免疫分析法(CLIA)[5]和高效液相色谱法(HPLC)[6,7]。CLIA 法虽然操作相对简单、自动化程度高;但其配套的试剂盒成本较高,且易受代谢产物的干扰和发生交叉反应,会影响测定结果的准确性。HPLC 法虽然灵敏度高、选择性较好;但存在样品前处理复杂、分析时间较长等缺点,难以满足临床时效性和大样本的快速检测。相比而言,LC-MS/MS 法具有灵敏度高、特异性强、检测速度快、检测限低等优势。
综上所述,骨肉瘤患者经HD-MTX 化疗后,进行治疗药物监测,指导临床个体化用药是很有必要的。本研究建立了一种快速、简单、灵敏度高、准确度好的LC-MS/MS 检测方法,用于同时监测MTX及其代谢产物7-OH MTX 的血药浓度,对临床实施个体化HD-MTX 联合CF 治疗方案、保障治疗效果及用药安全具有指导意义。