硅热还原炼镁中固体废渣的氨浸提钙
严艳文,刘 燕,毛帅东,李小龙,张廷安
(东北大学 冶金学院,沈阳110819)
我国原镁产量自20世纪90年代末超过美国以来,长期保持世界首位并持续快速增长,在2017年已突破100万t.目前,硅热还原法生产金属镁[1]仍然是主要方法,据统计,每生产1 t金属镁,要产生6.5~8 t镁渣[2],以此推算我国每年产生的镁渣高达数百万吨.其中,少部分的镁渣应用于生产建筑材料[3-4]、工业脱硫剂[5-6]、农业肥料[7-8]或微晶泡沫玻璃[9]等领域,然而大部分的镁渣通过填埋或堆积的方式处理,这不仅浪费和污染土地资源,而且极易造成空气污染,引起呼吸系统疾病.因此,镁渣的资源化利用具有良好的环境效益和经济效益.
此外,我国也是碳排放大国,随着工业化进程的不断深入,导致煤炭等化石燃料的大量消耗,产生大量的CO2等温室气体.为了实现2060年争取碳中和的目标,减少CO2的排放刻不容缓.当前,冶金生产中主要通过调整能源结构、优化过程工序、改善管理水平等途径来从源头上减少CO2排放,但由于替代能源发展尚不成熟,这些措施的作用受到一定限制.目前,CO2的捕收与储存受到学者们的广泛关注[10-12].捕集封存CO2的技术有地质掩埋、生物固定、海洋储存以及CO2矿物碳酸化固定等[13].“矿物碳酸化”的概念由Seifritz[14]提出,是指利用矿物发生碳酸化反应生成碳酸盐来固定CO2,相较于其他CO2储存方式,该技术得到的产物性质稳定且可长期存放.近年来已有许多利用冶金固体废弃物碳酸化固定CO2的研究,如Baciocchi等[15]采用直接湿法工艺,探讨了不锈钢钢渣的粒径对其CO2储存能力的影响,结果表明,随着粒径尺寸的降低,钢渣能够储存的CO2的重量减少,在最佳颗粒粒径条件下,1 kg不锈钢钢渣可以固定130 g的CO2;日本学者Kodama等[16]则提出了一种以NH4Cl溶液浸出钢渣的间接碳酸化固定CO2的工艺路线,该工艺下钢渣中钙的浸出率达60%,获得的产品CaCO3纯度高,且可实现NH4Cl溶液的循环利用;张慧宁等[17]研究了NH4Cl溶液浸出电弧炉钢渣的过程,考察了NH4Cl浓度、钢渣粒度、浸出时间、浸出温度等参数对钙离子浸出的影响,建立了动力学模型,结果表明,随着NH4Cl浓度和浸出温度的增大,钙离子的转化率升高,且浸出反应受扩散过程的控制.
镁渣作为一种富含钙、镁元素的碱性固体废弃物,是固定工业排放CO2的理想原料.基于此,本文提出了“氨浸提钙—碳化固钙”的新工艺路线,即采用NH4Cl溶液浸出镁渣,将钙元素转变为溶液中的离子形态,再将CO2气体与浸出液反应,同时固定碳和钙,获得高纯碳酸钙粉体,碳化后的NH4Cl溶液可返至浸出工序,实现氨的循环利用.其完整的工艺流程如图1所示.

图1 “氨浸提钙—碳化固钙”工艺流程图Fig.1 Process including ammonia extraction of calcium and carbonation fixation of calcium
本文重点研究了氨浸提钙工序,主要考察浸出温度、浸出时间、液固比、NH4Cl质量分数和粒度等工艺参数对镁渣中钙元素浸出行为的影响,并获得适宜的工艺参数,为镁渣的资源化利用提供理论基础.
1 试 验
1.1 试验材料
本试验所用硅热还原炼镁渣来自陕西某镁厂,经研磨后筛分为150~270μm,96~150μm,74~96μm和≤74μm四个粒度等级.采用X射线荧光光谱仪分析了镁渣的主要成分,如表1所示.采用X射线衍射仪分析了镁渣的物相组成,并在20°~40°之间局部放大,如图2所示.

图2 镁渣的XRD图Fig.2 XRD pattern of magnesium residue

表1 镁渣的化学成分(质量分数)Table 1 Chemical composition of magnesium residue(mass fraction) %
从表1可以看出,镁渣的主要化学组成是CaO和SiO2,而MgO,Fe2O3等含量较低.XRD分析结果表明,镁渣中的主要含钙物相为Ca2SiO4,除此之外还有少量的MgO,其中Ca2SiO4有γ相和β相两种形态,这是由于镁渣在出炉后缓慢冷却,当温度降至400~500℃,大部分亚稳态的β-C2S转变为稳态的γ-C2S所致[18].
1.2 试验方法
本试验采用100 mL烧杯作为NH4Cl溶液浸出镁渣的反应容器.首先按某一液固比量取一定体积的去离子水,加入烧杯后置于恒温水浴锅中加热,待水温达到设定温度后,加入5 g镁渣和一定质量分数的NH4Cl,开启搅拌模式,转速为400 r/min,并控制浸出时间.表2为浸出实验设计参数.
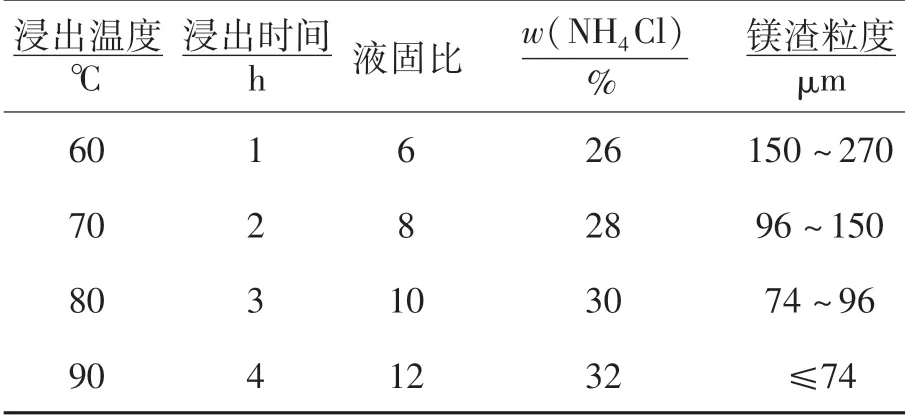
表2 浸出实验设计参数Table 2 Leaching experiment parameters
待浸出结束后,进行固液分离,并将滤液定容至250 mL.使用移液管从中取1 mL溶液,根据EDTA滴定法测定溶液中钙的浓度,以此计算钙的浸出率,计算公式如式(1)所示:
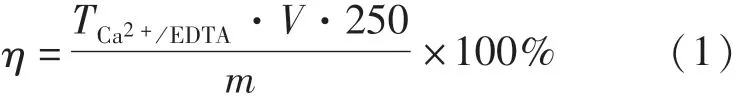
式中:η为钙的浸出率,%;TCa2+/EDTA为1 mL EDTA标准溶液相当于钙的质量,g/mL;V为滴定时消耗EDTA标准溶液的体积,mL;m为镁渣中钙的质量,g.
2 结果与讨论
2.1 浸出过程的热力学计算
镁渣中的含钙物相在浸出过程中发生的化学反应如式(2)所示,Ca2SiO4在NH4Cl的作用下分解为Ca2+和SiO2,NH4Cl则转变为氨水,并进一步分解产生氨气.

在298~373 K的温度范围内,假定NH4Cl质量分数30%,钙浸出率80%的条件下,根据范特霍夫方程:ΔG=ΔGɵ+RTlnK,其中K为该过程的化学平衡常数,计算得出实际反应的吉布斯自由能与温度的变化关系如图3所示.

图3 浸出反应在不同温度下吉布斯自由能的变化Fig.3 Variety of Gibbs free energy of leaching reaction at different temperature
由图3可以看出,随着反应体系温度的升高,该反应的吉布斯自由能不断减小直至小于零,表明升高温度有利于镁渣的浸出.此外,随着NH3气体分压的降低,反应进行的趋势增大.当p(NH3)/pɵ=1时,反应在358 K时才能发生;然而当p(NH3)/pɵ=0.2时,浸出反应发生的起始温度下降为328 K.由于本实验是在敞口体系中进行的,反应生成的NH3不断挥发,则NH3分压必然小于pɵ.因此在本实验条件下,镁渣中的Ca2SiO4可不断地被分解产生钙离子溶液.
2.2 硅热还原炼镁渣的氨浸实验
采用单因素研究方法,分别考察了浸出温度、浸出时间、液固比、NH4Cl质量分数、镁渣粒度等因素对镁渣中钙浸出效果的影响.
2.2.1 浸出温度的影响
采用质量分数为30%的NH4Cl溶液作浸出剂,液固比10,反应时间2 h,镁渣粒度≤74μm,考察氨浸过程中温度对钙浸出率的影响,结果如图4所示.
由图4可知,随着温度的升高,钙的浸出率显著增大.NH4Cl在水溶液中电离后,NH+4水解生成NH3·H2O和H+,其标准状态下(25℃)的水解常数为5.71×10-10[19],计算公式如下:

图4 浸出温度对钙浸出率的影响Fig.4 Effect of leaching temperature on leaching efficiency of calcium
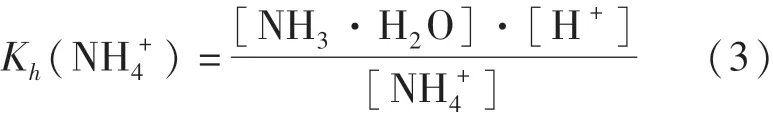
2.2.2 浸出时间的影响
采用质量分数为30%的NH4Cl溶液作浸出剂,液固比10,反应温度90℃,镁渣粒度≤74μm,考察氨浸过程中浸出时间对钙浸出率的影响,结果如图5所示.
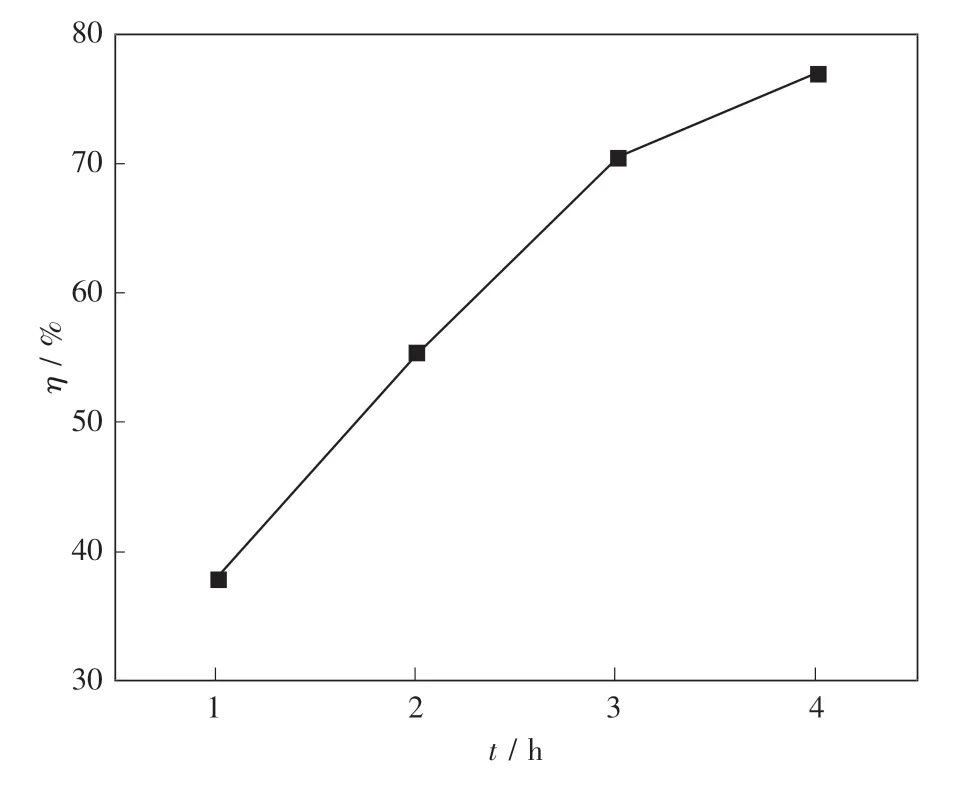
图5 浸出时间对钙浸出率的影响Fig.5 Effect of leaching time on leaching efficiency of calcium
由图5可以看出,钙的浸出率随着浸出时间的延长而增加,始终呈上升趋势,但上升的速度逐渐减缓,在浸出4 h后钙的浸出率达到77.01%.根据热力学计算结果可知,当NH3分压较低时,在浸出温度范围内镁渣中主要含钙物相Ca2SiO4可以被浸取,延长反应时间,可以增大反应的进行程度,溶液中钙的浓度随之增加.同时镁渣中的Si开始析出,形成硅胶,易在镁渣颗粒表面形成保护膜,阻碍NH4Cl溶液和镁渣接触,导致钙的浸出速度降低.由于颗粒表面的SiO2被吸附沉淀需要一定时间,综合考虑浸出时间取2 h为宜.
2.2.3 液固比的影响
采用质量分数为30%的NH4Cl溶液作浸出剂,反应温度90℃,反应时间2 h,镁渣粒度≤74μm,考察氨浸过程中液固比对钙浸出率的影响,结果如图6所示.
由图6可以看出,浸出反应的液固比从6升至12的过程中,钙的浸出率逐渐增大.在液固比增大到10之前,浸出率增加的速度较快,但从10增至12时,浸出率变化不大.随着液固比的增加,浸出体系中镁渣的含量越低,单位质量的镁渣对应的NH4Cl溶液越多,使得镁渣与浸出剂的反应概率增大,从而提高了钙的浸出率.考虑到更大液固比对钙浸出率影响较小,因此液固比取10为宜.

图6 液固比对钙浸出率的影响Fig.6 Effect of liquid-solid ratio on leaching efficiency of calcium
2.2.4 NH4Cl质量分数的影响
采用不同质量分数的NH4Cl溶液作浸出剂,液固比10,反应温度90℃,反应时间2 h,镁渣粒度≤74μm,考察氨浸过程中NH4Cl质量分数对钙浸出率的影响,结果如图7所示.

图7 NH 4 Cl质量分数对钙浸出率的影响Fig.7 Effect of NH 4Cl mass fraction on leaching efficiency of calcium
由图7可以看出,在浸出过程中,NH4Cl质量分数对钙浸出率的影响相对较小,随着NH4Cl质量分数的增加,钙的浸出率逐渐有所提高,这是因为浸出液质量分数增加,使得镁渣颗粒表面的含钙相与之有效碰撞的机会增多,反应速率随之加快,从而促进了镁渣中钙的浸出.在NH4Cl质量分数增大到30%时,镁渣浸出过程接近平衡,继续增大NH4Cl质量分数,钙的浸出率变化不大,因此NH4Cl质量分数取30%为宜.
2.2.5 粒度的影响
采用质量分数为30%的NH4Cl溶液作浸出剂,液固比10,反应温度90℃,反应时间2 h,考察氨浸过程中不同粒度等级(150~270μm,96~150μm,74~96μm和≤74μm)对钙浸出率的影响,结果如图8所示.
由图8可以看出,粒度越细,镁渣中钙的浸出率越高,这是因为物料的粒度越小,其比表面积越大,与溶液中NH4Cl的接触越充分,越有利于钙的浸出,反应进行的程度越大.
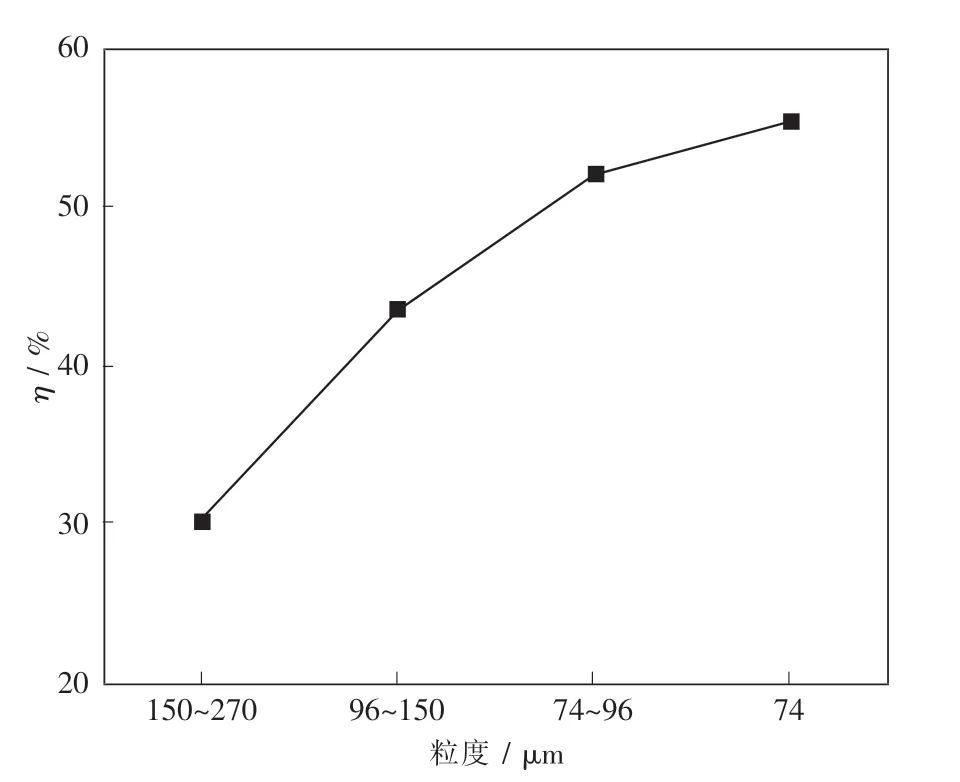
图8 粒度对钙浸出率的影响Fig.8 Effect of particle size on leaching efficiency of calcium
2.3 镁渣浸出产物物相分析
图9所示为试验条件NH4Cl质量分数30%,浸出温度90℃,液固比10,浸出时间4 h的浸出渣与未处理镁渣的XRD图比较.由图9可以看出,镁渣中以γ相和β相存在的Ca2SiO4的衍射峰明显削弱,说明镁渣中钙、硅的含量大幅降低,而MgO则始终留在渣相中.

图9 原料与浸出渣的XRD图Fig.9 XRD patterns of raw material and leaching residue
3 结 论
(1)在328~363 K的温度区间内,当NH4Cl质量分数30%,钙浸出率80%的条件下,p(NH3)/pɵ=0.2时,镁渣中Ca2SiO4物相浸出反应的吉布斯自由能ΔG<0,表明Ca2SiO4可以被分解生成Ca2+溶液.
(2)粒度越细,温度越高,钙的浸出率越大;增大液固比,提高NH4Cl质量分数,钙的浸出率随之增加.
(3)在NH4Cl质量分数30%,浸出温度90℃,液固比10,浸出时间4 h的条件下,钙的浸出率可达77.01%.浸出渣的物相分析表明,镁渣中的钙能够浸出,而MgO仍残留在渣相中.浸出的钙离子溶液可用于后续CO2的矿化固定,制备碳酸钙粉体.本试验为镁渣中钙基组分浸出及镁渣的综合利用提供了新的思路,为后期碳酸化固定提供了理论参考.

