颅内孤立性纤维瘤复发伴颅内多发转移1例☆
孙冬冬 狄广福 周欢 江晓春
孤立性纤维瘤(solitary fibrous tumor,SFT)是一种间质来源的纤维增生性肿瘤,好发于胸膜、脑膜和胸外软组织[1]。近年来,研究发现SFT与血管外皮细胞瘤(hemangiopericytoma,HPC)有重叠病理和免疫组织学特征[2],颅内SFT较少见,绝大多数是良性,很少复发或转移。皖南医学院弋矶山医院神经外科收治了1例8年前因SFT行手术治疗,术后定期复查提示肿瘤复发并颅内多发转移,现报告如下。
1 临床资料
患者,男,67岁,因“间断头昏2月余”入院。专科查体:神志清,精神可,12对脑神经未见异常,左侧额颞部可见一长约15 cm手术疤痕,切口愈合良好,四肢肌力、肌张力正常,生理反射存在,病理反射未引出。无家族遗传病史。8年前因“间断头昏4月余”收住我科,头颅MRI平扫+增强(2012年5月16日 皖南医学院弋矶山医院)提示:左侧颞部见6.0 cm×5.0 cm×4.0 cm不规则团块状占位,呈稍短T1、等T2混杂信号,病灶周围少许水肿信号影(图1A、B);增强后明显不均匀强化,占位效应明显(图1C、D、E),脑膜尾征不明显。治疗采用“左侧额颞颧入路中颅底脑肿瘤病变切除术”,术中见左颞叶皮层下肿物,质地较硬,色灰黄,血供丰富。瘤内有钙化、囊变、坏死,肿瘤与颞骨和小脑幕相贴,易分离。术后患者头昏症状消失,无术后并发症,术后 3个月复查 MRI提示肿瘤全切除 (图 1F、G、H)。病理回报提示左侧中颅窝底中间型SFT,免疫组化:CD34(+)、AE1/AE3(-)、EMA(-)、S-100(-)、Desmin(-)、SMA(-)、Ki-67(+,5%)、ER(-)(图 2),术后未接受放化疗。本次入院行头颅MRI平扫+增强(2020年9月29日 皖南医学院弋矶山医院)提示:左侧颞顶部颅板下多发大小不等结节状、团片状类圆形稍长T1、稍长T2信号病灶,较大截面约4.0 cm×3.8 cm(图3A、B),增强扫描病灶明显不均匀强化,邻近脑膜增厚(图 3C、D、E)。颈、胸、腰椎 MRI检查提示未见转移灶(图3J)。完善检查后原切口入路行手术治疗,术中见部分脑组织粘连,分离颞叶软化灶,见多发孤立肿瘤6枚,基底分布于颞底硬脑膜及小脑幕上,肿瘤呈红色,血供丰富,质地软硬不均(图 3F)。术后复查提示肿瘤全切除(图 3G、H、I)。病理回报提示非典型SFT,细胞中度异型,每10个高倍视野核分裂象5~10个,未见坏死。免疫组化:瘤细胞CD34(+),CD99(+),EMA(-),PR(-),S-100(-),SMA(-),Desmin(-),AE1/AE3(-),Ki-67(+,12%~15%),STAT6(+)(图 4)。术后随访8月余,未见肿瘤复发,头昏症状未出现。
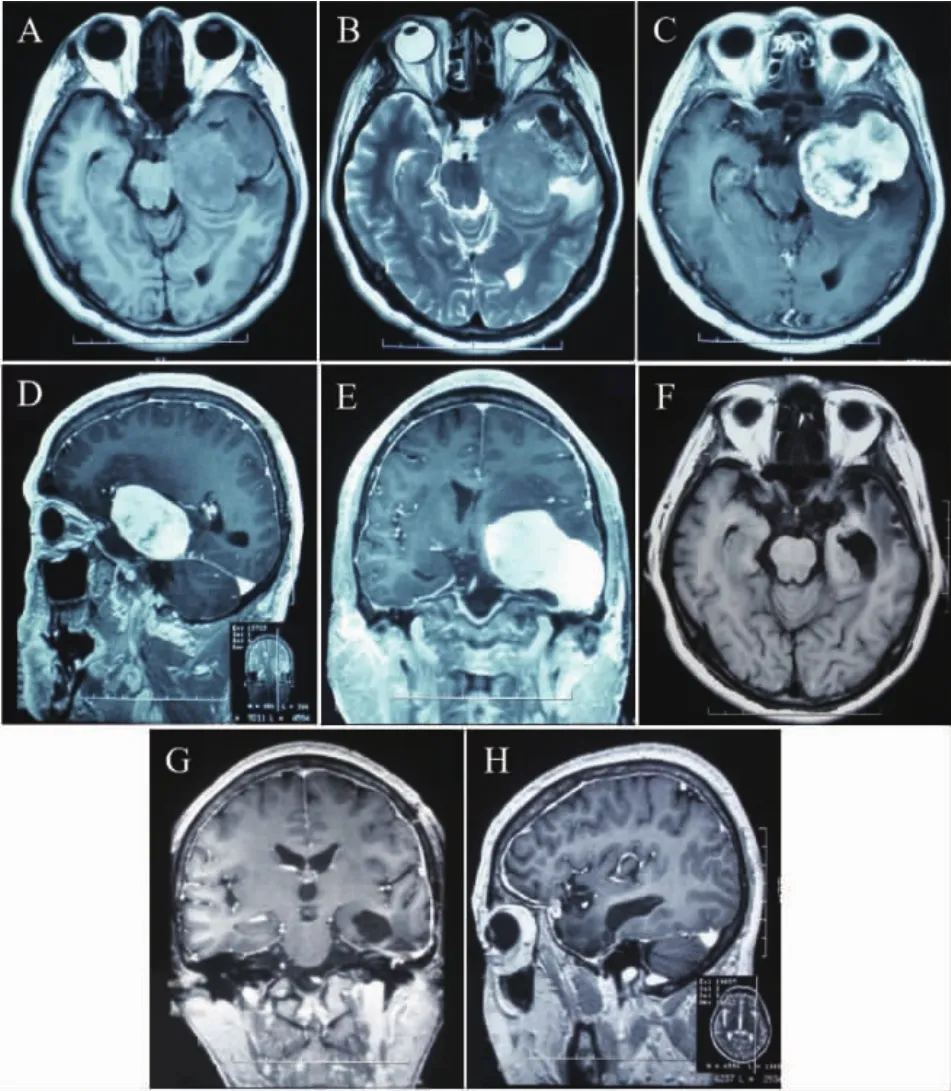
图1 第1次术前头颅MRI平扫+增强及术后3个月MRI A、B.头颅MRI轴位T1、T2像见左侧颞部不规则团块状占位,呈稍短T1、等T2混杂信号,病灶周围伴水肿;C~E.MRI增强轴位、矢状位、冠状位见肿瘤明显不均匀强化,占位效应明显;F~H.术后3个月头颅MRI复查见肿瘤全切除。
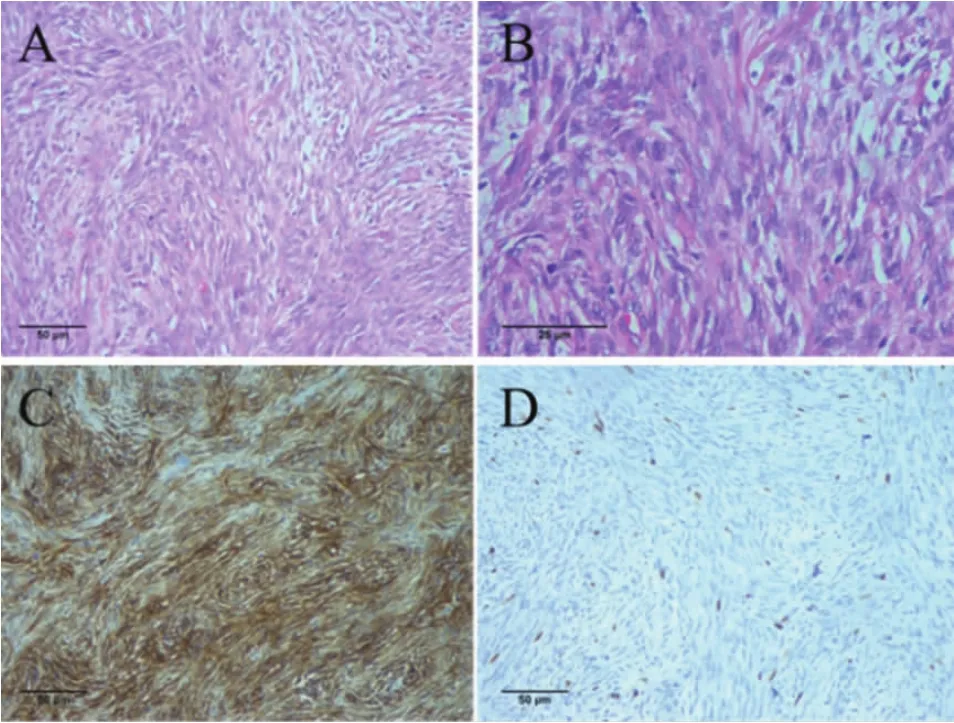
图2 第1次术后病理 A、B.HE染色(A 200×、B 400×)见肿瘤由梭形细胞及不同比例的胶原纤维组成,肿瘤细胞富于细胞区与疏松区交替排列,富于细胞区,瘤细胞多呈梭形,染色质呈点状均匀分布或边集核膜,核仁可见,细胞异性不明显,无核分裂;C.免疫组化 CD34阳性(200×); D.Ki-67指数约 5%(200×)。

图3 第2次术前头颅MRI平扫+增强、术中影像及术后3个月MRI AB.头颅MRI轴位T1、T2像见左侧颞部团片状稍长T1、稍长T2信号占位;C-E.头颅MRI增强轴位、矢状位、冠状位见病灶显著欠均匀强化,小脑幕缘多发大小不等结节,邻近脑膜增厚;F.术中见颞底硬脑膜及小脑幕多发肿瘤,肿瘤之间相互独立,肿瘤呈淡红色,血供丰富,质地软硬不均;G~I.术后3个月头颅MRI复查见肿瘤全切除;J.全脊椎MRI平扫未见肿瘤转移。
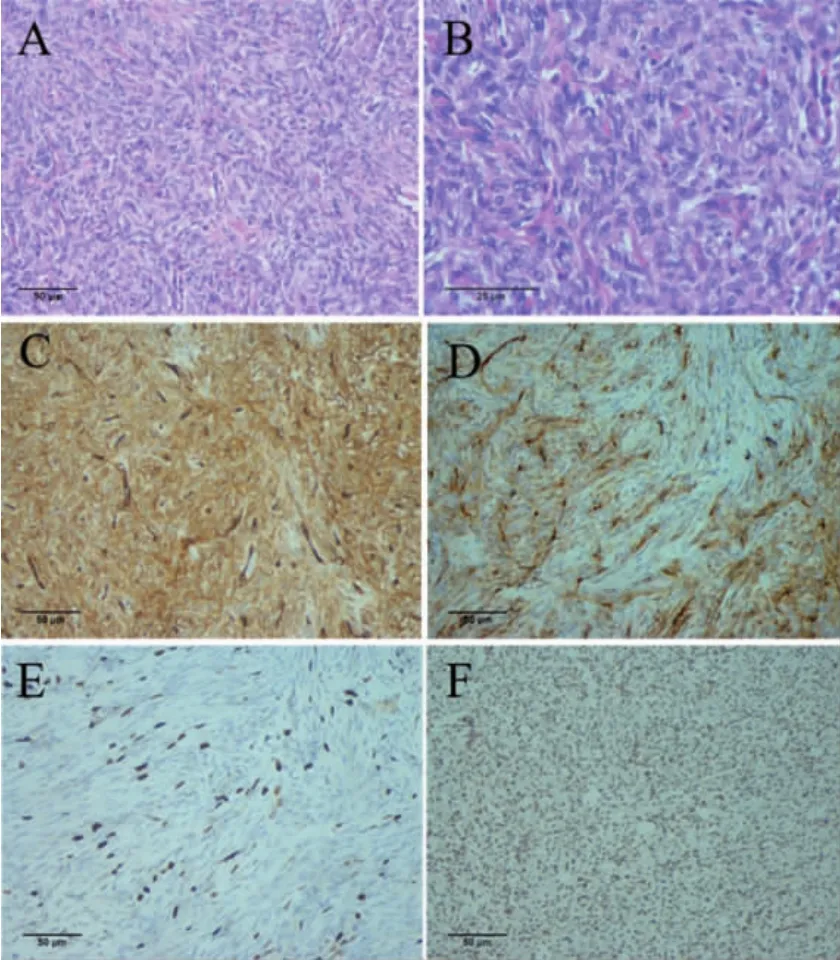
图4 第2次术后病理 A、B.HE染色(A 200×、B 400×)见肿瘤梭形细胞及不同比例的胶原纤维组成;C.免疫组化提示 CD34 阳性(200×);D.CD99 阳性(200×);E.Ki-67指数约 12%~15%(200×);F.肿瘤细胞免疫反应提示STAT6 阳性(200×)。
2 讨论
CARNEIRO等[2]在1996年首次描述颅内SFT,中枢神经系统SFT/HPC占所有脑膜肿瘤0.09%。肿瘤本身并没有特定临床症状,只有在达到一定大小或者对脑组织产生明显占位效应时,才会出现临床症状。大多数SFT/HPC病例病理呈良性、预后良好[3]。
本病例中,第1次术前MRI可见肿瘤主要以左侧颞部为主,无其他部位播散及转移,术后免疫组化提示Ki-67为5%。术后患者症状缓解且复查MRI提示肿瘤全切除,未接受放化疗治疗。8年后头颅MRI复查提示第1次手术部位肿瘤复发伴小脑幕多发转移。术中可见小脑幕上6处多发且相互独立的肿瘤,肿瘤血供较丰富,术中肿瘤全切除,术后免疫组化提示 STAT6(+),Ki-67为 12%~15%。Ki-67是反映细胞增殖指数的重要相关抗原,柯代波等[4]报道22例颅内孤立性纤维瘤,其中4例恶性肿瘤的增殖指数均大于5%,而良性肿瘤的增殖指数均小于1%。提示Ki-67>5%是颅内孤立性纤维瘤恶性的预测指标,术后应根据免疫组化结果,辅以放化疗,同时应加强术后随访,防止肿瘤的复发。SCHMID等[5]发现具有恶性行为的SFT,Ki-67指数明显增高,可作为患者生存率的预测因素。本例患者第2次术后Ki-67指数较第1次增高,提示存在复发及转移的风险较高。本例患者行全脊椎MRI平扫提示未见脊髓内转移。
颅内SFT因术前体征和影像学特征与脑膜瘤相似,容易误诊[6]。脑膜瘤的MRI表现多有明显的“脑膜尾征”。增强时均匀强化,肿瘤内出现钙化的较多。SFT根据T2WI的病理解剖和MRI原理,低信号反映致密的胶原纤维,高信号代表肿瘤细胞粘液变性或坏死,稍高信号则表示肿瘤致密区,T2WI通常显示稍高的信号,伴有散在的低信号区,出现“阴阳征”或“黑白征”时一般认为这是颅内SFT/HPC的特征。T2WI上的低信号区增强后明显强化形成“黑白反转征”被认为是颅内SFT/HPC的典型表现[7]。术前的影像学特征有助于肿瘤的病理预测,而术后的病理诊断及病理分级才是诊断的金标准。在免疫组化方面,SFT/HPC的常规阳性标记物包括CD34、CD99和Bcl-2。HAN等[8]对53例SFT/HPC进行了免疫组化检测发现CD34阳性47/53例(88.7%),CD99阳性 50/53例 (94.3%),Bcl-2阳性 51/53例(96.2%)。自NAB2-STAT6融合基因被鉴定以来,STAT6染色已成为常规SFT/HPC最敏感、特异的标志物,STAT6对SFT/HPC的特异性和敏感性分别为100%和96.6%[9]。
不论肿瘤的组织学等级,SFT/HPC的首选治疗是手术切除[10]。第1次手术时肿瘤切除范围对于术后肿瘤的控制至关重要,肿瘤完全切除患者预后明显好于肿瘤部分切除患者。由于肿瘤周围往往被动脉、静脉以及神经包绕,完全切除肿瘤很困难。除了手术治疗,其他治疗方法还包括术前栓塞、术前化疗和术后辅助放疗。而对于SFT/HPC的术后放疗仍存在争议,因为放疗不能阻止肿瘤的转移,但大多数神经外科医生仍主张术后辅助放疗,因能控制肿瘤的复发率。因病例数有限,目前还不能就这些措施的有效性得出统一结论。
综上,SFT是罕见的颅内肿瘤,容易误诊为脑膜瘤。临床症状主要根据肿瘤的部位及肿瘤的大小决定。手术切除是最好的治疗方式,在治疗时应尽可能做到肿瘤全切除。在病理确诊后,应根据患者的病理及免疫组化制定个性的术后治疗,包括术后的定期随访、术后放疗等,以便及时发现肿瘤的复发及转移,及时对患者进行治疗。

