青少年自发性纵隔气肿临床及影像学分析
毕 伟 丁长青 刘绪军 王文生
南通大学附属丰县医院 江苏省丰县人民医院 1 胸外科 2 影像科,江苏省丰县 221700
纵隔内除气管及食管外的其他区域均不应存在气体,一旦出现病理性的游离气体,即被称为纵隔气肿(Pneumomediastinum),也称纵隔肺气肿(Mediastinal emphysema)。其病因可为原发性(特发性)和继发性[1]。临床上还常将纵隔气肿分为自发性(Spontaneous pneumomediastinum,SPM)、外伤性或医源性,其中SPM 较为少见。SPM常在健康的年轻人中发现,发病后常无典型症状,而易漏误诊。SPM可致纵隔内气压升高,纵隔组织受压,严重时可致呼吸功能及循环系统异常甚至衰竭死。因而,早期明确诊断、及时干预对获得良好预后至关重要[2]。鉴于本病文献报道较少,为提高认识,现回顾性分析我院2015 年1 月—2020年12月收治的30例青少年SPM 患者的临床及影像学资料,并复习相关文献,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析我院2015年1月—2020年12月收治的30例青少年SPM 患者的临床及影像学资料。其中男19例,女11例;年龄13~39岁,平均年龄(23.5±2.06)岁;发病至就诊的时间1~24h,平均时间(4.62±0.87)h。本研究获得本院医学伦理学委员会审核批准及患者本人或其监护人的知情同意。
1.2 纳入及排除标准 纳入标准:具有与SPM相关的突发胸痛、呼吸困难、皮下气肿等症状及体征;胸部CT证实纵隔间质内存在异常气体积聚;年龄>12岁。排除标准:胸部创伤、医源性因素、食管穿孔、纵隔内产气菌感染等所致的纵隔气肿。
1.3 影像学检查方法 胸部X摄片使用荷兰飞利浦幻影、日本岛津CH-200DR设备,CT使用飞利浦 Brilliance16及64排螺旋CT机。CT检查主要参数:管电压120kV,管电流250mA,扫描层厚5mm,扫描范围从下颈部至肺底,部分患者根据需要加扫咽喉及全颈部。在专用工作站上1~2mm薄层重建并行冠状位及矢状位多层面重建。本组DR与CT检查相距时间均为24h以内。
2 结果
2.1 临床表现特征及可能的病因 患者主要临床表现为胸痛(30例)、颈部疼痛(21例)、咽喉痛(6例)和不同程度呼吸困难(3例)。主要的体征是皮下气肿(15例)、 Hamman’s征(6 例)。可能的病因为上呼吸道感染(10例)、剧烈咳嗽(7例)、哮喘(3例)、肺尖部大疱性肺气肿(2例)、肺结核(1例)、间质性肺病(1例)及严重呕吐(1例)等,5例病因不明。本组患者肥胖体型6例,瘦高体型8例,余16例为正常体型。
2.2 影像学表现 本组胸部DR诊断26例,CT均获得确定性诊断。胸部X线主要见胸腺帆征(26例)、环动脉征(20例)、动脉管征(18例)、双支气管壁征(15例)、连膈征(13例)和胸膜外征(12例)。胸部CT扫描典型病例见图1,可见纵隔(30例)、颈部(24例)、咽部(4例)、皮下(17例)及椎管内(2例)积气。本组2例椎管内积气均位于下颈部上胸部(颈5~胸3椎体水平)。CT还显示了2例气管内痰栓,2例肺气肿、1例肺结核及1例间质性肺病等潜在疾病及其他伴发病变。
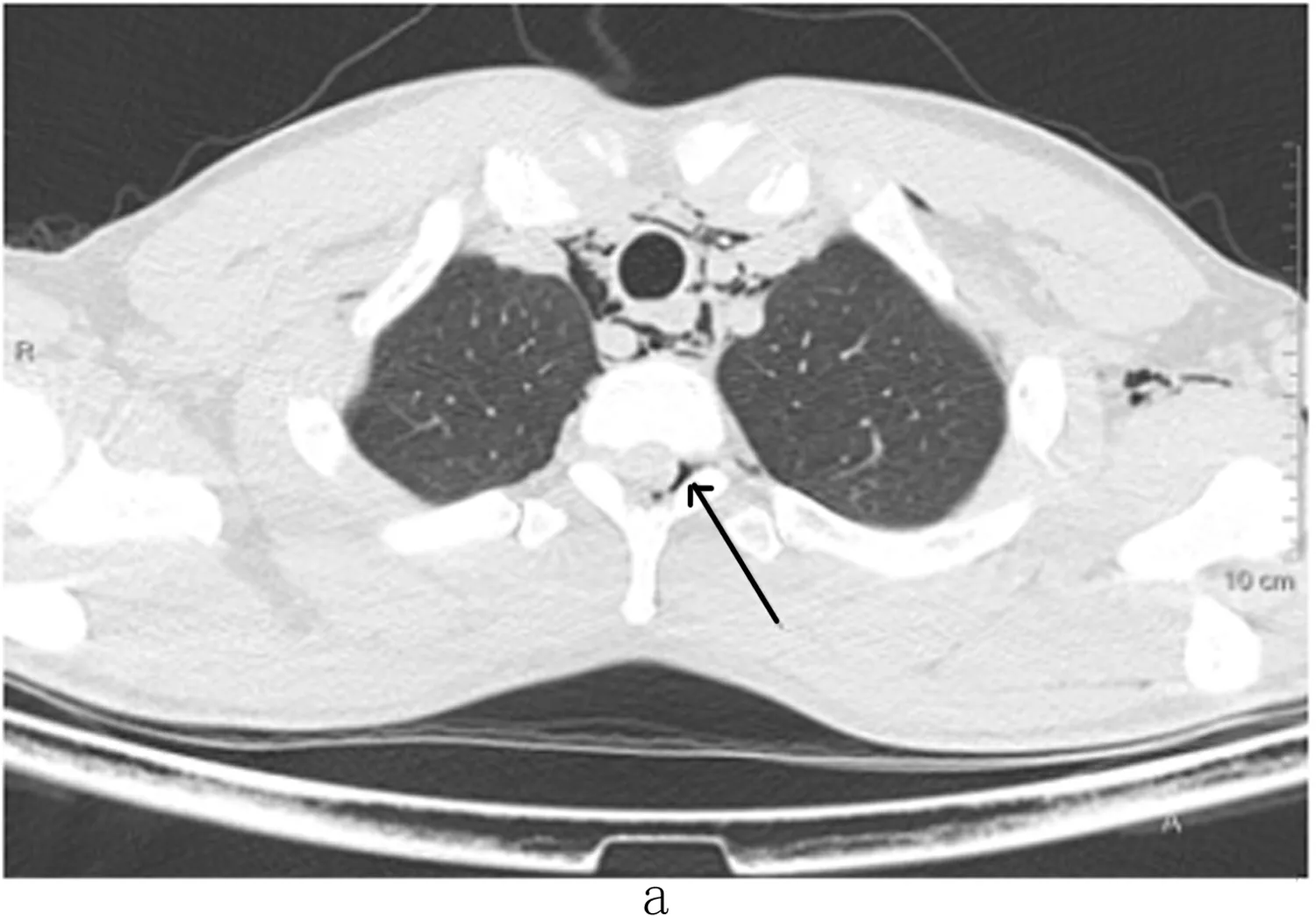
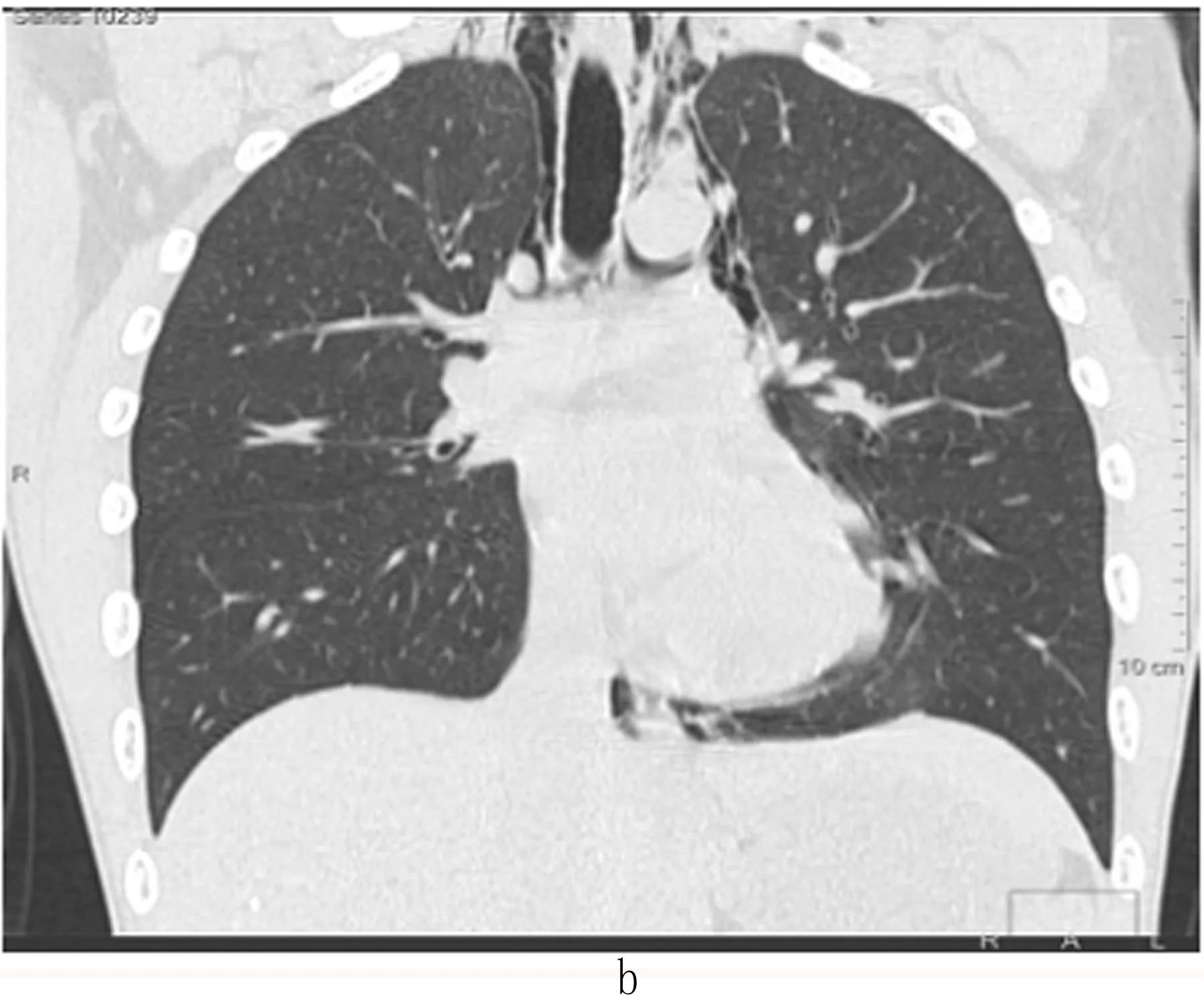
2.3 治疗及预后 主要予以休息、监测生命体征、吸氧、止痛、平喘止咳、预防感染及对症支持治疗3d~2周,患者均预后良好,未见不良并发症的发生。门诊随访1~6个月,本组均未见复发。
3 讨论
SPM多指除外伤及医源性病因所致的纵隔内病理性气体积聚。尽管最早的文献报道出现于1618年,但1939年Louis Hamman较为系统描述了这种纵隔及皮下自发性气肿性疾病,因此也称Hamman’s 综合征(汉曼氏综合征)[3]。有些学者认为SPM还应除外肺部基础性疾病所引起的纵隔气肿[4]。但随着胸部高分辨率CT的日益广泛应用,年轻患者肺尖部大疱性肺气肿的发现率越来越高,其发生机制及与SPM的关系尚待研究,本组也将此类患者纳入。SPM患病率为1∶2 000~1∶100 000[3]。 在5~34岁约为1∶25 000;而大多数患者是男性(本组63.3%)。但是,由于SPM的自限性倾向,许多轻症患者可能将症状归因于焦虑或肌肉疼痛等而未能就医,因此,实际的发病率可能更高[5]。
SPM的发病诱因在不同年龄及体型的人群中可能不同。Duarte等研究认为本病在17~25岁且瘦长的男性患者中更常见[6],本组正常体型最多,瘦高体型次之,肥胖者最少。赵佳佳等研究发现,6岁以下患儿纵隔气肿的病因以下呼吸道感染最多见,其次是支气管异物。重体力劳动及体育训练[7],吸烟,持续吸毒,慢支肺气肿,剧烈呕吐、咳嗽,便秘,上呼吸道感染,哮喘,冠状病毒感染,皮肌炎等系统性疾病所致的致间质性肺炎,分娩时第二产程过长、自发性食管破裂(Boerhaave综合征)及糖尿病性酮症酸中毒等可能为SPM的独立危险因素或病因。虽然本病多能自愈,但鉴于其发病的部分危险因素的持续存在,极少数患者可能存在复发倾向。本组随访半年均未见复发征象。
SPM发生的机制,多认为是与Valsalva动作相关的胸腔内压升高,导致远端肺泡破裂,气体经破裂口溢入肺泡周围间质内,继续沿肺间质向肺门方向走行,并进入纵隔。其病理生理学由M. T. Macklin和C.C.Macklin于1944年首次描述,这也被称为Macklin 效应。
SPM的典型症状是伴有呼吸困难的胸闷胸痛,听诊可有呼吸急促、呼吸音减弱、心动过速等,触诊多可见皮下气肿[8]。部分患者可听到与心跳同步的咔嚓声或水泡破裂音,即Hamman’s征。但此征的敏感性较差,本组仅20%的患者存在此征象,与闫庆贺等报道相近[9]。
胸部X线片仍旧是目前各级医院,尤其是基层医院诊断SPM最方便、快捷、廉价的筛查手段。但其敏感性稍差,诊断的准确性约为75%。这可能与X线的分辨率较CT低,为重叠影像,积气较少时易漏误诊。X线可有以下几种征象:胸腺帆征(胸腺呈三角帆状出现)、环动脉征(在侧位X线片上由纵隔游离气体引起的沿右肺动脉的透明线)、动脉管征(主动脉主要分支周围的游离气体呈线状低密度透亮带)、双支气管壁体征(游离气体勾勒出的支气管壁)、连膈征(膈肌上方透明带,多提示纵隔内的积气量较多)和胸膜外征(胸膜纵隔旁线与纵隔边缘凸显条带状低密度影)。
胸部CT检查凭其优良的图像分辨率、图像无重叠、多窗宽窗位观察,对SPM的诊断具有极高的敏感度及特异度,可提示部分患者的可能病因等优势,成为诊断本病的金标准[10]。CT易于发现游离气体积聚的位置并可大致判断气体量,需要注意气体位置与患者体位及扫描或重建图像层面有关。CT还可发现X线无法提示的、伴发的、更为罕见的椎管内积气。本组仅2例伴椎管内积气。
临床及影像学诊断上主要需进行病因学诊断,尽快找出或排除食管穿孔、酮症酸中毒等严重威胁生命的潜在原因,进而及时干预,以获得良好预后。还需与胸部骨及软组织疾患、肺动脉栓塞、心包炎、心包填塞、纵隔炎、心绞痛、心肌梗死、主动脉夹层、气胸、气腹、食道痉挛和反流病、注射药物的毒副作用等鉴别。
SPM病程通常是良性的,经过镇痛在内的保守治疗后,大多数患者的症状会逐渐缓解,而无须任何进一步的干预或治疗。但是,有些学者仍建议使用预防性抗生素,而另一些学者则建议仅控制疼痛和治疗其他伴发的疾病。
本研究的不足之处:本研究为回顾性研究,缺乏随机对照;病例较少,未能对其发病的可能诱因及不同年龄组的病因进行统计学对比分析等。尚需积累更多病例进行深入研究。

