递进式问题链在高二化学复习课中的应用


摘 要: 复习课在学生期末复习时对各科知识网络的形成和刻苦钻研的品质培养等方面起到了核心作用.复习课的教学目标比较广泛,没有具体的教学编排,完全需要依靠教师自己去思考和挖掘.学生掌握知识往往需要经过领会、理解、应用三个环节.由于复习课时紧张、教学内容繁多,教师通常按照教学进度或者按照班级的整体进度向前推进教学,导致班级中一些有个体差异的学生呈现出一种差生“消化不了”、好学生“吃不饱” 的现象,无法鼓励学生在学习方面的独立性和自觉性.
关键词: 递进式问题链;复习课;高中化学
中图分类号: G632 文献标识码: A 文章编号: 1008-0333(2022)12-0128-03
收稿日期: 2022-01-25
作者简介: 谷士娟(1993.7-),女,吉林省农安人,研究生,中学二级教师,从事高中化学教学研究.
1 核心概念解读
问题链是指教师根据课堂教学目标,针对学生在学习中经常错的点或容易忽略之处,转化成为一环扣一环的具有层次性的教学问题.在课堂中,根据不同目的所设计的不同的问题也会收获不同的教学效果,而递进式问题链是由几种事物之间的相互联系提出的一系列由易到难的问题集合,将问题与问题进行衔接与递进.
师生问答是常用的一种教学样式,在研讨中进行讲解知识、开发脑筋、获得定论.但是这类传统的问答的式样使学生处在比较被动的状况,头脑思维 不充足,问题的编排缺乏接续性、整体性.递进式问题链教学区别于一般的问题教学,强调用问题激发学生思考,将同一内容的教学目标进行分层,控制好知识的难易程度,做到逐级增加,用链的形式把问题引向深处,符合学生的认知心理发展历程.在问题链的教学中,以知识为载体,问题为策略,探究知识本质的过程.
2 教学案例
电解池是高中人教版选修四第四章第三节的内容,是以氧化还原反应为核心,以原电池原理为铺垫的加深拓展的重要内容.复习课进行时没有教材作为载体,复习内容的广度与深度需要教师自己去挖掘,这就要求教师要做到以教材内容为基础,结合课程标准的相关要求,对问题进行整合,想尽一些办法调整学生的学习心态,提高学生解决问题的能力.
2.1 对电池原理的回顾——典型题型变换
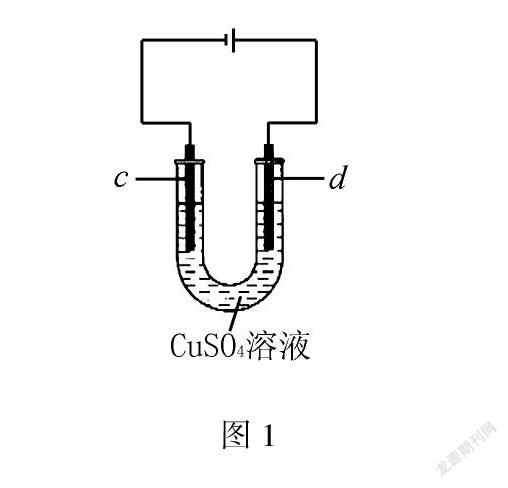
问题1 观察电解稀硫酸铜溶液(如图1所示)的装置 ( c为铁,d 为石墨),可以 图1 看到什么实验现象?推断两电极的产物什么?分别写出两个电极发生的反应.
设计意图:以化学必修一的理论认知为基础,依据实验现象推测化学反应产物,并能正确地书写各电极的电极反应式.结果显示,学生能够由实验现象推测出何种反应产物,也能够正确地写出电极反应式和对的总化学方程式.
问题2 如果将图1的装置的两个电极互换,观察有什么实验现象?写出两电极反应式,探究其原因.
设计意图:此题是在问题1基础上进行的拓展.学生需要分辨出问题1中的离子在哪一极放电,并且要熟练掌握离子的放电先后.当电极互换时,需要考虑到阳极的放电顺序,当阳极板是活泼电极(除Pt、Au)时,活泼电极优先于溶液中离子的放电.在学生掌握的基础上增加了难度,考查了学生能否根据实验现象写出电极反应的能力.
问题3 以实验2为背景,将两电极均换成铁电极(如图2所示),其他条件不变,仅向溶液中滴加少量的K 2 Cr 2 O 7 溶液.問溶液中的Cr 2 O 2- 7 浓度怎么变化?请说明其原因.
设计意图:要想判断出向电解液中加K 2 Cr 2 O 7 溶液对反应的影响,就需要学生掌握必修一所学的常见的氧化剂和还原剂.基础知识相对过关的学生就会知道K 2Cr 2O 7溶液属于强氧化剂,在酸性条件下,遇到还原性较强的Fe 2+ 能够发生氧化还原反应.很多学生在做题的过程中会忽略阳极产生的Fe 2+ 具有还原性,出现审题错误,根据Fe 2+ 与 Cr 2 O 2- 7 反应的离子方程式,能够判断出Cr 2 O 2- 7 的变化情况.
问题4 重金属离子Cr 3+ 有毒,如何避免产 生Cr 3+ .
设计意图:对于该问题的设计,学生虽然很容易想到溶解度表中相关知识(金属离子除Na + 、K + 、Ba 2+ 外都不能与OH - 共存)即Cr 3+ 与OH - 结合产生Cr(OH) 3 ,却不知道在此实验条件下如何能够使得Cr 3+ 和OH - “偶遇”.在原电池习题应用中,学生已经明确了阴、阳离子交换模的作用,为进一步了解可以通过控制外界条件使电解反应向需要的方向发展提供了理论依据,达到学以致用的目的.
设计第一环节是为了加强学生的基础知识和技能,对基础薄弱的学生,再次对知识进行加工内化,掌握较好的学生起到温故而知新的作用.复习课不只是简单的对所学内容进行回顾,而是把课程中零散的知识内容进行梳理,协助学生建立知识网络,有益于提升学生处理问题的技能.为了看习题配置是否符合学生知识网络的形成,因此设计第二环节. 2.2 对电解原理的拓展——混合体系探究
问题1 用石墨作电极电解NaCl和CuSO 4 (等体积混合)混合溶液,写出各电极反应式和电极总反应.
设计意图:在上一环节中,学生接触了电解单一溶液的习题,可以根据电极反应、离子放电顺序判断实验现象和正确书写电极反应式.在混合系统中,学生在书写电极反应式要多考虑一些内容,不仅需要注意离子放电的先后次序,还需要注意“量”的问题,两个电极联系的“纽带”是电子转移的量相同.转移电子量不同,电极反应也可能出现差异.
问题2 以问题1为基础电解10min后,测得电解过程中溶液pH随时间 t 的变化如图3所示,试求溶液中 c (KCl)、 c (CuSO 4 ).
设计意图:问题2是以问题1为基础,在学生掌握了如何书写混合体系的电极反应时后,由于反应 过程中转移的电子数相同,按先后顺序分类的书写电极反应式.本题对学生有一定的难度,主要在于学生对图像的题不太“敏感”,不能抓住题中主要的信息.重点强调“拐点”是解决问题的关键点,培养学生发现新旧知识的内在联系,从而使学生获得真知和技能.
问题3 用铂作电极电解CuSO 4 溶液,转移电 子的量与气体体积的关系如图4所示(同 T、同p测定).Q 点时向溶液中加 使溶液恢复原溶液状态.
设计意图:恢复电解质溶液是电解原理的一个重要应用,围绕问题1、2的综合性问题.电解10min后,如何能够将溶液恢复到原溶液.要求学生要关注图像中的数据,注意“量”的问题,对学生如何进行处理数据提出了新的挑战.
通过第2环节,学生能够分析由单一溶液到混合溶液,对电池原理有进一步的理解和认识.以两电极转移电子数相同为核心,并能根据相关计算确定某些具体的数值,达到由定性到定量的的转化.对混合物的分析有一定的理解之后,在未接触的问题背景中,学生是否能够应变自如?设计第三环节.
2.3 对电池原理的应用——综合实践提升
问题1 如图5所示,三个烧杯分别盛放KOH溶液、CuSO 4 溶液和 Na 2 SO 4 溶液,铂为电极.反应结束后, c 上有固体产生.判断电源的正负极及电解前和电解后溶液中 c (H + )的变化.
设计意图:根据本节课所学的知识,学生能够直观的通过装置中是否含有电源来判断是原电池还是电解池.此题有电源,学生能够确定这是电解池,而多个电池串联在一起的装置图,学生还没有接触过.经过知识整合与分析,能够学到处理问题办法,这样有益于鼓励学生积极思考、敢于探究的精神.
问题2 如圖6所示,判断甲池是 池,若甲池中消耗224 mL(标准状况)O 2 ,丙池产生 g沉淀,此时乙池中溶液的体积为400 mL,该溶液的pH= .
设计意图:准确判断原电池、电解池是关键,注意从是否能够自发进行的氧化还原角度来判断.主要考查学生结合电解理论对新背景下的题干信息提取和处理的能力.
问题3 如图所示装置中, X是铁电极, Y是铂电极, a是K2SO4溶液,实验前,在U形管的两侧各滴2~3滴酚酞,将开关K1、K2分别断开与闭合会有什么实验现象.
设计意图:围绕问题1、2,让学生自行“设计”电池,考察学生是否能够根据实际情况,用正确的语言描述实验现象.对学生思维提出新挑战.
本环节主要考察学生处理综和问题的能力.意在考察学生如何在新的问题情景中,拨开“情景”的层层面纱,看到问题的本质,进一步提升学生分析问题、处理问题的能力.
教师将教学内容编排成难度由易到难、具有一定层次性的问题链时,符合学生的认知情况,就能有效的引领学生以问题为中心去思考和探究,在一环扣一环的问题设计中引发学生思考,提升学生的处理综合问题的能力、培养学生良好的学习品质.
参考文献:
[1]杜雪文.例析热化学方程式书写技巧 [J ].数理化学习(高中版),2020(03):59-61.
[2 ] 王中恺.新课标下高中化学课程教学的策略研究 [J ].新课程研究(上旬刊),2018(04):101-102.
[3 ] 任友明.浅议高中化学冲刺阶段的备考策略 [J ].问答与导学,2019(33):35.
[责任编辑:季春阳]

