基于蛋白质组学的透明质酸寡聚糖抗炎活性研究及验证
郑博文,王斌雅,肖婉玲,孙亚娟,赵炳天,杨成
(合成与生物胶体教育部重点实验室,江南大学 化学与材料工程学院,江苏 无锡,214122)
蛋白质组是指“一个基因组所编码表达的全部蛋白质”,这一概念最早是由澳大利亚的WASINGER等[1]提出并加以阐释的。通过蛋白质组学的研究,可以整体地对细胞内蛋白质的组分情况、表达情况进行分析,从而对于蛋白之间的作用与联系,以及蛋白质对于生命活动的影响进行探索,进而揭示不同蛋白的具体潜在功能及其应用价值[2]。随着技术的发展,液相质谱联用逐渐成为蛋白组学中主要的检测手段,然而,研究人员选取的研究策略仍存在着差异。其中,数据非依赖性采集(data independent acquisition, DIA)技术具有检测量大,数据易得,可重复性好等优势[3],近年来应用范围较广。在食品领域,蛋白质组学被广泛应用于乳制品、水产和肉制品的生产过程以及产品的研究中,此外,发酵用菌株及发酵过程中的蛋白质变化过程也可以采用蛋白组学进行研究[4-6]。
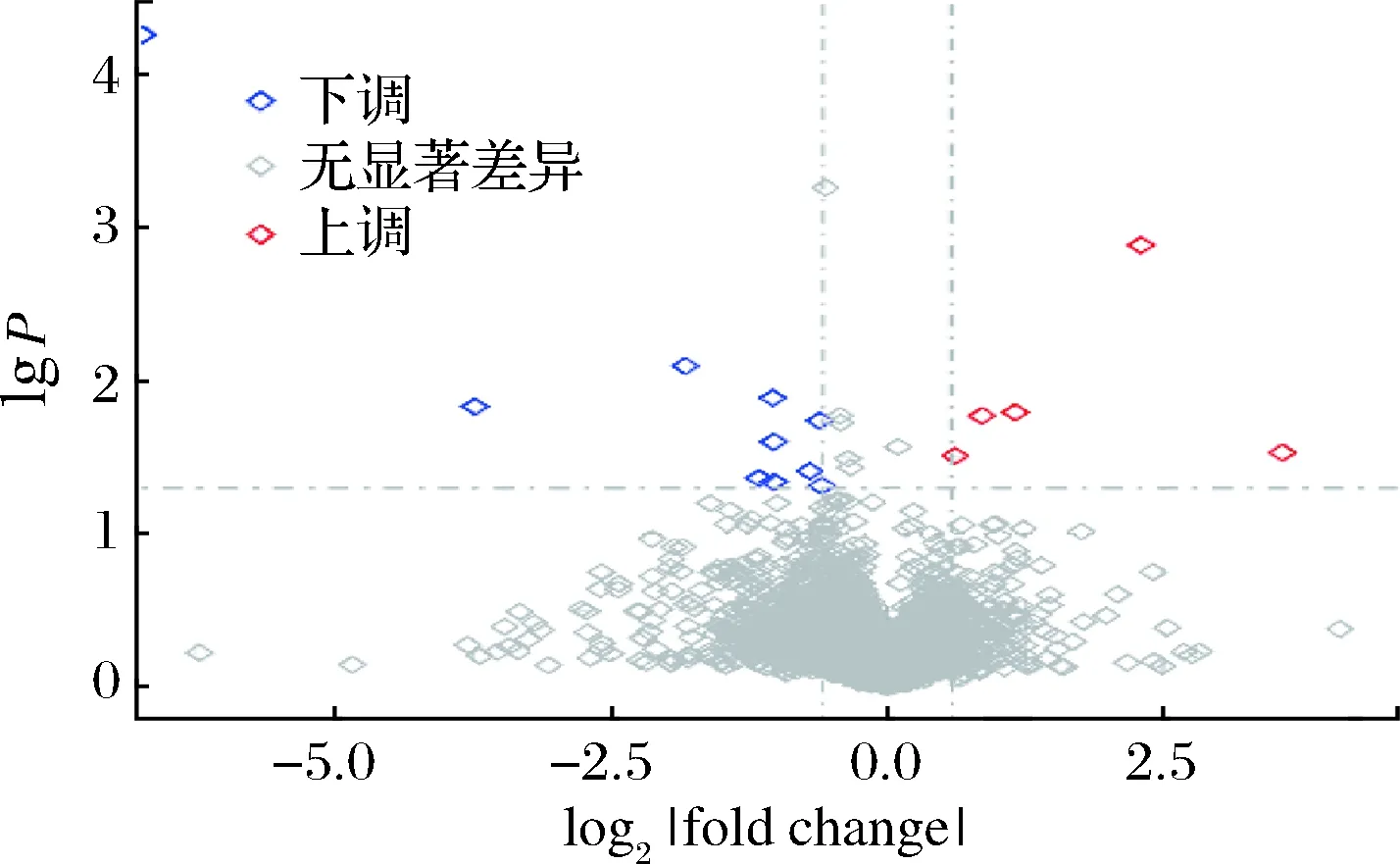
透明质酸(hyaluronic acid, HA)是一种广泛存在于动物组织的细胞间质中的糖胺聚糖[7],具有促进伤口修复、组织再生、免疫调控、抗炎等多种生物活性[8]。根据分子质量(molecular weight,Mw)的差异,可将透明质酸划分为高分子透明质酸(Mw≥100 kDa),低分子透明质酸(10 kDa 本文通过蛋白组学检测oligo-HA处理后的脂多糖(lipopolysaccharides, LPS)刺激的RAW264.7细胞,从蛋白水平对其在炎症免疫反应中的作用进行研究,并通过斑马鱼的十二烷基硫酸钠(sodium dodecyl sulfonate, SDS)刺激模型,验证其对炎症的舒缓功效。 透明质酸寡聚糖发酵液,由江苏瑞霆生物科技有限公司提供,经冷冻干燥后低温保存。RAW264.7小鼠巨噬细胞系,北纳创联生物技术有限公司。转基因中性粒细胞绿色荧光品系斑马鱼,杭州环特生物科技有限公司。 LPS,Sigma-Aldrich公司;SDS,上海阿拉丁生化科技有限公司;iST试剂盒,PreOmics公司;色谱级乙腈,上海泰坦公司;其余试剂均为AR级且购自国药试剂。 EASY nano LC 1200液相色谱系统、Orbitrap FusionTMLumosTMTribridTM质谱仪,美国Thermofisher公司。 1.3.1 细胞培养及蛋白提取处理 将冻存的RAW264.7细胞复苏后,采用DMEM完全培养基(含10%胎牛血清及1%双抗,体积分数),在细胞培养箱中于37 ℃,5% CO2,饱和湿度下培养。当细胞生长至培养皿面积的80%以上时,进行传代。将处于对数生长期的细胞接种于60 mm小培养皿中(1×106个/mL),培养24 h后,弃去旧培养基,分为HAD组(oligo-HA及LPS处理)及HAB组(仅LPS处理)。HAD组加入用DMEM稀释至500 μg/mL的HA溶液(HAB组改为空白DMEM培养基),继续培养18 h后,弃去旧培养基,加入用DMEM稀释至1 μg/mL的LPS及500 μg/mL的HA溶液,继续培养6 h。将处理完成的细胞收集至离心管中,在1 000×g,4 ℃下离心5 min,弃去上清液,向细胞中加入裂解液,涡旋振荡,于超声波细胞破碎仪中超声处理2 min后,在冰上裂解30 min,期间每10 min振荡混匀1次。在12 000×g, 4 ℃条件下离心20 min,取上清液进行BCA定量。采用iST样本前处理试剂盒对所得蛋白样品进行前处理,经高温变性,酶解,肽段除盐,洗脱过程后,将所得肽段抽真空于-80 ℃保存备用。 1.3.2 nano-HPLC-MS/MS分析 将样品加入30 μL的0.1%(体积分数)甲酸水溶液制成悬浮液。取9 μL样品溶液与1 μL 10×iRT肽段混合后,采用nano-LC分离,经在线电喷雾串联质谱分析。实验选用Acclaim PepMap C18柱,柱温55 ℃,进样流速为300 nL/min,进样量为2 μL。流动相A为0.1%甲酸的水溶液,流动相B为含有0.1%甲酸的80%乙腈水溶液。洗脱条件为4% B相起始,平衡5 min,在120 min升至50%后,在1 min内升至95%,保持9 min。 质谱仪在数据非依赖采集模式下运行[13]。设置质谱参数为:(1) MS:扫描范围(m/z) 350~1 200;分辨率:120 000;Normalized AGC target 250%;最大注入时间:100 ms;(2) HCD MS/MS:分辨率:50 000;Normalized AGC target 200%;最大注入时间:86 ms;碰撞能量:33。 1.3.3 蛋白注释与生物信息学分析 采用Spectronaut 15.0默认参数对DIA数据进行分析。序列数据库为 uniprot homo sapiens(version201907, 20428 entries)数据库,设置胰蛋白酶酶解。Spectronaut 进行自动校正,采用局部归一化策略进行数据归一化处理。<1.0% FDR的前3个肽段的峰面积的平均值用来进行蛋白组的定量。差异筛选标准:One way ANOVA Test分析后取P<0.05,|fold change|>1.5 的差异蛋白。对筛选得到的差异蛋白基于GO(Gene Ontology)、KEGG(Kyoto Encyclopedia of Genes and Genomes)进行注释及通路分析。 1.3.4 斑马鱼刺激试验 1.3.4.1 最大试验浓度的确定 随机选取受精后2 d的斑马鱼,按每孔30尾置于六孔板中。以质量分数0.12%、0.25%、0.5%、1.0%、2.0%、4.0%将oligo-HA样品添加到六孔板中,定容至3 mL,同时设置正常对照组。将斑马鱼置于28 ℃条件下避光孵育18 h。孵育结束后,在显微镜下观察并统计各组斑马鱼存活情况及活力,确定样品的最大试验浓度。 1.3.4.2 SDS刺激舒缓功效测试 根据最大浓度试验结果确定样品处理浓度,并梯度设置3个浓度。采用1%(体积分数)甘油葡糖苷作为阳性对照(positive control, PC)。随机选取受精后2 d的斑马鱼,按每孔30尾置于六孔板中,将SDS溶液加入孔中并定容至3 mL,使得SDS终质量浓度为60 μg/mL。 将斑马鱼置于28 ℃条件下避光孵育18 h。孵育结束后,每组随机选择10尾斑马鱼在荧光显微镜下拍照保存,对皮肤中性粒细胞进行计数。刺激抑制率按公式(1)进行计算,并根据抑制率评估舒缓功效。 (1) 式中:E1,刺激抑制率,%;Nc,模型组中性粒细胞数量,个;Ns,样品组中性粒细胞数量,个;Nb,空白对照组中性粒细胞数量,个。 2.1.1 主成分分析 研究中采取主成分分析方法,对数据进行降维分析,将多维数据转化为蛋白主成分表达量,从而评估样品的相似及差异情况。如图1所示,所检测的两组样品中,各组内蛋白距离较近,主成分相似,说明测定结果重复性较好。且HAD组与HAB组间存在明显距离,区分较大,说明oligo-HA样品处理对LPS刺激的细胞内蛋白表达产生调控作用。 图1 RAW264.7细胞蛋白的主成分分析Fig.1 PCA of proteins in RAW264.7 cells 2.1.2 差异表达蛋白的筛选及鉴定 经过分离检测,共鉴定到肽段48 592个,蛋白6 119个。经过ANOVA分析后筛选出的显著性差异蛋白共124个,其中,HAD组相对于HAB组上调的为76个,下调的为48个,如图2所示。 2.1.3 差异表达蛋白GO富集分析 根据挑选出的差异蛋白,采用GO分析,计算出现富集的差异基因,从而确定不同样品的差异基因与基因功能改变之间可能的关系。如图3所示,富集后差异表达蛋白主要分为生物学过程、功能分子与细胞组成三类,每类中,取P值最小的10个富集结果进行作图。oligo-HA的作用主要包括参与细胞周期及羧酸和氨基酸的代谢过程(生物学过程),调控组蛋白丝氨酸、苏氨酸、酪氨酸激酶及转移酶等活性,调控类视黄醇和类异戊二烯的结合(功能分子),影响细胞内成分与细胞器(细胞组成)等。 图2 差异表达蛋白火山图Fig.2 Volcano plot of differentially expressed proteins注:中部灰色点表示无显著性差异表达的蛋白,上调蛋白采用红色点表示,下调蛋白采用蓝色点表示 图3 差异表达蛋白GO富集分析主要结果Fig.3 Main results of GO analysis of differentially expressed proteins 2.1.4 差异表达蛋白KEGG富集分析 与GO分析类似,在KEGG分析中,通过对富集情况进行计算,根据P值筛选出存在明显差异的蛋白,从而分析oligo-HA的主要作用。计算后统计富集筛选中P值最小的15个蛋白条目进行绘图,结果如图4所示。oligo-HA主要参与到糖胺聚糖生物合成,破骨细胞分化,泛酸和辅酶A生物合成,氨酰基-tRNA生物合成,甲状腺激素、T细胞受体和ErbB信号通路,以及多种癌症相关通路的调控中。 图4 差异表达蛋白KEGG富集分析主要结果Fig.4 Main results of KEGG analysis of differentially expressed proteins 2.2.1 oligo-HA的最大耐受浓度测试 最大耐受度实验测试结果如表1所示,尽管在质量分数为2%的组中,斑马鱼死亡率为0,但其活力存在明显降低,状态较差,故判定2%的oligo-HA对斑马鱼的正常生存有影响,确定最大耐受质量分数为1%,用于后续实验。 表1 透明质酸寡聚糖最大耐受浓度实验Table 1 The maximum tolerance dose of oligo-HA for zebra fish 2.2.2 oligo-HA的舒缓功效测试 根据确定的斑马鱼对oligo-HA样品的最大耐受浓度,并梯度设置3个浓度,对斑马鱼进行处理,同时采用SDS对斑马鱼进行刺激,从而评估样品的舒缓功效。结果如图5所示,0.5%(P<0.05)及1%(P<0.01)质量分数的oligo-HA处理的斑马鱼中性粒细胞数量显著性降低,刺激抑制率达25%以上,证明样品具有明显的舒缓功效。 SDS-仅加入刺激的模型组;PC-加入1%甘油葡糖苷的阳性对照组a-斑马鱼中性粒细胞荧光典型照片;b-中性粒细胞计数;c-刺激抑制率图5 Oligo-HA样品对斑马鱼SDS刺激舒缓功效Fig.5 Effects of oligo-HA sample on SDS-stimulated zebra fish注:#表示P<0.05与空白组相比,*表示P<0.05,**表示P<0.01与SDS组相比 透明质酸作为生命体中的一种重要成分,一直以来在美国等地被用作膳食补充剂使用[14]。根据日本的一项双盲试验研究,经过一段周期的HA口服食用,受试人员的皱纹减轻,同时皮肤的光泽和柔软度得到了提升[15]。随着我国卫健委批准透明质酸钠为“新食品原料”,对于其在食品中的功效及应用研发值得投入更多关注。 本实验中,首先通过蛋白质组学分析,对oligo-HA在LPS刺激的RAW264.7细胞中的作用效果进行了探究。根据蛋白质组学的结果,经过样品处理的细胞与未处理组相比,主要存在124个差异蛋白,其中表达显著上调的蛋白76个,显著下调的蛋白48个。它们主要参与的生理活动包括细胞周期及羧酸和氨基酸的代谢过程等,主要影响的通路包括细胞分化,生物信号分子合成以及部分癌症相关通路等。表2中列举了存在显著性差异表达,且参与到炎症反应及免疫应答调控中的主要蛋白。 oligo-HA处理组中,T细胞受体信号通路相关蛋白AKT1, PAK4表达显著性下调:AKT/PI3K信号通路在炎症及免疫细胞的调控起到重要作用,根据FU等[16]的研究,通过抑制AKT/PI3K信号通路,RAW264.7细胞中的炎症因子水平显著下降,起到了抗炎效果。这与HAN等[10]的报道中oligo-HA的下调炎症因子的抗炎功效一致。PAK4蛋白在癌症中常常大量表达,并进一步诱导癌细胞的增殖与转移扩散。一项研究表明,通过抑制PAK4的表达,可以阻止癌细胞在癌症小鼠模型中的增殖,以及促进癌细胞的凋亡[17]。对于PAK4的抑制效果,也为透明质酸在食品与医药中的应用提供了可能的方向。FCGR2及NAL10主要参与到免疫细胞的信号传导中,实验结果中这些蛋白的表达显著性上调。FCGR家族是免疫细胞上分布最广的受体,其可以主导免疫复合物的内吞作用[18]。FCGR2被发现分布于B细胞,巨噬细胞,中性粒细胞等表面,当FCGR被激活后,它们会磷酸化并促进细胞对病原体及被感染的细胞做出反应[19]。NAL蛋白参与到Th细胞的免疫应答作用中并调控炎症反应。MIYAI等[20]的研究中,在特应性皮炎的患者皮肤中,NAL10的表达可以抵御细胞凋亡刺激,并抑制其并发的炎症小体激活,从而起到抑制炎症的作用。oligo-HA的抗炎作用,也与这些相应蛋白的表达上调密不可分。通过对蛋白质组学的结果进行深入分析,可以对oligo-HA的抗炎作用效果以及作用产生的机理得出更深入的了解与认识,拓宽其应用前景。 表2 参与炎症及免疫调节的主要差异蛋白Table 2 Major differentially expressed proteins involved in inflammation and immune regulation 斑马鱼作为常用的模式动物之一,因其繁殖能力强、周期短,便于观察且免疫细胞与人类相似等优点,已被广泛应用于免疫、生理等研究中[21]。本研究中,采用SDS对斑马鱼进行刺激,建立炎症模型,通过对中性粒细胞进行计数,体现炎症反应情况。结果表明0.5%与1%质量分数的oligo-HA处理的斑马鱼实验组中,中性粒细胞数量显著性降低,证明样品能够显著性的抑制炎症反应,调控免疫细胞的作用,这与蛋白质组学结果中体现的oligo-HA的抗炎效果是相一致的。 综上所述,本研究采用oligo-HA对LPS诱导的RAW264.7巨噬细胞进行预处理,通过对细胞样本的蛋白质组学分析,分析确认了其参与调控的抗炎与免疫调控等多项生理活动及相关的信号通路,并采用SDS诱导的斑马鱼刺激模型,验证了oligo-HA的抗炎效果,为其作为“新食品原料”的应用提供了更多潜在价值。1 材料与方法
1.1 材料与试剂
1.2 仪器与设备
1.3 试验方法
2 结果与分析
2.1 透明质酸对LPS刺激的RAW264.7细胞作用的蛋白组学分析



2.2 oligo-HA舒缓SDS对斑马鱼的刺激功效测试


3 讨论与结论


