发热合并肝功能异常的妊娠期干燥综合征一例
李佳雯,李濛,应豪,赵婷婷,殷科,黄璐
干燥综合征(Sjögren's syndrome)是一种自身免疫性疾病,是由外分泌腺的淋巴细胞浸润而引起的腺体功能障碍,好发于唾液腺和泪腺,可累及全身多系统、多器官,包括呼吸系统、消化系统、泌尿系统、血液系统和神经系统等[1]。干燥综合征与妊娠相互影响,患者可能出现病情进展、自然流产、胎儿发育异常等情况。妊娠期间干燥综合征的治疗目的主要是终止或抑制患者体内的异常免疫反应,保证胎儿在宫内正常生长发育,预防妊娠期并发症及新生儿并发症。治疗主要包括对症治疗和系统性治疗,系统性治疗又包括糖皮质激素和免疫抑制剂等[2]。干燥综合征的患病率为0.043%,欧洲的患病率高于亚洲,分别为0.712%和0.045%,男女比为10.72[3]。该病起病多隐匿,大多数患者很难说出明确的起病时间,临床表现多样,病情轻重差异较大。本例患者于妊娠晚期出现体温升高及明显的肝功能异常,不伴随关节酸痛、肿胀等症状,入院后行剖宫产术分娩一足月儿,发育未见异常。住院期间予抗感染、保肝治疗,效果欠佳,后使用激素治疗,效果良好。出院后定期随访,未出现病情反复。
1 病例报告
患者 女,34 岁,孕2 产1,因停经37+1周,发热2 d,于2020 年6 月16 日收入南京医科大学附属无锡妇幼保健院(我院)。患者于2020 年6 月14 日下午无明显诱因出现发热症状,自测体温37.4 ℃,感畏寒、肌肉酸痛,无咳嗽、咳痰等症状,至外院就诊,查甲型、乙型流感病毒阴性;血常规示:中性粒细胞0.795,超敏C 反应蛋白44 mg/L;予口服头孢氨苄治疗,未明显好转。遂于6 月16 日至我院就诊,测体温38.4 ℃;血常规示:中性粒细胞0.833,超敏C 反应蛋白103.8 mg/L;肝肾功能示:丙氨酸转氨酶(ALT)192.8 IU/L、天冬氨酸转氨酶(AST)194.9 IU/L。B 超示:单胎骶左前(left sacroanterior,LSA)位,双顶径96 mm,羊水指数(amniotic fluid index,AFI)160 mm,胎儿估计体质量(3 626±350)g,子宫前壁下段肌层厚约2.8mm。胸部CT 未见明显异常。入院诊断:①孕2 产1,孕37+1周待产,LSA 位;②瘢痕子宫;③产前发热。入院后体格检查:体温38.8 ℃,心率118 次/min,呼吸17 次/min,血压125/75 mmHg(1 mmHg=0.133 kPa);专科检查:宫高31 cm,腹围102 cm,估计胎儿大小3 500 g,LSA 位,胎心170 次/min。考虑患者入院后体温持续偏高,且肝功能异常,胎心偏快,继续待产不排除胎儿窘迫、宫内感染、感染性休克及多脏器功能衰竭可能,与患者及家属沟通病情后决定立即终止妊娠。术前诊断:①孕2 产1,孕37+1周待产,LSA 位;②瘢痕子宫;③产前发热;④妊娠合并肝功能损害。手术顺利,新生儿1 min、5 min Apgar评分均为10 分,术中生命体征平稳,出血量400 mL,尿量200 mL,补液1 000 mL。术后予头孢西丁抗感染、还原型谷胱甘肽保肝治疗,体温持续升高,故更改抗生素为头孢哌酮钠舒巴坦钠3 g,每8 小时1 次(q8 h),并予物理降温及补液支持治疗。术后第1 天7:00 体温39.4 ℃,请多科会诊后更改抗生素为亚胺培南西司他丁钠1 g,q8 h,保肝药为甘草酸二铵,16:00 体温36.3 ℃。术后第3 天B 超示宫腔回声欠均匀区厚6~9 mm,肝胆B 超示脂肪肝,胸部CT 示双侧胸腔少量积液,宫腔分泌物培养示大肠埃希菌阳性,考虑患者已使用亚胺培南西司他丁钠3 d,体温仍较高,不排除药物使用时间较长产生耐药可能。根据宫腔分泌物培养及药敏试验,更换抗生素为五水头孢唑啉钠联合左氧氟沙星,体温较前下降。术后第8 天查胸部CT 示双侧胸腔少许积液较前明显吸收,宫腔分泌物培养阴性,血沉在正常范围内,类风湿因子阳性,抗核抗体滴度高于正常值,抗心磷脂抗体IgG、IgM 阴性,请无锡市第二人民医院风湿免疫科会诊,治疗建议:①停用抗生素;②发热可使用泼尼松10 mg,3 次/d 治疗;③保肝治疗;④对症处理,根据检查结果调整治疗。术后第10 天(6 月26 日),患者偶有咳嗽,无畏寒等不适,阴道出血不多,大小便正常;7:00 体温37.7 ℃,ALT 186.4 IU/L、AST 118.0 IU/L;予泼尼松10 mg 3 次/d 口服,签字出院,并建议进一步就诊。住院期间体温及肝功能变化见图1、图2(术1 指术后第1 天,术2 指术后第2 天,以此类推)。
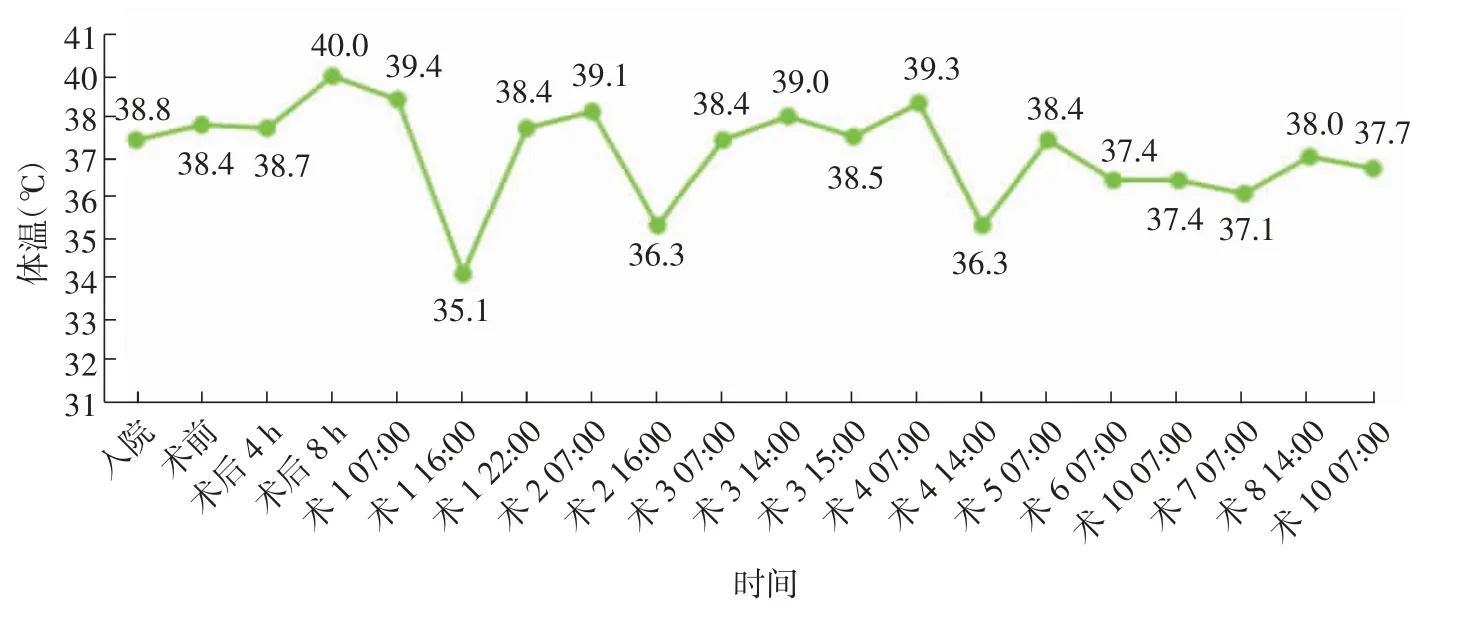
图1 住院期间体温变化图

图2 住院期间肝功能指标变化图
出院后拟诊“原发性干燥综合征”于外院风湿免疫科住院治疗,追问病史,患者诉妊娠晚期有口干、哭时无泪症状,入院查角膜染色试验阳性,予硫酸羟氯喹0.2 g,2 次/d 口服,予甲泼尼龙40 mg,1 次/d(4 mg×10 片)口服,体温维持在37.4~38.5 ℃。7 月3 日体温恢复正常予出院,出院后继续口服羟氯喹0.2 g、2 次/d,甲泼尼龙36 mg、2 次/d,甲泼尼龙每月减量1片(4 mg)。2020 年7—10 月体温正常且肝功能逐渐好转,10月26 日复查ALT 18.9 IU/L、AST 23.6 IU/L,抗核抗体谱滴度1∶320 高于正常值,抗SSA 抗体弱阳性,RO-52 抗体弱阳性,且已持续有3 个月以上的眼干、口干症状,故确诊为原发性干燥综合征,继续予羟氯喹及甲泼尼龙治疗,随访至今,患者再无发热,肝功能正常,无明显全身症状,婴儿发育未见异常。
2 讨论
2.1 诊断标准干燥综合征是一种系统性自身免疫性疾病,可分为原发性干燥综合征和继发性干燥综合征。原发性干燥综合征发生在没有其他自身免疫性疾病的情况下,其特征是干燥性角膜结膜(眼干)和口干燥症(口干)。相比之下,继发性干燥综合征与其他自身免疫性疾病,如类风湿性关节炎、系统性红斑狼疮等,一起出现。随着近年来诊断技术和重视程度的提高,多数患者在疾病早期就可以被诊断。诊断标准参照2016 年美国风湿病学会(ACR)/欧洲抗风湿病联盟(EULAR)原发性干燥综合征分类(诊断)标准[4]。发热是母体应激或多种妊娠并发症的常见临床表现,且目前尚无文献报道发热与妊娠期干燥综合征的关联性,故无法将其发生归因于此。但任何导致核心温度显著升高(>38.9 ℃)的母体高温源都有可能影响胎儿。体温过高的后果取决于体温升高的程度、持续时间、母亲的营养状况、合并症、药物治疗和遗传背景等。据报道,即使是短暂暴露在母体高温下也会导致细胞分裂、血管破裂和胎盘梗塞,从而存在导致后代结构和功能缺陷的风险[5]。因此,妊娠期出现难治性发热需要全面排查病因,包括干燥综合征等少见情况在内。尤其是首次发病的患者,由于鉴别诊断困难,易延误治疗导致病情进展,且可能出现严重的不良母儿结局,及时、正确地诊断及治疗可明显改善母儿预后。本例孕妇的首诊表现为发热及肝功能异常,在对症予以抗感染及保肝治疗后,病情仍有波动,结合患者类风湿因子阳性,考虑患者可能因妊娠诱发了自身免疫性疾病,追问患者相关病史,于妊娠晚期出现了皮肤干燥症状。综合风湿免疫科会诊意见,停用抗生素,并予泼尼松10 mg、3 次/d治疗,病情明显好转。出院后完善相关检查,最终确诊为原发性干燥综合征。
2.2 治疗目标研究认为干燥综合征合并妊娠并不增加流产和胎儿生长受限的风险,但若患者有血清学异常(抗磷脂抗体、抗红细胞抗体、狼疮抗凝物等阳性)和血液学异常(血小板减少症、红细胞减少症),或继发性干燥综合征合并系统性红斑狼疮,都显著影响妊娠,增加自然流产率和早产率[6]。妊娠对干燥综合征的影响未有明确的定论。有研究认为约30%的干燥综合征患者症状和体征会因妊娠而加重,也有研究认为妊娠不影响干燥综合征的病情[7]。妊娠与干燥综合征之间的关系也逐渐得到重视。许多国外的研究发现,干燥综合征本身并不影响女性患者的生育能力,但患者体内的抗SSA 抗体、抗SSB抗体可以影响胎儿。妊娠期间干燥综合征患者的胎盘可作为靶器官受到免疫损害,造成胎盘功能障碍。母体的抗核抗体、抗SSA 抗体、抗SSB 抗体等IgG能够通过胎盘进入胎儿体内,导致胎儿的生长发育异常。母体的自身免疫还可以引起胎儿组织损伤,如导致胎儿窦房结、房室结和希氏束纤维化和钙化。母体抗SSA 抗体和(或)抗SSB 抗体是胎儿先天性心脏传导阻滞、新生儿狼疮综合征及新生儿血色病的致病因素[8]。
妊娠期间干燥综合征治疗目的主要是终止或抑制患者体内的异常免疫反应,保证胎儿宫内正常生长发育,预防妊娠期并发症及新生儿并发症。通过妊娠期严密监测及规范治疗,可维持病情稳定。本例孕妇于入院后完善相关检查,并与患者及家属充分沟通病情,指征明确的情况下行剖宫产终止妊娠,手术顺利,分娩一足月、健康女婴。分娩后因对症治疗效果欠佳,立即全面分析了发病原因,在多科讨论、指导后,于产后1 周即拟诊为自身免疫性疾病,并换用激素治疗,做到了早期诊断、早期治疗。患者出院后在此基础上接受了进一步的规范检查及治疗,病情控制良好。
2.3 治疗方案目前提倡的治疗方式主要包括对症治疗和系统性治疗,系统性治疗又包括糖皮质激素和免疫抑制剂治疗等[9]。①对症治疗:干燥综合征患者在妊娠期间应保持口腔清洁,勤漱口,减少龋齿和口腔继发感染。避免应用影响唾液腺分泌的药物,如阿托品、抗组胺药等。对于干燥性角结膜炎患者,使用外用眼膏保护角膜。②系统性治疗:如果妊娠期间干燥综合征患者出现严重内脏损伤等表现,一般建议终止妊娠后应用糖皮质激素和免疫抑制剂治疗。若妊娠期病情平稳,则定期随诊观察。妊娠期可考虑使用的药物包括糖皮质激素、抗疟药(羟氯喹)、柳氮磺吡啶、硫唑嘌呤和环孢素[10]。妊娠期禁用的药物包括甲氨蝶呤、环磷酰胺和霉酚酸酯等。糖皮质激素在妊娠期应用较为安全[11],泼尼松龙、甲泼尼龙在妊娠早、中、晚期均可使用。但由于其对水盐和物质代谢的影响,易出现妊娠期高血压和糖尿病,且易合并骨质减少和感染,影响孕妇健康和胎儿生长,故应避免使用大剂量糖皮质激素[1~2 mg/(kg·d)],建议尽可能用最小剂量激素维持疾病缓解状态,同时应积极控制血压、血糖,积极补充钙质预防骨质疏松。羟氯喹是妊娠期可安全选择的药物之一。有研究显示超过100 例孕妇在妊娠早期口服羟氯喹250 mg或羟氯喹200~400 mg 治疗,结果并未增加胎儿先天性异常发生的风险[12]。分娩后,患者有疾病复燃或加重趋势,分娩后需加大糖皮质激素用量,以防止复发或反跳。本例孕妇终止妊娠后加大激素剂量,病情明显缓解,维持治疗至症状消失及肝功能正常。
本病例的诊治过程提示,当孕妇出现体温持续升高、肝功能异常、高级别的抗生素治疗效果不满意时,结合眼干、口干的症状,往往需警惕妊娠合并干燥综合症的发生。妊娠期干燥综合症起病多隐匿,患者很难说出明确的起病时间,临床表现多样,比如本例孕妇术后第8 天才考虑干燥综合征可能,分娩后3 个月才明确诊断。临床医师对妊娠期出现原因不明的发热及肝功能异常的孕妇,在常规治疗效果差的情况下,应考虑妊娠合并自身免疫性疾病可能,并进一步完善相关检查以明确诊断。对于妊娠合并干燥综合征的孕妇,是否给予激素治疗、治疗时间、终止妊娠的时机,都应根据治疗效果、疾病严重程度及母儿情况综合分析,应予个体化分层管理,以期最大程度改善母儿结局。

