钾离子电池电解液的研究进展及展望
王轩臣,王 达,刘朝孟,高宣雯,骆文彬
(东北大学冶金学院,辽宁 沈阳 110000)
可充电锂离子电池(LIBs)由于其长寿命和高能量密度而广泛应用于移动电子设备和电动汽车[1-5]等。然而,由于锂资源的稀缺性和不均匀的地理分布,导致锂的成本增加,这可能会限制其在未来的可持续应用[6-7]。因此,基于地球上的Na、K、Mg等元素的下一代二次电池是未来能量存储系统中LIBs理想的替代品。其中,钾离子电池(PIBs)具有成本低、环境友好和高能量密度的优点引起了极大的关注[6-10]。钾离子电池的主要优点可总结如下:①自然界中的K元素丰富无毒,可从海洋中大量提取;②K/K+的氧化还原电位[-2.93 Vνs标准氢电极(SHE)]接近Li/Li+[-3.04 Vνs标准氢电极(SHE)],表明PIBs 也有类似的高电位平台;③K+的斯托克斯半径小于Li+和Na+,K+路易斯酸性比后者弱,故电解液中的K+迁移速率更快、迁移数更多,但去溶剂化能力更低[11];④铝箔可以用作PIBs 的集流体,因为K和Al之间没有合金化反应,可以显著降低电池的成本和重量[7,12-14]。
电极/电解液界面之间的关系可以帮助理解电解液对电化学性能的影响。电解液可以直接或间接地影响电池的电化学性能[图1(a)]。电解液对电池的容量、倍率性能、循环性能等电化学性能有重要影响[15-17]。因此,本文对近年来PIBs电解液的特点及研究进展进行了综述和讨论。首先集中在PIBs电解液的一些普遍问题。然后分别介绍了各种类型电解液的一般性质、优缺点、电化学性能。此外,我们还对一些新兴的电解液如固体电解质、离子液体电解液等进行综述。最后对电解液的发展提出了建议和展望。

图1 (a) 电池组件与电化学性能之间的关系;(b) 锂离子电池、钠离子电池和钾离子电池的能量密度比较[22];(c) Li、Na、K在地球中的分布[23];(d) 有机电解液、水系电解液、离子液体电解液、固态电解质的研究比例[24];(e) 钾离子电池电解液存在的问题[25]Fig.1 (a) Relationships between battery components and electrochemical performance; (b) Comparison of energy densities of lithium-ion, sodium-ion, and potassium-ion batteries[22]; (c) The distribution of Li, Na,and K in the Earth[23]; (d) Proportion of research on organic liquid electrolytes, aqueous electrolytes, ionic liquid electrolytes, and solid-state electrolytes[24]; (e) Problems in electrolyte of potassium ion batteries[25]
迄今为止,已经研究了4种电解液体系,包括有机电解液、水系电解液、离子液体电解液和固体电解质[图1(c)],且绝大多数研究都是有机电解液。PIBs 表现出与LIBs 相当的高电位平台和高能量密度[图1(a)]。此外,钾分布均匀,在地壳中占1.5%[图1(b)],几乎是锂的900 倍(仅20 ppm,1 ppm=10-6)[18-20]。但PIBs在电解液方面还存在相当多的问题,如图1(d)所示:①K金属会与电解液发生严重的副反应;②醚类溶剂与碳基材料配位时具有高电位平台,高电位下抗氧化性较差;③目前对固体电解质界面性质的研究明显不足;④普鲁士蓝及其类似物会溶于有机电解液[21]。
1 有机电解液
有机电解液因其优异的电化学性能以及与各种电极材料的良好相容性,在碱金属离子电池中得到了广泛的应用。通常,有机电解液需要满足以下要求:①具有良好的稳定性并且在工作电压范围内不会分解;②可以形成均匀且稳定的SEI膜;③可以抑制副反应。
PIBs 有机电解液通常是钾盐和非水溶剂的混合物[图2(a)]。一般来说,最高占据分子轨道-最低未占据分子轨道(HOMO-LUMO)能级是理解有机溶剂和盐的潜在电化学性能的重要参数。虽然HOMO-LUMO 间隙并不代表有机溶剂和钾盐的电位窗口,但它可以作为理解电解液提供或接受电子的能力的参考[26]。需要注意的是,钾盐的LUMO相对低于溶剂[图2(c)][25],这表明钾盐比溶剂更容易接受电子。而醚基溶剂的HOMO 能级相对高于碳酸盐溶剂,表明醚基溶剂在高电压下比碳酸盐溶剂更容易发生分解。Li 等[27]比较了DME 和EC/DEC电解液的电化学稳定性,并解释了SEI 形成机制。并通过密度泛函理论计算了钾盐和溶剂的HOMO和LUMO能级,确定SEI的形成机制。如图2(b)所示,KFSI 的LUMO 能级和还原能低于DME[28]。此外,FSI-的还原产物是无机化合物,形成了更致密的无机SEI 层。相比之下,EC/DEC 较低的LUMO能级会导致分解和严重的副反应,形成较厚的有机-无机SEI膜。

图2 (a) PlBs中常见的有机溶剂和钾盐的晶体结构以及溶剂分子;(b)钾盐的HOMO和LUMO能级:FSl-和DME在DME电解液中。EC/DEC电解液中的FSl-、EC和DEC[28];(c) PlBs中常用溶剂和钾盐的LUMO和HOMO能级[25]Fig.2 (a) Crystal structure of common organic solvents and salts of potassium ion batteries[25];(b) HOMO and LUMO energy levels of solvent molecules and potassium salts: FSl- and DME in DME electrolyte.FSl-, EC, and DEC in EC/DEC electrolyte[28]; (c) The LUMO and HOMO energy levels of commonly used solvents and potassium salts in PlBs
有机电解液主要分为两类:酯基电解液和醚基电解液。
1.1 酯基电解液
酯基电解液因其优异的电化学性能和高离子电导率成为了PIBs 中最受欢迎的电解液之一,常见的酯基溶剂是碳酸乙烯酯(EC)、碳酸丙烯酯(PC)、碳酸二乙酯(DEC)。一般来说,二元组合的使用具有更突出的电化学性能,如EC/PC或EC/DEC等,Zhao 等[29]研究了石墨在EC/DEC、EC/PC、EC/DMC 3 种不同的电解液组合中电化学储钾性能的差异。结果表明,以六氟磷酸钾(KPF6)为溶质,EC/DEC 和EC/DMC 为溶剂时,首次库仑效率很低,这是由于DMC 在低电位下的大量分解和还原产物的电化学稳定性较差所致。
通常,电解液溶剂是电池发生热失控起火的主要原因之一。故对于PIBs来说安全长期运行(即没有热失控和火灾)是不可或缺的。传统的电解液,主要是碳酸盐和醚基电解液,是高度易燃和危险的[图3(a)]。因此,为了保证电池的安全性,最好用不易燃的溶剂制备电解液。

图3 (a) 比较传统(碳酸盐和醚基)和不易燃(磷酸酯基)电解液危险特性的图解;(b) 各种电解液的燃烧试验[30];(c) 单斜K2FeFe(CN)6在K脱嵌过程中向立方FeFe(CN)6的可逆结构转变[31];(d) 电解液对Bi/rGO电极的SEl层的稳定作用的示意图[32];(e) 0.9 mol/L KFSl TEP钝化;(f) 2 mol/L KFSl TEP钝化下SEl形成的图示[33];(g) 在0.8 mol/L KPF6 EC/DEC、1 mol/L KFSl EC/DEC和3∶8(KFSl∶TMP)中在铜基底上的K金属镀层的原位光学图[34]Fig.3 (a) An illustration that compares the hazardous properties of traditional (carbonate and ether-based) and non-flammable (phosphate ester-based) electrolytes; (b) Flame tests of various electrolytes[30]; (c) Schematic illustration of the proposed stabilization effects of electrolyte on the SEl layer of Bi/rGO electrode[32]; (d) Cycling curves of K|K symmetric cells with different electrolytes at a current density of 1 mA/cm2; (e) 0.9 mol/L KFSl TEP passivation; (f) 2 mol/L KFSl TEP passivation[33]; (g) In-situ optical observations of K metal plating on copper substrate in 0.8 mol/L KPF6 EC/DEC, 1 mol/L KFSl EC/DEC, and 3∶8 (KFSl∶TMP)[34]
Fan 等[30]研究了一种由三(2,2,2-三氟乙基)磷酸酯(FTEP)和KFSI组成的低浓度(1 mol/L)电解液,使得PIBs安全和耐用。由于FTEP溶剂的溶剂化能力较弱,故该电解液(1 mol/L KFSI FTEP)促进了阳极表面SEI膜的形成。该团队还对常用的碳酸酯和磷酸酯电解液进行了燃烧试验,以研究其可燃性[图3(b)]。碳酸酯电解液如EC、PC、DMC、EMC和DEC 的溶剂高度易燃。相比之下,以磷酸三甲酯(TMP)、磷酸三乙酯(TEP)和FTEP为溶剂的磷酸酯电解液不可燃。从而可以显著降低火灾风险,提高电池的安全性。
同样为了降低火灾风险,提高电池的安全性,Liu 等[33]以KFSI 为盐、阻燃剂磷酸盐(TEP 等)为单一溶剂,研制了一种中等浓度的不易燃电解液,用于钾金属和钾离子电池。在PIBs 中,当使用TEP作为单一溶剂时,石墨电极以2 mol/L KFSI TEP为电解液时,性能可以显著提高(与0.9 mol/L KFSI TEP相比),理论和实验结果表明,在低浓度的电解液中存在大量的游离溶剂分子,溶剂和盐都被分解,并且它们会形成不均匀和不稳定的SEI膜。电解液的连续分解造成了不可逆的容量衰减[图3(e)]。相比之下,在2 mol/L KFSI TEP中,SEI膜主要由FSI-分解形成,均匀且稳定,可有效抑制溶剂分解并提高了循环稳定性[图3(f)]。与传统碳酸盐电解液相比,2 mol/L KFSI TEP 电解液不仅增强了K 金属、石墨阳极和PTCDA|钾化石墨全电池的电化学性能,而且还提高了安全性,该电解液在金属和石墨阳极上均表现出优异的电化学性能和安全性。
Guo等[34]报道了由磷酸三甲酯(TMP)和双(氟磺酰基)酰亚胺钾(KFSI)组成的电解液,盐∶溶剂摩尔比为3∶8。它与石墨阳极高度相容,并显示出优异的电化学稳定性。在对称的K/K 电池中,KFSI/TMP 电解液中的K 金属表现出稳定的镀覆和剥离,且极化电位很小(0.12 V)。相反,在EC∶DEC电解液中观察到电压分布存在波动和大极化电位,这可能是由于K 的不均匀镀覆和枝晶生长造成的。如铜基底上K 电镀的原位光学视图如图3(g)所示,在0.8 mol/L KPF6EC/DEC中,镀钾使铜表面出现气泡,导致沉积不均匀,枝晶较大。伴随着生长,观察到大量的死K 从铜基底上脱落。1 mol/L KFSI EC/DEC中也存在不均匀镀覆和K枝晶等相同的问题[32-33]。相比之下,在3∶8(KFSI∶TMP)电解液中镀K 致密且均匀,30 min 后未观察到枝晶或死K。K/K 电池在-50~50 ℃的温度范围内工作状况良好,但当温度低于-40 ℃时极化变大。EC/DEC电解液不能在极端温度下进行稳定的K 电镀和剥离。这种兼容电解液的优异温度性能表明其在全气候应用中的巨大潜力。
电解液添加剂可以有效地改善PIBs 的电化学性能特别是氟代碳酸亚乙酯(FEC),添加剂主要通过参与SEI膜形成、改变K+的溶剂化结构、增加电解液润湿性、降低黏度、防止过充电和改善热稳定性来改善PIBs的电化学性能。例如,He和Nazar等[30]使用K1.7Fe[Fe(CN)6]0.9作为阴极材料,FEC作为电解液添加剂探究添加剂对PIBs 性能的影响。图3(c)显示了循环后的预期结构转变[34-35]。从KFeHCF-S(“K2Fe2+[Fe2+(CN)6]”)中完脱K以形成Fe3+[Fe3+(CN)6],晶格转变为立方对称结构。当K+重新插入时,立方对称结构降低为单斜结构,这个过程是高度可逆的。在0.5 mol/L KPF6EC/DEC 电解液的循环过程中,充电过程逐渐变得不稳定,约80次循环后失活。当5% FEC添加剂添加到电解液中时,库仑效率和长循环性能显著改善,表明电解液添加剂有利于能量存储。然而,FEC添加剂对PIBs的循环稳定性的影响仍有争议。因为少数研究表明FEC添加剂可以提高库仑效率,但是它们不能完全防止副反应并且还可能引起更大的极化现象[36]。因此,寻找合适的电解液和添加剂来提高PIBs的电化学性能具有重要意义。
Zhang等[32]研究了Bi/rGO阳极在单一溶剂(EC/DEC)、不同钾盐(KPF6和KFSI)中的SEI形成机理,发现KPF6电解液中的SEI膜比KFSI更厚。在KPF6电解液中,重复构建的SEI膜不断消耗电解液,并且由于Bi纳米颗粒和SEI膜的破碎而使界面层越来越厚[图3(d)]。相比之下,在KFSI电解液中具有更完整和更薄的SEI膜。该团队还研究了不同钾盐电解液中SEI 膜的组成[6,38-39],发现在KPF6电解液中形成的SEI膜主要由有机组分组成,其可能主要来自于溶剂的还原产物。但对于KFSI电解液,SEI膜由无机/有机混合物组成,来源于盐和溶剂的还原产物。与有机组分相比,无机盐具有更好的机械强度以适应大的体积变化,从而形成更稳定的SEI膜[40-41]。
Peng 等[41]通过引入一种绿色无害的长链溶剂碳酸二辛酯(DCC),制备了1 mol/L KFSI EC/DCC的长链电解液,与1 mol/L KFSI的常规电解液相比,该长链电解液表现出更优异的电化学性能,且可以形成具有高弹性的长链富含有机物的SEI 膜(LOSEI),大大提高了PIBs的电化学性能。实验结果表明,在1 mol/L KFSI EC/DCC的长链电解液中,石墨半电池具有优异的循环稳定性(1500 次以上循环86.7%容量保持率),同时K||K 对称电池具有3700小时以上的长稳定性。此外,基于LO-SEI的全电池能够稳定运行超过130 个循环(84.3%的容量保持率)。该研究为构建长链弹性界面以实现高性能电池开辟了新思路。
1.2 醚基电解液
与酯基电解液不同,醚基电解液由于其较高的溶解度而广泛应用于LIBs 和SIBs[42-46],在PIBs 中同样很受欢迎,DME 作为一种常见的醚类溶剂已经得到了很多研究[47-49]。
Hosaka 等[48]报道了高浓度KFSI DME 电解液在石墨阳极中具有高的离子电导率以及形成稳定的SEI 膜。在7 mol/L KFSI DME 下,石墨阳极的平均库仑效率可达99.3%,全电池(石墨-K2Mn[Fe(CN)6])循环101次后容量保持在85%以上。除了醚类溶剂外,另一个不同之处在于这里使用了高浓度的电解液。
Gu 等[40]以二甲醚和环状碳酸酯为溶剂,以KPF6为溶质(1 mol/L KPF6在EC/DME 中,1∶1,体积比),在50 ℃预循环的电解液可使石墨阳极在室温下具有优异的循环稳定性。在50 ℃预循环时,DME与EC协同作用,在石墨表面形成稳定均匀的SEI膜[图4(a)]。稳定均匀的SEI膜可以提高石墨阳极充放电过程中的循环稳定性。结果表明,石墨阳极在50 ℃预循环的EC/DME 电解液中可提供约220 mAh/g的可逆容量,在50 mA/g下循环500次以上,容量衰减可忽略不计,且室温下PIBs 的平均库仑效率大于99%。

图4 (a)在石墨表面上形成的不同SEl膜及其在长循环后的演变[40];(b) Cu基体在不同电解液中以0.05 mA/cm2电流密度进行恒电流镀钾和剥除[47];(c)不同电解液中石墨钾脱嵌[52];(d)钾插层过程中的阶段结构演变[51];(e) SnSb/C电极中钾化/脱钾过程[56]Fig.4 (a) Schematic illustration of different SEl layers formed on the surface of graphite and their evolution after many cycles; (b) Comparing galvanostatic K plating and stripping on the Cu substrate among different electrolyte formulations at the rate of 0.05 mA/cm2[47]; (c) Schematic illustration for graphite response in different electrolytes[52]; (d) Stage structure evolutions during K intercalation[51]; (e) Schematic illustration of the potassiation/depotassiation process in SnSb/C electrode[56]
Xiao 等[47]在测试的不同电解液中,KFSI DME是唯一能够长期可逆镀钾和剥离的方案[图4(b)]。1 mol/L KPF6DME、1 mol/L KTFSI DME和0.8 mol/L KPF6EC/DEC(水<10 ppm,1 ppm=10-6)均无法进行可逆镀钾和剥离,并由于容量的快速衰减和低库仑效率,导致电池在10~20 个循环内失效。相比之下,使用稀释(摩尔比=0.1)和浓缩(摩尔比=0.5)KFSI DME 电解液可以在100 次循环中实现99%的高库仑效率,表明高浓度KFSI DME电解液与低浓度相比具有优异的氧化耐久性。理论计算表明[49-50],DME 在浓电解液中与K+的结合更加紧密,从而降低了HOMO 能级,减缓了电解液的氧化分解。
Yang 等[51]为了解决高性能金属磷化物的体积变化问题,制备了4 mol/L KFSI DME浓缩电解液以改善PIBs 的循环稳定性。团队以蛋黄-壳结构的CuP2@碳纳米球(CuP2@CNSs)为例,在不同的电解液中进行了研究和测试。与稀1 mol/L KFSI 相比,浓4 mol/L KFSI 在K 离子和K 金属电池中表现出良好的循环稳定性,这得益于阴离子衍生的富含无机物的SEI 膜,其在组成和形貌上均匀稳定。CuP2@Carbon 独特的蛋黄-壳结构,可以在一定程度上缓冲体积的变化,从而保持电极的完整性。进一步研究表明,浓缩电解液能抑制钾枝晶生长,避免发生副反应,提高PIBs的安全性。这项工作提供了一种可行的策略,以减轻金属磷化物的降解,建立高能量密度的PIBs。
Wang 等[52]研究了层状TiS2阴极材料,其在醚基电解液(1 mol/L KPF6DME与1 mol/L KPF6DMC)中表现出优异的储钾性能和倍率性能。恒电流间歇滴定技术(GITT)结果表明醚基电解液中K+嵌入TiS2的机理与EC/DMC 基电解液一致。如图4(d)所示,在K 嵌入的早期阶段(0<x<0.19),原始相迅速转变成亚稳单相,实际上是第二阶段缓冲相结构。在第二阶段(0.19<x<0.27),检测到两个相的组合。随着进一步的嵌入(0.27<x<0.56),第二阶段相消失,观察到第一阶段单相结构。
此外,Li等[53]还比较了石墨作为PIBs的阳极在1 mol/L KPF6DME和1 mol/L KPF6DMC中的电化学性能。与EC/DMC 基电解液相比,在DME 基电解液中的石墨阳极具有更高的工作电压,几乎可以忽略的固-液界面和更小的体积膨胀。而且在DME基电解液中,不是K+嵌入石墨形成KC8,而是K+-醚共同嵌入石墨,起到了电荷屏蔽作用。图4(c)显示了石墨阳极在不同电解液中与操作电压和功率比有关的不同电化学响应,可以看出DME 基电解液具有比EC/DMC 的更大的电子供体数(20νs16)[54-55],这使其具有更高的与K+形成K+-DME络合物的结合能。具有“鞘”的复合物插入石墨的同时,K+-DME溶剂的LUMO能级将高于石墨,使得它们没有发生电化学反应,未形成SEI 膜[56]。总的来说,[K-溶剂]+分子插入到石墨中而没有堵塞SEI,形成了热力学稳定相,体积膨胀也较小。这两项研究表明,溶剂的选择是至关重要的。
2 水系电解液
基于水系电解液的PIBs 是大规模应用的潜在候选者,因为与有机电解液相比,水系电解液成本低且不可燃。此外,钾的地球丰富度和高电导率使得水系PIBs 成为有前途的材料。目前对基于水系电解液的锌离子电池(ZIBs)、锂离子电池(LIBs)和钠离子电池(SIBs)进行了相当多的研究[58]。水系电解液通常分为常规水系电解液,例如KOH、KCl、K2SO4和KNO3盐溶液,以及盐包水电解液,例如CH3CO2K 和CF3SO3K。有机材料与水系电解液的相容性使它们成为水系PIBs 的理想候选者。大多数有机电极材料可溶于有机电解液;因此,水系电解液是有机电解液的理想替代物。但到目前为止,只有少数几种有机材料用于水系PIBs[59-62]。
有机阴极和阳极材料因其高的K+电导率和较差的溶解度而更适合于水系电解液,并在水系电解液中表现出优异的储钾性能[60,63]。例如,Li 等[60]以聚蒽醌基硫化物为阴极材料,1 mol/L KOH水溶液为电解液,在2 A/g的电流密度下,表现出128 mAh/g的高比容量[图5(a)],高于在相同电流下用有机电解液0.5 mol/L KTFSI在二氧六环(DOL)和乙二醇二甲醚(DME)]得到的比容量(106 mAh/g)。此外,高浓度的水电解液可以进一步提高容量。Liang 等[61]用聚蒽醌基硫化物阳极,Ni(OH)2阴极和10 mol/L KOH 电解液组装全电池。储钾机理如图5(c)所示,PAQS-Ni(OH)2全电池在2 A/g的电流密度下的比容量提高到186 mAh/g。

图5 (a)在1 mol/L、10 mol/L和30 mol/L KAc电解液中以1 mV/s的线性伏安曲线[59];(b)在1 mol/L和22 mol/L KCF3SO3电解液中的电位窗口[60];(c) PAQS中储钾机制[60]Fig.5 (a) Linear voltammetry curves recorded at 1 mV/s in 1 mol/L, 10 mol/L, and 30 mol/L KAc electrolytes[63];(b) The electrochemical stability window of the 1 mol/L and 22 mol/L KCF3SO3 electrolytes respectively[60];(c) A possible redox mechanism of potassium storage in PAQS
通常,水系电解液的电位窗口比有机电解液的电位窗口窄(1.23 V)。在电势窗口之外,会发生水的裂解,并伴有氧和氢的析出。电极的低利用率以及低电位降低了实际能量密度,这阻碍了水系PIBs 在商业电池中的应用。为了解决这个问题,开发了基于盐包水概念的电解液。盐包水电解液具有许多优点,如低含量的游离水分子而产生较宽的电位窗口,以及在高浓度电解液下有机阴极和阳极溶解的减少。目前,盐包水电解液中用CH3CO2K基的盐,其具有价格低廉、更宽的电位范围,与铝集流体相容性较好以及环境友好等优点。Leonard等[64]开发了一种高浓度(30 mol/L)CH3CO2K 基盐包水电解液,其具有3.2 V 的高电位窗口[图5(a)]。30 mol/L CH3CO2K 电解液可以提高Li TFSI 及其类似氟酰亚胺盐的电导率。但水系PIBs 在碱性环境中的不稳定,是应用的一大障碍。
Jiang 等[58]制备了高浓度(22 mol/L)KCF3SO3盐包水电解液,其具有3.0 V的高电位窗口(与1 mol/L电解液对比)[图5(b)],并研究了其对全电池性能的影响。因游离水分子含量低,浓电解液显著降低了有机电极材料的溶解,使全电池表现出优良的循环寿命,高容量保持率(在4 C下循环2000次后为73%),高能量密度(80 Wh/kg),以及在20~60 ℃宽温度范围内具备良好的倍率性能(20 C)。该团队还研究了几种用CH3CO2K基盐包水电解液的阴极材料。由于其在水中的高稳定性和在中性溶液(如K2SO4、KCF3SO3)中独特的晶体结构,使其显示出优异的电化学性能。然而,盐包水电解液通常比传统的水系电解液更贵。因此,迫切需要开发低成本、高稳定性、宽电位窗口的水系电解液来应用于水系PIBs。
3 固体电解质
用于LIBs 或PIBs 中的传统的有机电解液表现出优异的电化学性能和高的离子电导率。但LIBs和PIBs 中易燃、易挥发的有机电解液会带来严重的安全问题,阻碍了它们的实际应用。由于钾的高反应性,PIBs 有更严重的安全问题。固体电解质与有机电解液相比具有许多优点,如更好的安全性、优异的热稳定性、更宽的电位窗口和更好的循环稳定性[65-66]。特别是陶瓷基固体电解质具有优异的力学性能和高的离子电导率,而固体有机电解质具有良好的柔韧性和易加工性[67-68]。因此,固体电解质是克服下一代PIBs 中安全问题的替代传统有机电解液的理想电解质。固体聚合物电解质(SPEs)和无机电解质是固体电解质的一种,它们在PIBs中的应用得到了广泛的研究。固态电解质防止了有机活性物质在有机电解液中的溶解,并提高了PIBs的循环寿命[69-70]。
3.1 固体聚合物电解质
与传统的有机电解液相比,固体聚合物电解质(SPEs)具有许多独特的优点,如成本低、密度小、加工性好、灵活性高、安全性好、力学性能好以及优异的热稳定性和化学稳定性[71-72]。但钾的熔化温度(63.5 ℃)低于锂的熔化温度,且非常接近SPEs的工作温度,这阻碍了SPEs基钾金属电池的商业应用。聚乙二醇(PEO)、聚丙烯腈(PAN)、聚乙烯醇(PVA)和聚乙烯吡咯烷酮(PVP)等聚合物已被用作SPEs 的聚合物主体。SPEs 的主要缺点是它们在室温下的离子电导率很差(10-5~10-7S/cm)[73-74]。大多数关于SPEs的研究都是在高温下进行的,以实现高离子电导率。例如,在LIBs 中具有高离子电导率的PEO-SPE 的最低操作温度为60 ℃。本节主要讨论了SPEs在中等温度(60 ℃)下用于PIBs的离子电导率和电化学性能。
Stevens 等[72]研 制 了 第1 种K+导 电SPEs,PEO-KAg4I5,该SPEs 在室温下具有2×10-3S/cm的高离子电导率。Reddy等[74]将PVP和PVA的混合物与KBrO3溶液用浇注法混合,设计了一种SPEs。当PVP∶PVA∶KBrO3质量比为35∶35∶30时,共混SPEs 在33 ℃下的电导率为5×10-6S/cm,K+迁移数为0.97。Reddy 等[75]制备了PVC+KBrO3聚合物电解质(质量比80∶20),其在30 ℃下的离子电导率为7×10-8S/cm。
此外,Fei 等[76]首次报道了一种应用于PIBs 的具有非织造纤维素骨架的PPC-KFSI-SPE(PPCBSPEs)。并指出KFSI盐的浓度是影响SPEs离子电导率的关键因素。实验结果表明,随着盐浓度的增加,离子电导率先增大后减小,在20 ℃下,最佳的盐质量分数为18%,离子电导率最大值为1.36×10-5S/cm。通过线性扫描伏安法(LSV),发现PPCB-SPEs 具有良好的电化学稳定性。采用PTCDA 阴极和PPCB-SPE 组装的全固态钾电池[图6(a)]活化后的比容量为113 mAh/g,循环40 次后的比容量为91.71 mAh/g,每次循环容量损失约0.4%。相反,使用有机电解液的电池表现出快速的容量衰减,每次循环容量损失约为45.7%。结果表明,与有机电解液相比,SPEs通过阻止PTCDA阴极活性物质的溶解,提高了电池的容量和循环性能。

图6 (a) PPCB-SPE的全固态钾电池[76];(b) 1个循环;(c) 10个循环后,从固态PlBs分解的3 h Ni3S2@Ni电极的SEM图像[77]Fig.6 (a) All-solid-state potassium battery of PPCB-SPE[76]; SEM images of 3 h Ni3S2@Ni electrode decomposed from solid PlBs after (b) 1 cycle and (c) 10 cycles[77]
同一小组[78]后来开发了PEO-KFSI固体电解质。PEO-SPE在60 ℃下的最佳[EO]/[K+]摩尔比约为10,其表现出最高的离子电导率,为2.7×10-4S/cm。具有PEO-KFSI电解质的全固态Ni3S2/Ni电极显示出优异的循环性能,当循环次数增加到10个循环时,与先前的电极相比,形貌[图6(b)、(c)]仍然没有过多的变化,这进一步表明基于PEO的SPEs可以防止多硫化物溶解在电解质中,在100 次循环后依然有307 mAh/g的高容量。PEO-SPE具有优异的循环性能,这不仅可以避免安全问题,而且还可以抑制多硫化物的溶解。因此,固体聚合物电解质可以抑制枝晶的生长,提高电池的安全性。但是由于钾离子尺寸较大,通常SPEs的离子电导率较低。
3.2 无机固体电解质
无机固体电解质的K+离子电导率高于SPEs,且在过去几年中已经开发了各种无机固体电解质。Lu等[79]制备了一种新型的钾离子导电β-Al2O3作为K-S电池的固体电解质(K-BASE)。K-BASE 在300 ℃和150 ℃下的离子电导率分别为0.056 S/cm和0.01 S/cm,并且与Na-BASE和Na金属的界面润湿性相比,在150 ℃下K-BASE 和K 金属具有更优异的界面润湿性。因此,K-S电池在约150 ℃的较低温度下运行,会表现出更优异的循环寿命,在1000次循环中容量衰减可以忽略不计。循环寿命的提高归因于致密的β-Al2O3膜,其防止了电极之间的相互扩散和副反应。
Eremin等[80]通过高通量的几何拓扑方法和精确的DFT建模[图7(a)~(c)],获得了K+迁移能量较低的K2Al2Sb2O7和K4V2O7,其非常适合制备固态钾离子电池。此外,Wang 等[81]开发了一种新型的无机固体电解质KNH2,用于PIBs。图7(d)是在100 ℃和150 ℃下V0T0和V150T10的奈奎斯特曲线。在相同的测量条件下,V150T10的电阻分别比V0T0低8.1 倍和6.9 倍。图7(e)中,V150T10和V0T0的离子电导率图大致可分为3部分:室温至60 ℃、60~80 ℃和80~150 ℃,拐点温度分别与KNH2从单斜晶(P21/m)到四方晶(P4/nmm)和立方晶(Fm-3m)的相变温度一致。V150T10的离子电导率在150 ℃时达到3.56×10-4S/cm,比其在室温下的电导率高3 个数量级,比相同温度下V0T0(4.84×10-5S/cm)高7 倍。这意味着KNH2的离子电导率通过球磨得到了显著提高。后来,他们发现离子电导率与电解质中的氮缺陷浓度相似是有关系的。他们的工作为无机固体电解质的研究开辟了一条新的途径。

图7 (a) K2CoSiO4、(b) K4F2O5和(c) K6V2P4O16晶体结构中,通过几何拓扑方法获得空隙ZA的K+迁移图[80];(d)用不锈钢||KNH 2||不锈钢电池测试在100 ℃和150 ℃下V0T0(左)和V150T10(右)的奈奎斯特曲线;(e) V0T0和V150T10的离子电导率和活化能[81]Fig.7 K+ migration maps as Voronoi graphs (hereafter shown by green lines) of voids ZA obtained within the geometrical-topological approach in the K2CoSiO4 (a), K4Fe2O5 (b) and K6V2P4O16 (c) crystal structures[80];(d) Nyquist plots of V0T0 (left) and V150T10 (right) at 100 ℃ and 150 ℃, test with a stainless steel ||KNH2||stainless steel cell; (e) ionic conductivities and activation energies of V0T0 and V150T10[81]
Doux 等[82]制备了一种K3Sb4O10(BO3)化合物,其在400 ℃下具有相对较高的离子电导率,为1.5×10-4S/cm,活化能为0.325 eV。K+通过互连的1D隧道赋予K3Sb4O10(BO3)良好的电化学性能。Feng等[76]通过水热法制备了K2Fe4O7的三维开放框架,其中无序的开放通道可以填充K+。
与锂离子和钠离子相比,钾离子固体电解质的报道相对较少。目前的研究集中在提高固体电解质的离子电导率,而其他关键的电化学性能没有完全表征,包括力学性能、离子选择性、电化学稳定性和组装技术。
4 离子液体电解液
离子液体电解液(ILs)由无机或有机阴离子和有机阳离子组成,与水系和有机电解液相比具有许多优点,如低蒸气压、高温稳定性、宽的电位窗口、低挥发性和低可燃性。ILs 独特的电化学性质使其成为一种很有前途的电解液。与有机电解液相比,ILs 具有更好的电化学性能和更少的安全隐患。此外,钾基ILs有优异的抗钾金属稳定性。
目前用于PIBs 的ILs 的研究还很少。ILs 中使用的阳离子通常是咪唑(如[EMIM]+)、吡咯烷(如Pyr14)、铵(如[DEME]+)和硫(如[Me3S]+),而阴离子通常是四氟硼酸根(BF4-)、双(三氟甲磺酰基)酰亚胺(TFSI-)和双(氟磺酰基)酰亚胺(FSI-)。基于双(三氟甲磺酰基)酰胺钾(PTFSA)的ILs 已用于高电位的PIBs[83]。
Beltrop 等[84]证明了基于1-丁基-1-甲基吡咯烷二(三氟甲磺酰基)酰胺(Pyr14TFSA)中的双(三氟甲磺酰基)酰胺钾(KTFSA)的离子液体电解液作为钾双离子电池稳定性能的可行电解液,钾和双离子技术的结合产生了高的工作电位(>4.5 V),放电容量超过42 mAh/g(相对于阴极容量),库仑效率>99%。此外,1500 次循环后容量保持率为95%,表现出了优异的循环性能[图8(c)]。Souza等[85]对1-乙基-3-甲基咪唑四氰基硼酸盐([EMIM]+[B(CN)4]-)ILs 进行了分子动力学模拟,以确定Na+/K+[B(CN)4]-盐和聚环氧乙烷(PEO)对传输机制的影响,并指出ILs 是PIBs中有前途的电解液。
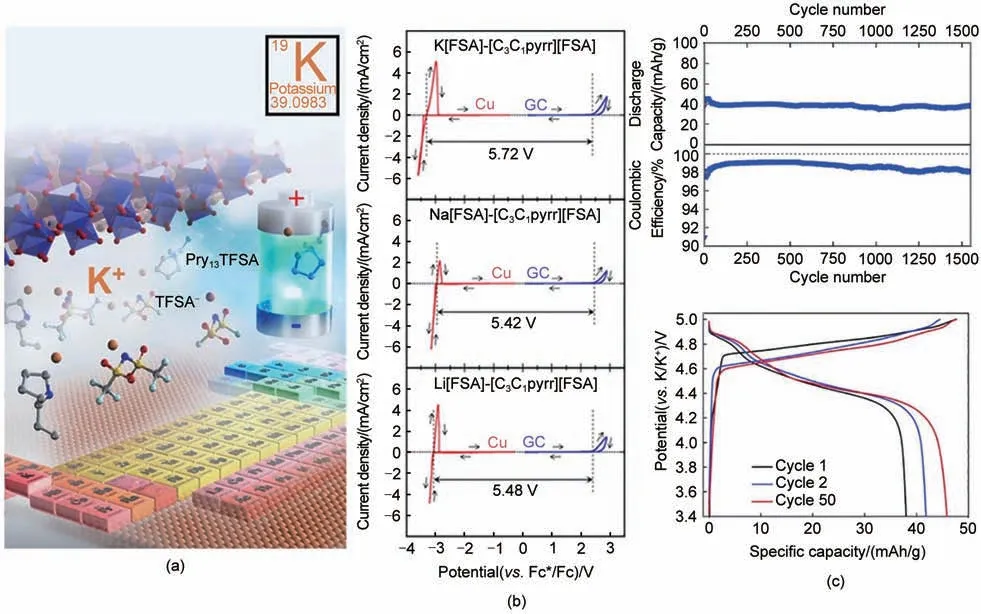
图8 (a)通过将高压蜂窝状层状框架与合适的阳极和基于1-甲基-1-丙基吡咯烷二(三氟甲磺酰基)酰胺钾(KTFSA)盐的离子液体电解液耦合的高压电池配置;(b) 5 mV/s K、Na、Li的循环伏安图[62];(c) 电解液:Pyr14 TFSl+0.3 mol/L KTFSl+2%ES。50 mA/g电流密度下的循环性能(上);石墨/K双离子电池在3.4~5.0 V的电位窗口下的充放电曲线(下)[84]Fig.8 (a) High voltage cell configuration by coupling a high voltage honeycomb layered framework with a suitable anode and an ionic liquid based on potassium 1-methyl-1-propylpyrrolidine bis(trifluoromethylsulfonyl) amide (KTFSA) salt; (b) Cyclic Voltammetric Curves of 5 mV/s K, Na, Li[62];(c) long-term cycling performance at 50 mA/g (up); Electrolyte: Pyr14TFSl + 0.3 mol/L KTFSl+2% ES,Potential profiles of graphite/K metal dual-ion cells for selected cycles between 3.4 V and 5.0 V vs.K/K+ at a charge/discharge current of 50 mA/g (down)[84]

图9 钾离子电池电解液的分类及优缺点Fig.9 Classification, advantages and disadvantages of electrolyte for potassium ion battery
Yoshii 等[62]使用双(三氟甲磺酰基)酰胺钾电解液组装了电池,并测试了蜂窝结构的层状K2Ni2TeO6和P2 型K2/3Ni1/3Co1/3Te1/3O2的循环性能和倍率性能,发现基于1-丙基-1-甲基吡咯烷三(Pyr13TFSA)中的KTFSA 盐的离子液体电解液在与高压层状氧化物如K2/3Ni2/3Te1/3O2耦合时表现出稳定的电化学性能[85],然而,基于KTFSA 盐的离子液体电解液的物理化学性质有待阐明,这是它们作为高压阴极材料的安全电解液的必要要求[图8(b)]。电化学测试显示[图8(a)],0.5 mol/L KTFSI/Pyr13TFSA的氧化还原电位低于Li 和Na 的氧化还原电位,并且具有高达6 V的高电位窗口。他们的工作不仅优化了层状阴极材料的性能,而且促进了对用于高能量密度钾离子储能系统的离子液体盐的发展。虽然离子液体电解液具有低可燃性、低挥发性等优点,但其高成本和高黏度可能会影响其在碱金属离子电池中的应用。因此,未来需要开发低成本的离子液体电解液以促进其商业化。
5 其他电解液
5.1 二元盐电解液
二元盐电解液由于黏度低、成本低的优点引起了研究者的关注,一些研究小组[87-88]最近也提出了一种二元盐(KPF6-KFSI)电解液。Zhu等[87]报道,与单盐KPF6电解液相比,MoS2电极在KPF6KFSI 电解液中的稳定性大大提高。Komaba 等[88]还研究了酯基溶剂中的二元盐(KPF6-KFSA)电解液。他们发现,当KPF6∶KFSA的摩尔比大于3时,电解液表现出优异的抗氧化性能,即使电位增加到4.6 V 持续100 h,集流体仍然没有明显的腐蚀现象。还成功组装了石墨|K(PF6)0.75(FSA)0.25/EC/PC|K2Mn[Fe(CN)6]全电池,其在500次循环后表现出优异的循环稳定性,远远优于传统的KPF6EC/DEC 电解液。与浓电解液相比,二元盐电解液在抑制铝腐蚀方面具有更好的效果和更低的成本。二元盐电解液虽有众多优点,但其最佳摩尔比以及每种盐起到的作用,在电化学性能中做出的贡献还未得到系统性地研究,这是二元盐电解液未来发展的重点。
5.2 混合/复合电解质
近年来,一些低成本的混合/复合电解液的出现也引起了广泛关注,Lu等[89]将普鲁士蓝钾@聚吡咯@布(KPB@PPy@Cloth)双极材料和聚乙烯醇-KCl复合凝胶聚合物电解质应用于PIBs。电解质具有优良的力学性能和柔韧性,该材料不仅可以提高电池的导电性,而且可以保证KPB粒子的均匀生长。此外,在电极材料和电解质的协同作用下,在500 mA/g的电流密度下循环200次后,容量保持率为82%,表现出优异的循环稳定性。混合/复合电解质的组分和结构还不能精确控制,不能对其力学性能、离子导电率、界面稳定性等物理化学性能进行有效的调控,K+的传导机理、各组分间的协同作用及界面性质研究得还不够充分,这些因素限制了混合/复合电解质的进一步发展。
有机电解液中酯基电解液因钾还原产生严重的副反应,循环稳定性较差且库仑效率较低。而醚基电解液可以减少副反应改善稳定性,形成稳定的SEI 膜。但醚基电解液在高电位下容易发生氧化,会降低工作电位和能量密度。水系PIBs 安全且便宜,但它们能量密度低且正/负极溶解较快。固体电解质表现出宽电位窗口和优异热稳定性,但离子电导率相对较低。离子液体电解液因其电化学稳定性高等优点,可以提高循环寿命和倍率性能,但成本太高限制了其在PIBs中的应用。此外,二元盐电解液可以显著改善循环寿命和倍率性能,并抑制集流体的腐蚀,与传统的浓电解液相比,它与混合/复合电解质都具有成本低的优势。不同电解液钾离子电池的电化学性能总结如表(1)所示。
6 结论与展望
PIBs 具有能量密度高、资源丰富、成本低等优点,是替代LIBs 的一种新型储能体系。然而,PIBs 的研究还处于初级阶段,尤其是电解液方面的一些问题还有待解决。电解液直接影响电池的能量密度、库仑效率、循环寿命、安全性和工作条件。本文对近年来PIBs 电解液的特点及研究进展进行了总结和讨论,介绍了有机电解液、水系电解液、固体电解质、离子液体电解液等4个主流电解质的优缺点[图(9)]以及未来的发展方向。
在PIBs 的设计和开发中,电解液应具有与正极、负极和全电池相同的优先级。电解液的设计应考虑以下要求:①高离子电导率;②电化学稳定性和热稳定性;③能够形成稳定且可持续的电极/电解液界面;④成本低,无毒害。有机电解液主要分为基于酯基和醚基的电解液,表现出宽电位窗口和高能量密度。酯基电解液因钾还原而产生严重的副反应,导致了较差的循环稳定性和低库仑效率。相比之下,醚基电解液可以改善稳定性,促进稳定SEI膜的形成,并减少副反应。但是醚基电解液在高电位下容易发生氧化,从而降低了PIBs 的工作电位和能量密度。为了解决这些问题,开发了KFSI 基电解液。KFSI 基电解液有利于形成稳定、均匀和坚固的SEI膜;但其与集流体的相容性需要进一步改善。高浓度的电解液有利于实现稳定的界面且可以依据溶剂化效应而抑制腐蚀反应。尽管水
系PIBs 相当安全且便宜,但它们能量密度低且正/负极溶解较快。固体电解质表现出宽电位窗口和优异热稳定性,有望实现高电位的可逆电化学反应。其机械强度高,可以减少枝晶形成并提高界面稳定性。因此固体电解质在PIBs中有良好的应用前景。ILs 具有挥发性低、高电化学稳定性和安全性好等优点,可以显著提高循环寿命和倍率性能,是下一代PIBs 的理想电解液。但在PIBs 中的应用很少,这可能是ILs 成本太高所造成的。开发低成本的PIBs 电解液是未来必要的研究方向。此外,二元盐电解液可以显著改善循环寿命和倍率性能,并抑制集流体的腐蚀,与传统的浓电解液相比,它与混合/复合电解质都具有成本低的优势。

表1 不同电解液钾离子电池的电化学性能Table 1 Electrochemical performance of K-ion batteries with various electrolytes
最后,为了确保PIBs 的安全性,需要用不易燃电解液替换易燃电解液。ILs 的诸多优点使其成为PIBs中有机电解液可行的中-短寿命替代品。在固体电解质中,固体聚合物电解质极有可能用于准固态和全固态电池。但相对较低的离子电导率和界面问题限制了它们的适用性。为了提高离子电导率,可以在SPEs中使用特殊添加剂或其他新型聚合物主体。对电解液和电极/电解液界面的研究有望帮助实现低成本、高能量密度的PIBs,进而实现大规模应用。合适的电解液不仅要在阳极表面形成稳定的SEI膜,还要在高压下稳定阴极材料。在K+重复脱嵌的过程中,需要稳定电极/电解液界面。开发化学稳定性更高的溶剂可以提高电解液工作的温度范围。还需要新的电解液添加剂来同时实现高库仑效率和长循环寿命。
对电解液的未来发展提出了以下策略:①调节电解液的浓度以建立稳定的SEI 膜;②通过配制局部高浓度电解液来降低经济成本;③开发比传统有机电解液具有更高模量和更轻重量的固体电解质;④使用电解液添加剂;⑤开发低成本的离子液体电解液;⑥探索新的钾盐、添加剂、溶剂等。我们期望所有可行的策略都能促进PIBs 在未来的实际应用。

