等离子体催化铁系金属催化剂氨分解制氢研究进展1)
高一博 胡二江 殷阁媛 黄佐华
(西安交通大学动力工程多相流国家重点实验室,西安 710049)
引言
在第七十五届联合国大会一般性辩论上,国家主席习近平提出“我国二氧化碳排放力争于2030 年前达到峰值,努力争取2060 年前实现碳中和”,“碳达峰”和“碳中和”成为我国新时代能源领域转型发展的总体方向和重点任务.为应对气候变化,各国也都面临由传统的化石能源向氢能、太阳能、风能和水能等可再生能源转换的问题.氢能作为一种最具发展潜能的绿色二次能源载体,发展和应用前景广阔,世界各国纷纷针对氢能关键技术开展广泛研究.
氢能拥有高效清洁、来源丰富、燃烧热值高和绿色零碳等诸多优势,但以制氢、储氢和输氢到用氢的氢能产业链存在两个关键问题: (1)氢具有高度易燃、易爆的特点,在储运方面存在诸多安全风险,这极大限制了其规模化应用;(2)氢的体积能量密度较低,在高压储运过程中(约为20 MPa)成本较高,还会发生氢逸出等安全问题.作为一种零碳燃料,以氨为储氢载体而发展衍生的“清洁高效合成氨,经济安全储运氨,无碳高效利用氨”的“零碳”技术路线,是一条实现“碳达峰,碳中和”目标的重要技术途径[1-3].国际能源组织(international energy agency,IEA)[4]预测,到2050 年对氨能的需求较2020 年将扩大3 倍.世界各国也在积极响应大力开发氨能的产业布局,日本和韩国对于氨能的开发和利用目前走在世界前列.中国也在大力推动氨能产业的规划和布局,2022 年科技部发布的国家重点研发计划中,提出包括分布式氨分解制氢技术与燃料电池、氨氢燃烧等与氢相关的技术.
氨作为储氢载体,极易被液化,含氢量高达17.8 wt%,氨的能量密度远高于电池,接近于化石燃料.氨最早被用以制作氨肥、氮肥等复合肥料以及硝酸、铵盐等化工产品,随着近些年氨能“制储输用”的快速发展和全面进步,其在高储氢新能源范围内的应用也愈加宽广.合成氨工艺最悠久的Haber-Bosch 法,制备工艺成熟,能源利用高效,基础设施完善.氨最大的优势就是不含碳,可直接用作清洁能源燃烧使用,不会产生含碳化合物.因此,无论是从技术分析、经济成本还是“双碳”目标出发,氨作为储氢载体都是可行的.氨分解反应(2NH3(g) → N2(g) +3H2(g),ΔH=92.4 kJ/mol)是吸热反应,高温有利于氨的分解.Web of Science 核心合集(SCI-E)数据库中关键词为“ammonia decomposition or NH3decomposition”的检索,2013 年至2023 年7 月,已公开发表催化氨制氢的文献约为356 篇,图1(a)是每年的发文量,图1(b)显示研究内容主要集中于催化剂、反应机理和反应器3 大方面.已报道的氨分解制氢方法主要有高温热解法、光催化、氨电解、等离子体法和研究最广泛的气-固两相催化反应.上述方法中,以氨制氢为目的的研究主要是气-固两相催化反应,其余方法则是理解合成氨和分解氨的反应机理.下面将对催化氨制氢的方法进行介绍.
1 催化氨分解反应机理
过去几十年,氨催化制氢的研究已取得长足发展.如图2 和图3(a) 中(1) 所示,氨的分解是一个3 步脱氢过程[5],首先,吸附的NH3分子经过N-H 键的断裂生成金属氮化物和吸附态的H[6],随后吸附的N 原子和H 原子重组解吸为N2和H2.由于合成氨和分解氨互为可逆反应,基于动力学的可逆性,大部分研究者认为合成氨和分解氨的活性金属催化剂应保持一致.但在不同工况下(比如氨浓度和压力等),具体的反应会发生较大变化.如图3(a)中(2)所示,在纯氨和稀氨低温(< 650 K)工况下,氨分解的反应速率决速步是N 原子的重组;而在稀氨高温(> 750 K)的工况下,反应的决速步变为N-H 键的断裂,因为金属氮化物的键能较高(高达500~630 kJ/mol).如图3(b)所示,氨分解的反应速率与N-H的键强有关,键强过强产物难以脱附,键强过弱反应物难以活化.根据反应工况的差异,合成氨和分解氨的反应压力也难以保持一致,这会直接影响到产物N2的吸附能

图2 NH3 在催化剂表面的吸附解离机理,蓝球、绿球和灰球分别代表N 原子、H 原子和催化剂原子[5]Fig.2 Representation of the general mechanism of ammonia adsorption and dissociation mechanism of NH3 on the catalyst surface,the blue,green and grey spheres represent N,H and the atoms of the catalysts,respectively[5]
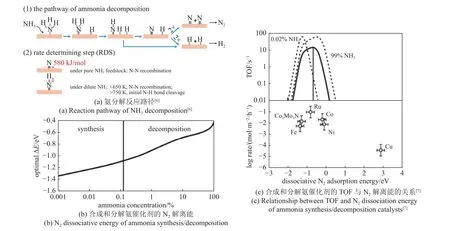
图3Fig.3
如图3(c)所示[7],金属与氮气之间的结合能呈火山型曲线,Ru 基催化剂接近于火山曲线的顶端,其合成氨和分解氨的反应活性均较高,其余氨分解催化剂则是铁系金属(Fe,Co,Ni)催化剂、过渡金属氮化物和碳化物催化剂等.研究者们通过实验和计算两方面对于氨分解活性金属进行研究.Ganley等[8]总结了13 种不同的金属催化剂氨分解活性,得出其活性顺序为: Ru > Ni > Rh > Co > Ir > Fe ≫ Pt >Cr > Pd > Cu ≫ Te,Se,Pb,这为氨分解的活性金属催化剂设计提供参考.Dasiveddy 等[9]对于氨分解反应进行机理研究和敏感性分析时,发现Ru,Co 和Ni 等金属与N 的脱附能变化符合理论计算的预测趋势,但Pd,Pt,Re,Mo 等与N 的脱附能预测结果相差较大,这说明不同金属基催化剂的氨分解反应决速步不同.根据火山型曲线分析,随着金属-氮(M-N)的键能增加,NH3中的N-H 键的断裂速率增加,但是生成产物N2的脱附速率降低.因此,探讨氨分解反应的活性最优金属,还与金属的分散度或速控步等多种因素相关.
2 Fe 基催化剂氨分解制氢研究
在合成氨工艺中,Fe 基催化剂是应用最为广泛的催化剂,Fe 基催化剂最早用于氨分解是去除热解煤制气所产生的氨气,并不是原位制氢.Fe 基催化剂分解氨的机理较复杂,因为在高温NH3气氛中,Fe 基催化剂会生成氮化铁(Fe2N,Fe3N 或Fe4N).而不同物相的Fe 基催化剂其催化活性也不同.
表1 列出了不同载体和催化活性的Fe 基金属催化剂,典型的Fe 基氨分解催化剂是碳纳米管为载体的Fe/CNTs 型催化剂,其氨分解的决速步是低温下N 原子的重组解吸和高温下N-H 键的解离.如图4和图5 所示,Ji 等[14]采用碳纳米纤维为Fe 基催化剂载体,通过改变碳纳米纤维的生长时间和氢的分压,调节其粒径、形貌和晶相.研究发现随着载体生长时间的延长和氢气分压的提高,其反应活性随之提高.制备所得Fe-CNFs/CMFs 催化剂同其他Fe 基催化剂相比,所表现出的氨分解活性最高.Yeo 等[20]使用密度泛函理论(DFT)研究了NH3在Fe(100)表面的逐步分解脱氢过程,比较了两种氨二聚体(2NH3)对局部吸附和氢键吸附的区别,发现NH3的局部吸附比氢键吸附更加稳定.此外,产物N2的重组和解吸具有极高的能垒,必须考虑NH3在N 覆盖的Fe表面的催化分解特性.如图6 所示,Fe 表面N 的覆盖改变了NH3分解的催化性能,而通过理论计算,同样证明Fe 基催化剂是一种有潜力的替代催化剂用于NH3分解制氢中.
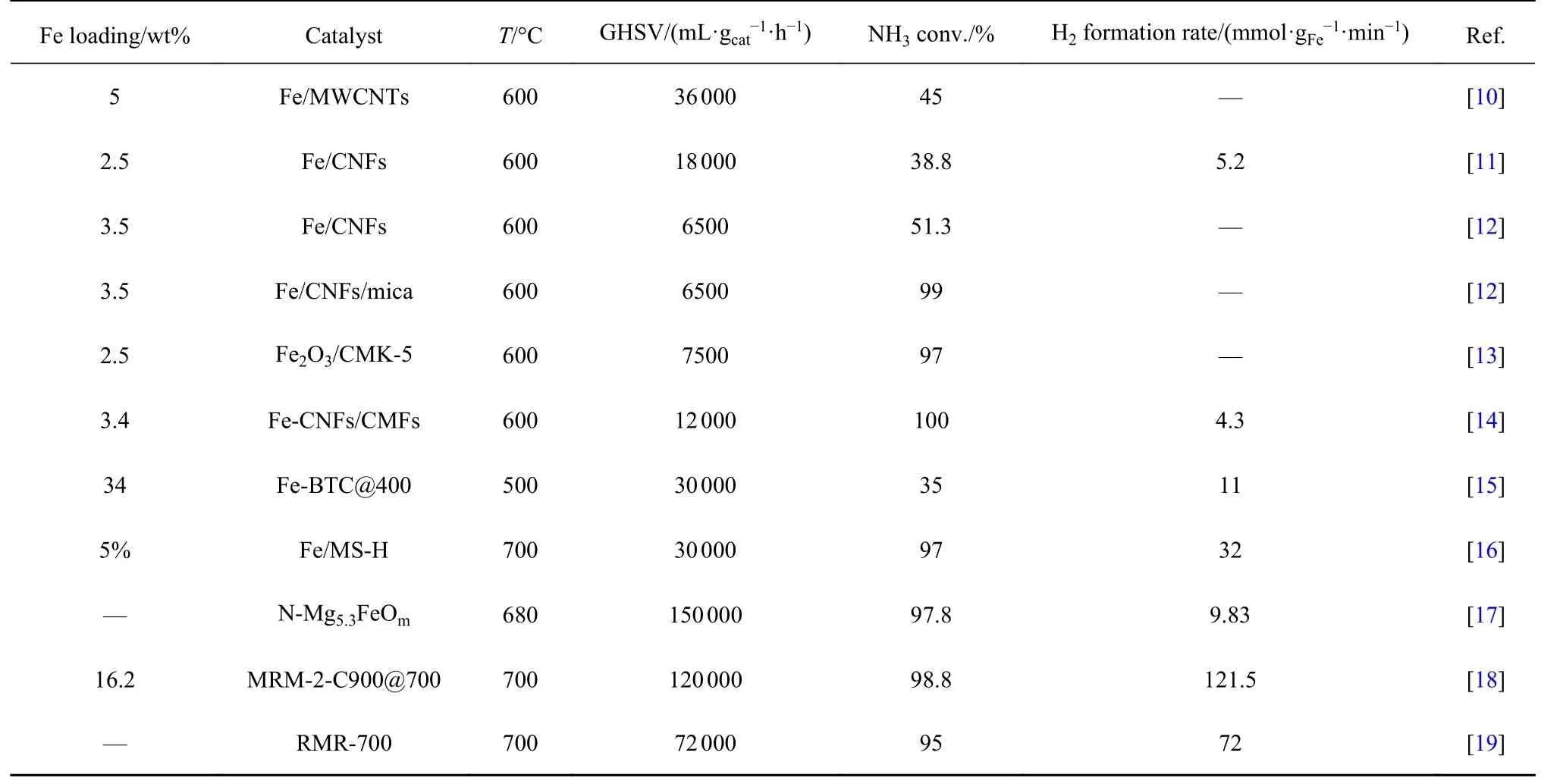
表1 Fe 基催化剂氨分解活性对比Table 1 The comparison of catalytic activity over Fe based catalysts for NH3 decomposition
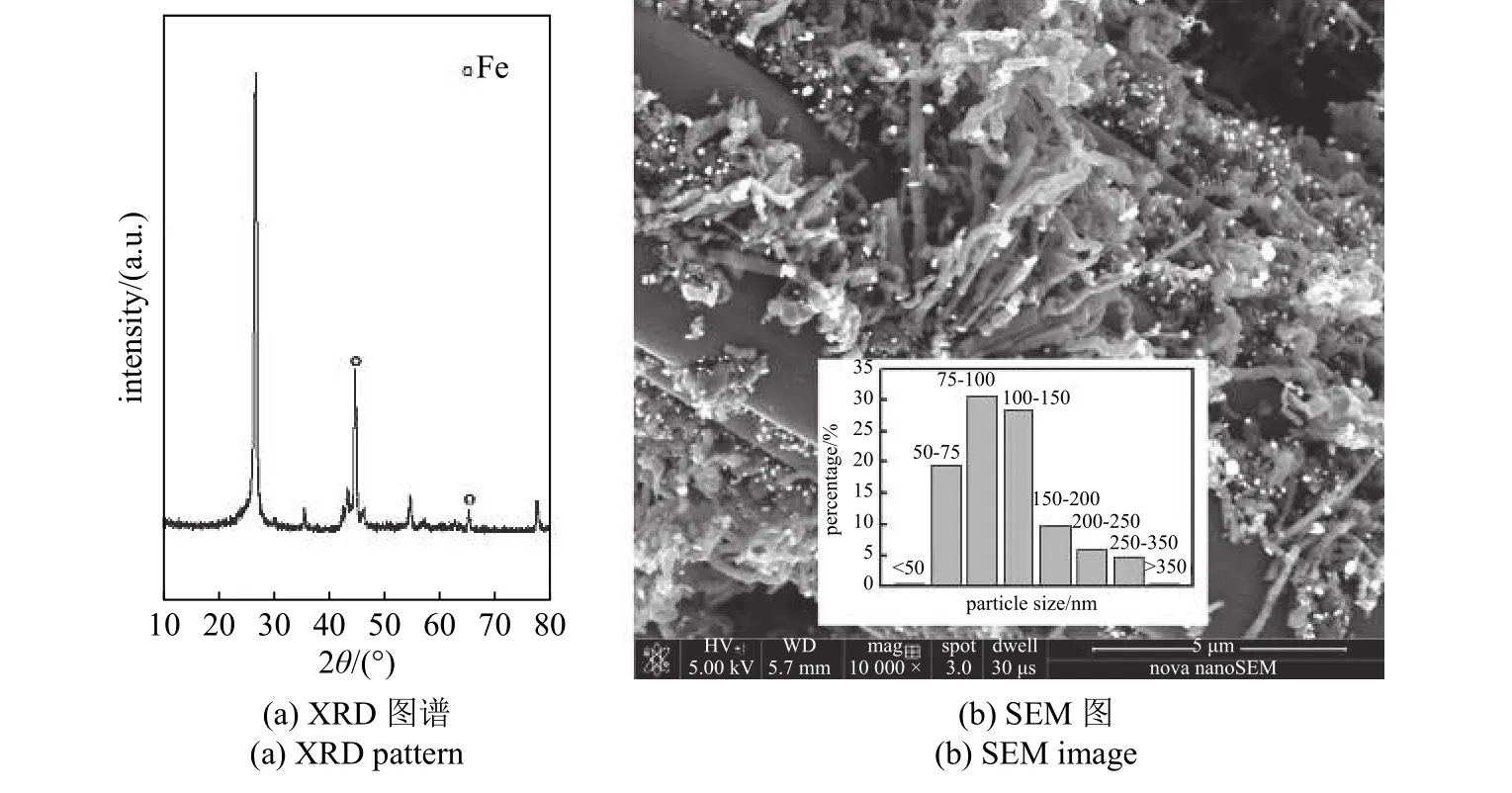
图4 Fe-CNFs/CMFs-5 催化剂的(a)XRD 图谱和(b)SEM 图[14]Fig.4 (a) XRD pattern and (b) SEM image of Fe-CNFs/CMFs-5 catalyst[14]
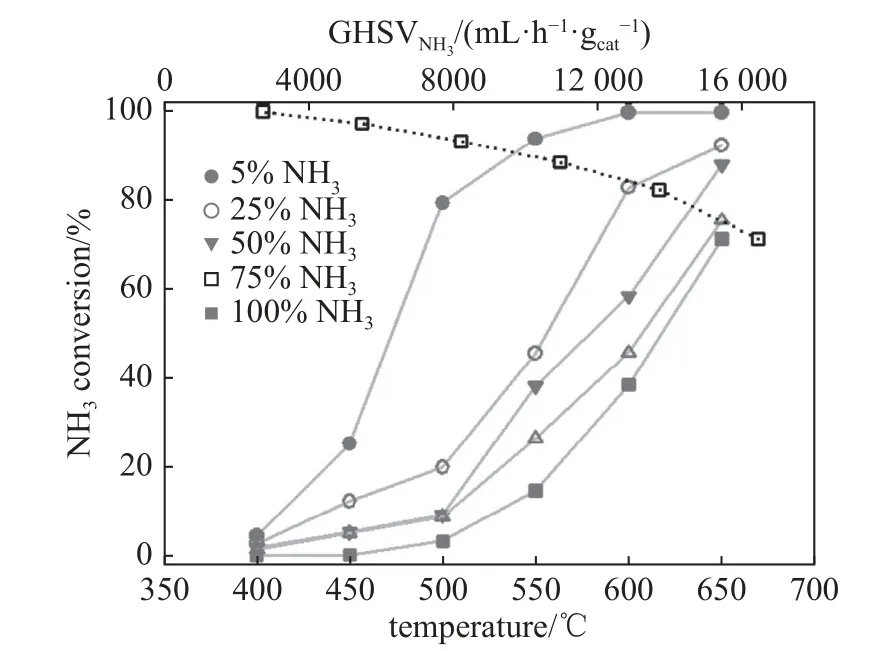
图5 Fe-CNFs/CMFs-3 催化剂的NH3 分解活性曲线[14]Fig.5 NH3 conversion of Fe-CNFs/CMFs-3 catalyst[14]
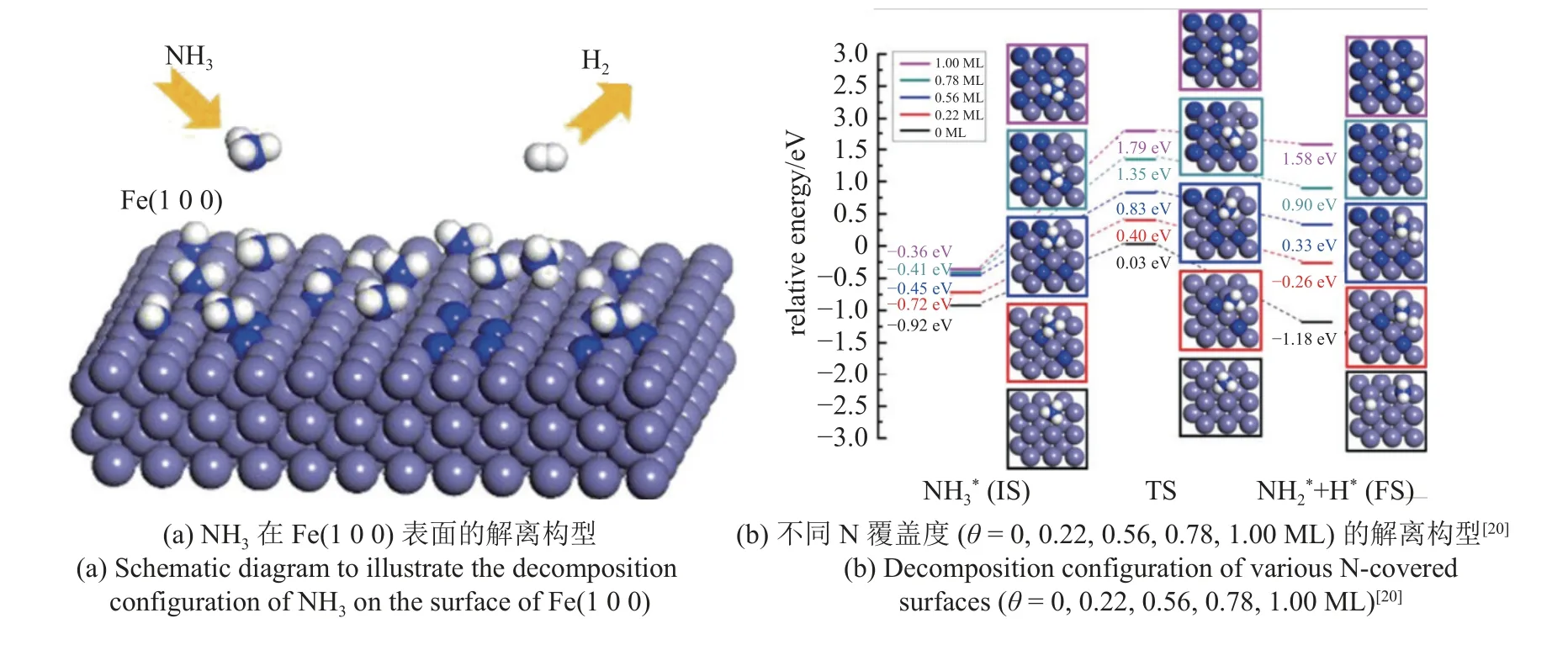
图6Fig.6
3 Co 基催化剂氨分解制氢研究
如表2 所示,铁系金属催化剂催化氨分解反应中,Co 基催化剂也得到广泛研究.Bell 等[29]使用Al2O3为载体,采用沉积沉淀法制备得到了Co/Al2O3型催化剂,当反应温度为500 °C 时,其 TOFH2=156.4 mmol·gCo-1·h-1,转化率约为55%.这说明起决定作用的是金属的种类、颗粒的大小和还原性的强弱,金属颗粒越小,催化剂与NH3接触的越充分,氨分解的催化活性也越高.如图7 所示,Huang 等[24]研究了催化剂的形貌对于Co 基催化剂的影响,制备得到的CeO2具有三维有序大孔(3DOM)、纳米管(NT)和纳米立方体(NC)的形貌,在工况为500 °C,6000 mL/(gcat·h)的空速下,其氢气生成速率顺序为:Co/CeO2-3DOM(4.2 mmol/(gcat·min)) > Co/CeO2-NC(3.5 mmol/(gcat·min)) > Co/CeO2-NT(3.2 mmol/(gcat·min)).Co/CeO2-3 DOM 的高活性归因于其较高的比表面积和更多的表面氧空位.Lara-Garcia 等[25]使用离子交换法将Co 纳米棒负载于钛酸盐的表面形成了钛酸钴.之后使用沉积沉淀法负载Co 颗粒获得较高的催化反应活性,因为钛酸盐纳米棒载体表面形成了可还原的纳米Co 小颗粒,使得反应速率与Co 颗粒的大小成反比.如图8 所示,Li 等[31]在氮气和空气气氛中分别煅烧了Co 纳米前驱体,得到了Co@C和CoOx@C 型催化剂用于氨分解反应,结果显示空气中煅烧的CoOx@C-700-A 比Co@C 的活性更高,在500 °C 时,NH3的转化率就达到了~ 55%(GHSV=15000 h-1).随着Co 颗粒尺寸的增大,催化活性逐渐降低.再一次证明了Co 基催化剂的氨分解反应速率与Co 颗粒大小成反比的关系.如图9 所示,Yu 等[27]研究了BaNH,CaNH 和Mg3N2对Co 基催化剂在NH3分解中的影响,H2生成速率依次为Co-BaNH >Co-CaNH > Co-Mg3N2≈ Co/CNTs.其中活性最高的Co-BaNH 催化剂在500 °C下的H2生成速率为20 mmol/(gcat·min),反应活性与同工况下的Ru/Al2O3(ca.17 mmol/(gcat·min)) 和Ru/AC(ca.21 mmol/(gcat·min))相当.而与同类Co 基催化剂相比,Co-BaNH 的催化活性最高,表征结果显示Co 与BaNH 的界面形成了类似[Co-N-Ba]的中间态物种,比纯Co 金属催化剂的NH3分解活性更高.
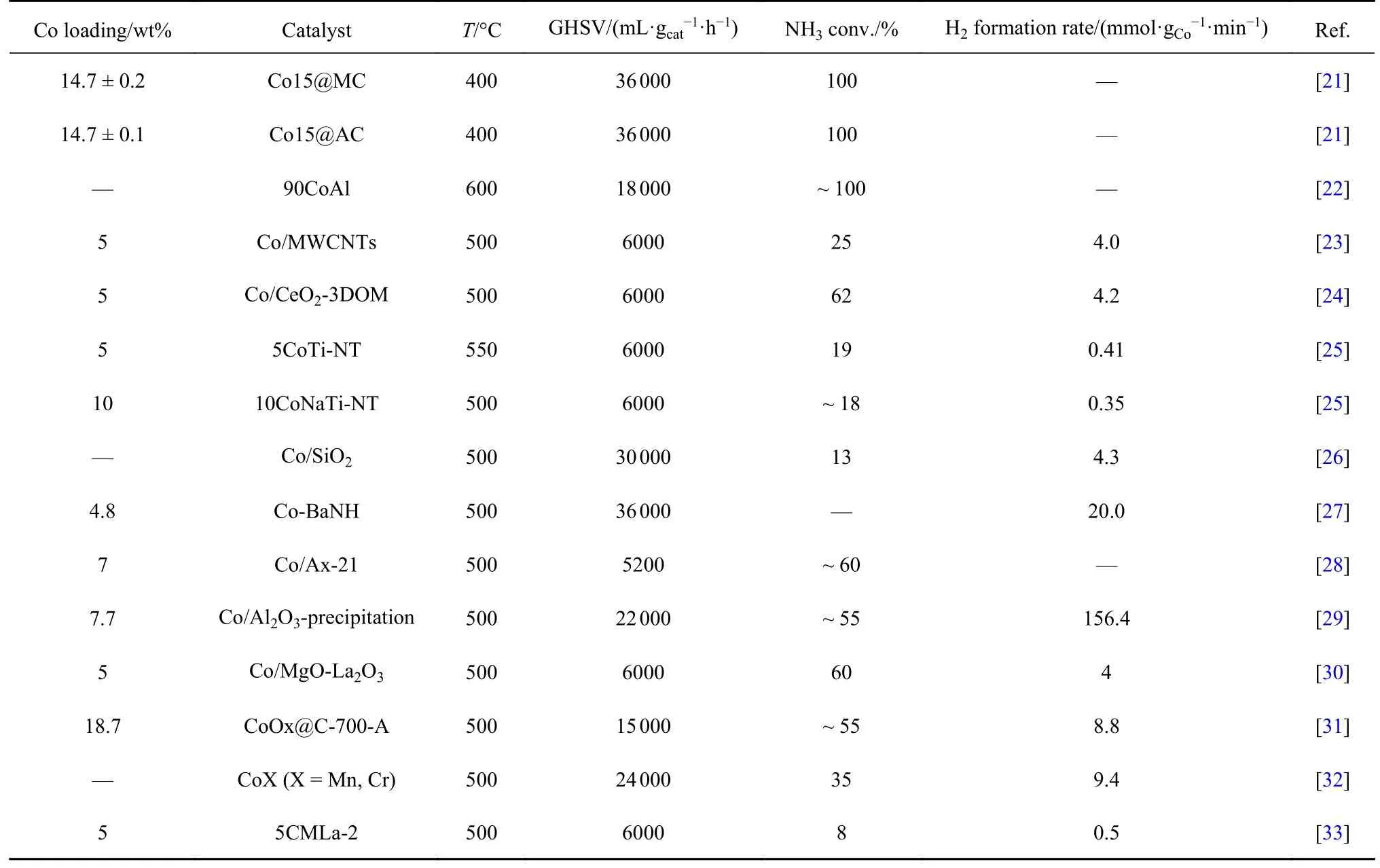
表2 Co 基催化剂氨分解活性对比Table 2 The comparison of catalytic activity over Co based catalysts for NH3 decomposition

图7Fig.7

图8Fig.8
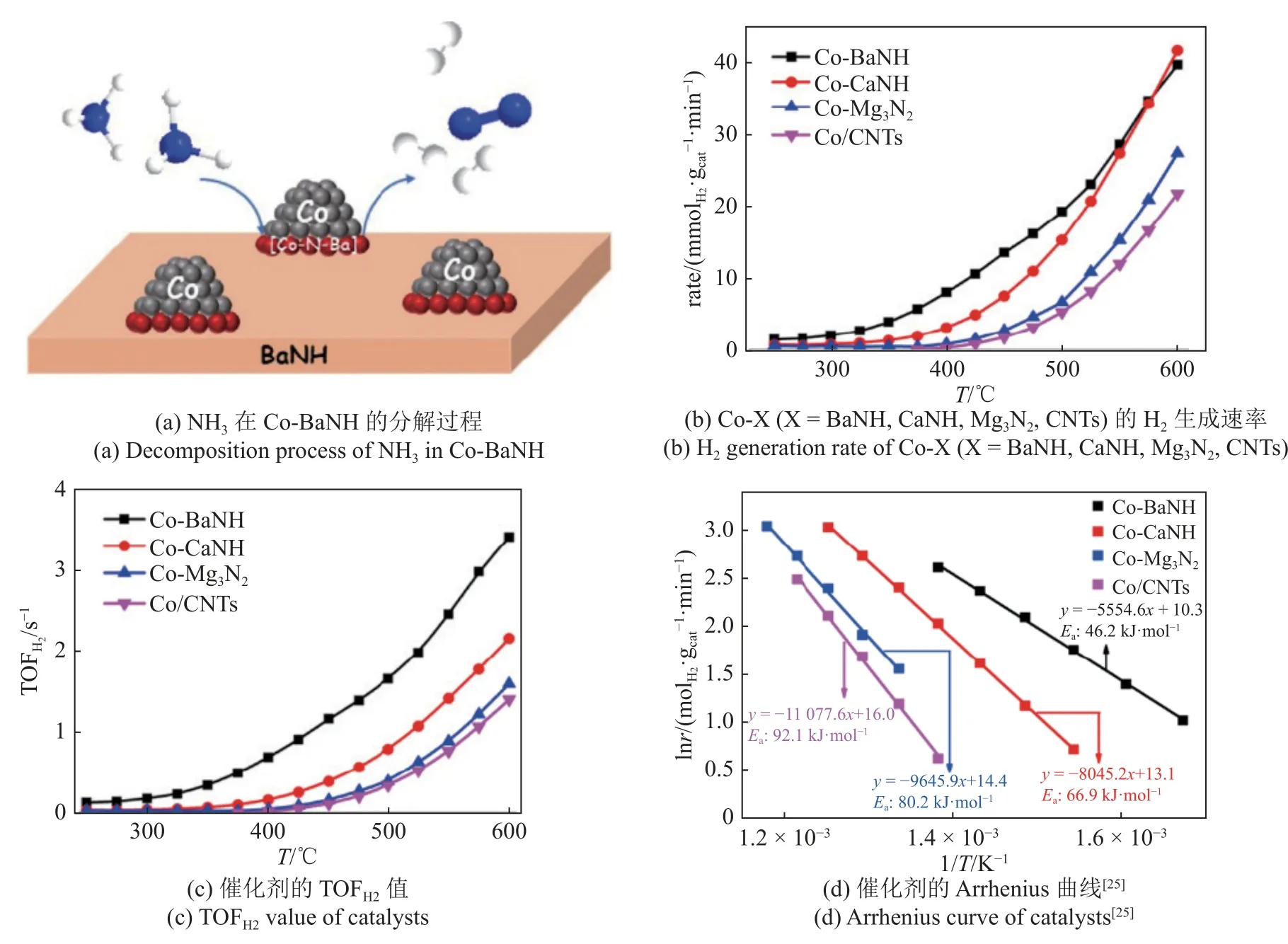
图9Fig.9
4 Ni 基催化剂氨分解制氢研究
铁系金属催化剂催化氨分解反应中,Ni 基催化剂最受欢迎,其催化活性高于Fe 基和Co 基,而成本又远低于Ru 基,具有极为广阔的应用前景.表3 列出了不同载体和催化活性的Ni 基金属催化剂,Takahashi等[46]从动力学角度分别研究了Ru 基和Ni 基催化剂氨分解反应的决速步,N 原子的重组脱附是Ru 基催化剂的决速步而N-H 键的断裂是Ni 基催化剂的决速步.目前,对于Ni 基催化剂的设计和制备主要集中于Ni 颗粒的分散度、形貌、载体、合金和助剂等方面.
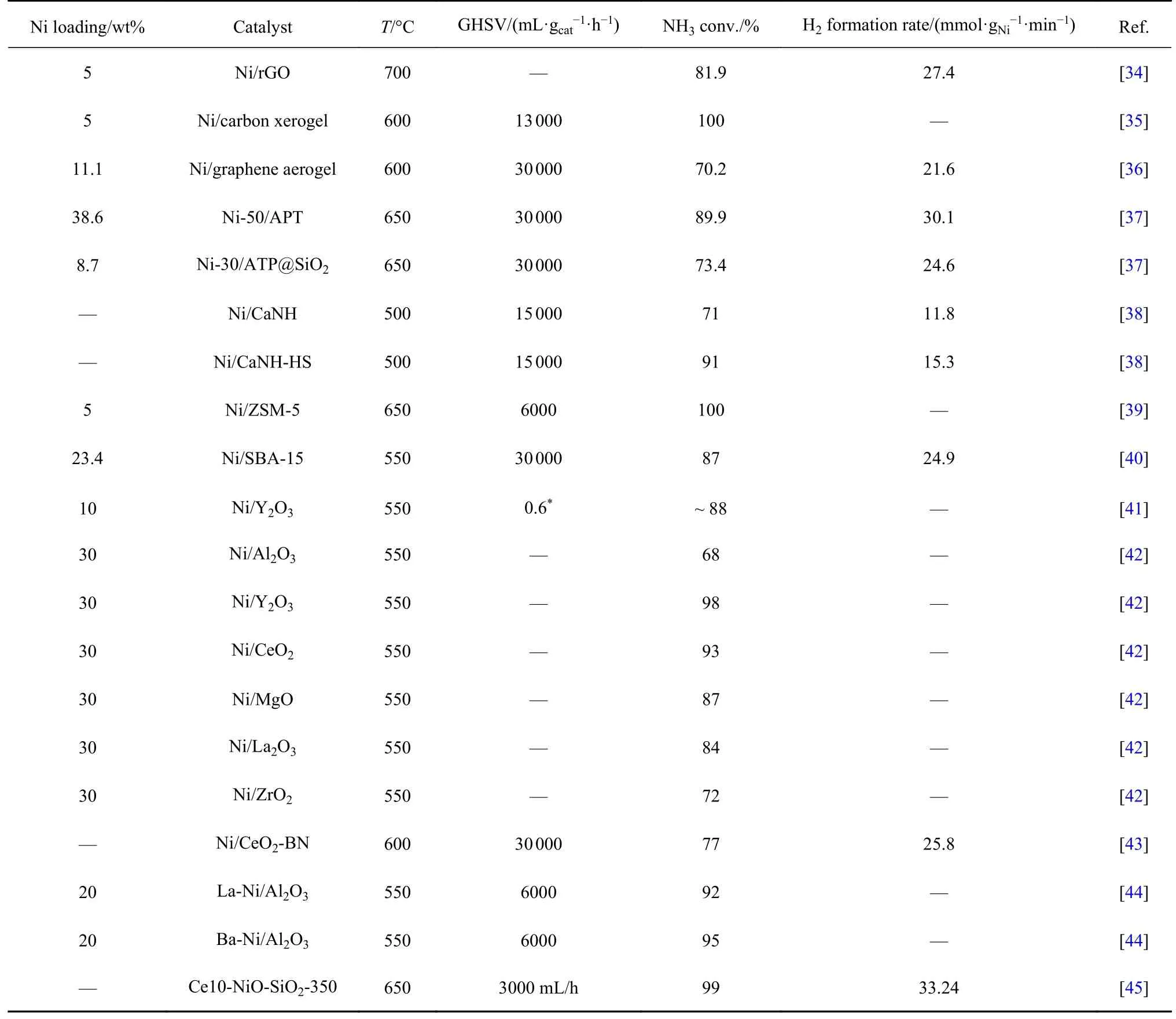
表3 Ni 基催化剂氨分解活性对比Table 3 The comparison of catalytic activity over Ni based catalysts for NH3 decomposition
如图10 所示,Zhang 等[47]研究了Ni0颗粒的尺寸对于NH3分解的影响,稳态动力学结果显示随着Ni 颗粒粒径的减小,其转化频率TOF 值先增大后减小,当Ni0颗粒为1.8~ 2.9 nm 时,所制备Ni/Al2O3催化剂的反应频率最高,说明Ni 基催化剂具有显著的颗粒尺寸敏感性.而La 的掺杂进一步降低了Ni0的粒径,提高了Ni 基催化剂的反应活性.Chen[48]则通过理论计算,构建了不同八面体尺寸的Ni 基小团簇(Ni19,Ni44,Ni85和Ni146),从动力学角度研究NH3分解纳米颗粒的尺寸效应.基于NH3的吸附能结果预测其催化活性顺序为: Ni44> Ni146≈ Ni85>Ni19.分子动力学结果表明,Ni146不仅催化活性好,而且稳定性较高.通过电荷结构分析表明,带负电荷的Mulliken 电荷作为活性中心,更有利于吸附N.如图11 所示,对于Ni 基载体,文献[44,49]分别制备了Ni 颗粒负载于不同碱性金属的铝酸盐载体Ni/MAl-O (M=Mg,Ca,Sr,Ba),随着催化剂的碱度增加(Mg < Ca < Sr < Ba),H2吸附逐渐减弱,NH3的分解性能随之提高.除金属氧化物Al2O3[50-51]外(图12),CeO2[43,52-54],Y2O3[41,55],La2O3[56]等也被作为Ni 基催化剂载体用于氨的分解反应.Nakamura等[42]着重讨论了Ni 负载Y2O3,CeO2,MgO,La2O3和Al2O3催化剂的NH3分解性能,发现Ni/Y2O3的反应活性最高,金属Ni 负载于上述载体所表现出的不同活性主要源于不同载体的SMSI 效应,Ni 颗粒的高分散性以及载体表面的氧空穴.
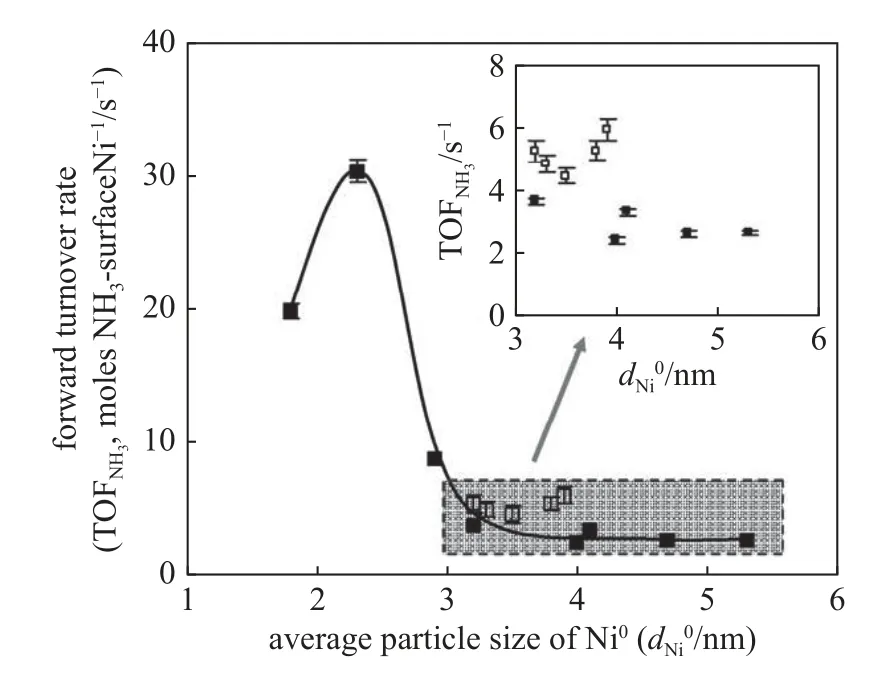
图10 Ni0 粒径与NH3 分解的转化频率(TOFNH3)关系(Ni/Al2O3(实心)和Ni/La-Al2O3(空心))[47]Fig.10 The relationship between Ni0 particle size and the NH3 turnover rate (TOFNH3) (solids: Ni/Al2O3;hollows: Ni/La-Al2O3)[47]
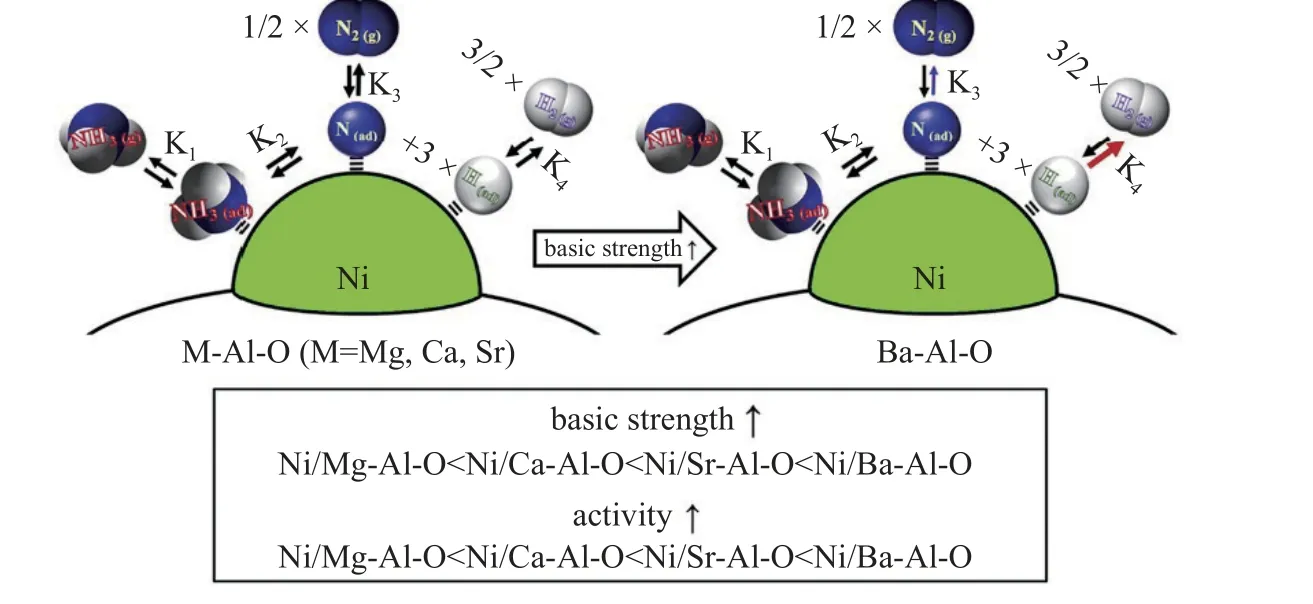
图11 Ni/M-Al-O (M=Mg,Ca,Sr,Ba)催化剂碱性性质与NH3 分解的活性关系[44]Fig.11 The relationship between alkaline properties of Ni/M-Al-O (M=Mg,Ca,Sr,Ba) catalyst and NH3 decomposition activity[44]

图12 Ni 颗粒负载在Al2O3 载体上(Ni@Al2O3)有效催化氨分解[50]Fig.12 Ni particles supported onto porous alumina matrix (Ni@Al2O3)used to effectively catalyze ammonia decomposition[50]
5 双金属多金属催化剂氨分解制氢研究
为了克服单一金属催化剂催化NH3分解的局限性,大量研究人员致力于开发双金属多金属催化剂用以催化氨分解制氢.这些催化剂具有成本低,催化性能好,热稳定性高等优势.如图3(c)所示,NH3分解火山曲线的峰值对应于最佳M-N 结合能(561 kJ/mol),贵金属Ru 与N 的结合能约为594 kJ/mol,与火山曲线峰值最接近.而其他铁系金属F e(620 k J/m o l),C o(523 k J/m o l),Ni(511 kJ/mol)和Mo(645 kJ/mol)活性较差的原因是M-N 结合能与火山曲线峰值相差较大.因此理论上讲,设计二元或多元金属催化剂使其与N 的结合能处于火山曲线峰值附近得到最佳的M-N 结合能,有利于促进NH3的分解和转化.
目前氨分解的多金属催化剂主要是二元金属催化剂.常见的二元铁系金属催化剂主要有Fe-Co[12,57-59],Fe-Ni[58,60-62],Co-Ni[58,61,63-65],Ru-Ni[40-41,66-67]和Co-Mo[68-74]等.Yi 等[60]制备了Mo-Ni,Fe-Co,Mo-Co 和Fe-Ni 4 种催化剂,6Fe-4Ni 的氨分解活性最高,原因是其NH3的吸附能力最强.如表4 所示,Wang 等[85]制备了不同形貌的NiCo2N 催化剂并研究其在析氢反应和电催化氨分解中的催化活性,发现泡沫镍负载的NiCo 纳米针的反应活性最高,其优点主要是较大的比表面积、暴露更多的活性位点、增加的电荷转移和较强的气体扩散能力.如图13 所示,Tabassum 等[65]制备了CoNi 合金负载于氧化物载体MgO-CeO2-SrO 上,经过助剂K 促进后,CoNi 合金分散良好,得到的K-CoNialloy-MgO-CeO2-SrO 在450 °C,6000 mL/(gcat·h)的工况下,实现了97.7%的转化率.结果表明CoNi 合金与氧化物载体界面上的活性位点促进了N 原子的吸附重组,使得氨分解的活化能显著降低,加速了反应发生.因此,两种金属合金化可以诱导协同效应以调节金属的局部结构.
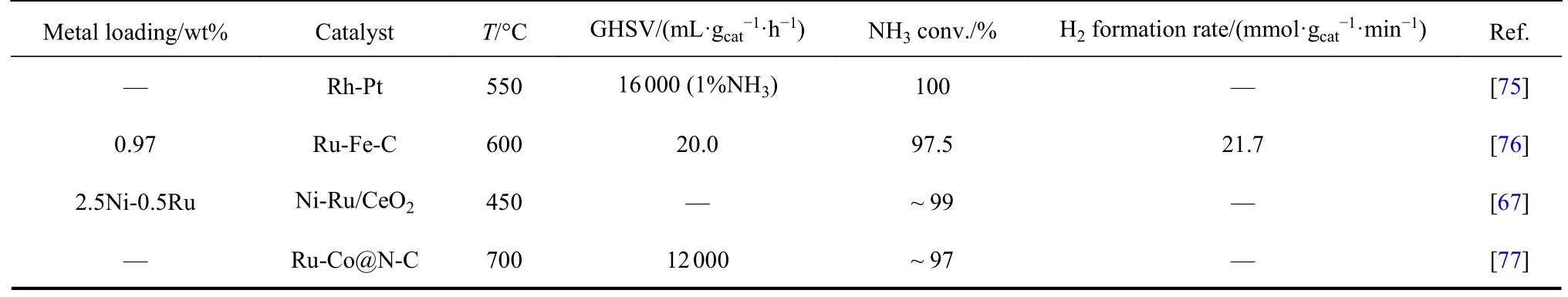
表4 多组分金属催化剂氨分解活性对比Table 4 The comparison of catalytic activity over multi-component-based catalysts for NH3 decomposition

图13 MgO-CeO2-SrO 氧化物载体上修饰的CoNi 合金[65]Fig.13 Schematic illustration for the decorated CoNialloy on the oxide support of MgO-CeO2-SrO[65]
21 世纪初,高熵合金(high-entropy alloys,HEAs)的概念被提出,HEAs 是由5 种或5 种以上的元素组成的多金属纳米颗粒,元素成分相对较大,它们经常表现出独特的性能.如图14 所示,Xie 等[73]成功制备出新型CoMoFeNiCu HEAs 用于催化NH3分解反应,所得HEAs 表现出较强的NH3分解活性和稳定性,与贵金属Ru 基催化剂相比,CoMoFeNi-Cu HEAs 的成本更低,而氨分解活性提升了20%,在500 °C 下,即可实现NH3的完全转化.通过调控非互溶二元金属CoMo 比例优化HEAs 的表面吸附性质,可在不同工况下优化反应活性,显示出HEAs在氨分解反应中的巨大应用潜力.

图14Fig.14
6 Fe,Co 和Ni 基催化剂结合等离子体氨分解研究
虽然Fe,Co 和Ni 基催化剂成本较低,但其催化氨分解的转化效率远远低于Ru 基.通过引入等离子体,可以提高铁系金属催化剂氨分解的反应活性.等离子体是一种由电子、离子、基态分子或原子、激发态分子或原子及自由基等多种活性粒子组成的电离化气态物质,由于正电荷粒子和负电荷电子等量分布其中,因而从整体上看等离子体呈电中性.
根据放电方式的不同,产生非平衡等离子体的放电技术主要有电晕放电、辉光放电和介质阻挡放电等.电晕放电可以在常压和电压较大的情况下进行,利用电极的不对称性形成曲率半径极小的强电场,从而使气体介质发生强烈的电离和激发,形成具有明显亮光的电晕层,放电声音也比其他形式更大.这种存在于不均匀电场中的局部自持放电现象相对稳定,但是难以获得大量的等离子体.辉光放电的工作电压通常很低(小于10 mbar),是一种低压放电形式,因此产生的电子能量也较低.通过将两个平行电极板放置在一个密闭容器中,中性分子便可以在与电子进行非弹性碰撞的过程中被激发,而辉光则是这些激发态组分返回基态时释放出的能量表现形式.辉光放电是目前低温等离子体研究中的一种重要放电形式,但由于受到低气压的限制,无法在工业生产中广泛应用.介质阻挡放电是在两个距离相对较近的放电电极之间充满气体,并将其中一个(单层介质阻挡)或两个电极(双层介质阻挡)用绝缘介质覆盖,或将绝缘介质直接插入放电空间,当正负电极上施加足够电压时,定向移动的电子便会获得足够高的能量与气体介质进行碰撞发生电离和离解,从而形成较强的放电通道.这种电极的布置形式为介质阻挡放电(dielectric barrier discharge,DBD)结构.介质阻挡放电属于无声放电,通常可以满足高气压(104~ 106)和宽频率范围(50~ 1 × 106MHz)的工作要求.另外,相比于无绝缘介质阻挡的电晕放电结构,介质阻挡放电使电源能量分布均匀,避免产生电弧,在放电空间内形成大量随机分布的放电细丝.综上,介质阻挡放电不但具有结构简单、无需高精设备的优点,而且便于产生高能量、高密度和大流量的非平衡等离子体,方便在较大空间内操作.
等离子体催化反应是等离子体化学的一个分支,它是指在等离子体的放电区域填入催化剂,催化剂的引入可以提高目标反应的转化率和选择性[86].等离子体催化具有响应速度快、实验设备简单和无需外热源加热等优点.催化剂与等离子体的协同效应主要体现在两个方面: 对于等离子体,催化剂的引入可以改变放电区域的放电特征与电场强度,进而改变目标反应的进程和路径,提高等离子体的能量效率,加速化学反应发生;而对催化剂,等离子体的引入可以改变催化剂的理化性质,同时会使反应气氛中生成更多的活性物种(激发态物种、自由基或离子),克服活化能垒,降低反应活化能,加速反应进行.总之,等离子体催化反应会使常规下难以活化的分子或不易实现的化学反应在等离子体的辅助下得以实现.
等离子体辅助催化氨分解的工作列于表5 中.最先研究等离子体辅助催化氨制氢的是大连理工大学的郭洪臣教授课题组.他们课题组的Wang 等[87]首先采用Fe 基催化剂进行等离子体辅助催化NH3分解实验.在没有等离子体参与的工况下,NH3分解后强吸附的N 原子抑制了NH3分解的反应速率;而加入等离子体后,氨的转化率由7.8%提高至99.9%.通过15NH3的同位素示踪和发射光谱(OES)研究了电子激发态(NH3*,NH2*,NH*,N*和H*)在等离子体和催化剂协同分解NH3的作用.结果表明,与基态NH3相比,NH3*吸附在了催化剂的表面,具有更高的吸附容量和更强的吸附强度.因此,被激发的NH3表面吸附物种被认为是等离子体与非均相催化剂协同反应的另一重要作用.如图15 所示,Wang 等[88]继续研究催化剂载体(fumed SiO2,SiO2-ball,TS-1 nm,TS-1 μm,r’-Al3O2,HZSM-5,NaZSM-5 和TiO2)负载廉价金属催化剂对于等离子体辅助NH3分解的影响.结果证实了M-N 强度和载体的介电常数(εd)对催化剂和等离子体的协同作用会产生较大影响.当Fe,Co,Ni 和Cu 负载于SiO2载体上时,M-N 的强度顺序为: Cu-N < Ni-N < Co-N < Fe-N,其中Co/fumed SiO2与等离子体的协同作用更强,等离子体辅助催化NH3分解的效率更高.εd较小的fumed SiO2,SiO2-ball 和r’-Al3O2负载的Co 基催化剂与等离子体的协同作用更强,转化率更高.这项工作直接证明了制备材料的εd是等离子体催化的重要参数,而M-N 的键能是廉价金属催化剂催化NH3分解的决速步骤.2019 年,Wang 等[89]采用等离子体煅烧技术对传统的Co/fumed SiO2催化剂进行改进.等离子体处理后催化剂的Co 物种分散度增加,金属Co 与载体之间的SMSI 效应增强,催化剂的酸性增强.处理后的Co/fumed SiO2的NH3转化率较处理前提高了47%,制氢效率由2.3 mol/(kW·h)提高至5.7 mol/(kW·h).说明等离子体煅烧是一种有效提升催化活性的方法.如图16 所示,除研究等离子体辅助单金属催化氨分解外,Fu 等[60]同时制备了Ni-Mo,Co-Mo,Fe-Co 和Fe-Ni 4 种双金属催化剂与10Ni,10Fe,10Mo 和10Co 单金属催化剂进行氨分解的活性对比,6 Fe-4 Ni 表现出最高的反应活性和与等离子体的协同能力,在500 °C 时实现了NH3的完全转化,产氢速率和产氢能耗分别达到了0.96 mol/(g·h)和0.05 kW·h/(mol·g-1),6Fe-4Ni 催化剂表现出较好的热稳定性,连续工作200 h 不失活.经过OES 测试,NH3被等离子体活化为激发态(NH3,˙NH2,˙NH),而6 Fe-4 Ni 催化剂对于激发态的NH3,˙NH2,˙NH 吸附能力最强,这是其活性最高的根本原因.如图17 所示,Gao 等[58]采用氧化铈纳米球(CeO2-S)为载体,制备了铁系金属(Fe,Co 和Ni)单/双掺杂的氧化铈基催化剂用于等离子体辅助NH3分解反应.FeCo/CeO2-S 的氨转化效率最高,在36000 mL/(gcat·h)的空速下,其在550 °C 下实现了NH3的完全转化,而在500 °C 下的H2生成速率最高,为29.3 mmol/(gcat·min).催化剂高活性的原因是FeCo 之间适中的M-N 结合能、CeO2纳米球较大的比表面积以及掺杂后CeO2基催化剂增加的氧空位.
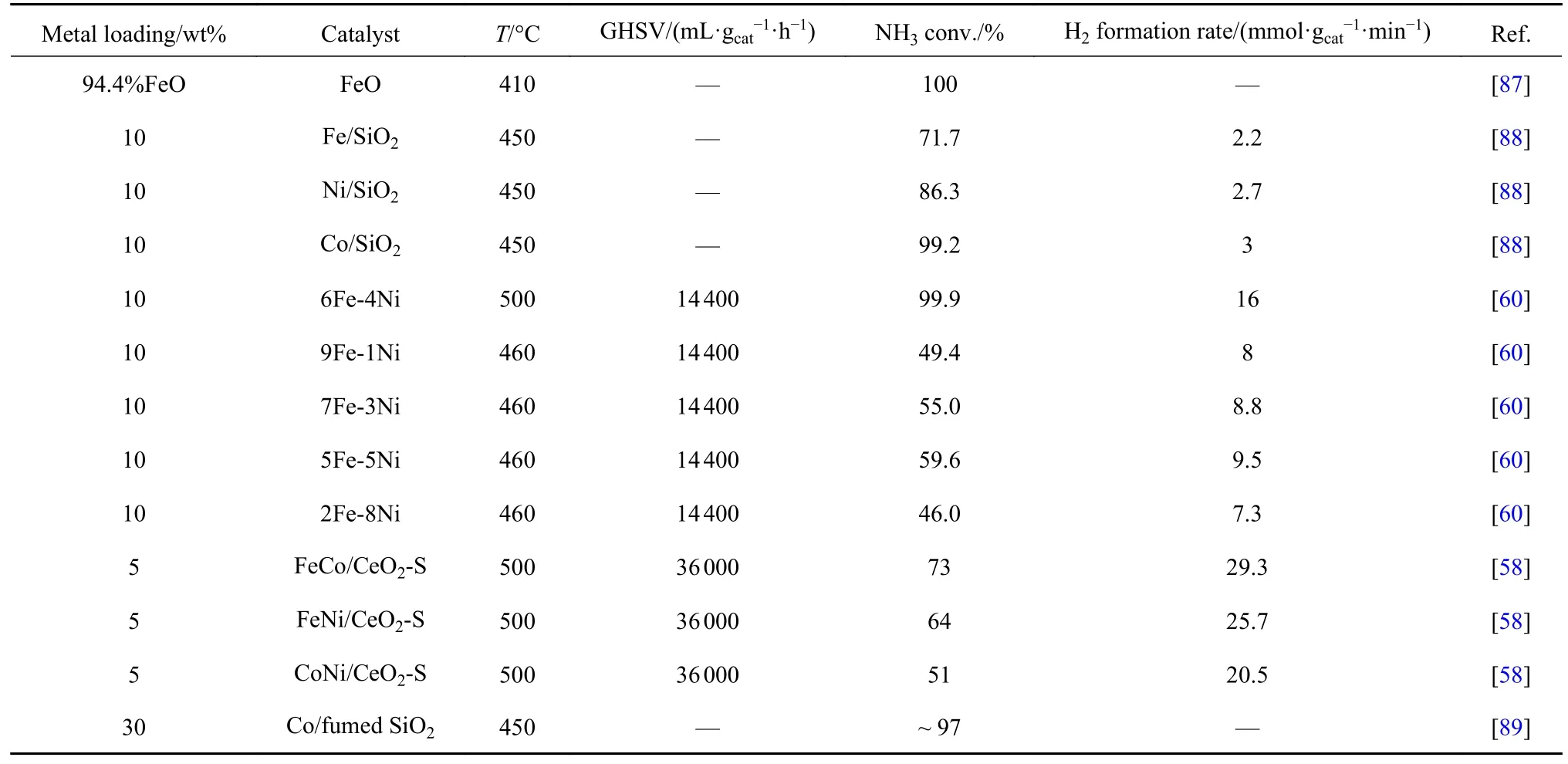
表5 等离子体辅助过渡金属基催化剂氨分解活性对比Table 5 Comparison of ammonia decomposition activity of plasma-assisted transition metal-based catalysts

图15Fig.15
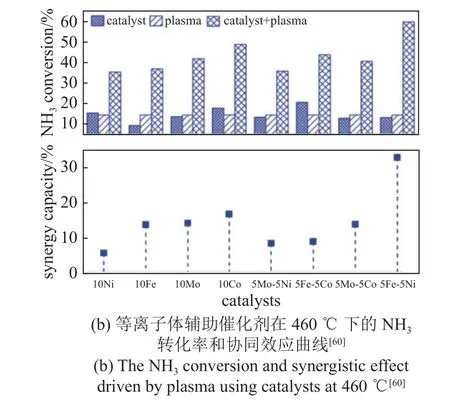
图16Fig.16

图17Fig.17
7 结语和展望
氨作为一种零碳氢载体,从热力学角度分析,在相对较低的400 °C 下,NH3的转化率就可达到99%;但NH3的分解动力学依旧缓慢,这一问题制约了NH3在实际储氢工业中的应用和发展.低温低压下,Ru 被认为是氨分解制氢活性最高的金属,但贵金属Ru 储量少,成本高,极大限制了其工业化的应用.铁系金属(Fe,Co 和Ni)与Ru 基金属催化剂相比具有明显的价格优势,通过精准调控金属颗粒的大小、载体、复合材料结构、促进剂和合金效应等特征,可以增加材料的比表面积、提高金属位点的分散度、稳定性和导电性等性质,进而提高氨分解的转化效率.目前所用氨分解催化剂载体主要包括碳基材料(CNTs,CNFs,CMK-5 和rGO 等)、金属氧化物(Al2O3,SiO2,CeO2,Y2O3和MgO 等)、分子筛(ZSM-5,SBA-15 和TS-1)等.对于铁系金属Fe,Co和Ni 而言,第二金属和助剂的加入可诱导电子性质发生变化,稳定金属粒子团聚、抑制催化剂中毒,最大限度地提升原子的利用率,从而提高催化剂氨分解的反应效率.而金属类型、成分和多金属的相互作用(核壳、合金和异质结等)等因素也为设计新的催化剂体系,预测和调节M-N 结合能,提供了无限可能.
等离子体辅助催化氨分解反应,在等离子体高压高频电场中引入铁系金属催化剂,将等离子体技术与铁系金属催化剂有效耦合以提高氨分解的转化率和选择性.等离子体辅助催化技术具有响应速度快、目标产物选择性高和能量转换效率高的特点.对于等离子体而言,催化剂的引入可以改变放电区域的放电特征与电场强度,进而改变目标反应的进程和路径,提高等离子体的能量效率,加速化学反应的发生;而对于铁系金属催化剂而言,等离子体的引入可以改变铁系金属催化剂功函数等理化性质,使NH3中生成更多的活性自由基(NH3*,NH2*,NH*,N*和H*),克服活化能垒,降低反应活化能,加速反应进行,提高制氢能量效率.
为了进一步提高NH3分解的转化效率和等离子体辅助催化氨制氢的低温活性,主要从铁系金属催化剂和等离子体两方面进行展望.
(1)深入理解NH3分解的反应机理,NH3分解的反应路径需要经过多次电子转移,NH3在不同金属表面的吸附和脱附过程不同,因此不同金属之间NH3分解的决速步也不同,通过理论计算(CFD 或DFT)与实验结合的方式对于揭示NH3分解的复杂机制至关重要,也将为设计更具潜力的氨分解催化剂提供理论指导.
(2)新型氨分解催化剂的开发,目前氨分解催化剂的失活会发生在高温高压下,需要对金属活性组分,载体和助剂进行调节和整合,以获得高活性、高选择性、高热稳定性、可回收和低成本的催化剂,以供实际使用.催化剂目前只是在实验室理想条件下测试,对于其是否可以产业化运用尚且存疑,这对催化剂的抗毒性和耐久性都提出了较高要求.
(3)等离子体在催化氨分解中处于辅助角色,但等离子体的放电方式、放电类型和放电参数会直接影响催化剂的放电效果,进而影响催化剂的反应活性.在等离子体参与反应的条件下,需要进一步优化放电效果,降低反应能耗,提高综合效率,促进更多NH3分子在催化剂表面进行吸附和活化.
(4)从基础研究的角度发现等离子体协同催化具有与传统热催化不一致的现象和规律,等离子体协同耦合催化的作用机理也尚不清晰,后期需要采用VASP,Chemkin,ZD-Plaskin 和BOLSIG+等工具对于等离子体辅助氨分解过程中的反应路径和速控步骤进行反应动力学研究,揭示氨分解催化剂的结构敏感性根源,以便加快推动氨氢的实际应用.

