等离子体电化学法制备金、银纳米颗粒与碳量子点的研究进展及关键问题1)
马雨彭雪 王若愚 秦晓茹 张 卿 陈 强 钟晓霞 ,
* (上海交通大学物理与天文学院,区域光通信网与新型光纤通信系统国家重点实验室,激光等离子体教育部重点实验室,上海 200240)
† (厦门大学电磁声学研究院,福建省等离子体与磁共振重点实验室,福建省电子设计自动化工程研究中心,电磁波科学与探测技术福建省高校重点实验室,厦门市电子信息多物理场重点实验室,福建厦门 361005)
引言
金、银纳米颗粒和碳量子点因其不同于宏观材料的独特物理与化学性质,而被广泛关注.当颗粒尺寸进入nm 量级时,将引起量子尺寸效应、量子限域效应、宏观量子隧道效应和介电限域效应等,使得金、银纳米颗粒和碳量子点在非线性光学、催化、生物医学和光电子器件等领域具有广阔的应用前景.但是常见的合成金、银纳米颗粒的方法,例如纯化学还原法,往往需要添加额外的还原剂,并且通常涉及多步骤过程.类似地,对于碳量子点的制备,大多在密闭的反应空间,需要高温(200 °C~ 300 °C)、高压(~ 6 MPa)、长时间(6~ 10 h)的反应条件,反应过程存在高能量消耗等问题.因此,需要寻找更加环保、快捷和高效的替代方法来制备金、银纳米颗粒和碳量子点.
大气压低温等离子体具有电子密度高(1013~1015cm-3)、电子温度可达到几个eV,且无需真空(可在大气压环境下稳定放电)等特点.若将含有荷电、荷能及反应活性组分(包括电子、离子和各种中性反应活性原子、基团等)的放电等离子体代替传统电化学系统中的一个或两个固体电极,就可形成一个等离子体电化学反应系统.等离子体电化学系统具有高反应活性的等离子体-液体界面,具有多种实际应用.等离子体电化学法合成纳米材料技术即是其近年发展起来的众多应用之一,该方法耗能低、环境友好,是一种特殊的绿色合成技术.其主要原理是利用等离子体内荷电、荷能反应活性组分在等离子体-液体界面形成电荷和各种活性成分的转移,将等离子体的反应活性传递给前驱体,不需要使用其他化学试剂,即可快速合成金、银、金银合金和碳量子点等纳米颗粒[1-5].同时,等离子体放电气体的组分(如氮气、氧气、氩气等)、放电方式(如直流、交流、脉冲等)以及溶液的组分等提供了较大的反应参数空间,这使得可从溶液及等离子体两个方面来有效调控纳米材料的制备过程.
当前,对等离子体电化学法合成纳米材料已有相关的文章进行了综述[6],但对金、银纳米颗粒与碳量子点的等离子体电化学法制备仍缺乏相关的综述,因此本文通过调研国内外相关文献,介绍了等离子体电化学系统的原理,并对近年来基于等离子体电化学反应的金、银纳米颗粒和碳量子点的合成进行综述,对其研究进展及关键问题进行阐述.
1 等离子体电化学
等离子体是以自由电子和带电离子为主要成分的一种物质状态,广泛存在于宇宙中,常被视作除固体、液体和气体以外物质的第4 种状态.人们在自然界和日常生活中经常遇到的火和闪电就是两种常见的等离子体.等离子体中含有自由电子、正离子、多种反应性成分并具有独特的光学和电学性质,因此无论在基础研究还是工业应用领域都有着极其重要的地位.
由于等离子体含有荷能及荷电粒子,当其与溶液接触时,在气-液界面会产生物质能电荷的转移,引发一系列物理和化学过程[7-9].另外,在气-液界面也会发生类似于传统电化学中固体电极和电解质之间的电化学过程.为了区别于传统电化学,等离子体引起的电化学反应通常被称作等离子体电化学[10-14].在等离子体-液体界面发生的这些物理、化学及电化学过程会将气相等离子体的反应活性转变为液体的反应活性,从而使得等离子体-溶液系统可作为一个多相反应器,在众多领域具有极其广阔的应用前景.
在传统电化学反应中,电荷转移发生于固相和液相之间,而等离子体电化学与此不同,电荷转移发生于气相等离子体和液相电解质之间.因此等离子体电化学具有许多不同于传统电化学的特点,例如在界面处,除了电荷转移,还存在许多的物理和化学过程,如溅射、蒸发等,因而也使得在等离子体电化学反应中,界面间的电荷转移通常偏离法拉第电解定律.
虽然美国科学家欧文·朗缪尔(Irving Langmuir)在19 世纪20 年代才提出“等离子体”的概念[15],但是最早的等离子体电化学研究可追溯至1785 年物理学家亨利·卡文迪许的著名工作——关于空气的实验 (experiments on air)[16].在该研究中,卡文迪许通过在空气中放电并使其与水接触而合成了硝酸.1887 年,Gubkin[17]利用放电等离子体还原硝酸银溶液,得到了一种金属薄膜,他认为等离子体中的电子转移到溶液中,从而还原了溶液中的银离子.随后一百多年的发展,等离子体电化学已被应用于多个方面,如氨基酸合成[18-20]、纳米材料合成[7,21-22]、分析化学[23]、等离子体医学[24-30]、植物增殖[31]、水处理[32-37]和食物保存[38-40]等.
图1[41]以直流等离子体电化学合成某种金属(M)纳米颗粒为例,简要说明了传统电化学与等离子体电化学过程异同.在传统电化学过程中,两个固体电极均浸没电解质中,当施加电压于固体金属(M)电极时,在电极和电解质(离子导体)界面会发生电化学反应以提供使电路导通的电荷.在阳极处,金属电极发生阳极溶解,在电解质中释放出金属离子(Mn+)
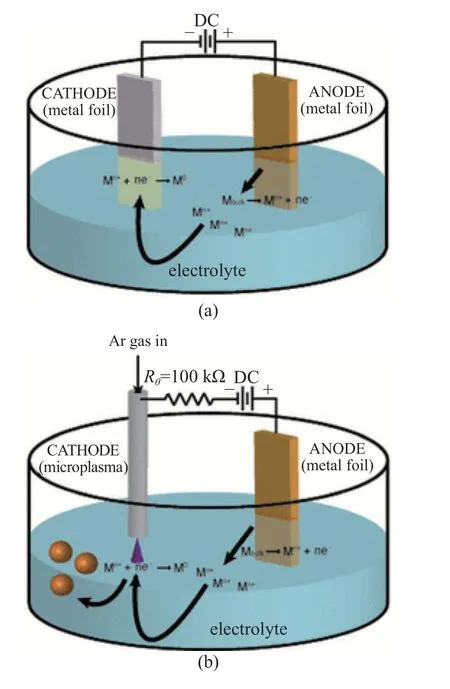
图1 (a) 具有两个固体金属电极的标准传统电化学系统和(b) 大气压直流氩气等离子体作为阴极的等离子体电化学系统(合成纳米材料).M 和Mn+ 分别代表金属元素和金属离子[41]Fig.1 Schematics of (a) a standard conventional electrochemical system with two solid metal electrodes,and (b) a plasma electrochemical system with atmospheric pressure DC argon plasma as the cathode(synthetic nanomaterials).M and Mn+ represent metal elements and metal ions,respectively[41]
在电场的作用下,金属离子在电解质中向阴极移动,当其移动到固体阴极时,在阴极处金属离子得到电子被还原为金属原子,该物质一般会以单质形式在固体阴极沉积一层薄膜,电镀即是利用这一原理.
在等离子体电化学过程中,阳极溶解形成金属离子及金属离子向阴极移动的过程和传统电化学过程都是一致的,但因为等离子体是气相的,移动到阴极的金属离子被还原后没法在阴极沉积形成薄膜,从而使得在阴极处会出现金属原子的积累,当其达到一定数目时就会在溶液中形核、生长从而得到金属纳米颗粒.除了阴阳两极的电化学过程,等离子体中存在的荷能粒子也会造成等离子体物质和溶液成分之间的转移,例如蒸发、溅射等,电场效应在液体表面引起的泰勒锥有时候也可能造成液体的直接喷射[42].这些都使得等离子体电化学过程不同于传统的电化学过程.
在等离子体电化学合成金属纳米材料过程中,合成纳米材料的前驱物可以有多种来源,阳极溶解是其中之一,也可在电解质中直接添加要合成金属纳米材料的金属盐[43].另外,当等离子体作为阴极来使用时,阴极处的电压降在有些情况下可以溅射出阴极材料来作为纳米颗粒的前驱物.无论等离子体作为阴极或者作为阳极,等离子体-液体相互作用都可以产生还原性成分,因此在合成纳米颗粒时,等离子体既可以作为阴极、也可以作为阳极来使用.
按照等离子体产生的位置来说,等离子体与液体接触可以分为液面等离子体和液中等离子体.虽然具体的电极构型与电源形式有多种组合,但是这两种形式都存在一个气-液界面,在液面直流放电等离子体中,关于气-液界面物质及电荷转移的讨论对所有的等离子体电化学过程都具有普适性.
目前对等离子体电化学气-液界面过程的研究已经取得了一定的进展.Sankaran 等[44-45]研究了等离子体-液体界面的电荷转移过程并给出了等离子体中的电子进入水中形成水合电子的实验证据,他们指出正是电荷转移过程驱动了界面处的化学和电化学反应.Rumbach 等[46]通过建立分析模型,考察了等离子体-液体相互作用中产生的高活性成分水合电子及OH 在水溶液表面的行为,他们发现这两种成分在水溶液表面的平均穿透深度和浓度相似,均为~ 100 nm 和~ 1 mM.Kaneko 等[47]研究了等离子体-液体界面的电场结构,发现了液体作阴极和阳极时不同的放电机制,即相比于液体作为阳极,液体作阴极时,等离子体-液体界面存在阴极电压降,从而使得界面处的物理化学过程更剧烈.Chen 等[48]通过计算机模拟考察了等离子体成分和含水生物膜的相互作用并讨论了等离子体成分进入生物膜的深度问题.
这些研究结果为等离子体电化学方法在实际中的应用奠定了一定的基础,如在纳米材料合成中,需要考虑等离子体成分的穿透深度以及电极极性不同造成的液中反应成分差异等.
2 等离子体在金银纳米颗粒制备中的应用、机理及调控
金银纳米颗粒的制备可以追溯到19 世纪中叶[49],当颗粒尺寸进入nm 量级时,将引起体积效应、表面效应、量子尺寸效应、量子限域效应、宏观量子隧道效应和介电限域效应,展现出许多不同于宏观材料的物理化学性质,因此被广泛应用于非线性光学、催化、生物医学及功能材料等诸多领域[50-51].
常见的合成金银纳米颗粒的方法,例如纯化学还原法,往往需要额外的还原剂,并且通常涉及多步骤过程,而等离子体电化学法可作为单步合成金银纳米颗粒的可行的替代方法.等离子体可以提供大量的高能电子,可以使气体分子解离而产生高浓度的活性自由基[6,52],活性自由基可以直接与前驱物反应,因此不需要额外的还原剂.另外,自由基可以加速还原金属离子的电化学反应,促进纳米粒子的成核,同时,等离子体附近的局部加热和气体湍流可以加速扩散过程,从而加速纳米粒子的成核和生长[6].因此,用等离子体电化学法合成金银纳米颗粒的过程非常快,只需几分钟,而许多传统的化学过程通常需要几个小时甚至几天.等离子体电化学法制备金银纳米颗粒是在室温和大气压环境条件下的单步过程,不需要真空、加热和其他设备.
Sankaran 等[53]在2008 年首次证明了微等离子体很容易与液体电极耦合以形成气液电化学反应器,气体放电中电子和离子的存在使得电流经过水溶液而驱动电化学反应(包括阳极的金属溶解和阴极的金属阳离子的还原),因此可以直接从大块金属或含水金属盐中轻松、快速地制备出高纯度的纳米级金属颗粒.如图2(a)所示,随着反应时间的增加,在400 nm 处出现了球状银纳米粒子的特征吸收峰,其强度随着反应时间的增加而增强,特别是在15 min后,吸光度非常大,表明了极高的还原速度,即等离子体快速制备了高浓度的纳米颗粒,同时制备出的银纳米颗粒分散性良好,没有出现沉淀现象.类似的结果也出现在金中,如图2(b)所示,特征吸收峰出现在530 nm 处,这是球形金纳米颗粒的特征峰.相比之下,金颗粒生长较慢,但也能产生稳定的胶体.
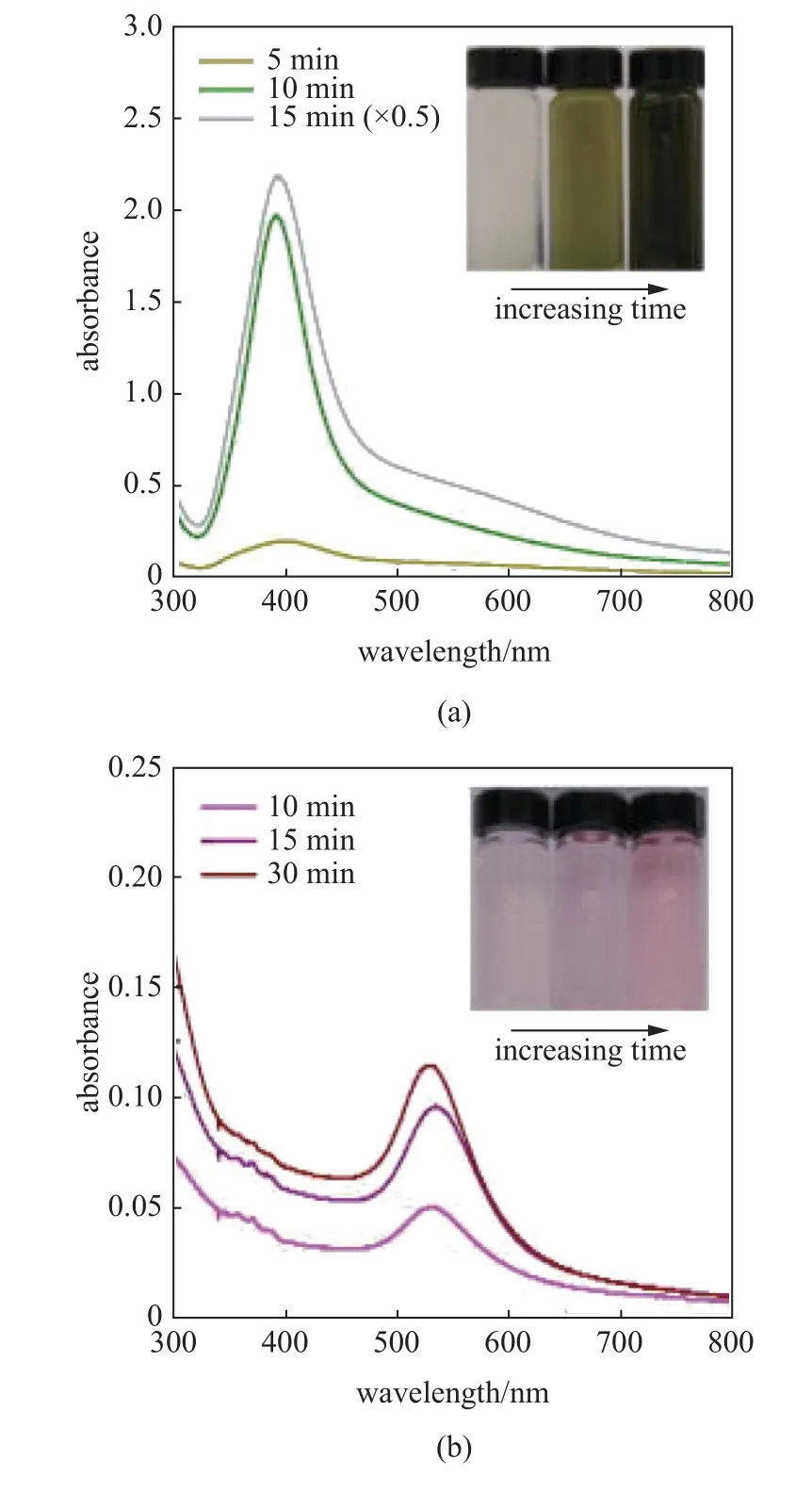
图2 (a)用银箔制备银胶体,时间间隔为5 min,10 min,15 min (插图: 相应时间的银纳米粒子溶液照片)和(b)用金箔制备金胶体,时间间隔为10 min,15 min,30 min (插图: 相应时间的金纳米粒子溶液照片)的紫外-可见吸收光谱[53]Fig.2 UV-Vis absorbance spectroscopy of (a) Ag colloids prepared from Ag foil for process intervals of 5,10,and 15 min (inset: photo of Ag colloids for corresponding times) and (b) Au colloids prepared from Au foil for process intervals of 10,15,and 30 min (inset: photo of Au nanoparticle solutions for corresponding times)[53]
近年来,越来越多的学者尝试利用等离子体电化学系统来制备金、银纳米颗粒,并探究等离子体在金、银纳米颗粒合成过程中所起的作用.Gong 等[54]以硝酸银水溶液为阳极,在等离子体电化学系统中合成了银纳米颗粒(silver nanoparticles,AgNPs),发现在银纳米颗粒形成过程中同时存在Ag+的还原和Ag 的氧化.如图3 所示,随着溶液中电子去除剂浓度的提高,AgNPs 在400 nm 处的局域等离子体共振吸收峰的强度也随之下降.这就说明在直流等离子体电化学系统中,溶液里的Ag+的还原过程在加入5-BrU 之后被显著地抑制了,因此等离子体电子溶解形成的水合电子是Ag+还原的主要还原剂,而等离子体-液体相互作用产生的过氧化氢则起到了将形成的银纳米颗粒蚀刻成Ag+的作用.
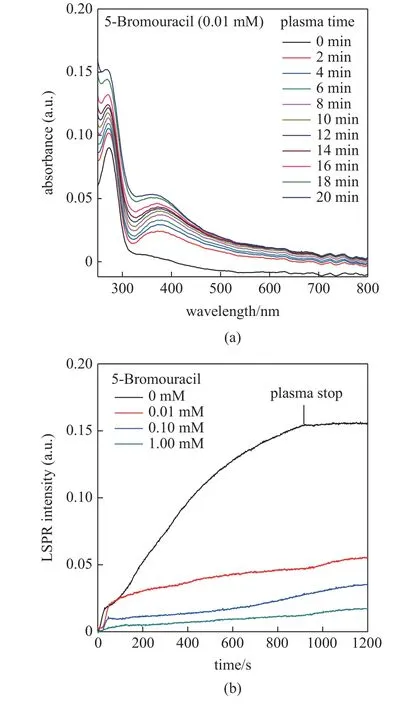
图3 (a) 等离子体处理加入5-BrU(0.01 mM)的AgNO3/PVP 溶液的吸收光谱图和(b) 等离子体处理含有不同浓度5-BrU 的AgNO3/PVP 溶液时AgNPs 位于400 nm 附近的局域等离子体共振吸收峰的强度随时间变化情况对比图[54]Fig.3 (a) Absorbance of the plasma treated AgNO3/PVP solution with 0.01 mM electron scavenger,5-Bromouracil,and (b) the evolution of LSPR peak (~400 nm) intensity for the formed AgNPs with different 5-Bromouracil concentration[54]
等离子体与液体相互作用时会产生许多活性物质,如光子、离子、电子和亚稳自由基,这些活性物质在等离子体和溶液之间的转移和进一步转化的同时也会改变溶液的pH 值、电导率等物理性质,而溶液pH 值是影响纳米颗粒制备的重要因素,Wu 等[55]采用大气压直流双氩气等离子体,在H 型电化学反应器中研究了溶液pH 值(1.99~ 10.71)对银纳米颗粒形成的影响.图4 显示了不同pH 值的等离子体处理过的AgNO3(0.1 mM)水溶液的时间图像,在这种情况下,H 型反应器左端的溶液充当阴极,右端的溶液充当阳极.结果表明,除pH 值为1.99 的溶液外,其余均可在阳极处形成银纳米颗粒;而在阴极,银纳米颗粒只出现在pH 值为10.71 的溶液中.

图4 等离子体处理的AgNO3 水溶液(0.1 mM)在pH 值为(a) 1.99,(b) 3.89,(c) 6.86,(d) 8.57 和(e) 10.71 时的时间照片.左侧反应器中的溶液作为阴极,而右侧反应器中的溶液作为阳极.通过加入HNO3 溶液(pH 值1.99)或NaOH 溶液(pH 值10.71)来调节AgNO3 溶液的pH 值.磷酸盐缓冲液调节AgNO3 溶液的其他pH 值(缓冲液强度为10 mM)[55]Fig.4 Temporal photographs of the plasma treated aqueous solutions of AgNO3 (0.1 mM) at pH values of (a) 1.99,(b) 3.89,(c) 6.86,(d) 8.57,and(e) 10.71.The solution in the left cell acts as the cathode,while in the right cell as the anode.Some pH values of the AgNO3 solution are adjusted by adding HNO3 solution (pH 1.99) or NaOH solution (pH 10.71).The other pH values of the AgNO3 solution are adjusted by phosphate buffers (10 mM in buffer strength)[55]
Liu 等[56]采用上述H 型电化学反应器,合成了金纳米颗粒(gold nanoparticles,AuNPs),并证实了过氧化氢和等离子体-液体相互作用产生的水合电子在溶液中起还原剂的作用,而原子氢和分子氢的还原作用是最小的.图5 为不同pH 值下形成的AuNPs 的SEM 形貌成像图.可以看出对于作为阴极的溶液,颗粒的大小随着pH 值的增加而减小,在pH 值为3.34,7.20 和8.81 时观察到一些棒状颗粒,当pH 值接近11.22 时,产物为小颗粒聚集的AuNPs.对于作为阳极的溶液,在pH 值为3.34 时,存在一些棒状和三角形颗粒,在其他pH 值下获得的颗粒或多或少是小型AuNPs 的聚集.

图5 等离子体处理过的HAuCU (0.1 mM)/PVP (0.1 mM)水溶液在pH 值为3.34,7.20,8.81 和11.22 时的SEM 图像.通过向预制的HAuCU/PVP 溶液(pH=3.34)中加入NaOH 将溶液调整为中性,然后在等离子体处理过程中使用磷酸盐缓冲液(缓冲强度为10 mM)维持溶液的pH 值为7.20 和8.81,而仅在预制的溶液中加入NaOH 溶液即可获得11.22 的pH 值[56]Fig.5 SEM images of plasma treated aqueous solutions of HAuCU (0.1 mM)/PVP (0.1 mM) at pH values of (a) 3.34,(b) 7.20,(c) 8.81,and (d) 11.22.The pre-prepared HAuCU/PVP solution (pH=3.34) is adjusted to neutral by adding NaOH solution,and then a phosphate buffer (10 mM in buffer strength) is used to sustain the pH values of 7.20 and 8.81 during the plasma treatment,while the pH value of 11.22 is obtained by only adding some NaOH solution into the pre-prepared solution[56]
本课题组采用大气压微等离子体辅助电化学技术合成了银纳米颗粒、金纳米颗粒和金银合金纳米团簇,并通过调控实验参数(电解液浓度、温度、电流、稳定剂、pH 值等) 有效控制了纳米颗粒的大小、分散及稳定性[57-60].
图6[57]为不同溶液浓度下银胶体的紫外可见吸收光谱(AgNO3与果糖的比例设为0.02,具体AgNO3/果糖加入量分别为1 mM/0.05 M,0.5 mM/0.025 M,0.2 mM/0.01 M,0.1 mM/0.005 M),随着AgNO3浓度的增加,峰值位置明显移至红色(即随着浓度的增加,从402 nm 移至420 nm).这种反应与经典的米氏理论相一致,该理论指出,较大的粒子表现出红移的吸光度峰,这表明通过增加AgNO3浓度获得的AgNPs (平均)大于低AgNO3浓度情况下的AgNPs.随着AgNO3浓度的增加,峰值强度的增加也表明在高浓度情况下产生了更多的AgNPs.
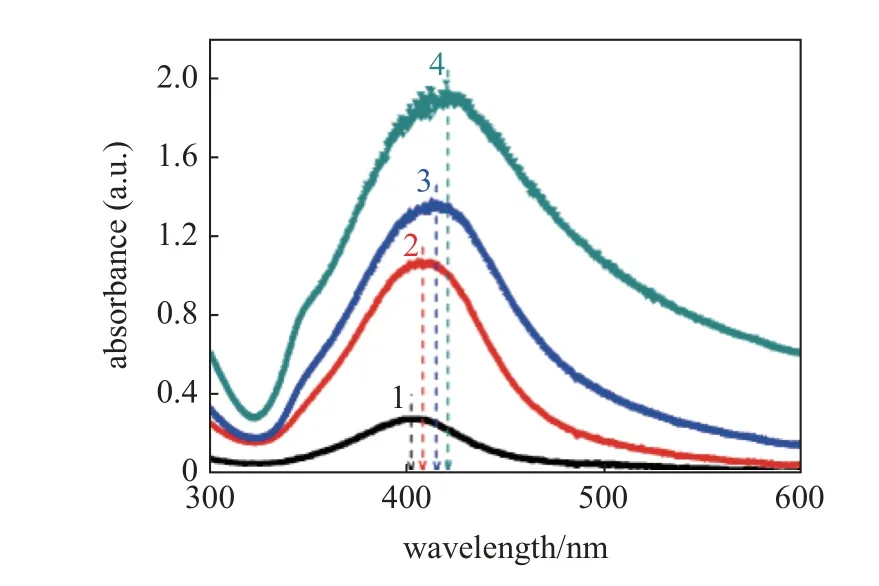
图6 电解液中AgNO3 和果糖含量的变化对微等离子体辅助电化学合成银纳米粒子紫外可见吸收光谱的影响,其中AgNO3 和果糖含量分别为: 1=0.1 mM,0.005 M;2=0.2 mM,0.01 M;3=0.5 mM,0.025 M;4=1.0 mM,0.05 M[57]Fig.6 The effect of varying the AgNO3 and fructose content in the electrolyte solution on the UV-Vis absorbance spectra of AgNPs produced via microplasma-assisted electrochemical synthesis,where AgNO3 and fructose are: 1=0.1 mM,0.005 M;2=0.2 mM,0.01 M;3=0.5 mM,0.025 M;4=1.0 mM,0.05 M[57]
图7(a)为Au 粒子在室温(25 °C)和高温(70 °C)下的UV-Vis 吸收光谱图,可以看出,两个吸收峰都在530 nm 左右,即在不同温度下产生的金纳米粒子的最可能尺寸几乎相同.在70 °C 时生成的AuNPs的吸光度曲线在长波长处呈小幅上升趋势,表明温度越高,越大的AuNPs 的生长越快,但温度的影响还不够大,不能使吸光度曲线的峰发生红移.在25 °C和70 °C 下制备的AuNPs 的TEM 图像和PSD 分别如图7(b),图7(b′)和图7(c),图7(c′)所示.在25 °C和70 °C 下制备的AuNPs 的平均尺寸分别为32.78 nm和36.87 nm.虽然在70 °C 下制备的Au 颗粒的平均尺寸较大,但在这两种温度下制备的AuNPs 的最可能尺寸几乎相同,该结果与UV-Vis 吸光度给出的结果非常吻合(图7(a))[59].
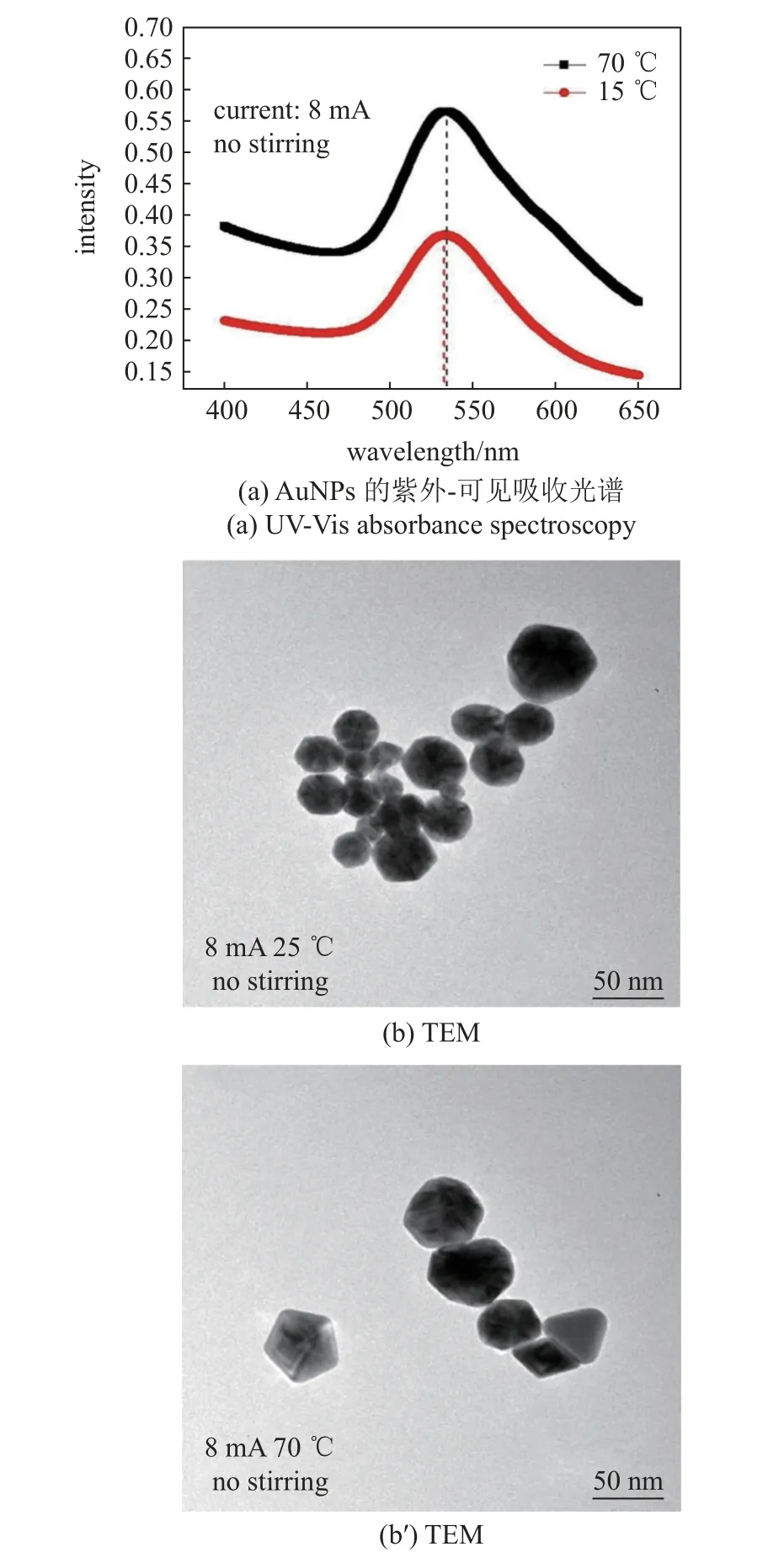
图7 AuNPs 的紫外-可见吸收光谱、TEM 图像和PSD.合成温度为25 °C 和70 °C,使用8 mA 电流,无搅拌[59]Fig.7 UV-Vis absorbance spectroscopy,TEM images,and PSD of AuNPs.Synthesized at temperatures of 25 °C and 70 °C,using 8 mA of current with non-stirring condition[59]
图8(a) 显示了利用大气微等离子体电化学在8 mA 和15 mA 电流下产生的金胶体的紫外可见吸收光谱.两项实验均在室温下进行,没有任何搅拌.在15 mA 下产生的Au 纳米粒子的紫外-可见吸收峰的蓝移表明,在较高电流值下制备的纳米粒子最可能的尺寸较小.在8 mA 和15 mA 电流下产生的AuNPs 的TEM 图像和PSD 分别如图8(b),图8(b′)和图8(c),图8(c′)所示.在8 mA 下产生的AuNPs的平均尺寸为32.78 nm,在15 mA 下产生的AuNPs的平均尺寸为28.79 nm,可以看出,在较高的电流值下产生的AuNPs 的平均尺寸较小.所得结果与紫外-可见吸收光谱结果吻合较好,两种结果都表明,在较高的电流值下产生的AuNPs 的平均尺寸比在较低的电流值下产生的AuNPs 小[59].
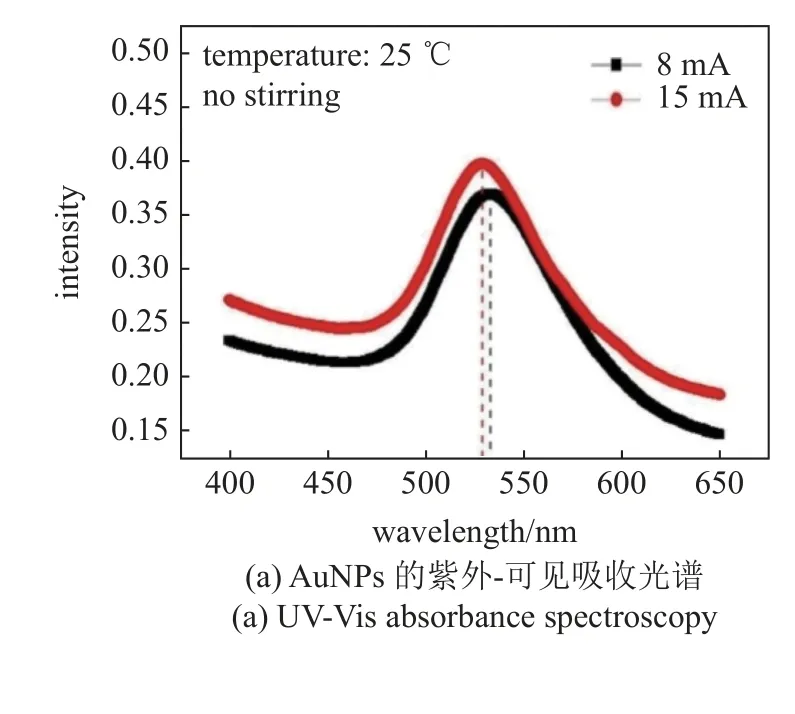
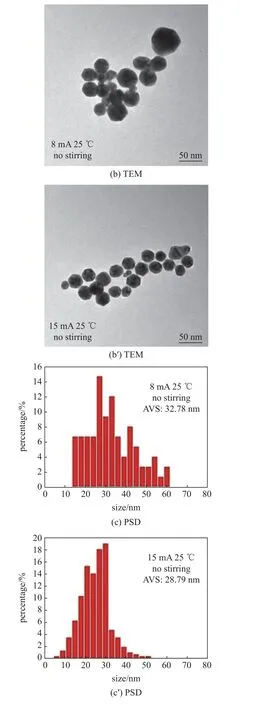
图8 在室温25 °C 下,使用(8,15) mA 电流,无搅拌条件下合成[59]Fig.8 Synthesized at room temperature of 25 °C,using (8,15) mA of currents with non-stirring condition[59]
图9 显示了用微等离子体处理硝酸银、NaHCO3(1.5 mM)和(a)蔗糖、(b)葡萄糖、(c)乳糖和(d)麦芽糖1.5 min 制备的AgNPs 的TEM 结果,并得到了AgNPs 的粒径分布(particle size distributions,PSD).从图7(a)可以清楚地看出,使用蔗糖作为稳定剂得到的AgNps 比使用葡萄糖、乳糖和麦芽糖作为稳定剂得到的AgNps 尺寸分布更窄.此外,使用蔗糖作为稳定剂的AgNPs 溶液吸光度谱的FWHM更小.因此,蔗糖产生的AgNPs 最小,分散最窄,合理的解释为蔗糖是一种不还原性的双糖.
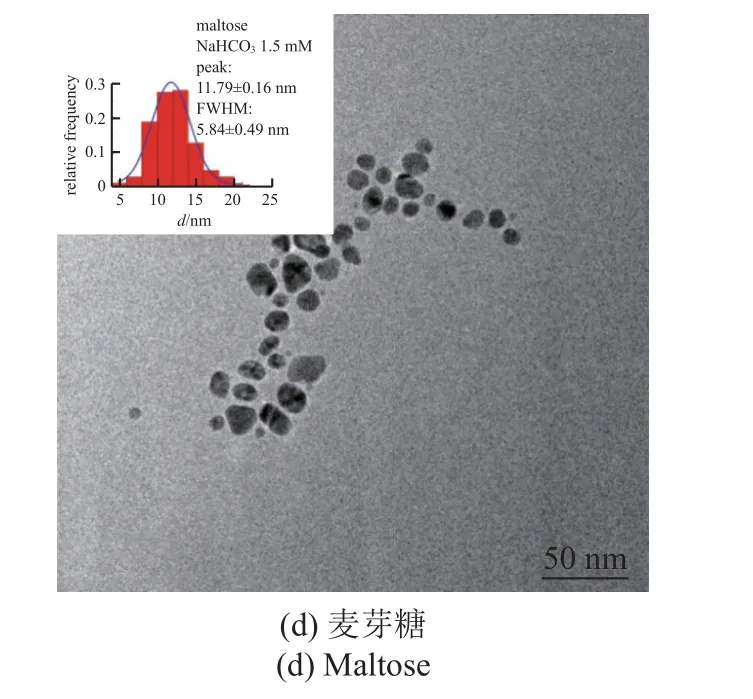
图9 用1.5 mM NaHCO3 和(a)蔗糖、(b)葡萄糖、(c)乳糖、(d)麦芽糖制备AgNPs 的TEM 和PSD[60]Fig.9 TEM and PSD of AgNPs produced using 1.5 mM NaHCO3 and(a) sucrose,(b) glucose,(c) lactose,(d) maltose[60]
图10[60]显示了NaHCO3浓度对AgNPs 稳定水溶液紫外-可见吸收光谱的影响,在NaHCO3浓度为0.5,1.0 和1.5 mM 时,pH 值分别为6.0,6.6 和7.0 左右,且在1.5 min 反应时间内基本保持不变.从图10 中可以看出,随着溶液pH 值的降低,紫外可见吸收光谱峰的高度逐渐下降,并向较长波方向移动,这意味着可以通过改变pH 值来控制AgNPs 的大小.该溶液以蔗糖作为稳定剂,可保存2 个月.
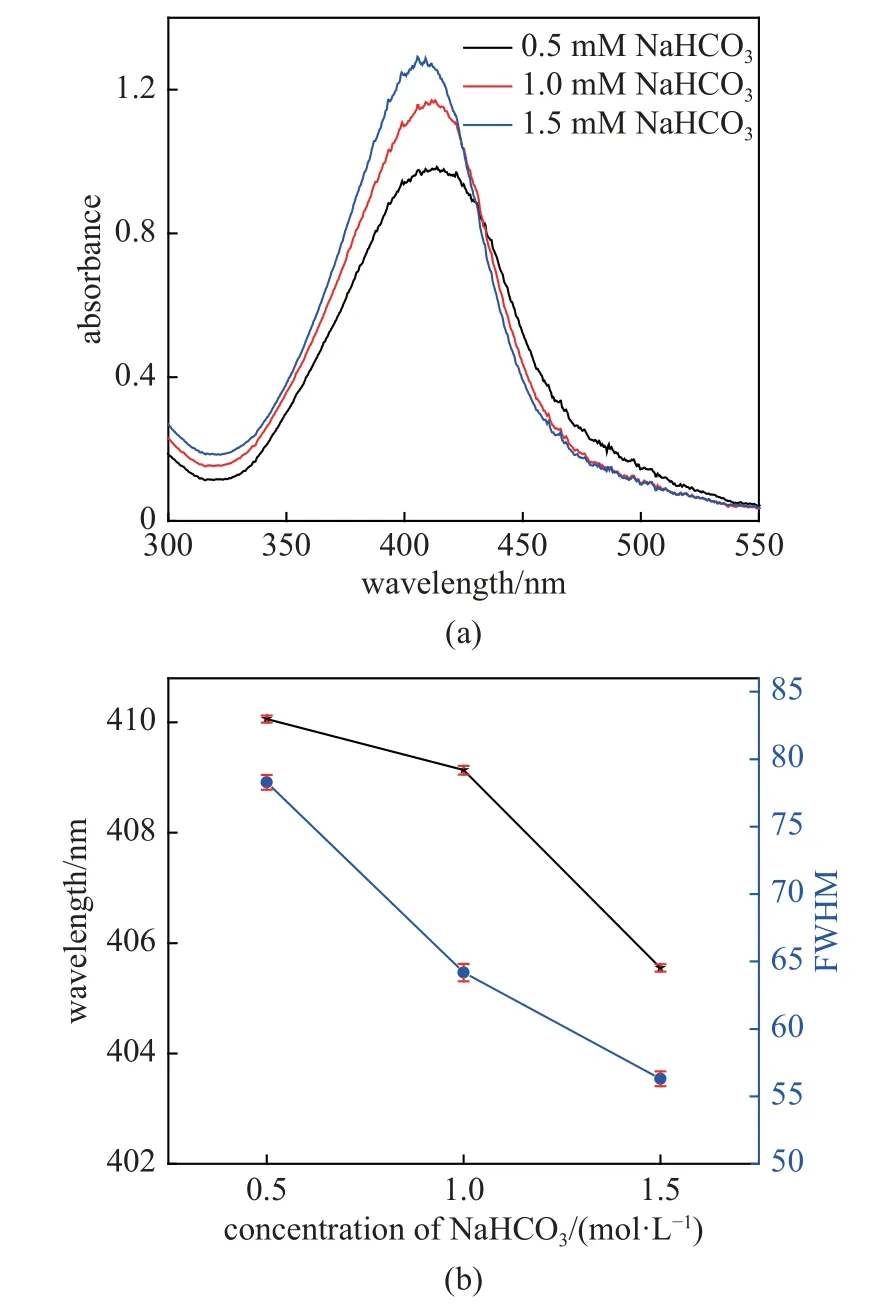
图10 (a)不同pH 溶液样品的紫外-可见吸收光谱和(b) FWHM 和UV-Vis 吸收波长峰值图[60]Fig.10 (a) UV-Vis absorbance spectra of samples produced with a different pH solution and (b) graphs of FWHM and peak UV-Vis absorbance wavelength[60]
综上,基于等离子体电化学反应,可实现金银纳米颗粒的制备,同时,通过调控电解液浓度、温度、电流、稳定剂和pH 值等多反应参数,可实现对金银纳米颗粒的性质调控,对于金银纳米颗粒的发展具有重要意义.
3 等离子体在碳量子点制备中的应用及机理研究
作为尺度更小的纳米材料,碳量子点于2004 年被首次发现,是一种尺寸小于10 nm 的新型碳基纳米材料,被业界称为“next big small thing”[61],碳量子点具有以下优点: (1)良好的生物相容性和低毒性;(2)良好的光学稳定性;(3)独特的依赖于激发波长的荧光发射性质,随着激发波长红移,荧光波长红移;(4)具有双光子吸收上转换特性,可在红/近红外光谱区域(600~ 1200 nm)进行光激发和荧光辐射检测;(5)表面富含官能团,易于表面修饰和功能化.因此,碳量子点在生物医学[62-65]、光电子器件[66-68]和光催化[69-70]等领域具有广阔的应用前景.
目前碳量子点的制备,大多需要密闭的反应空间,高温(200 °C~ 300 °C)、高压(~ 6 MPa)、长时间(6~ 10 h)的反应条件,反应过程存在高能量消耗、反应产物荧光性质无法在线原位监测的困难,使得研究者们无法对碳量子点的生长过程进行原位分析,反应参量与碳源分子的作用机制尚不清楚.目前制备出的碳量子点,其荧光多需要紫外光(< 400 nm)激发,且以(390~ 550 nm)的蓝绿色荧光为主,存在生物组织穿透深度低、易造成光损伤的缺点.另外,碳量子点可控性制备仍存在困难,具有近红外荧光发光(700~ 1700 nm),适合生物医学应用的肿瘤靶向功能碳量子点的可控性制备无法实现[65,71-74].
等离子体通过高电压击穿气体进行放电,具有电子密度大(1013~ 1015cm-3)、温度高、反应活性物质种类丰富的特点[75-77].大气压等离子体电化学反应,具有开放的反应空间、低温、大气压条件(0.1 MPa)、快速和低能耗的反应特点.同时,通过可调的气体组分(如氮气、氧气和氩气等)、多样的放电方式(如直流、交流和脉冲等)与溶液物质的相互作用,共同形成了一个变化丰富的电化学作用系统,可为碳量子点的制备、反应过程监测和反应参数调控提供良好的技术平台.
2015 年,本课题组首次以果糖为碳源,采用等离子体电化学法快速制备出了蓝色荧光碳量子点,其UV-Vis 吸收光谱和PL 光谱如图11 所示.从UVVis 吸收光谱中可以清楚地看出,碳点在256 nm 处吸收,而从PL 光谱中,它们在蓝色波段发射.当激发源波长在360~ 410 nm 范围内随发射峰变化时,发射峰从443 nm 左右位移到456 nm 以上.随着发射峰红移,峰值强度逐渐降低,这是由于激发源波长越来越远离吸收峰波长,激发源与碳点之间的相互作用减弱.另外,通过对比对溶液加热的结果,发现欧姆加热不是碳量子点合成的主要原因,且与之前报道的纯化学方法相比,所需的氢氧化钠减少了约100 倍.[78]
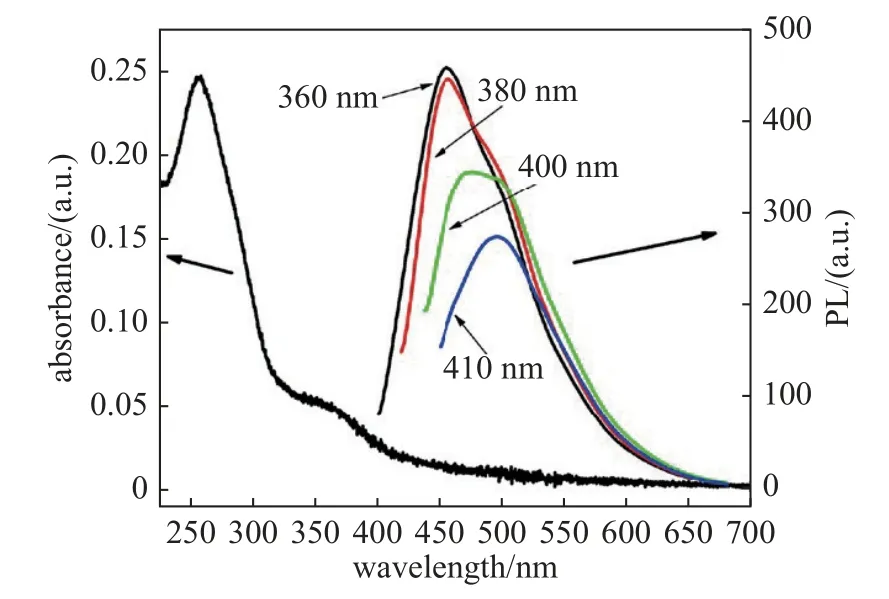
图11 UV-Vis 吸光度(左)和PL (右)光谱[78]Fig.11 UV-Vis absorbance (left) and PL (right) spectra[78]
同年,Wang 等[79]使用直流大气压微等离子体处理柠檬酸和乙二胺,制备出了具有尺寸均匀、蓝色荧光的碳量子点.如图12(a)所示,在微等离子体处理过程中,阳极侧的溶液在几分钟内由无色变为黄色,表明微等离子体方法是一种快速的碳量子点制备技术.随后,随着反应时间的增加,溶液颜色逐渐变深,这可能是由于碳量子点含量的增加,说明所制备的碳量子点具有良好的水溶性.同样,在相同的反应时间下,更高的电流可以制备更多的碳量子点(图12(b)).TEM 图像表明,制备的碳量子点彼此分离良好,尺寸分布在1~ 3 nm 之间,尺寸分布相对较窄,并可用于溶液pH 值检测和铀探测.

图12 (a)不同反应时间和(b)不同放电电流的微等离子体阳极处理碳量子点溶液的照片;(c) 碳量子点的TEM 图像[79]Fig.12 The photographs of CD solutions treated by microplasma anode with (a) different reaction times and (b) different discharge currents.(c) TEM image of CDs[79]
Mohammadzaheri 等[80]利用基于介质阻挡放电的大气压低温等离子体射流在水介质中合成了氮掺杂的碳量子点,其荧光发射光谱如图13(a)和图13(c)所示.当激发波长从320 nm 增加到420 nm 时,发射峰红移到更长的波长.图13(b),图13(d)给出了二维颜色转换等高线图,揭示了光致发光强度随激发波长变化的行为.在曝光时间为30 min 时,N 掺杂CQDs的最大激发波长为320 nm,发射波长为411 nm(3.01 eV),量子产率为5.72%,随着曝光时间延长至60 min,最大发射峰逐渐移至418 nm (2.96 eV),激发波长为340 nm,量子产率达到15.89%.量子产率的提高可能归因于来自等离子体的OH 和O 等含氧自由基的存在,以及杂原子的掺杂,这些杂原子可以连接到CQDs 表面并去除悬空键,从而提高量子产率.

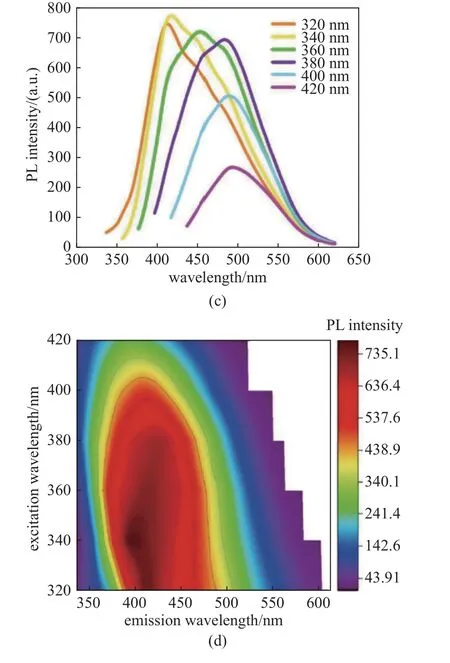
图13 (a,b) 曝光时间30 min 时,N 掺杂碳量子点的光致发光光谱及其二维激发发射等高线图.(c,d) 曝光时间60 min 时,N 掺杂碳量子点的光致发光光谱及其二维激发发射等高线图[80]Fig.13 (a,b) Photoluminescence spectra of N-doped carbon quantum dots at an exposure time of 30 min and its two-dimensional (2D)excitation-emission contour map.(c,d) Photoluminescence spectra of Ndoped carbon quantum dots at an exposure time of 60 min and its 2D excitation-emission contour map[80]
Kurniawan 等[81]成功地利用微等离子体合成了具有可调谐尺寸、功能、发光和带隙的氮掺杂石墨烯量子点.不同NGQDs 的pH 传感实验表明,NGQD7的pH 传感性能最好(图14),并假设是NGQD7 的质子化和去质子化程度最平衡的原因,可能与NGQD7中最突出的含—OH 官能团有关.NGQDs 的pH 敏感性也可能不仅仅来自于—OH 的存在,因为在所有NGQDs 中也观察到—OH 的存在.相反,—OH、吡咯N 和粒径的组合可以产生pH 调制带隙可调性的协同效应,这是NGQDs 具有pH 敏感性的重要原因.

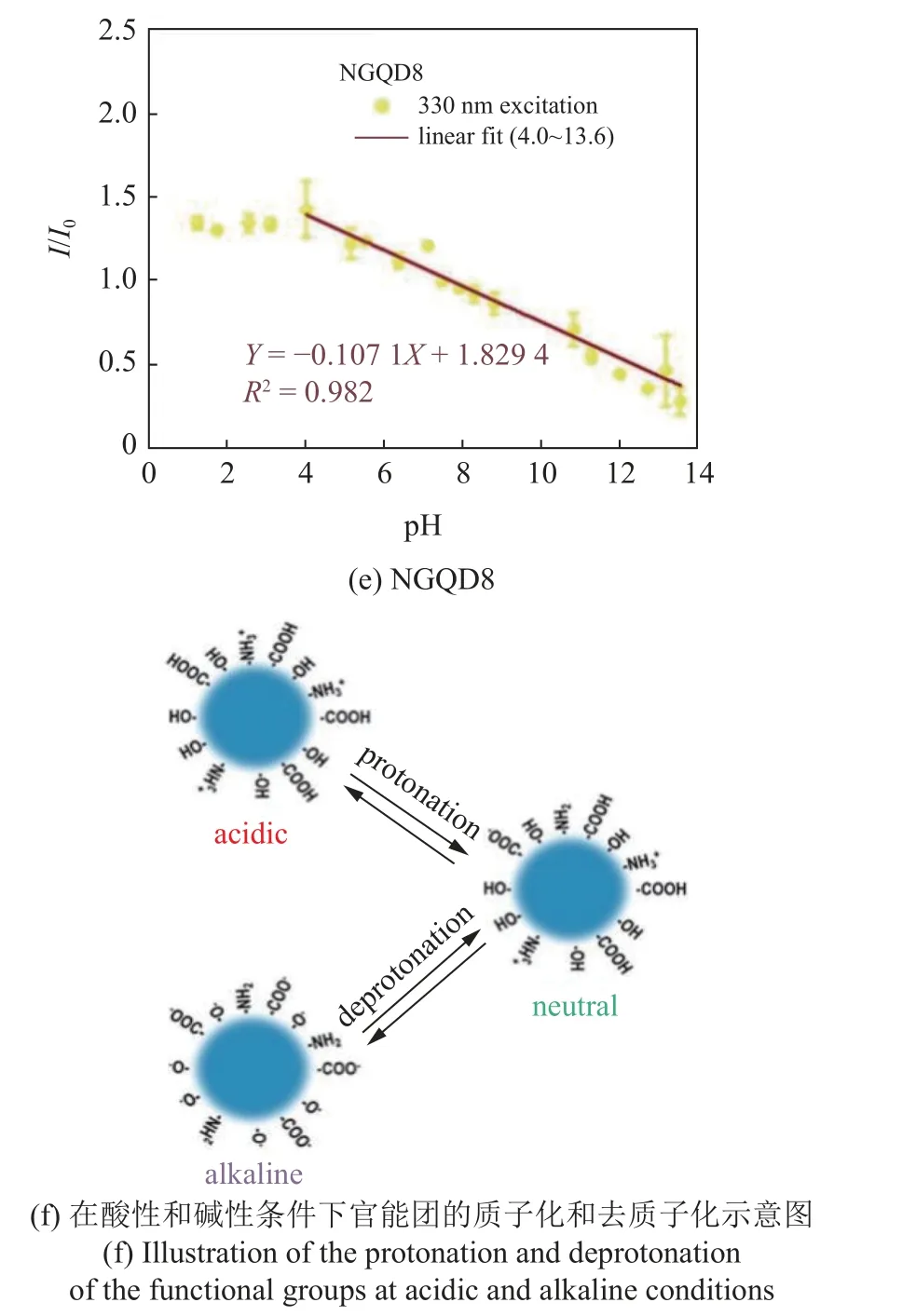
图14 不同酸处理NGQDs 的pH 传感性能.(a) NGQD1,(b) NGQD2,(c) NGQD3,(d) NGQD7,(e) NGQD8 的pH 传感性能.(f)在酸性和碱性条件下官能团的质子化和去质子化示意图[81]Fig.14 pH sensing performance of different acid-treated NGQDs.pH sensing performance of (a) NGQD1,(b) NGQD2,(c) NGQD3,(d) NGQD7,and (e) NGQD8.(f) Illustration of the protonation and deprotonation of the functional groups at acidic and alkaline conditions[81]
等离子体制备出的碳量子点可以兼具优异的荧光性质和良好的肿瘤靶向等生物医学功能,可选择性富集于肿瘤细胞或肿瘤组织中,实现肿瘤靶向诊断和精准治疗.本课题组以叶酸、邻苯二胺等为碳源,采用等离子体电化学法制备出了多种功能性碳量子点,进一步探究了碳量子点的形成机理,并尝试将碳量子点应用于医学领域.
以叶酸为碳源,本课题组[82]采用等离子体电化学法,制备出了荧光峰位于445 nm (370 nm 激发)的蓝色荧光叶酸碳纳米颗粒,该碳纳米颗粒相对于叶酸分子,荧光量子产率提升了26 倍,达到13%.图15为细胞荧光图像结果,图15(a)是MCF-7 细胞在光场作用下的图像.由于细胞种植密度相对较高(105mL-1),幻灯片上的细胞聚集在一起,在图片中形成灰色区域,图15(b)是细胞在激发下的图像.可以观察到,这些乳腺癌细胞被叶酸碳纳米颗粒的荧光发射明显标记,表明其具有良好的标记能力.

图15 (a) MCF-7 细胞光场和(b) 激发波长330~ 440 nm 的荧光显微镜下图像[82]Fig.15 (a) The images of MCF-7 cells under the light field and(b) under fluorescence microscope with excitation wavelength ranging of 330~ 440 nm[82]
为了进一步探究碳量子点医学应用的可行性,本课题组[83]用等离子体电化学法,以邻苯二胺为碳源,制备了具有很好的生物相容性的碳量子点,该碳量子点可清楚标记肿瘤细胞(HeLa 细胞),发出明亮的黄绿色荧光(550 nm@460 nm 激发),如图16(a)所示.为了检测细胞毒性,将终浓度为0~ 400 μg/mL的CQDs 处理HeLa 细胞24 h,图16(b)显示,通过MTT(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑)测定,95%以上的细胞存活,这表明CQDs 具有低细胞毒性和高生物相容性,具有良好的生物成像前景.如图16(c)所示,CQDs 和蓝光单独处理的HeLa细胞的生存能力没有差异,CQDs 和蓝光同时处理显著降低Hela 细胞的细胞活力,这取决于光暴露的持续时间.在460 nm 照射15 min 后,CQDs 显示出明显的抗肿瘤活性;浓度为200 μg/mL 时,HeLa 细胞活力下降约40%.为了进一步检测CQDs对Hela 细胞的抑制作用,采用MTT 法测定CQDs对Hela 细胞的半最大抑制浓度(IC50).结果表明,CQDs 在Hela 细胞上作用10 min 后的IC50 约为427.5 μg/mL (95%CI 366.7~ 498.7 μg/mL),在蓝光作用15 min 后的IC50 约为255.1 μg/mL (95% CI 220.9~ 249.8 μg/mL).这些结果表明,激发后的CQDs 能像临床上一些抗癌药物一样有效杀伤肿瘤细胞,因此CQDs 在抗肿瘤治疗中具有广阔的应用价值.
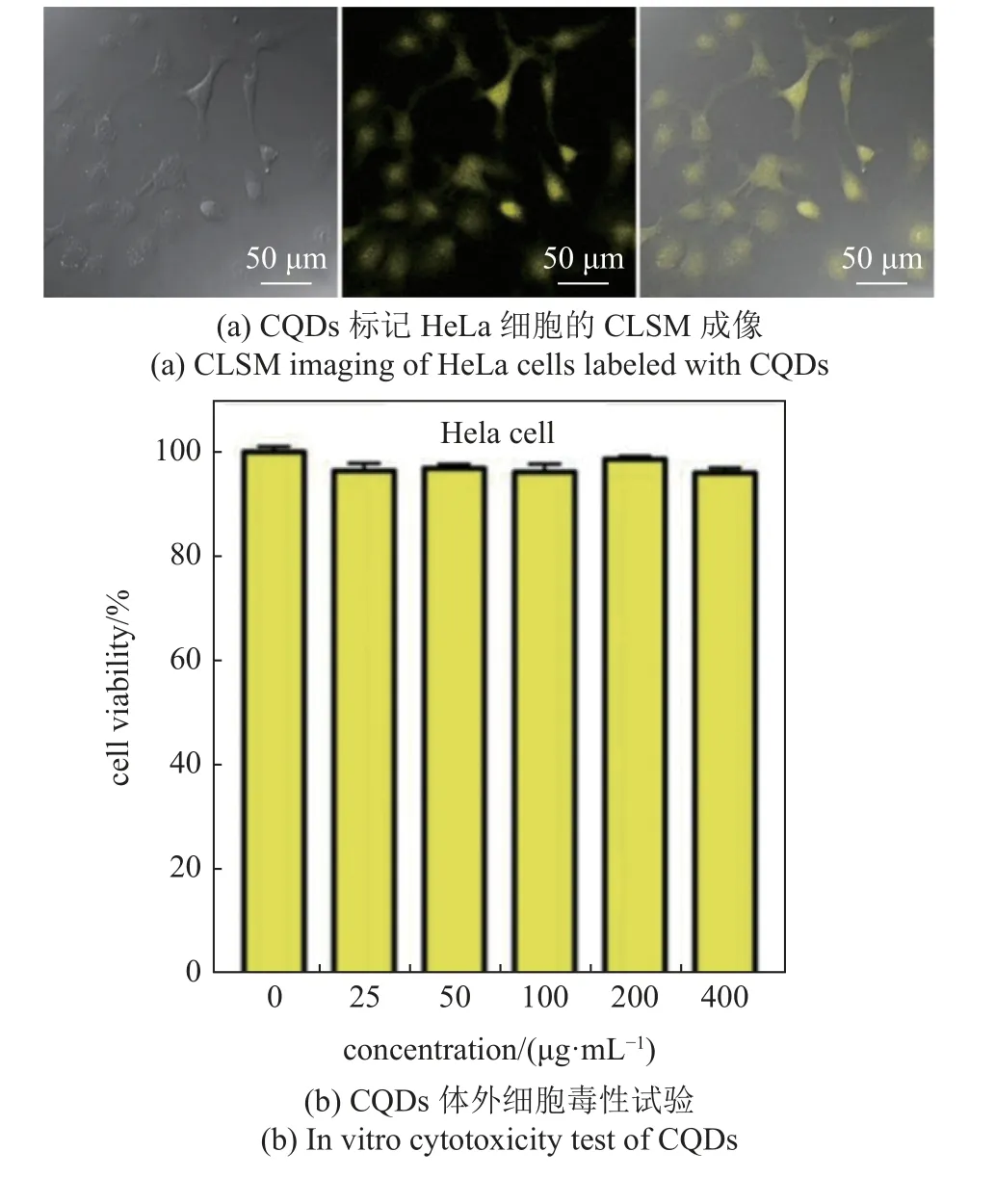
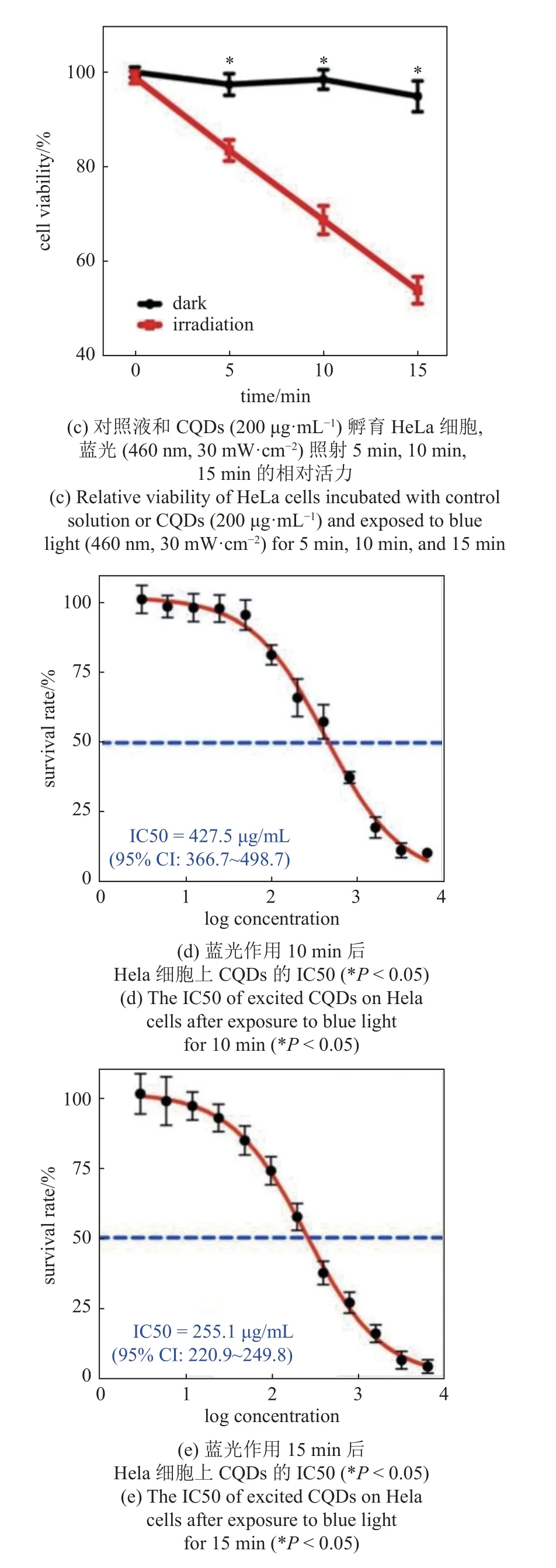
图16 CQDs 的应用[83]Fig.16 Application of CQDs[83]
综上,等离子体电化学法是一种制备碳量子点的有效方法,且通过筛选合适的前驱物,制备出的碳量子点可具有良好的生物相容性,在医学等领域具有广阔的应用前景.
4 等离子体制备纳米材料的关键问题
等离子体辅助电化学法作为一种高效、便捷、环境友好的制备纳米颗粒的方法,近年来被越来越多的学者关注和研究.等离子体为纳米颗粒的制备提供了独特的物理化学环境,这种强烈的非平衡的环境能够存储密度在几十kW/cm 到MW/cm 之间的能量,因此,光子或带电粒子形式的能量也可以通过等离子体有效地释放出来.此外,大气压低温等离子体的非平衡特性使其在相对较低的气体温度下仍能保持其他成分具有较高的能量状态(如电子、激发态原子或分子等).在这种非平衡和高能量密度的条件下,可以产生大量的电子、离子、自由基和其他受激、电离态反应成分[77].
由于引入了非平衡等离子体,增加了对纳米颗粒控制上的影响因素,但同样也增加了研究的难度,等离子体在纳米颗粒制备过程中的作用和影响的理论体系尚未完善.目前,基于等离子体电化学反应制备的纳米颗粒趋于丰富且具有巨大应用潜力,但其形成机理及可调控性仍存在巨大挑战,关键科学问题如下.
(1) 理论、实验与模拟仿真的结合来阐明等离子体在纳米材料合成中的多重作用: 当等离子体被引入时,许多基于等离子体的过程表现出巨大的变化,理论、实验与模拟仿真的结合可以更好地理解这些过程,从而能够量化和区分不同反应性物质(如电子、离子、自由基、激发态分子、光和热等)对所得纳米材料的影响.针对这一问题,需大力发展基于流体-电磁场耦合模型的数值模拟方法,研究等离子体内荷电、荷能反应活性组分的时空演化和随实验参数的演变;同时,采用实时时空分辨光学诊断技术,并使用不同波长和滤波宽度的滤光片,研究等离子体,特别是气-液界面附近等离子体内荷电、荷能反应活性组分的时空演化和随实验参数的演变.
(2) 对金银纳米颗粒形貌、尺寸、化学结构和功能化等的调控: 为追求材料的卓越性能,追求形态更加新颖和尺寸更加均一的金银纳米颗粒是科研人员面临的一个巨大挑战,同时,对金银纳米颗粒化学结构和功能化的有效调控也使其可以更具针对性地应用于各个领域,因此,实现对金银纳米颗粒的调控是非常必要的.针对这一问题,需大力发展对液相物理化学过程的实时考察技术,例如可以采用在线光吸收技术对溶液吸收进行检测,实时考察样品吸收峰位、吸收峰展宽的变化,由此判断金银纳米颗粒的尺寸变化、尺寸均匀性等.
(3) 对碳量子点波长的调控: 等离子体辅助制备的碳量子点其荧光多需要紫外光(< 400 nm)激发,且以(390~ 550 nm)的蓝绿色荧光为主,存在生物组织穿透深度低、易造成光损伤的缺点.为了获得长波长荧光碳量子点,学术界在碳量子点的发光机制,特别是碳量子点荧光波长红移机制研究中进行了大量的探索工作.通过使用聚丙烯酰胺凝胶电泳、硅胶柱色谱层析、高效液相色谱等分离方法,研究人员证实石墨氮和碳-氮键(C—N)、碳氧单键(—C—O)、羧基(—COOH)官能团等在促使碳量子点荧光峰红移(400~ 450 nm 至620~ 680 nm)的过程中起着决定作用.然而,目前有关碳量子点合成机理的研究还非常落后,这使得对碳量子点光学性质的调控非常困难.对于基于等离子体电化学反应的碳量子点制备技术,等离子体-液体相互作用是核心,碳源是关键.等离子体-液体相互作用本质就是等离子体中的荷电、荷能反应活性组分和溶液成分的相互作用.等离子体,特别是气-液界面附近等离子体内荷电、荷能反应活性组分受气、液两相相互作用的影响最为突出,其复杂的时空演化和随实验参数的演变,是等离子-液体相互作用的体现,也给等离子体-液体相互作用研究带来了机遇.鉴此,针对这一问题,需深入研究等离子体-液体相互作用、“等离子体-液体相互作用、碳源→生长状态(包括成分、结构、官能团等)→荧光特性”的内在关联,探索基于等离子体电化学反应的长波长荧光碳量子点可控制备技术.
5 结论
等离子体辅助电化学法提供了一种高效、便捷、环境友好的纳米颗粒制备方法,对于纳米材料的发展具有重要意义.本文首先对等离子体电化学特点及其应用于纳米材料制备的可行性进行了介绍,其次,综述了近年来大气压等离子体制备金、银纳米颗粒和碳量子点的研究进展,最后,探讨了等离子体制备纳米材料在形成机理及可调控性方面面临的一些关键问题.

