基于网络药理学探讨柴胡-黄芩治疗青春期后痤疮的作用机制*
李天举,刘永瑞,陈燕辉,丁治云,王维,张阳,付黎影,曹学辉,陈羽佳
河南中医药大学第五临床医学院,郑州人民医院,河南 郑州 450000
痤疮是一种好发于面部的慢性毛囊皮脂腺疾病。现代研究认为,毛囊皮脂腺导管角化过度、皮脂腺细胞分泌的皮脂增多、痤疮丙酸杆菌增殖和炎性细胞因子是痤疮发病的主要因素[1-3]。现代研究发现,成人痤疮发病率呈上升趋势,尤以女性为多见,美国发病率约为61.9%,法国则有41%的女性在青春期后患痤疮[4],病程中患者会因疾病进展、自我形象不佳、治疗干预及社会支持等产生各种负性情绪[5]。其治疗与寻常痤疮一致,有医生指出,女性青春期后痤疮可能更易复发或对西医常用口服药物(如异维A酸胶囊)产生耐药性[6],而中医疗法存在一定治疗优势。有研究发现,青春期痤疮病例组鼻背受累者比例较高,青春期后痤疮病例组则以口周、下颌部受累比例较高[7]。有学者根据《素问·刺热》的论述,并结合历代医家的有关论述,特别是结合痤疮的皮损分布特点,提出将痤疮按照面部脏腑经络分属,耳前、下颌角(含左右颈)属肝胆[8]。中国痤疮治疗指南(2019修订版)指出冲任不调证皮损好发于额、眉间或两颊,认为该证型与情绪压力相关,并明确指出该中医证型相当于有高雄激素水平表现的女性痤疮[3]。现代中医家马丽俐认为,青春期后痤疮多与肝气郁结,日久化热有关,从而导致面部红斑丘疹脓疱[9],故治疗中多选用疏肝解郁清热之药物。而柴胡-黄芩作为疏泄的常用药对,是皮肤科治疗痤疮的常用药对[10]。
《中华人民共和国药典》2020年版指出柴胡为伞形科植物柴胡或狭叶柴胡的干燥根,按性状不同,分别习称“北柴胡”和“南柴胡”,春、秋二季采挖,除去茎叶和泥沙,干燥。其性味辛、苦、微寒,归肝、胆、肺经。黄芩为唇形科植物黄芩的干燥根,春、秋二季采挖,除去须根和泥沙,晒后撞去粗皮,晒干。其性味苦、寒,归肺、胆、脾、大肠、小肠经。柴胡-黄芩最早见于张仲景《伤寒杂病论》中小柴胡汤,是经典药对。柴胡-黄芩药对应用广泛,柴胡苦平,散邪开郁,既有发散之功,又增理气之意;黄芩苦寒,清热燥湿,泻火解毒,施今墨认为两药相合,升清降浊,调和表里,既可疏调肝胆之气机,又可外泻内蕴之湿热。
网络药理学是一门以系统生物学理论、生物系统网络分析、多靶点药物分子设计特异性信号节点选择为基础的新兴学科。中药复方的作用机制具有多靶点、多层次的特点,其机理类似于网络药理学的完整性、系统性和综合性,因此网络药理学适用于中药复方药理作用机制的研究[11]。
1 资料与方法
1.1 相关靶点筛查利用中药系统药理学数据库与分析平台检索“柴胡”“黄芩”,以口服生物利用度(oralbioavailability,OB)≥30%、类药性(drug-likeness,DL)≥0.18为筛选标准[12-13],得到药物有效成分和其对应的蛋白质靶点,将其录入Uniprot数据库,从而获得标准基因名。
OB表示口服药物到达体循环的百分比,是药物筛选中最常用的药代动力学性质之一。DL作为分子参数,被用于测量受药代动力学影响的药物分子的吸收、分布、代谢和排泄。
1.2 青春期后痤疮的相关靶点筛查青春期后痤疮是痤疮的一种类型,英文名仍为ACNE,故以“ACNE”为关键词,寻求GeneCards数据库中青春期后痤疮的相关靶点。
1.3 蛋白质相互作用(protein-protein interaction,PPI)网络的构建及核心靶点筛选将药物活性成分相关靶点与疾病相关靶点取交集,通过VENNY在线工具绘制韦恩图,得到柴胡-黄芩治疗青春期后痤疮的潜在靶点,将数据导入Cytoscape 3.9.0软件构建“活性成分-潜在靶点”图,并将潜在靶点在STRING 11.0数据库进行网络模型构建得到PPI网络,结果导入Cytoscape 3.9.1进行可视化分析,使用CytoNCA插件挖掘核心靶点(参数为默认设置),利用EXECL取交集靶点,即柴胡-黄芩作用于青春期后痤疮的潜在靶点。
1.4 潜在靶点的基因本体(gene ontology,GO)功能富集分析和京都基因与基因组百科全书(kyoto encyclopedia of genes and genomes,KEGG)信号通路富集分析将最终得到的潜在靶点录入微生信平台进行GO功能及KEGG信号通路富集分析,设置P<0.01,并采用Cytoscape 3.9.1软件构建“潜在靶点-信号通路”网络图。
2 结果
2.1 相关药物靶点以OB≥30%且DL≥0.18为筛选标准,剔除未找到相关靶点的化合物后得到柴胡活性成分13种、黄芩活性成分33种,见表1、表2。将得到的柴胡、黄芩活性成分作用靶点合并,共获得216个药物相关靶点。
2.2 青春期后痤疮相关靶点、PPI网络与核心靶点青春期后痤疮英文名为ACNE,故以“ACNE”为关键词,从GeneCards数据库中获得青春期后痤疮的相关靶点,青春期后痤疮靶点共1 899个。将216个活性成分相关靶点与1 899个青春期后痤疮相关靶点导入VENNY在线工具(https://bioinfogp.cnb.csic.es/)进行映射,得到86个柴胡-黄芩治疗青春期后痤疮的潜在作用靶点,并绘制韦恩图。将数据导入Cytoscape 3.9.1软件,构建活性成分潜在靶点网络图(紫色菱形为潜在靶点,矩形为药物活性成分)。

表1 柴胡有效成分
将潜在靶点输入STRING11.0数据库构建 PPI 网络,并导入Cytoscape 3.9.1中进行可视化分析,图中节点为潜在靶点,边则为靶点间的相互关系。
使用CytoNCA插件挖掘核心靶点,参数为默认设置,通过EXECL取交集,即柴胡-黄芩作用于青春期后痤疮的核心靶点,排名前6位的靶点主要有肿瘤坏死因子 (tumor necrosis factor,TNF)、肿瘤蛋白p53 (tumor protein p53,TP53)、RelA(NF-κB亚型)、表皮生长因子受体(epidermal growth factor receptors,EGFRs) 、白细胞介素(interleukin,IL)-6、IL-1β。
结果见图1—图4,degree值越大,则图形中节点越大、颜色越深,说明该成分或该潜在靶点在柴胡-黄芩作用于青春期后痤疮中越重要。

图1 柴胡-黄芩药对治疗青春期后痤疮潜在靶点韦恩图

表2 黄芩有效成分

图3 柴胡-黄芩药对治疗青春期后痤疮潜在靶点PPI图
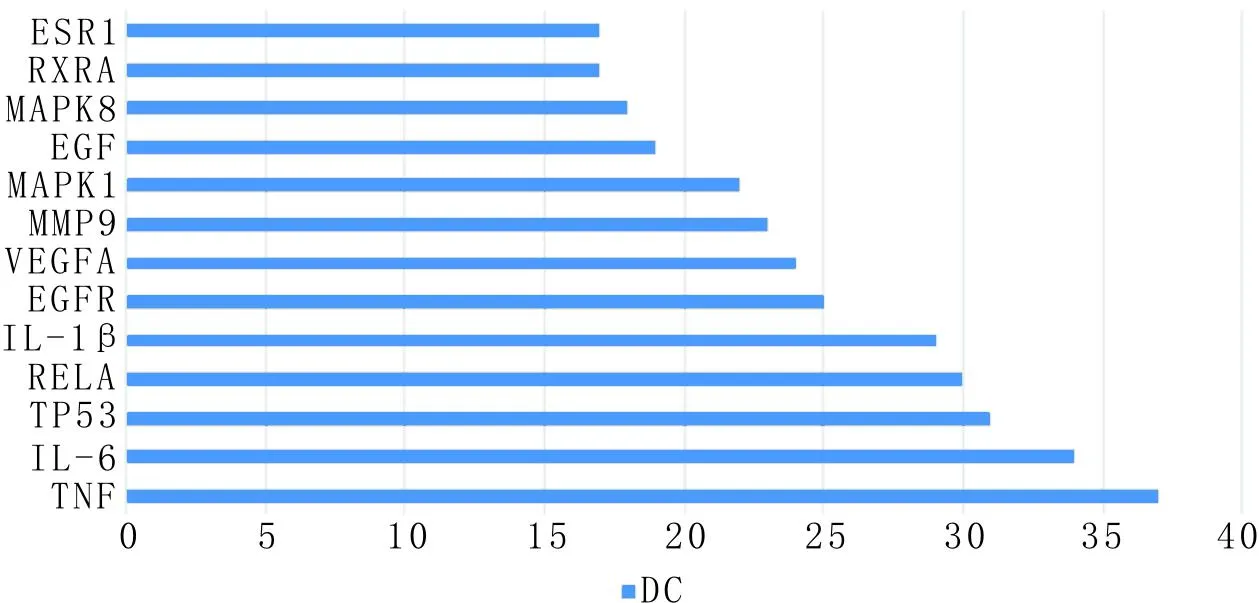
图4 柴胡-黄芩药对治疗青春期后痤疮的核心靶点预测
2.3 GO功能富集分析及KEGG信号通路富集分析GO功能富集分析共得到3 526个BP条目,设置P<0.01,根据P值排序后,选取排名前10位的条目绘制条形图,主要包括对脂多糖的应答(response to lipopolysaccharide)、对细菌的应答(response to molecule of bacteria origin)等。KEGG信号通路富集分析得到信号通路230条,设置P<0.01,并根据P值排序,选取前10位绘制气泡图,主要涉及通路糖尿病并发症相关通路(AGE-RAGE pathways in diabetic complications)、脂质和动脉粥样硬化(lipid and atherosclerosis)、流体剪切应力和动脉粥样硬化(fluid shear stress and atherosclerosis)、化学形式的癌症激活受体(chemical carcinogenesis-receptor activation)、IL-17 信号通路(IL-17 signaling pathway)、TNF信号通路(TNF signaling pathway)等。详见图5、图6。
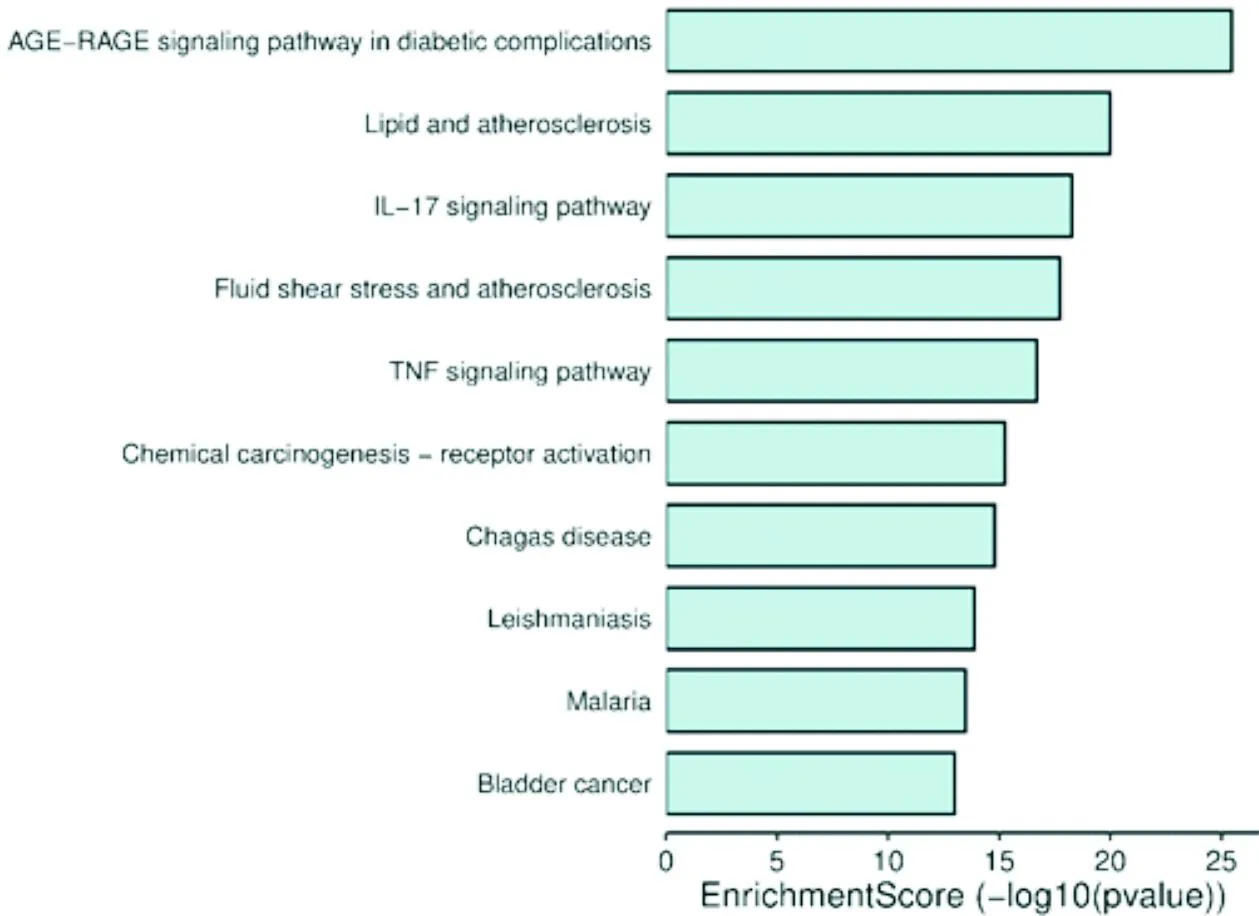
图5 柴胡-黄芩药对治疗青春期后痤疮 有效成分KEGG 富集

图6 柴胡-黄芩药对治疗青春期后痤疮GO富集
3 讨论
青春期后痤疮发病机制仍未完全阐明,发病机制涉及多种因素之间复杂的相互作用,目前普遍认为其发病与痤疮丙酸杆菌等毛囊微生物增殖及炎症和免疫反应、毛囊皮脂腺导管角化、遗传背景下激素诱导的皮脂腺过度分泌脂质异常相关[3]。本研究得出柴胡-黄芩治疗青春期后痤疮的潜在作用靶点86个,筛选出6个核心靶点,包括TNF、IL-6、TP53、RELA(P65)、IL-1β、EGFRs。根据KEGG富集分析预测通路主要为TNF信号通路、AGE-RAG信号通路及IL-17通路。GO富集分析结果显示,其主要生物过程包括对脂多糖(response to lipopolysaccharide)及对细菌的应答(response to molecule of bacteria origin)等。
脂多糖是发现于革兰阴性菌外膜的糖脂,可诱导单核细胞/巨噬细胞分泌促炎细胞因子,如TNF-α、IL-1及IL-6[14]。痤疮丙酸杆菌脂多糖与单核细胞受体上的膜突蛋白之间的结合可能是痤疮中单核细胞活化并随后释放各种炎性细胞因子的一种方式[15]。因此预测柴胡-黄芩可通过对细菌、脂多膜的应答来抑制痤疮丙酸杆菌增殖,从而抑制引起的炎症反应。作为正常皮肤菌群的一部分,痤疮丙酸杆菌在阻塞的毛囊中的增殖被认为是关键[16]。研究发现,痤疮丙酸杆菌可促进毛囊导管口角化,诱导皮脂生成,以及通过促炎分子的分泌和先天免疫的激活来刺激炎症反应,即通过激活TLR2信号通路产生IL-1β、IL-6和TNF-α,从而引起痤疮炎症[17-18]。
TNF信号通路可活化TNF-α,TNF-α是一种主要的致炎细胞因子,可通过多种信号通路诱导炎症反应。有研究认为,TNF-α基因多态性与痤疮的发病存在一定的相关性,TNF-α突变影响其表达,从而导致炎症反应改变[19]。TNF-α不仅可参与炎症反应,还促进人皮脂腺细胞的脂肪生成[20]。此外,有实验证实了痤疮丙酸杆菌在体外通过诱导特异性CD4(+)T细胞分泌IL-17A来促进Th17/Th1混合反应,因此,青春期后痤疮皮损中IL-17A阳性T细胞的存在和Th17相关细胞因子的激活表明Th17通路可能在疾病过程中发挥关键作用[21]。近年来的研究进一步阐明了痤疮的发病机制中免疫炎症因素在其中发挥重要作用[22]。一些学者认为,炎症是痤疮发病的关键组成部分,通过组织病理学和免疫组化检查发现痤疮患者面部无红肿炎症表现的痤疮皮损(如粉刺),甚至在皮损周围无皮损处的皮肤可以检测到炎症[23-25]。痤疮患者血清中 TNF-α、IL-6、IL-1β等炎症因子水平明显升高,且随着痤疮的严重程度而升高[26-28]。IL-1β已被证明是皮脂腺细胞的强IL-6诱导剂,IL-6是炎症反应的激动剂和催化剂,IL-6的高表达可介导并加剧痤疮样皮损的炎症反应[29-30]。炎症因子不仅在痤疮的一系列炎症过程中发挥重要作用,在痤疮诱导的增生性瘢痕的发展中也起关键作用:IL-1β的表达与痤疮后瘢痕的发生呈显著正相关[28];瘢痕疙瘩或增生性瘢痕组织中存在IL-6,有学者认为,针对这些细胞因子的生物抗体可能是未来预防和治疗痤疮及痤疮引起的瘢痕的潜在策略[31]。因此,可通过TNF信号通路抑制下游炎症因子表达,不仅减轻炎症反应,还可减少痤疮后期瘢痕的风险。
痤疮患者血清EGFR水平和表达水平是健康者的10倍[32]。EGFRs在皮肤发育和稳态中具有重要作用,有临床实验证实,重组人表皮生长因子可以改善中重度痤疮[33],这可能是由于EGF/EGFR信号在炎症和先天免疫反应中发挥重要作用,研究发现,抑制EGFRs可使由痤疮丙酸杆菌刺激的角质形成细胞中TLR2的表达及NF-κB活性下调,抑制 IL-1α、IL-8和TNF-α等促炎细胞因子[34]。不仅如此,EGFRs还可令皮脂腺过度增殖、使皮脂生成增加[1]。柴胡-黄芩作用于EGFR,减轻痤疮丙酸杆菌引起的炎症反应的同时,还可减少皮脂分泌。
有研究发现,抑制RELA的表达可改善痤疮炎症反应[35-36]。RELA是NF-κB的一种亚型,又称为p65。NF-κB是一组调节炎症反应、免疫系统、细胞死亡、细胞增殖和上皮细胞分化的蛋白,是许多促炎细胞因子基因上调的关键转录因子,可控制多种基因的表达,并形成细胞内信号转导系统的中心轴,在调节皮肤免疫稳态和炎症中发挥作用[37-38]。人类皮肤表达p65(RELA)和p50(NF-κB1),两者形成功能性NF-κB复合物,在非激活状态下p65和p50与细胞质中的IκB抑制剂结合,从而阻止 NF-κB 复合物进入细胞核;当机体出现炎性反应时,TNF-α和IL-1β激活IκB激酶复合物,经过磷酸化及泛素化后降解,释放p50/p65,从而使 NF-κB 复合物转运到细胞核,激活靶基因转录[16,39]。
AGE-RAGE是由晚期糖基化终末产物受体(receptor for advanced glycation end products,RAGE)与糖基化终末产物(advanced glycosylation end products,AGEs)结合而来,可以激活并促进炎性反应,最终可导致胰岛素抵抗[38,40-41]。有研究认为,青春期后痤疮与胰岛素抵抗有关[42]:表皮角质形成细胞表达胰岛素受体,高胰岛素血症可导致毛囊皮脂腺导管内的角质形成细胞异常增殖及脱屑,从而引起或加重痤疮。因此,有学者认为,痤疮和胰岛素抵抗存在共同的信号通路[43]。AGE-RAGE信号通路可激活下游通路:正常组织细胞中RAGE表达水平相对较低,当机体处于炎症、创伤等应激状态时,RAGE出现异常表达,产生氧自由基,引起氧化应激,激活NF-κB转录因子,进一步引发炎症连锁反应,使IL-6及TNF-α等炎症因子大量释放[44-45]。有学者认为,晚期糖基化末端受体可能与痤疮的发病机制有关[46]。AGE-RAGE信号的抑制可能有助于抵消炎症级联反应的进展[46]。
从中医角度分析药物发现,柴胡性轻清,主升散,味微苦,能祛散肌表。黄芩为苦寒清肃之药,功在除热邪。《本草汇言》载:“柴胡无黄芩不能凉肌达表”,即柴胡与黄芩相配,透邪散表兼清热。增值的痤疮丙酸杆菌通过分泌促炎分子和激活先天免疫来刺激炎症反应,面部出现丘疹、脓疱的过程从中医的角度理解,可以被认为是外邪侵袭肌表而致生热,柴胡-黄芩的功效重在祛邪清热,即祛除痤疮丙酸杆菌——外来邪气,兼清炎症反应之热。
柴胡-黄芩不仅可能参与对脂多糖及细菌的应答,减少痤疮丙酸杆菌增殖,通过作用于各通路(AGE-RAGE信号、TNF信号通路及IL-17通路)、各靶点(TNF、IL-6、RELA、IL-1β、EGFRs)来抑制痤疮丙酸杆菌引起的青春期后痤疮的炎症和免疫反应,还能通过TNF-α及EGFRs靶点作用于皮脂腺,从而抑制皮脂生成,来治疗青春期后痤疮,从而发挥有效的抑菌抗感染作用,还能抑制痤疮瘢痕的形成。

