电解水催化剂界面结构调控研究进展
王 硕,张浩楠,杨 英
(中国石油大学(北京)化学工程与环境学院,北京 102249)
近年来,随着政策的持续发力和技术的不断升级,我国可再生能源实现跨越式发展。《氢能发展规划》明确了氢能的三大战略定位:氢能是未来国家能源体系的重要组成;氢能是用能终端实现绿色低碳转型的重要载体;氢能是战略性新兴产业和未来产业重点发展方向。氢能按照其制取方式,可以分为灰氢、蓝氢和绿氢3种。与通过化石燃料燃烧发生化学反应制灰氢、甲烷蒸汽或自热蒸汽重整制蓝氢不同,利用可再生能源制绿氢具有零碳排放的优点。其中,电解水制绿氢可规模化、可持续性生产。电解水制氢过程主要涉及析氢反应(HER)与析氧反应(OER)。目前,电解水制氢由于其效率较低、成本较高还无法大规模应用。因此,开发高效催化剂来提升电解水效率是当前工作的核心。众所周知,优良的电解水催化剂应具有丰富的催化活性位点、高电子导电率和优异稳定性等特点。而界面工程能够调变催化剂以获得新的物化性质和协同效应,大幅提升电催化活性与稳定性。
在纳米催化剂中界面是纳米催化技术的核心,任何化学反应都是在界面处吸附、反应、脱附,完成整个反应历程。催化剂界面能否成为多相催化反应的主要场所是由物体界面处原子排布或分子结构所决定的,不同界面具有不同的吸附选择性,界面所呈现的反应性能与界面结构密切相关。催化剂的界面结构具有多样性,其种类、制备方法及化学环境会影响界面结构。只有研究催化剂界面结构,了解不同界面的性质,建立界面结构与催化性能的构效关系,才能更好指导高效催化剂的设计与制备。然而,目前多集中于界面调控的具体研究,尚缺乏对界面结构调控强化电解水性能的系统总结。因此,对此领域工作进行全面综述至关重要,以期为后续研究提供参考。基于此,以下重点综述HER和OER高效电解水催化剂界面工程的研究进展,具体深入探讨界面工程对电解水催化剂性能的影响,主要介绍支撑界面、核壳界面及异质界面相关催化剂及界面结构调控策略,并综述其发展前景。
1 电解水原理
水分解[1]被认为是最有前途、可持续的产氢途径,该方法具有诸多优势:①原料是地球上丰富的可再生资源;②不排放温室气体或污染气体;③可产生纯净的H2。然而,实现电解水高效产氢,需要克服电解池阳极析氧过电位高、动力学缓慢的问题。因此,高效电解水催化剂需兼具优异的HER、OER性能。图1展示了HER和OER的作用机制。HER是发生在阴极表面产生氢分子的双电子转移过程,主要有两种机制,Volmer-Heyrovsky[图1(a)]与Volmer-Tafel[图1(b)];OER是四步电子转移(AEM)过程[图1(c)],涉及多个反应中间体。

图1 HER和OER的作用机制
1.1 HER
通常,HER是一个多步电化学过程,根据电解液pH的不同,会遵循不同的路径。在碱性条件[2]下,电解液中的H+极少,HER进行较为困难,其反应所需的质子一般由水分子解离提供。因此,与酸性条件相比,碱性环境中HER解离水分子需要更高的能量。
第一步是电化学氢吸附过程(Volmer反应),方程式如下:

(1)

(2)
第二步有两种路径生成H2。当H*覆盖度较低时,发生Heyrovsky反应,方程式如下:

(3)
碱性溶液:

(4)
当H*覆盖度较高时,发生Tafel反应,方程式如下:

(5)
其中H*为化学吸附在电极表面的活性位点。这些反应路径依赖于电极表面固有的化学和电子特性,可从极化曲线的Tafel斜率确定决速步骤。
1.2 OER

基础反应式为:

(6)

(7)

(8)

(9)

(10)
酸性或中性溶液中反应式为:

(11)

(12)

(13)

(14)

(15)
OER的两条路径均由反应中间体的吸附和脱附组成,其中反应中间体代表催化剂表面的活性位点。对于析氧反应,最困难的一步是*OOH的生成。理论上,从*O开始形成*OOH需要1.23 V的电位,因此需要1.23 V的电压来驱动OER过程。从OER机理来看,调控反应中间体在催化剂表面的吸附和脱附是实现高OER性能的重要策略。
2 界面分类
界面结构调控策略[3-5]被广泛用于增强电催化活性。电解水催化剂界面结构的合理设计可有效构建并增加活性位点、提升电导率和优化中间体的吸附/脱附行为。由于单组分结构催化剂的性能不尽人意,三组分以上的多界面具有复杂性,因而,双组分界面结构成为研究热点。以下主要介绍如图2所示的3种双组分界面结构[6]。
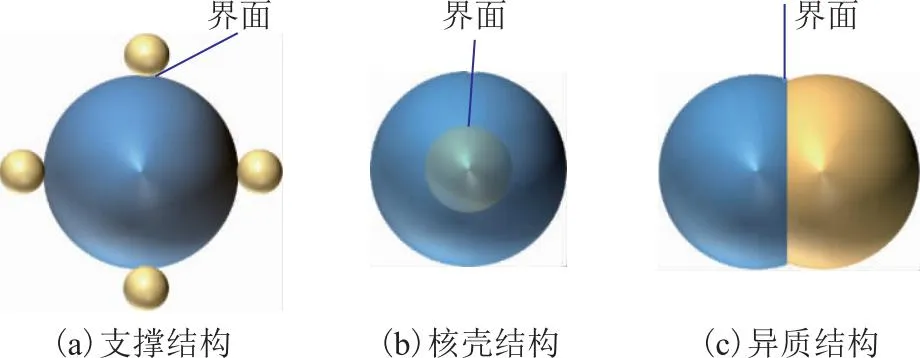
图2 3种典型的界面结构—组分1; —组分2
2.1 支撑结构界面
支撑结构是指在尺寸较大的物种表面负载尺寸较小的活性物种,如一维纳米线上的0D纳米点、二维纳米片上的0D纳米颗粒、三维块体上的0D纳米颗粒[7]、三维集流体上的2D纳米片和一维纳米线上的2D纳米片等。如图2(a)所示,通过组装一定量的组分1,可以合成具有支撑结构的材料。在这种模式下,组分1和组分2之间的界面面积离散,通常可以通过调整组分1和组分2的相对比例来调节界面面积的分布。Lü Xinding等[8]采用可控的阳离子交换策略,制备了自支撑的Co掺杂NiP纳米片阵列电极,粗糙的纳米片阵列结构使电极具有超疏气-亲水的能力。Wu Libo等[9]制备了一种Ni和MoN纳米颗粒负载到非晶态MoN纳米棒上的非均相催化剂,分级的纳米棒-纳米粒子结构以及大的比表面积和多维边界缺陷赋予催化剂丰富的活性位点。
2.2 核壳结构界面
核壳结构参照图2(b),其是组分1生长在组分2表面的复合结构,内层组分被外层组分完全包裹,组分1表面暴露在外作为活性组分。由于核与壳之间的多重相互作用,核壳材料引起了广泛关注,在电解水上的应用探索与日俱增。Zhang Wen等[10]通过一步湿化学法合成了具有特定形貌和(111)晶面的新型Ag@Pt二十面体纳米晶HER催化剂,该Ag@Pt(111)纳米颗粒的d带中心比Pt(111)纳米颗粒远离费米能级,使H*在其上的最佳吸附自由能(ΔGH*)远低于在Pt(111)纳米颗粒上的最佳吸附自由能,削弱了H*的吸附,进而促进HER过程。Sheng Hongbin等[11]利用晶态材料设计了一种花椰菜状Fe掺杂Co-Ni亚磷酸盐核壳结构的催化剂,这种晶态@非晶态核壳纳米棒组装的花椰菜状分级结构可有效避免纳米棒团聚,实现催化反应中气体扩散和离子传输的协同优化。Jiao Jiqing等[12]通过热解-氧化磷化等策略制备出Co@Co-P@N核壳结构与P共掺杂碳纳米管耦合的催化剂,这种核壳结构界面不仅保护Co不被腐蚀,还促进Co参与电子转移。
2.3 异质结构界面
宏观上,异质结是由两种不同的半导体相接触所形成的界面区域。按照材料导电类型不同,异质结可分为同型异质结(p-p结或n-n结)和异型异质结(p-n结)。微观上,如图2(c)所示,尺寸相近的组分1和组分2被一个连续的表面束缚形成单个颗粒,形成异质结构,并在两个组分之间形成界面。复合材料的典型异质结构体系一般包括金属/金属(合金)[13-14]、化合物/化合物[15]、金属/化合物[16]、基底中的杂化物[17]等类别。其中,金属/化合物异质界面对于调控复合材料的物理化学性质具有重要意义。特别地,异质结构中的协同效应和强界面相互作用可以提高电荷转移能力并诱导电子耦合效应,最终优化反应步骤的自由能并提高活性。几种异质结构催化剂的性能见表1。由表1可知,过渡金属磷化物[18-19]、过渡金属硫化物[20]、层状双金属[21]等是制备异质结构材料的首选。
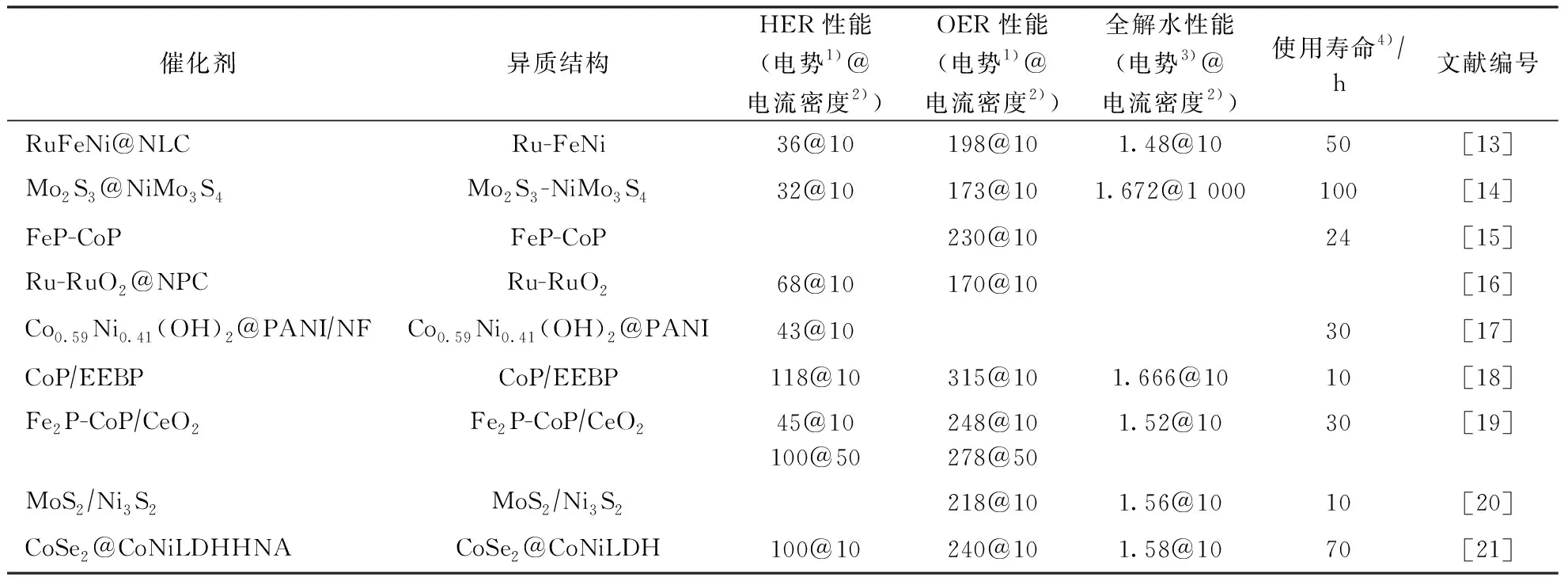
表1 几种异质结构催化剂的性能

表2 不同界面调控策略下的催化剂性能
3 界面结构调控策略
界面作为催化剂发生反应的主要场所,其结构与催化剂活性、稳定性直接相关。目前,界面结构调控策略包括引入缺陷、重构表面、调节晶面、形成合金结构、结合应变工程以及构建单原子界面等,下文将对这些调控策略进行详细介绍。
3.1 引入缺陷
缺陷可以调节材料的表面和电子性质,在电化学反应中发挥着积极作用。缺陷普遍存在于催化剂中,可诱导电荷重新分布,提高导电性,优化催化剂的吸附能,进而影响电催化活性。缺陷类型包括0D点缺陷、1D线缺陷、2D面缺陷和3D体缺陷[22]。本部分将重点综述不同类型缺陷调控界面结构方法。
3.1.1掺杂杂原子
杂原子掺杂是能源相关应用中最受欢迎和广泛使用的方法。通过掺杂少量杂原子可简易调控材料的电子结构。N,P,S,B,Co,Fe,Al等元素已被证明是高效的掺杂剂。目前,直接将杂原子掺杂到基体中或双重掺杂主要有3种途径:第一种是通过各种化学试剂和气体进行后处理;第二种是在合成含杂原子前躯体材料的过程中进行原位掺杂;第三种是通过热解金属有机框架(MOF)或生物质。众所周知,杂原子的种类、掺杂量和掺杂位置都很大地影响催化性能。Guo Mengzhi等[23]采用四乙基戊胺(TEPA)还原策略合成了NC包裹的Ni3Fe合金纳米片Ni3Fe-NC/NF,TEPA中丰富的胺基易与镍、铁结合,使其自身能较好地吸附在NiFe-LDH表面。Xia Liucheng等[24]以壳聚糖为生物质N和C源,通过简单方法合成了一维S修饰的MnCo2O4纳米棒与二维N掺杂的C纳米片复合的多维杂化材料,其中S掺杂可以促进弱的M—O键和M—S键(M代表金属原子)形成,有效优化活性位点,改变决速步骤并降低能垒。
3.1.2引入空位
空位引入是提升电催化性能的有效策略之一,主要包括O空位、S空位及金属阳离子空位等。理论和试验结果表明,空位可以降低反应能垒,有利于水分子或中间反应物种的吸附/脱附,从而优化反应动力学。空位也可以促进活性位点的暴露或提高活性位点的密度。此外,空位的引入可以形成新的带隙态或缩小催化剂的带隙,从而提高催化剂的导电性。因此,理性设计材料中的空位可以提升电解水催化剂的性能。
O空位是氧离子从含氧化合物晶格中逸出而留下的缺陷。理论计算证明O空位可以激活相邻O原子对H原子的吸附,有利于水分子的解离,提高对HER和OER的催化活性。Li Guanglan等[25]采用水热与H2煅烧法制备出一种负载N-NiMoO4/Ni异质结纳米颗粒的三维网络结构碳纳米管催化剂。在还原性气氛煅烧后,N-NiMoO4/Ni异质结纳米颗粒中产生大量的氧空位,协同调控异质结构的电子结构,促进反应中间体的脱附,加速HER和OER过程。硫空位与氧空位类似,硫空位与异质界面之间的协同作用也有利于提高电解水的催化性能。Xiao Yuanhua等[26]通过溶剂热法合成双金属CuCo2S4,热解后产生的不连续异质结构界面富含S空位。同时,通过密度泛函理论(DFT)模拟,证明S空位和异质结构界面优化了电子结构和HER中间体的吸附。由于多样的电子和轨道分布,引入金属阳离子空位可显著改变催化剂的特性。Wang Liming等[27]利用简便温和的原位氧化技术获得层状α-NixFe1-x(OH)2/CNTs负载的Pt单原子催化剂。Fe(OH)2被氧化为FeOOH并形成Fe空位,Pt原子被原位锚定在Fe空位上,从而形成稳定的Pt单原子催化剂,具有优异的电解水性能。
3.1.3形成边缘位点
边缘位点的引入也被证明有利于提升OER和HER性能。边缘丰富的缺陷和杂原子掺杂缺陷可以重新分配局域电子密度,对中间体有更强的亲和力,对确定活性位点至关重要。Thomas等[28]确定了纳米颗粒MoS2的HER活性位点。DFT计算结果表明,MoS2纳米粒子的边缘位点对HER具有活性。从MoS2面积覆盖率和MoS2边缘状态的关系可以得知,反应速率与边缘位点数量成正比,与颗粒大小无关,即边缘位点为活性位点。
合理设计催化剂的纳米结构以充分暴露边缘位点,对于优化其电催化性能极为重要。Wang Bingqing等[29]以金属有机骨架纳米片阵列为结构导向模板,通过结构继承策略合成了具有丰富配位不饱和位点的边缘富集NiFe双氢氧化物纳米阵列(NiFe-LDH)。研究显示,NiFe-LDH边缘位点中存在大量的铁空位和氧空位。DFT计算结果表明,这些氧空位和铁空位能有效地调节水滑石的电子结构,优化其对OER中间体的吸附,大幅提高电催化析氧性能。Jiao Han等[30]以钼酸盐NiFe(MoO4)x棒作为前体合成出超细Mo修饰NiFeOxHy的氢氧化物纳米片阵列(Mo-NiFeOxHy),这种致密的超细纳米片阵列表面存在丰富的阶梯状边缘平面,暴露出大量的活性位点,优化后的催化剂具有优异的OER催化性能。
3.2 重构表面
随着原位表征技术的发展,越来越多的报道揭示了前催化剂表面位点动态重构为真实的活性物种的机理。这种原位重构过程可以调节吸附、活化和脱附等电催化行为,从而提高催化性能。因此,研究者们利用电解水催化剂的重构现象来获得大量的活性物种。Zhai Wenfang等[31]设计了双金属NiM(M为Fe或Pd)共价限域耦合的p型黑磷(BP)结构,并研究层间限域对其析氢/析氧性能的影响。研究发现,在非氧化物体系会出现表面抗重构现象,揭示了其金属位点缺电子态表面重构增强机制。得益于限域封装的保护作用,NiFe-BP和NiPd-BP粉体催化剂在碱性电解质中表现出优异的电催化活性和稳定性。
研究人员发现某些化合物在碱性水解过程中可作为催化剂模板[32],其产生的不可逆重构层作为真正的催化剂参与产气过程,提高了其催化活性和动力学。Ji Pengxia等[33]开发了一种负载在泡沫镍上的富氟氟化镍(NiF2)作为牺牲模板,在碱性介质中快速构建高效的HER和OER双功能催化剂。研究表明,仅经过100次CV(循环伏安法)循环,NiF2模板完全重构为HER用Ni(OH)2和OER用NiOOH,两者都具有相互连通的纳米催化单元、丰富的缺陷和多孔的大比表面结构等特点,可显著降低过电位,从而表现出优异的HER和OER稳定性。
3.3 调节晶面
对于特定物相催化剂,不同晶面之间的化学组成和界面数量对电催化活性有显著影响。众所周知,费米能级的d带和p带中心可以很好地反映HER和OER过程中间体的吸附能和活化能垒。界面工程被认为是实现组分间界面电荷转移的d带中心调控的有效手段。目前关于过渡金属异质结构的报道主要是晶体-晶体复合物,界面晶格畸变会在一定程度上受到晶格电阻或结构刚性的阻碍。在此背景下,建立非晶-晶体[34-36]异质结构将是调控d/p带中心和电子结构的一个新兴方向。Liu Yaoda等[37]从理论上描述并构建了由CoBOx和NiSe组成的非晶-晶体异质结构,作为非贵金属催化剂用于电解水。研究表明,由于Co—Co配位键的缩短和B活性位点的离域,结晶-非晶界面调节了表面原子的d-p带中心能级。降低的d-p带中心差和增强的d-p带相接近,平衡催化中间体的相互作用,进而提升析氢反应与析氧反应的活性。
3.4 形成合金结构
合金一般是指由两种或两种以上的金属共同形成的化合物,其结构能有效提高催化剂活性。双金属合金是合金家族的主体,其中过渡金属合金作为碱性析氢反应的电解水催化剂受到广泛关注。Wang Jinsong等[38]通过对一系列Ni-M双金属合金的氢吸附能(ΔGH)的研究发现,ΔGH与修正后的d带中心呈线性关系,NiCu电解水催化剂具有最佳ΔGH。研究还表明,这种为水解反应定制的电催化位点可协同加速多步碱性HER过程。
高熵合金(HEA)作为一种具有特殊微观结构的新型材料,具有比传统材料更优异的力学和化学性能,在电催化领域也有优异表现。HEA中多组元协同产生许多新的活性位点。Liu Hao等[39]通过一步法脱合金制备了纳米多孔NiCoFeMoMn高熵合金,可作为HER和OER的双功能催化剂,并经过调幅分解过程形成类异质结结构。DFT计算结果表明,独特的类异质结结构在优化氢吸附过程的同时增强了水吸附能,协同促进了高熵合金催化剂的HER性能。
3.5 结合应变工程
应变工程是一种很有前景的策略,可以设计用于可持续能源存储和转换的各种电化学催化剂,然而在此方面仍面临众多挑战。因此,研究者们希望通过应变工程来调变电化学催化剂的本征活性,为多功能催化剂的设计开辟新途径。Jiang Zhuoli等[40]设计了一种非传统的肖特基催化剂,即在氮修饰的碳纳米片上负载具有晶格压应力的均匀超细钌纳米粒子,用于HER。晶格应变和肖特基结的双重调控确保RuNPs/NC催化剂具有适当的氮含量,在碱性介质中表现出极好的析氢性能。
核壳结构可以通过结合应变和配体效应调控中间体的吸附/脱附动力学,通过调变d带中心调控HER催化剂中间体结合能,进而优化反应活性。Qiu Yu等[41]将晶格失配应变核/壳Ru/RuO2纳米晶体锚定在氮掺杂碳纳米片上,制备了一种优异的三功能电解水催化剂。核/壳Ru/RuO2纳米晶体具有约5个原子层的RuO2壳,可消除配体效应并产生约2%的表面压缩应变,显著提高催化剂的三功能活性。Li Yapeng等[42]通过热控制氧化Ru/C杂化微片精确地合成出一种核-壳异质结构,成功在Ru核上形成富含氧空位的RuO2亚纳米皮层。Ru@V-RuO2/CHMS催化剂由于核-壳异质结构调制的界面电子结构与应变效应,在宽pH范围内具有优异的双功能HER和OER性能。
3.6 构建单原子界面
单原子催化剂因其孤立的活性位点、独特的电子结构和几何结构以及100%的利用率,在催化领域具有重要研究价值。近年来,催化机理逐渐拓展到原子尺度,进一步揭示了单原子与载体之间的界面效应对电解水的影响机制。Feng Chen等[43]以CoOOH为载体,构造具有相似IrO6配位的两种Ir单原子催化剂,研究提出单原子界面对电化学析氧反应的调控机制。根据DFT计算及原位谱学表征,晶格掺杂中Ir—Co之间的电子相互作用导致Co的d带中心上升,两者之间的电子效应促进了OER反应中间体的吸附强度;对于吸附的Ir—Co来说,它们之间的电子效应并不明显,而是通过几何效应协同Co位点改变了对中间体的吸附,相比电子效应更有效降低了OER反应能垒。
单金属位点与载体之间存在较强的共价键和离子键,因而表现出优异的稳定性。然而,在电催化过程中,单原子更容易发生迁移和团聚,因此如何稳定和制备高密度的单原子催化剂仍然是一个难题。Gao Taotao等[44]设计了氧配位单原子铁位点(Fe-O4)修饰的多孔碳纳米管作为锚定钌(Ru)团簇的高效载体,CNT-V-Fe-Ru 在酸性和碱性介质中均表现出优异的电催化析氢性能。该载体可以显著提高Ru活性位点的本征活性。
此外,单原子金属物种稳定性差、大电流密度低的问题也引起了高度重视。Mu Xueqin等[45]发现,亲氧金属(Ru)物种在FeCo-LDH中的单原子位掺杂可有效破坏其对称结构,形成Ru-O-TM类纳米化合物。试验和DFT计算结果表明,FeCo-LDH被Ru原子部分取代,杂原子界面的长程有序被打破,从而在对称性处进行原子尺度重构,Ru单原子和FeCo-LDH基体之间形成强耦合肖特基界面,催化剂在工业标准电流密度下表现出非凡的水解性能。
总之,界面作为反应发生的场所,在催化反应中发挥着关键作用,因此调控策略会为电解水催化剂带来多种多样的催化性能。不同界面调控策略下的催化剂性能如表2所示。
4 总 结
电解水制绿氢是可再生能源领域关键技术之一,通过设计和调控电解水催化剂界面结构开发高性能电极材料为当前的研究热点。界面结构调控可赋予催化剂更大的电化学活性面积、优化的电子结构、适宜的吸附能及更强的协同效应,从而产生优异的电催化性能。综述了通过界面工程设计HER和OER高效电解水催化剂的最新研究进展,为制备高效电解水催化剂提供指导。尽管目前该领域的研究已取得长足进展,但是仍有几个关键问题亟待解决。
众多界面调控策略已被报道,但其不同组分之间界面效应的决定性因素仍不清楚。因此,还需要对反应过程及催化剂进行分子-原子尺度结构研究,以深入理解电催化反应机理。大多数电解水催化剂的界面构筑通常受限于两种或三种组分的化学键合,纳米组装的多界面构筑及调控尚面临挑战。从实际应用角度考虑,应开发更简便、更可靠的合成策略,以制备具有高质量界面、低成本、高效催化剂,并拓展电解水催化剂的功能。在实际反应条件下,活性位的电催化性能受多种因素影响,界面结构越接近理论模型,其构效关系越明确。将理论计算与试验相结合,弥补理论与试验研究之间的鸿沟,将有助于高性能界面构筑。

