7-甲氧基黄酮及衍生物的合成与体外抗乳腺癌细胞活性
郑高亮,孔 飞,谷 沚,余心哲,郁建平*
1贵州大学药学院;2贵州大学生化营养研究所,贵阳 550025
黄酮是一类重要的天然有机化合物,研究发现黄酮类化合物具有抗肿瘤以及逆转肿瘤多药耐药的活性。由于黄酮类化合物的作用明确,毒性较低,因此对黄酮类化合物的研究仍是寻找具有较好抗肿瘤活性的先导化合物的重要方向之一,并且有着广泛的应用前景。药理活性也是多种多样,包括抗肿瘤、抗病毒[1]治疗心血管疾病、骨质疏松等。
Hussein 等[2]先后预测和发现了黄酮类化合物具有防癌抗癌作用。黄酮类化合物主要通过三种途径来达到防癌、抗癌的作用,即抗自由基作用、直接抑制癌细胞生长和抗致癌因子等[3]。Yerra 等人[4]将黄酮母核的A,B 环进行化学修饰,合成了一系列黄酮A,B 环的甲氧基取代物,并研究它们对细胞分裂周期进程及肿瘤细胞增长的影响。黄酮母核上各取代的结构如图1 所示:
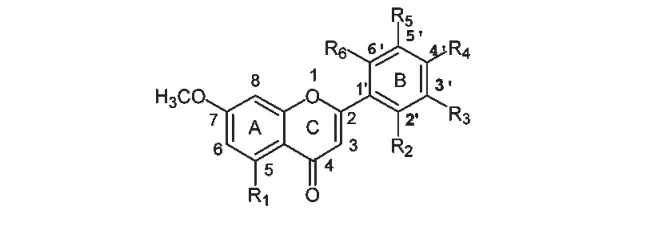
图1 黄桐A、B 环上的结构取代Fig.1 Structural substitution of flavone A and B rings
以上化合物对淋巴癌细胞周期进程的影响如下:当R1为羟基时,R2亦为羟基或R2和R3同时有甲氧基取代的化合物能选择性的阻断细胞的G2/M期;其中R2和R3同时有甲氧基的化合物对细胞周期进程影响最显著。当R1为甲氧基时,R2,R3或R2,R5也同时有甲氧基取代的化合物也能选择性的阻断细胞的G2/M 期;但没有化合物对淋巴癌细胞S 期有抑制活性。
Jean 等人[5]对黄酮的A 环和B 环进行结构修饰,并在结肠癌细胞(HT-29)中进行诱导Caspase 体外活性筛选。Caspase 蛋白家族在肿瘤细胞凋亡途径中发挥着不可替代的作用,活化Caspase 诱导肿瘤细胞凋亡是肿瘤治疗的一条新途径。
参考了以上内容我们合成了7-甲氧基黄酮及衍生物并对合成的目标化合物进行体外抗乳腺癌MDA-231 细胞活性实验。希望得到有抗癌活性的先导化合物,为进一步抗癌药物结构优化和活性研究奠定基础。
1 仪器与材料
1.1 仪器
数字熔点测定仪WRS-1B(苏州市丰盛电子科技有限公司);Varian INOVA-400MHz 型核磁共振仪(CDCl3、DMSO 作溶剂),TMS 为内标,美国瓦里安公司;FINNIGAN-LCQADVATAGE MAX 型质谱仪(赛默飞世尓科技公司);ZF-2 型三用紫外仪(上海安亭电子仪器厂);RE-52AA 旋转蒸发仪(上海亚荣生化仪器厂);电磁式空气压缩机(广东海利集团有限公司);78-1 型磁力热搅拌器(上海纵跃电子科技有限公司)。
1.2 试剂
柱层层析硅胶(100~200 目,300~400 目,青岛海洋化工厂);实验原料(2,4,6-三羟基苯乙酮,2,4-二羟基苯乙酮,DMF,固体氢氧化钠,30% H2O2,各种苯甲醛类化合物);分析纯(乙酸乙酯,甲醇,石油醚,二氯甲烷,氯仿,硫酸二甲酯,上海晶纯生化科技股份有限公司提供)未经处理,直接使用。
2 实验原理
2.1 黄酮及黄酮醇[6]化合物1~9 的合成路线
黄酮及黄酮醇化合物1~9 的合成路线如图2所示:
2.2 黄酮衍生物的合成路线
2.2.1 化合物10 的合成路线
化合物10 的合成路线如图3 所示:
2.2.2 化合物11 的合成路线
化合物11 的合成路线如图4 所示:
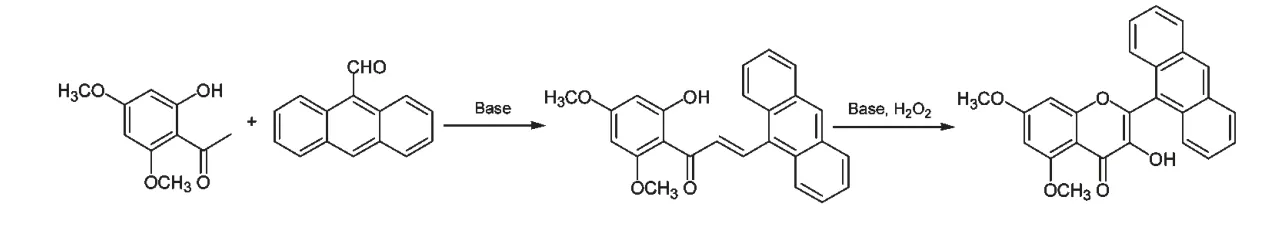
图3 2-蒽基-5,7-二甲氧基黄酮醇的合成Fig.3 The synthesis of 2-anthryl-5,7-dimethoxy flovonol
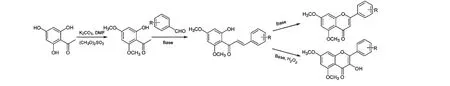
图2 5,7-二甲氧基黄酮及黄酮醇的合成Fig.2 The synthesis of 5,7-dimethoxy flavone and flavonol
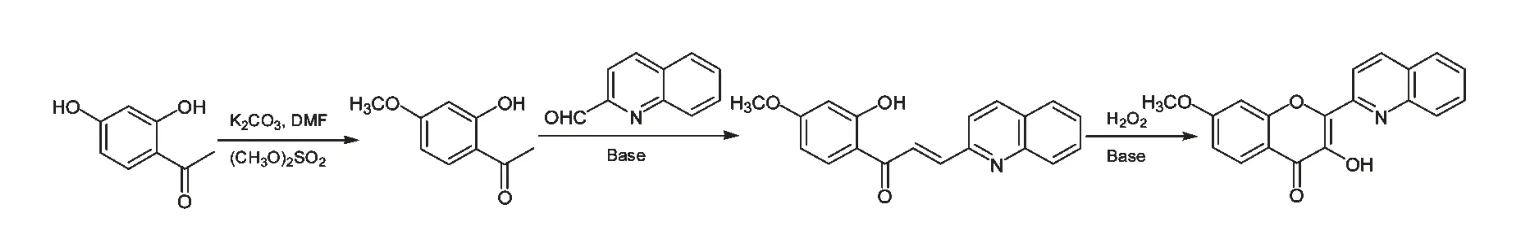
图4 2-喹啉基-7-甲氧基黄酮醇的合成Fig.4 The synthesis of 2-quinolyl-7-methoxy flovonol
2.2.3 化合物12 的合成路线
化合物12 的合成路线如图5 所示:

图5 7,2',3',4'-四甲氧基黄酮醇的合成Fig.5 The synthesis of 7,2',3',4'-butamethoxy flovonol
3 实验步骤
3.1 酚羟基苯乙酮的甲基保护
在250 mL 圆底烧瓶中加入40.0 mmol(6.72 g)2,4,6-三羟基苯乙酮,并加入25 mL 98% N,N-二甲基甲酰胺使之充分溶解,再加入82.0 mmol(11.32 g)K2CO3固体,在常温下,在磁力搅拌器中充分搅拌15 min,后加入84.0 mmol(10.58 g)Me2SO4,在常温下充分搅拌5 h,加入10 mL 水,再分别用15 mL 乙酸乙酯萃取若干次直到乙酸乙酯层在薄层板上层析没有原料为止,将萃取所得有机层在旋转蒸发仪中除去溶剂。将所得的浓缩液拌样,60 ℃烘干,并用石油醚:乙酸乙酯(15∶1)柱层析,得到4,6-二甲氧基-2-羟基苯乙酮,白色固体产率,75%;mp:77.0~77.1 ℃。1H NMR (400 MHz,CD3OD)δ:2.64(3H,s,COCH3),3.85 (3H,s,CH3O),3.86 (3H,s,CH3O),5.92(1H,s,C3-H),6.25(1H,s,C5-H),12.92(1H,s,OH);ESI-MS m/z:197([M+H]+),219([M+Na]+),415([2M+Na]+)。
3.2 新型黄酮、黄酮醇及其衍生物的合成
在100 mL 的圆底烧瓶中加入3.0 mmol 2-羟基苯乙酮类化合物和3.0 mmol 苯甲醛类化合物混合均匀,加入30 mL 的无水乙醇充分溶解,再加入2.5 mol/L NaOH 溶液1.5 mL,控制温度在30 ℃条件下充分搅拌,利用薄层层析确定反应终点,所得的物质乙酸乙酯-石油醚成比例进行梯度柱层析,所得物质通过质谱、核磁共振确定2-羟基查尔酮类化合物的结构,后在过氧化氢的碱性条件下合成相应的黄酮化合物。具体如下化合物及图谱数据表征:
3.2.1 黄酮化合物的合成
5,7-二甲氧基-2',3'-氯黄酮1,淡黄色固体,产率:78%,mp.220.3~220.8 ℃;1H NMR(400 MHz,CDCl3)δ:3.96(3H,s,CH3O),4.01(3H,s,CH3O),6.19(1H,d,J=4.0 Hz,H-3),6.41(1H,d,J=4.0 Hz,H-6),7.23(1H,d,J=8.0 Hz,H-8),7.26(1H,d,J=8.0 Hz,H-5'),7.49(1H,d,J=8.0 Hz,H-6');13C NMR(100 MHz,CDCl3)δ:180.1(s,C=O),169.3,169.1,159.7(s,C-2),149.1,133.7,133.5,132.9,130.5,129.9,127.1,105.7(d,C-3),94.3,89.4,77.3,77.0,76.7,56.3,56.2,29.7;ESI-MS:353(M+H)。
5,7,2'-三甲氧基-3',5'-二溴黄酮2,灰色固体,产率:82%;mp.193.8~194.5 ℃;1H NMR(400 MHz,DMSO)δ:3.82(3H,s,CH3O),3.91(3H,s,CH3O),3.94(3H,s,CH3O),6.39(1H,d,J=4.0 Hz,H-3),6.69(1H,d,J=2.8 Hz,H-6),6.80(1H,d,J=1.6 Hz,H-8),7.97(1H,d,J=2.0 Hz,H-4'),8.23(d,J=2.4 Hz,1H,H-6');ESI-MS m/z:493(M+Na),963(2M+Na)。
3'-硝基-5,7-二甲氧基黄酮3,深黄色固体,产率:66%;mp.230.2~231.9 ℃;1H NMR(400 MHz,DMSO)δ:3.91(3H,s,CH3O),3.95(3H,s,CH3O),6.74(1H,d,J=4.0 Hz,H-3'),6.81(1H,d,J=1.2 Hz,H-6),7.52(1H,d,J=4.0 Hz,H-8),7.80(1H,d,J=8.0 Hz,H-5'),8.26(1H,dd,J=1.2 Hz,2.0 Hz,H-4'),8.35(1H,d,J=16.4 Hz,H-6'),8.76(1H,dd,J=2.0 Hz,4.0 Hz,H-2');ESI-MS m/z:350(M+Na)。
5,7,2',4',5'-五甲氧基黄酮4,橘黄色固体,产率:61%,mp.211.5~212.0 ℃.1H NMR(400 MHz,DMSO)δ:3.72(3H,s,CH3O),3.79(3H,s,CH3O),3.82(3H,s,CH3O),3.91(s,CH3O),3.92 (s,3H,CH3O),6.23(d,J=2.0 Hz,1H,H-3),6.47(d,J=4.0 HZ,1H,H-8),6.62(3H,d,J=2.0 Hz,1H,H-6),7.72(1H,s,H-3'),8.24(1H,d,J=10.0 Hz,H-6');13C NMR(100 MHz,CDCl3)δ:180.7(s,C=O),169.1,168.7,159.3(s,C-2),153.0,147.2,139.3,127.8,111.3(d,C-3),108.4,104.9,93.9,89.1,77.3,77.0,76.7,60.8,56.0,55.9,49.1,48.9,48.7,29.5;ESI-MS m/z:373(M+H),375(M +Na),767(2M+Na)。
5,7,3',4',5'-五甲氧基黄酮5,黄色固体,产率:65%;mp.208.0~209.2 ℃;1H NMR(400 MHz,DMSO)δ:3.75(3H,s,CH3O),3.78(3H,s,CH3O),3.91(3H,s,CH3O),3.94(1H,s,CH3O),3.96(3H,s,CH3O),6.34(1H,s,H-3),6.70(1H,s,H-8),6.74(1H,s,H-6),7.13 (1H,d,J=1.2 Hz,H-C2'),7.27(1H,d,J=2.0 Hz,H-6');13C NMR(100 MHz,CDCl3)δ:178.9(s,C=O),168.9,168.2,158.9(s,C-2),153.0,146.7,139.0,127.6,110.0(d,C-3),108.7,104.0,94.5,90.0,79.0,60.2,56.6,56.2,56.0,40.1,39.9,39.7,39.5,39.3,39.1,38.9;ESIMS m/z:373(M+H),395(M+Na),767(2M+Na)。
5,7,2'-三甲氧基黄酮6,黄色固体,产率:58%;mp.224.8~225.0 ℃;1H NMR(400 MHz,CDCl3)δ:3.90(3H,s,CH3O),3.92(3H,s,CH3O),3.94(3H,s,CH3O),6.14(1H,d,J=2.0 Hz,H-3),6.39(1H,d,J=1.8 Hz,H-6),6.94(1H,d,J=8.0 Hz,H-8),7.02(1H,dd,J=8.0 Hz,15.2 Hz,H-5'),7.05(1H,dd,J=8.0 Hz,15.6 Hz,H-4'),7.35(1H,d,J=4.0 Hz,H-3'),8.23(1H,d,J=8.0 Hz,H-6');13C NMR(100 MHz,CDCl3)δ:181.0 (s,C=O),169.0,168.8,159.4(s,C-2),158.5,147.8,131.5,130.9,121.3,120.6,110.6(d,C-3),105.3,105.2,93.8,89.1,77.3,77.0,76.7,56.0,55.9,55.4,49.5,49.3,49.1,48.8,48.6,29.6;ESI-MS m/z:313(M +H),335(M+Na)。
3.2.2 新型黄酮醇化合物的合成
3'-羟基-5,7-二甲氧基黄酮醇7,深黄色固体,产率:55%,mp.189.8~190.2 ℃;1H NMR(400 MHz,CDCl3)δ:3.64(3H,s,CH3O),3.73(3H,s,CH3O),6.38(1H,d,J=2.0 Hz,H-6),6.60(1H,d,J=2.0 Hz,H-8),6.94(1H,d,J=2.0 Hz,H-4'),7.35(1H,dd,J=8.0 Hz,16.0 Hz,H-5'),7.69(1H,d,J=8.0 Hz,H-6'),7.74(1H,s,H-2'),9.19(1H,s,H-3');ESI-MS m/z:305(M+H);327 (M+Na)。
4-甲基-5,7-三甲氧基-黄酮醇8,淡黄色晶体,产率:72%,mp.194.6~194.7 ℃;1H NMR(400 MHz,DMSO)δ:2.05(3H,s,CH3),3.93(3H,s,CH3O),3.97(3H,s,CH3O),6.16(1H,d,J=2.0 Hz,H-8),6.38(1H,d,J=1.2 Hz,H-6),7.54(2H,d,J=4.0 Hz,H-3',H-5'),7.72(2H,d,J=8.4 Hz,H-2',H-6'),8.22(1H,s,H-3);ESI-MS m/z:313(M+H),335(M+Na),647 (2M+Na)。
5,7-二甲氧基-2',3',4-三甲氧基黄酮醇9,橙黄色固体,产率:65%,mp.228.9~229.2 ℃;1H NMR(400 MHz,CDCl3)δ:3.81(3H,s,CH3O),3.83(3H,s,CH3O),3.89(3H,s,CH3O),3.91(3H,s,CH3O),3.95(3H,s,CH3O),6.49(1H,d,J=2.0 Hz,H-6),6.63(1H,d,J=2.0 Hz,H-8),6.94(3H,d,J=8.4 Hz,1H,H-5),7.21(1H,d,J=9.0 Hz,H-6),8.42(1H,s,H-3');ESI-MS m/z:389(M +H),411(M +Na),799 (2M+Na)。
2-蒽基-5,7-二甲氧基-黄酮醇10,橘红色固体,产率:72%,mp.220.7~222.1 ℃;1H NMR(400 MHz,CDCl3)δ:3.82(3H,s,CH3O),4.04(3H,s,CH3O),6.45(1H,d,J=2.4 Hz,H-3'),6.79(1H,s,H-6),7.25(1H,s,H-8),7.50(1H,dd,J=2.0 Hz,4.4 Hz,H-4),7.72(1H,d,J=4.0 Hz,H-3),7.85(1H,d,J=3.6 Hz,6.0 Hz,H-5),8.08(1H,d,J=14.4 Hz,H-2),8.63(1H,s,H-6);13C NMR (100 MHz,CDCl3)δ:171.8(s,C=O),164.5,160.9,160.3(s,C-2),141.8,140.4(s,C-3),131.2,130.9,130.2,130.1,128.8,128.4,127.0,126.1,126.0,125.5,125.3,123.5,107.7,107.1,96.0,92.6,77.3,77.0,76.7,65.5,56.5,55.8,30.5,19.1,13.7;ESI-MS m/z:399.0 (M+H)。
7-甲氧基-2-喹啉黄酮醇11,红色固体,产率:55%,mp.224.5~225.5 ℃;1H NMR(400 MHz,DMSO)δ:3.97(3H,s,CH3O),6.95(1H,d,J=2.4 Hz,H-8),6.97(1H,d,J=2.4 Hz,H-6),7.22(1H,d,J=2.4 Hz,H-5),7.57(1H,dd,J=7.6 Hz,15.6 Hz,H-5'),7.77(1H,d,J=8.0 Hz,14.4 Hz,H-8'),7.94(1H,dd,J=8.0 Hz,16.0 Hz,H-6'),7.98(1H,d,J=8.0 Hz,H-7'),8.12(1H,d,J=8.0 Hz,H-3'),8.36(1H,dd,J=10.0 Hz,18.0 Hz,H-4'),9.39(1H,s,H-3);ESI-MS m/z:342(M +Na),661(2M +Na)。
7-甲氧基-2',3',4'-三甲氧基黄酮醇12,橘红色固体,产率69%,mp.173.2~173.9 ℃;1H NMR(400 MHz,DMSO)δ:3.91(3H,s,CH3O),3.93(3H,s,CH3O),3.94(3H,s,CH3O),3.96(3H,s,CH3O),6.83(1H,d,J=8.8 Hz,H-6),6.89(1H,s,H-8),7.01(1H,d,J=8.0 Hz,H-5),7.34(1H,dd,J=4.0 Hz,12.0 Hz,H-5'),8.15(1H,d,J=8.4 Hz,H-6');13C NMR (100 MHz,CDCl3)δ:172.6(s,C=O),164.0,157.7,155.6,152.3,144.9 (s,C-2),142.5,138.3(s,C-3),126.8,125.6,117.5,115.2,114.7,107.3,99.9,77.3,77.0,76.7,61.6,60.9,56.1,55.8;ESI-MS m/z:381(M+Na)。
3.3 体外乳腺癌[7]细胞抑性活性的测定
供试化合物1、2、3、7、9、10 用DMSO 配成1.0×10-2mol/L 浓度的储备液,稀释溶液浓度为50 μmol/L 的1、2、3、7、9、10 六种化合物对乳腺癌MDA-231 细胞的抑制活性检测,应用MTT 比色法检测OD 值,并选取起始原料,中间体查尔酮以及顺铂进行实验对照,分别进行三组平行试验。应用MTT比色法检测OD 值,计算对照组和各实验组MDA-231 细胞的抑制率,活性实验与检测数据由贵州省中科院天然药物研究所完成,具体数据如下:
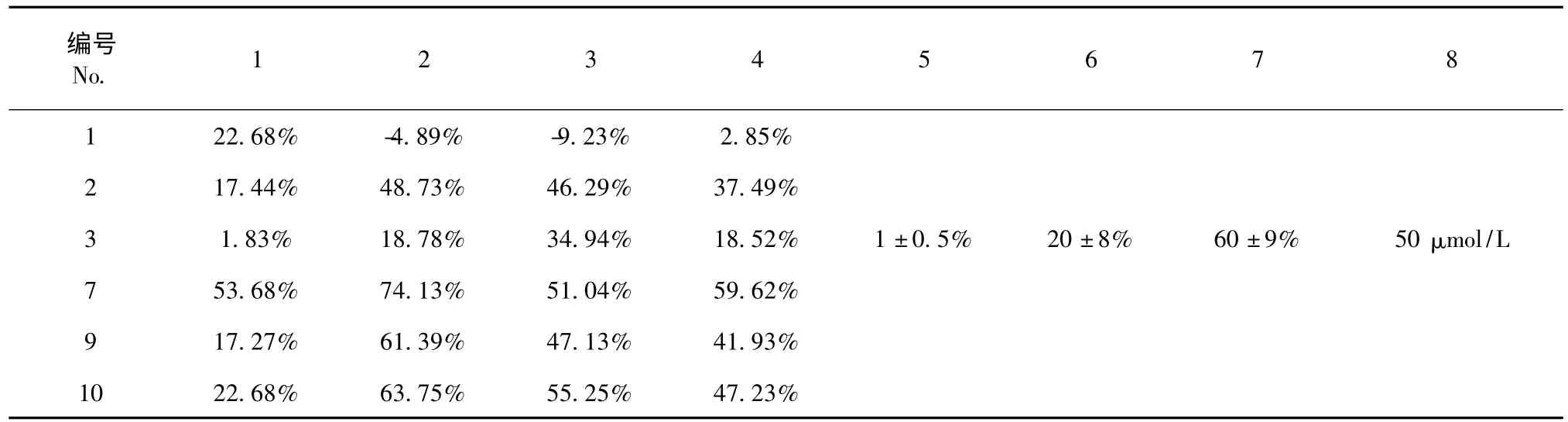
表1 化合物1、2、3、7、9、10 对乳腺癌MDA-231 细胞的抑制活性数据Table 1 Inhibition activity of compounds 1,2,3,7,9,10 against breast cancer cell line MDA-231
4 结果及分析
4.1 结构表征
化合物1~6 在ESI-MS 中与目标化合物的分子量相吻合,在1H NMR 中δ 区间3.71~4.01 内出现多组甲氧醚C-H 特征峰。化合物1、2、4、5、6 在δ 区间6.21~6.35 出现明显的黄酮C 环中C3-H 峰,其中3 化合物中受B 环间位硝基的影响,使C3-H 中的δ:6.74 大于其他化合物,δ 区间6.41~7.23 为黄酮化合物A 环中C6-H,C8-H,δ 区间7.32~8.76 为黄酮化合物B 环中C-H 的1H NMR 值。化合物7~9 在ESI-MS 中的分子量与目标化合物黄酮醇及其衍生物的数值相等,其中目标化合物的C3-OH 的活泼H 在氘代试剂中不表现强的吸收峰,7 化合物在δ:9.19 表现明显的C3'-OH 酚羟基峰,8 化合物在δ:4.31 出现明显的甲苯中的甲基C-H 峰,9 和10 化合物分别在对应黄酮醇化合物的δ 区间中出现相应的苯环C-H 峰,化合物11、12 由1H NMR 和ESI-MS数值确定为目标化合物。上述部分化合物的表征可参照表2(Table 2)中13C NMR 特征峰的具体数值。
4.2 黄酮类化合物骨架类型的判断[8]
在黄酮类化合物的13C NMR 谱中,不同类型的黄酮类化合物,则根据C 环的三个碳原子信号中母核结构不同而各具特征,它的化学位移和裂分情况,能有助于推断黄酮类化合物的骨架类型。具体请参见表2(Table 2)
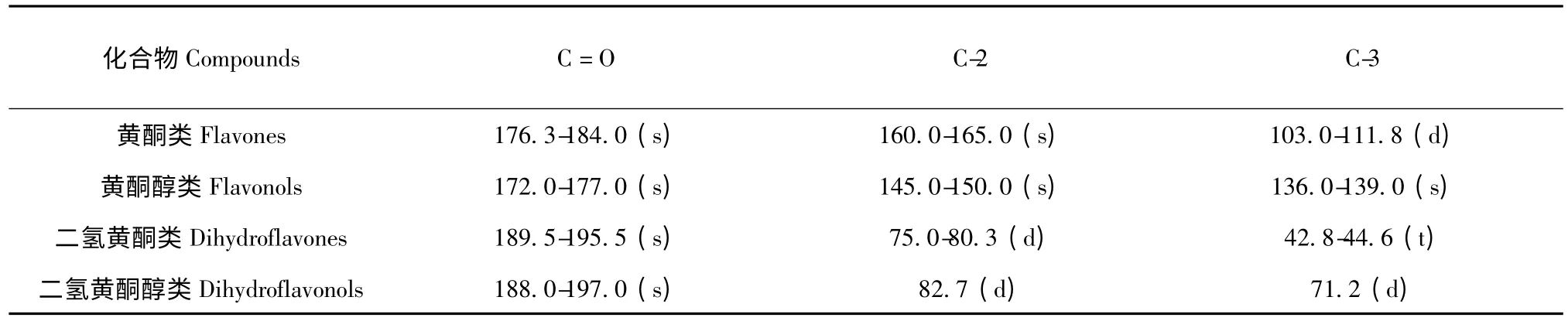
表2 黄酮类化合物C 环三个碳核的化学位移Table 2 Chemical shift of three carbon nuclei of flavonoids C ring
4.3 药理活性
在Yerra KR 和Jean BD 等人的基础上对黄酮和黄酮醇及其衍生物进行修饰,表1 的体外对乳腺癌MDA-231 细胞活性结果表明,由于起始原料和中间体及目标产物1~3 对乳腺癌MDA-231 细胞株表现较低的细胞毒作用,而目标产物2、7、10 表现较强的抑制活性如表1(表1),从而发现7-甲氧基黄酮醇构效关系中的B 环为蒽环时有较强的细胞毒性,B环的3'-OH 具有增强抗癌活性。浓度为50 μmol/L时,活性测试结果表明目标化合物7 对乳腺癌MDA-231 细胞的抑制可达到60%~70%,具有作为先导化合物的研究价值,目标化合物9 的对乳腺癌MDA-231 细胞的抑制可达到70%~80%的,该目标化合物具有作为乳腺癌抑制药物的进一步研究价值。
1 Wang H(王慧).Progress in bioactivity of flavonoids.Food Drug(食品与药品),2010,12:347-350.
2 Yan X(延玺),Liu HQ(刘会青),Zou YQ(邹永青),et al.Physiological activities and research advance in synthesis of flavonoids.Chin J Org Chem(有机化学),2008,28:1534-1544.
3 Zhang T(张氽),Kan JQ(阚建全),Chen ZD(陈宗道).Research progress of bioflavonoid antitumous effect.Chin Food Addit(中国食品添加剂),2003,83(3):17-20.
4 Yerra KR,Shih HF,Yew MT.Synthesis growth inhibition and cell cycle evaluations of novel flavonoid derivatives.Bio-org Med Chem,2005,13:6850-6855.
5 Jean BD,Flore D,Lionel V,et al.Effects of flavonoids on cell proliferation and caspase activation in a human colonic cell line HT 29:An SAR Study.J Med Chem,2005,48:2790-2804.
6 Liao TG(廖头根),Wang QA(汪秋安),Fang WQ(方伟青),et al.Study on the synthesis of novel chalcone and biological activity.Chin J Org Chem (有机化学),2006,25:685-689.
7 Wu X(吴茜),Li ZY(李志裕),Tang WF(唐伟方),et al.Chemical modification of flavones and biological activities of modified flavones.Nat Prod Res Dev(天然产物研究与开发),2008,20:557-562.
8 Kuang HX(匡海学).Chinese Medicine Chemistry(中药化学).Beijing:People's Publishing House(北京人民出版社),2003.165-168.

