氢对纯镍及690合金在弱碱性溶液中电化学行为的影响
夏小峰,吕战鹏,陈俊劼,肖 茜,熊茹,夏 爽,姚美意,周邦新
(1. 上海大学 材料科学与工程学院 材料研究所,上海 200072;2. 中国核动力研究设计院 反应堆燃料及材料国家重点实验室,成都 610041)
氢对纯镍及690合金在弱碱性溶液中电化学行为的影响
夏小峰1,吕战鹏1,陈俊劼1,肖 茜1,熊茹2,夏 爽1,姚美意1,周邦新1
(1. 上海大学 材料科学与工程学院 材料研究所,上海 200072;2. 中国核动力研究设计院 反应堆燃料及材料国家重点实验室,成都 610041)
采用电化学方法研究了预充氢对690合金在25,50,70 ℃下弱碱性溶液中电化学行为的影响。结果表明,预充氢使得690合金在碳酸氢钠溶液中的自腐蚀电位负移、电化学阻抗降低,尽管不影响阳极极化曲线的形状,但增大了阳极极化曲线中一次过钝化电位之前的阳极电流密度。此外,预充氢使镍在碳酸氢钠溶液中的阳极极化曲线出现新的阳极电流峰,增大了阳极极化曲线中过钝化电位之前的电流密度,并降低了电化学阻抗。氢对金属或合金电化学行为的作用与电极反应类型、速率控制步骤以及表面膜的稳定性有关。
690镍基合金;氢;弱碱性溶液;电化学腐蚀
镍基合金广泛应用于核电站关键结构部件的制作,如蒸汽发生器传热管和控制棒驱动机构套管等。早期压水堆核电站蒸汽发生器传热管曾采用600合金,发生过严重的应力腐蚀开裂事故,之后广泛使用690合金作为蒸汽发生器传热管材料[1-5]。我国的压水堆核电站除部分采用800合金传热管和不锈钢传热管外,大多采用690合金作为蒸汽发生器传热管材料。镍基合金在压水堆冷却剂中的环境持久性是核电站长期安全稳定性的重要保证。由于压水堆核电站冷却剂中含有一定浓度的溶解氢,与其接触的合金材料长期处于低电化学电位环境中,存在氢进入合金内部并影响其服役性能的可能。有关氢对铁、镍、管线钢、不锈钢和镍基合金阳极溶解和钝化膜稳定性的作用已有一些报道[6-21],并提出了有关氢作用的一些机理[17-21]。曾一民[10]等研究了氢对镍在Na2B4O7溶液中钝化膜的影响和在NaCl溶液中点蚀的影响。但体纯等[16]研究了预充氢对60 ℃下690合金在含有SO42-的H3BO3溶液中电化学行为的影响。第一性原理[22-23]计算表明氢会影响金属的氧化反应。本工作通过电化学方法研究了预充氢对690合金在25,50,70 ℃ 3种温度下弱碱性溶液中电化学行为的影响,并对比研究了氢对纯镍电化学行为的影响,以期为停堆间歇较低温度工况条件时的材料服役性能评价提供参考。
1 试验
1.1 试验材料
试验材料采用99.9%纯镍和690合金。690合金为核级材料,其化学成分(质量分数/%)为:Fe 10.13,C 0.02,Si 0.11,Mn 0.16,Ni 59.42,S 0.001,Cr 29.35,P 0.006,Cu 0.01。最终热处理状态为TT处理(700 ℃, 15 h)状态,690合金的显微组织见图1。

图1 690合金的金相组织Fig. 1 Metallographic structure of Alloy 690
1.2 预充氢条件
预充氢溶液为含有0.5 g/L硫脲的0.5 mol/L硫酸溶液,通过恒电流阴极极化充氢。选择与电化学测试条件相同温度下充氢以尽量减少由于温度变化而导致的氢在金属中的固溶度差异。因为70 ℃下充氢时间过长会导致金属电极与封存物环氧树脂之间的脱离,因此70 ℃下的充氢时间选择为2 h,而25 ℃和50 ℃下选择较长的充氢时间。
1.3 电化学测量方法
电化学测试采用三电极体系,电极为辅助电极,铂饱和甘汞电极(SCE)为参比电极(文中所有的电位均是相对于SCE),工作电极采用工作面积为5 mm×5 mm的纯镍或者10 mm×10 mm的690合金。
未充氢及充氢试样采用环氧树脂密封固化,用水砂纸打磨至1 500号后丙酮清洗,采用科斯特(Corrtest)电化学工作站进行电化学测试。电化学测试用介质采用弱碱性的0.5 mol/L NaHCO3溶液以模拟核电站局部浓缩介质条件。电化学测试包括开路电位测量、动电位扫描阳极极化曲线、恒电位极化电流响应和电化学阻抗谱(EIS)。阳极极化曲线的扫描速率为100 mV/min;EIS测试采用恒电位模式,测试频率范围为10 mHz ~100 kHz,扰动信号为±10 mV正弦波。试验数据均有良好的重现性。
2 结果与讨论
2.1 有、无充氢纯镍在弱碱性溶液中的电化学行为
图2为有、无充氢(充氢电流为1 mA/cm2)的纯镍在25 ℃下0.5 mol/L NaHCO3溶液中的开路电位随时间的变化曲线。由图2可见,未充氢纯镍的开路电位约为-0.335 V,充氢48 h后试样的开路电位显著负移,为-0.412 V;充氢2 h后的试样在浸泡初期,开路电位先正移,然后出现负移,较长时间浸泡后稳定在-0.368 V左右。
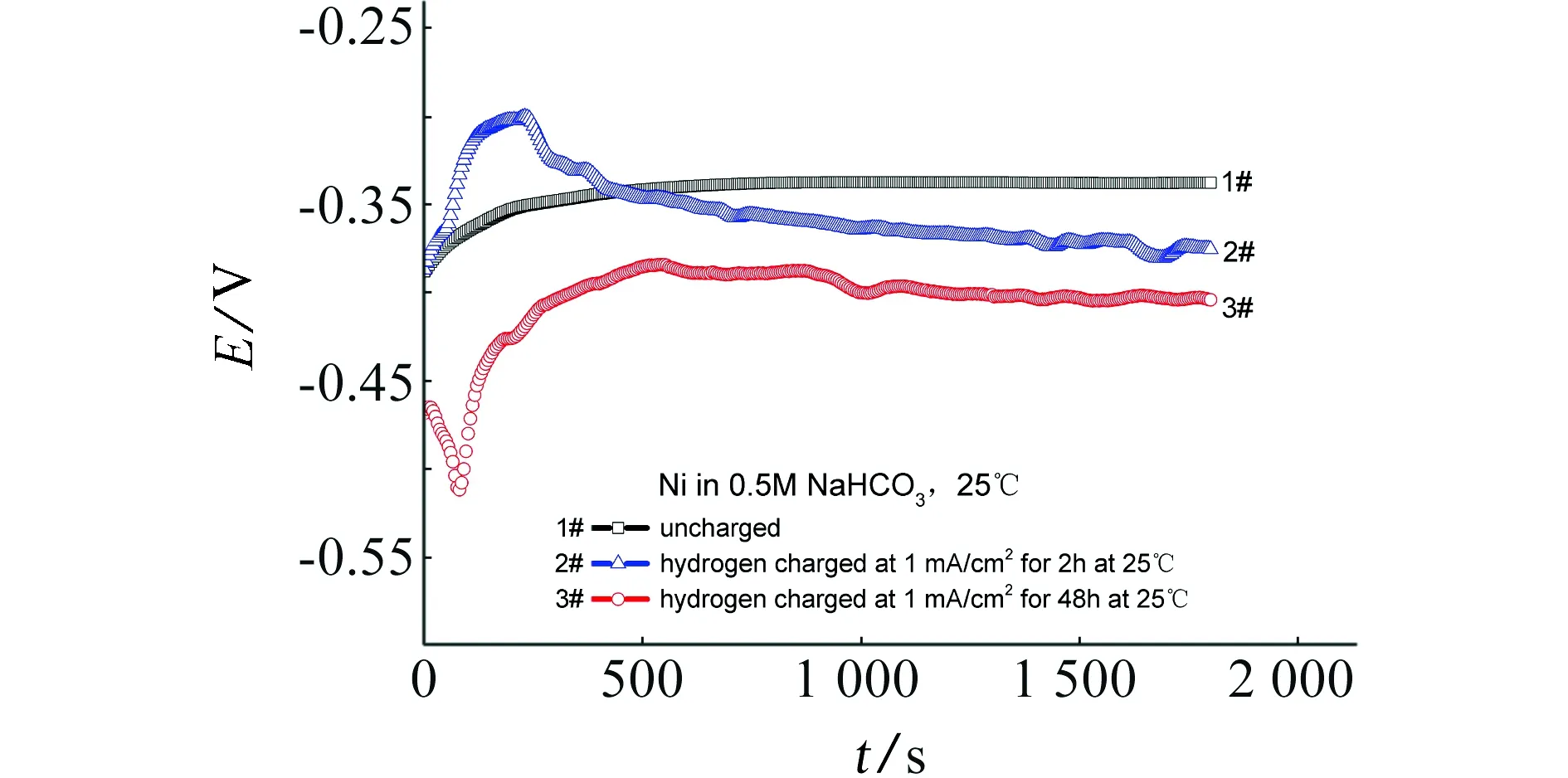
图2 有、无充氢(充氢电流为1 mA/cm2)的镍在25 ℃下0.5 mol/L NaHCO3溶液中的自腐蚀电位Fig. 2 Corrosion potential for uncharged and hydrogen-charged (charged at current density of 1 mA/cm2) Ni in 0.5 mol/L NaHCO3 at 25 ℃
图3为有、无充氢(充氢电流为1 mA/cm2)的纯镍在25 ℃下0.5 mol/L NaHCO3溶液中的阳极极化曲线。由图3可见,与未充氢试样相比,充氢后纯镍的阳极极化曲线出现明显的阳极电流峰值,且随着充氢时间的增加,维钝电流密度(取阳极极化曲线中电位0.2 V时的电流密度值)显著增大;未充氢试样约为15 μA·cm-2,充氢2 h约为39 μA·cm-2,充氢48 h约为116 μA·cm-2。图4为E=0.4 V下恒电位极化电流-时间曲线。可以看出,充氢后纯镍的电流密度大于未充氢的纯镍,且充氢48 h后纯镍的电流密度显著大于充氢2 h。由于极化方式不同,图4中恒电位极化下达到稳定后的电流密度值显著低于图3中动电位扫描所得阳极极化曲线中相同电位下的值。
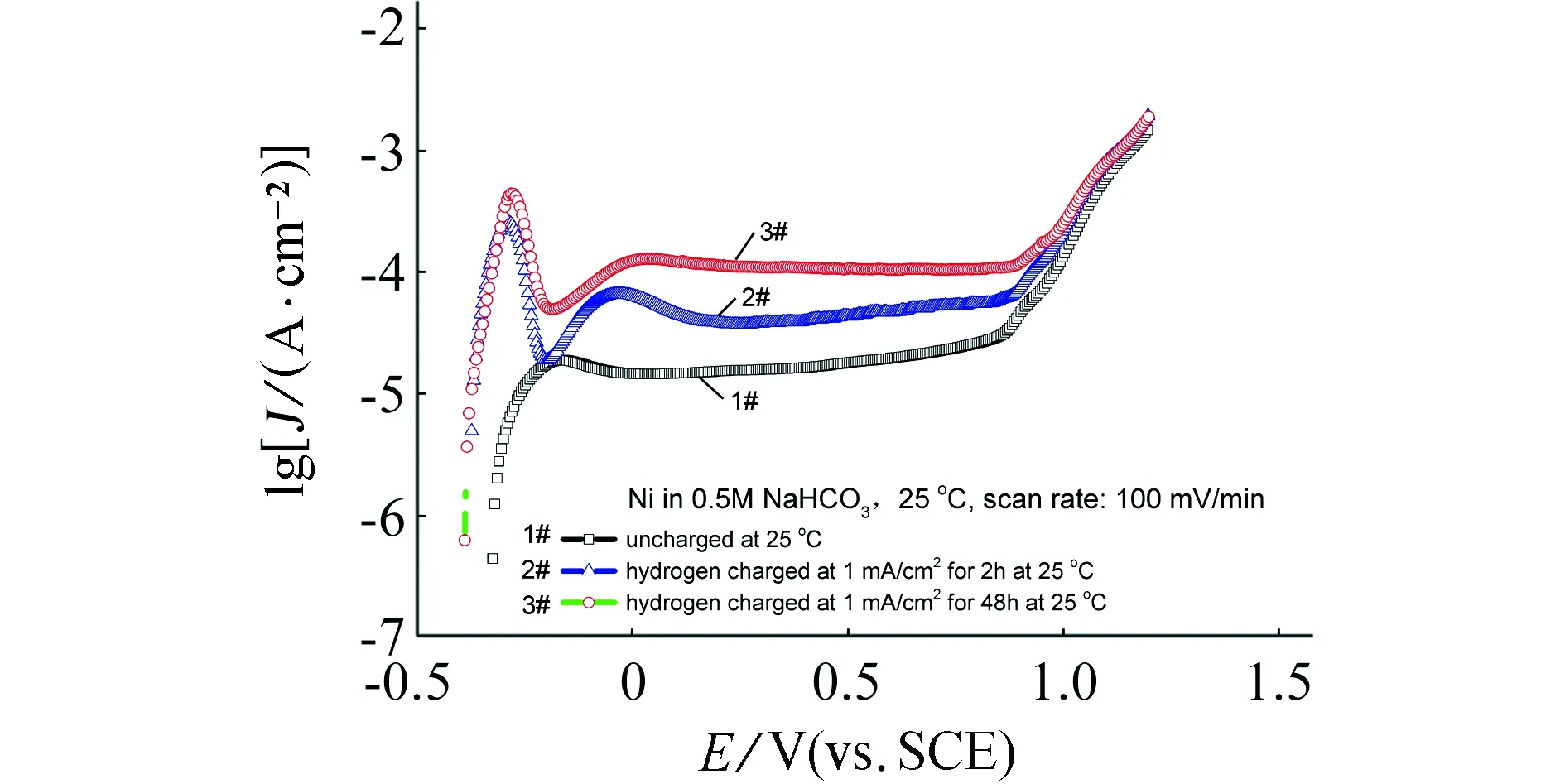
图3 有、无充氢(充氢电流为1 mA/cm2)的镍在25 ℃下0.5 mol/L NaHCO3溶液中的阳极极化曲线Fig. 3 Anodic polarization curves for uncharged and hydrogen-charged (charged at current density of 1 mA/cm2) Ni in 0.5 mol/L NaHCO3 at 25 ℃

图4 有、无充氢(充氢电流为1 mA/cm2)的镍在25 ℃下0.5 mol/L NaHCO3溶液中0.4 V下的恒电位极化电流响应Fig. 4 Current response in potentiostatic polarization at 0.4 V for uncharged and hydrogen-charged (charged at current density of 1 mA/cm2) Ni in 0.5 mol/L NaHCO3 at 25 ℃
图5为有、无充氢(充氢电流为1 mA/cm2)的纯镍在25 ℃下0.5 mol/L NaHCO3溶液中电化学阻抗谱。由图5可见,充氢显著影响纯镍的电化学阻抗谱。未充氢纯镍的阻抗谱主要表现为容抗弧特征;充氢2 h纯镍的电化学阻抗在高频区表现为容抗弧特征,在低频区表现出扩散阻抗特征,显著低于未充氢试样;充氢48 h纯镍的电化学阻抗在中高频区表现为容抗弧特征并与2 h充氢纯镍的高频区阻抗接近,低频区未出现明显的扩散阻抗谱特征。充氢后镍的阻抗在低频区显著低于未充氢镍的值,而在中高频区则与未充氢镍的阻抗接近。

(a) Nyquist
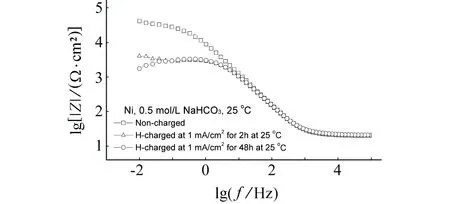
(b) Bode图5 有、无充氢(充氢电流为1 mA/cm2)的镍在25 ℃下0.5 mol/L NaHCO3溶液中开路电位下的电化学阻抗谱Fig. 5 EIS results at open circuit potential for uncharged and hydrogen-charged (charged at current density of 1 mA/cm2) Ni in 0.5 mol/L NaHCO3 at 25 ℃
2.2 有、无充氢690合金在不同温度弱碱性溶液中的电化学行为
图6~图9为25 ℃下,有、无预充氢的690合金在0.5 mol/L NaHCO3溶液中的电化学测试结果。由图6可见,在同一浸泡时间下,预充氢2 h的试样的稳定开路电位比未充氢的负移约0.052 V,预充氢12 h的试样的稳定开路电位比未充氢试样负移约0.24 V。
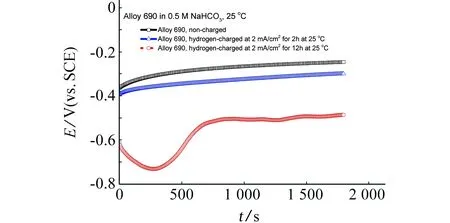
图6 有、无充氢(充氢电流为2 mA/cm2)的690合金在25 ℃下0.5 mol/L NaHCO3溶液中的自腐蚀电位Fig. 6 Corrosion potential for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 25 ℃

图7 有、无充氢(充氢电流为2 mA/cm2)的690合金在25 ℃下0.5 mol/L NaHCO3溶液中的阳极极化曲线Fig. 7 Anodic polarization curves for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 25 ℃
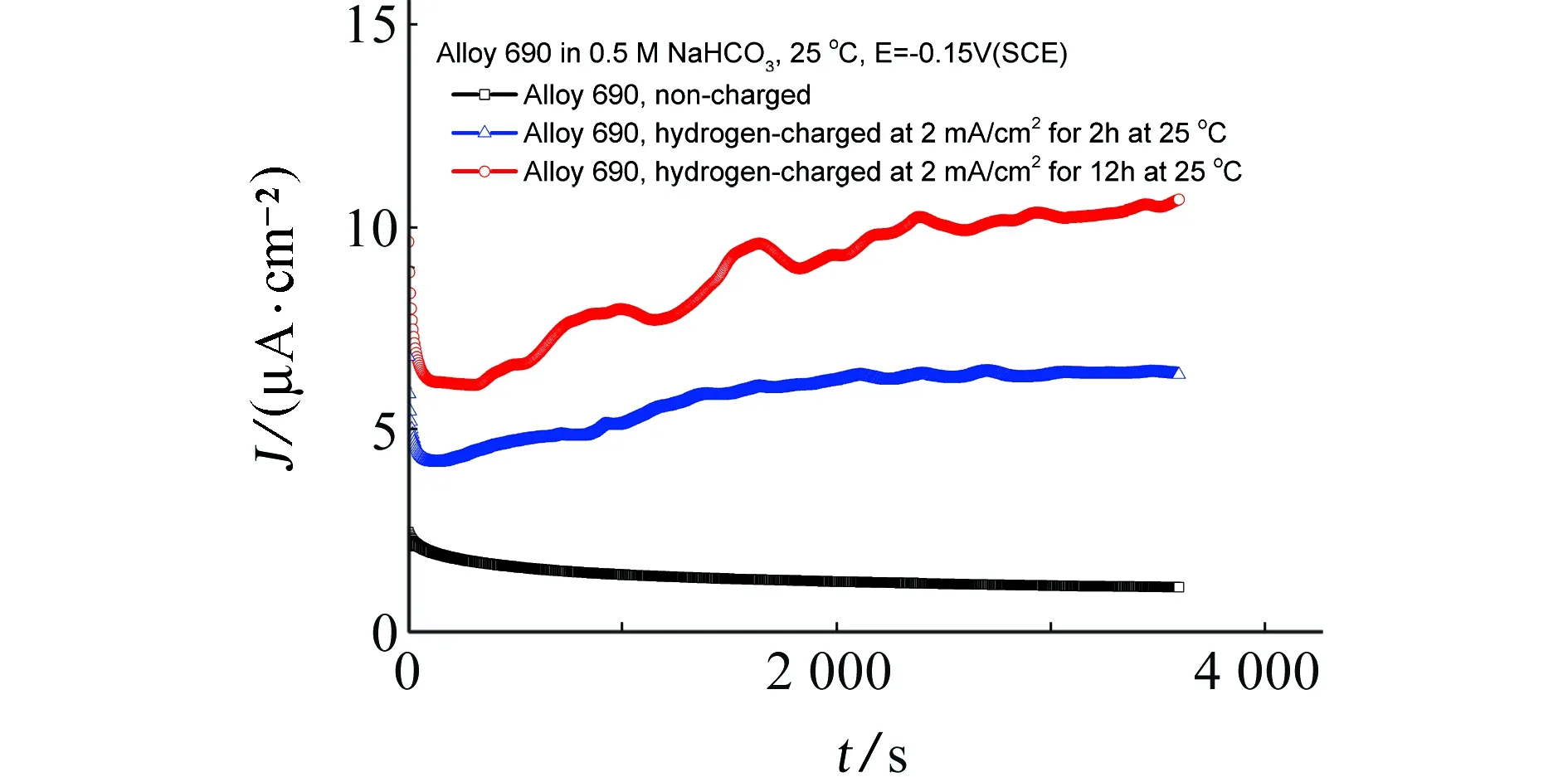
图8有、无充氢(充氢电流为2 mA/cm2)的690合金在25 ℃下0.5 mol/L NaHCO3溶液中的恒电位极化下电流响应Fig. 8 Current response in potentiostatic polarization at -0.15 V for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 25 ℃

(a) Nyquist
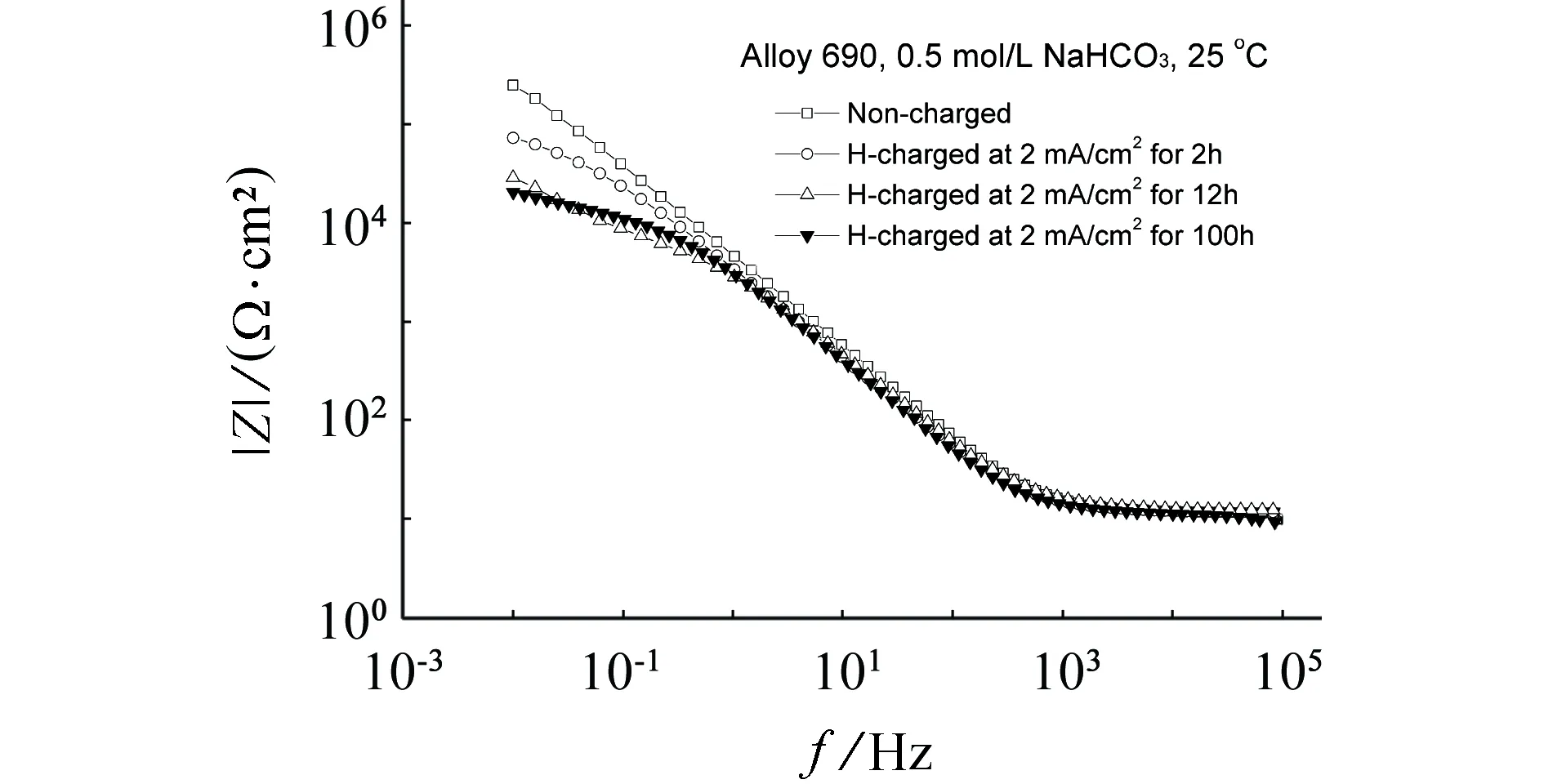
(b) Bode图9 有、无充氢(充氢电流为2 mA/cm2)的690合金在25 ℃下0.5 mol/L NaHCO3溶液中的开路电位下电化学阻抗谱Fig. 9 EIS results at open circuit potential for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 25 ℃
图7中结果表明,未充氢690合金的阳极极化曲线大致分为5个区间:AB区间电流密度随极化电位增加而增加,BC区间为电流密度几乎不随电位变化的电流平台区(维钝电流),CD区间电流密度随极化电位增加而增加并在D点(约0.6 V)出现电流密度峰值,DE区间电流密度随电位增加而减少,EF区间电流密度随电位增加而增加。
铁在25 ℃下0.5 mol/L NaHCO3溶液中的阳极极化曲线在0.6 V电位附近也处于钝化区[24],不出现阳极电流峰;图3中镍在25 ℃下0.5 mol/L NaHCO3溶液中在0.6 V电位附近也处于钝化区,不出现阳极电流峰。这表明,电流上升的CD区与电流下降的DE区与金属铬低价态氧化物转变为高价态氧化物有关,D点电位与Cr-H2O体系电位-pH图中相应pH下3价铬氧化物与6价铬氧化物的转变电位有对应性[25]。充氢后690合金的阳极极化曲线AB和BC区间的阳极电流密度高于未充氢690合金,而在电位正于D点电位之后预充氢690合金与未充氢690合金的阳极极化曲线接近。未充氢690合金的维钝电流密度约为5.7 μA/cm2,预充氢2 h对690合金维钝电流密度的影响很小;预充氢12 h后690合金的维钝电流密度约为13 μA/cm2。图8表明,在-0.15 V电位下恒电位极化时,预充氢690合金的电流密度随预充氢时间的增加而增大。图9表明,未充氢690合金在0.5 mol/L NaHCO3溶液中的阻抗表现为接近容抗弧并且阻抗值很高;预充氢2 h的690合金试样阻抗显著降低,并表现为容抗弧特征;预充氢12 h后690合金的阻抗进一步降低。
对比图5和图9可见,在25 ℃下0.5 mol/L NaHCO3溶液中,有、无预充氢690合金的电化学阻抗显著高于有、无充氢的纯镍;未充氢690合金的维钝电流密度约为纯镍维钝电流密度的一半,预充氢690合金的维钝电流密度也显著小于预充氢纯镍。
图10为有、无预充氢的690合金在0.5 mol/L NaHCO3溶液中不同温度下的开路电位随时间变化曲线。可以看出,预充氢使得690合金的开路电位负移:50 ℃下12 h充氢690合金在50 ℃溶液中的开路电位相比未充氢试样负移约0.3 V;70 ℃下2 h充氢690合金在70 ℃溶液中的开路电位相比未充氢试样负移约0.21 V。
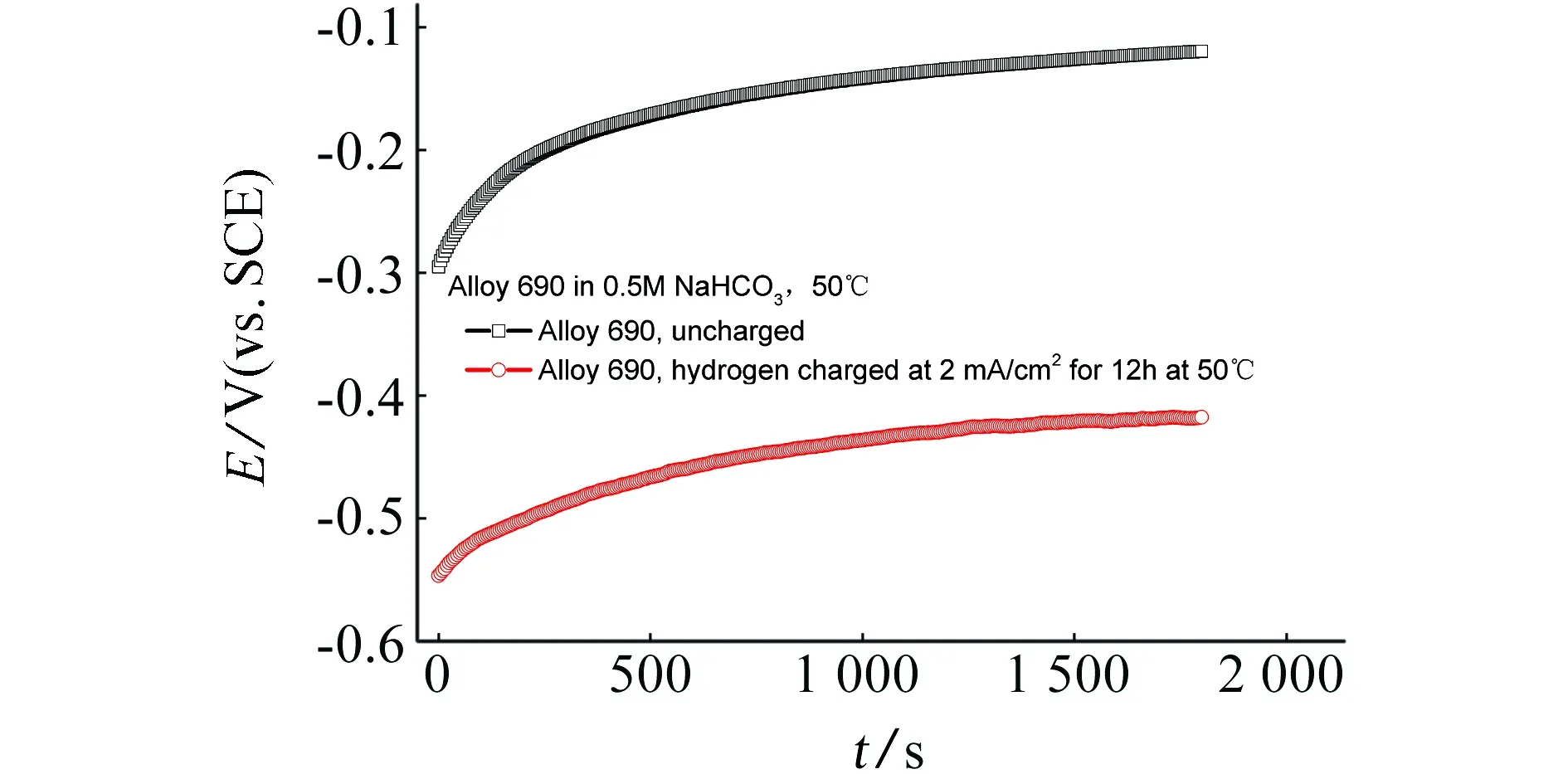
(a) 50 ℃

(b) 70 ℃图10 有、无充氢(充氢电流为2 mA/cm2)的690合金在不同温度下0.5 mol/L NaHCO3溶液中的自腐蚀电位Fig. 10 Corrosion potential for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at different temperatures
由图7和图11可见,预充氢690合金在50 ℃和70 ℃ 0.5 mol/L NaHCO3溶液中的阳极极化曲线在AB和BC区高于未充氢试样,在更正的电位区间与未充氢试样接近。在50 ℃与70 ℃下未充氢690合金阳极极化曲线上的维钝电流密度值接近,均显著高于25 ℃下。这与不同温度下氧化速率以及生成的氧化物保护性有关。在25~70 ℃区间预充氢690合金阳极极化曲线上的维钝电流密度随温度升高而增大。在50 ℃与70 ℃下恒电位阳极极化下电流-时间曲线结果表明,预充氢690合金的电流密度值高于未充氢试样的值(图8、12和图14),预充氢对阳极过程的加速作用与外加电位有关。
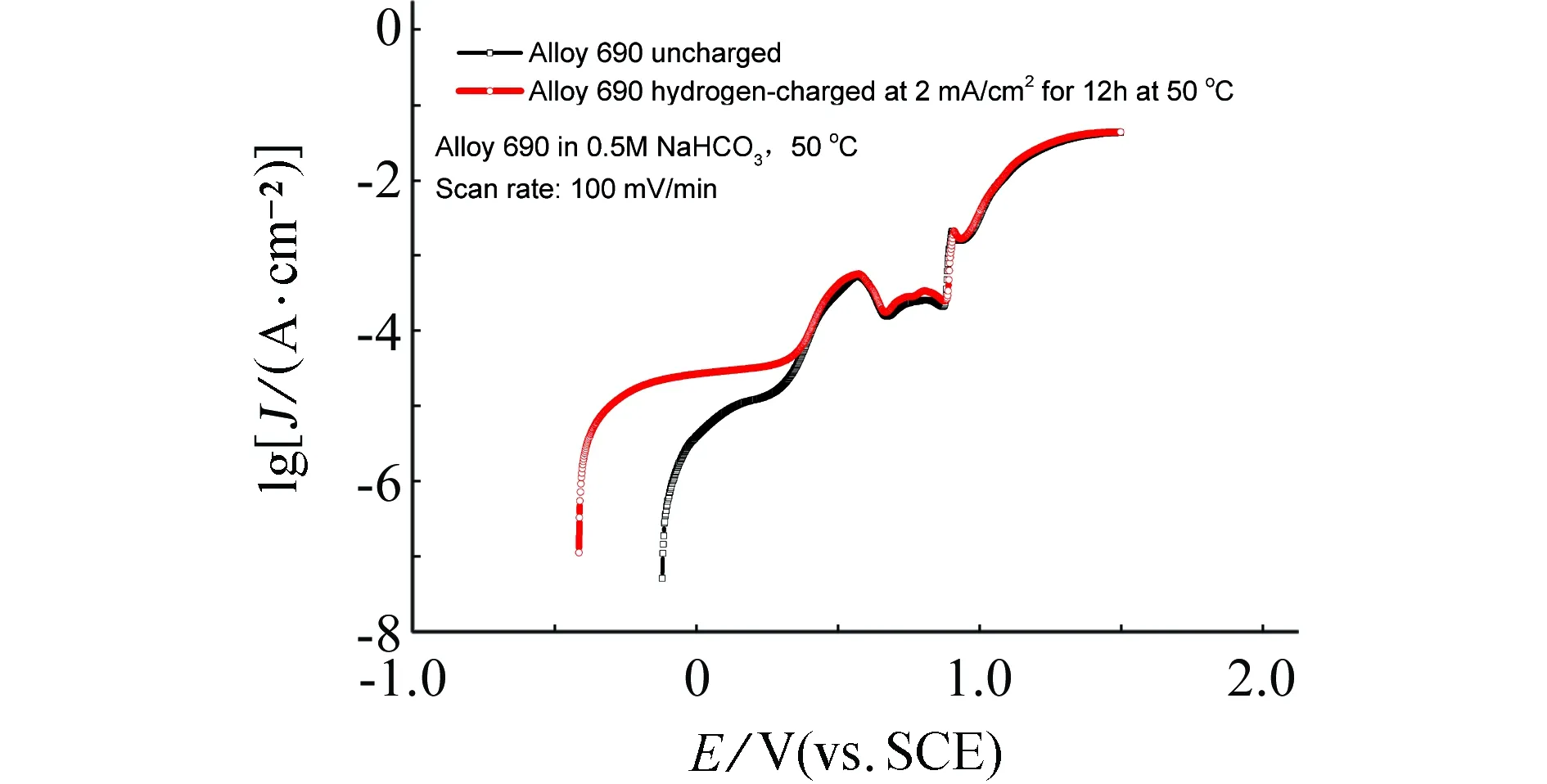
(a) 50 ℃

(b) 70 ℃图11 有、无充氢(充氢电流为2 mA/cm2)的690合金在不同温度下0.5 mol/L NaHCO3溶液中的阳极极化曲线Fig. 10 Anodic polarization curves for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at different temperatures
图9、图13和图15表明,在0.5 mol/L NaHCO3溶液中,未充氢690合金在50 ℃和70 ℃下的阻抗值显著低于25 ℃时的值。在50 ℃和70 ℃ 0.5 mol/L NaHCO3溶液中,预充氢690合金的电化学阻抗在较低频区域(<0.2 Hz)时显著低于同样温度下未充氢690合金的值,而在中高频区域充氢的影响不明显。高频区(>10 kHz)区域预充氢的作用呈现出复杂特征。
2.3 镍和690合金在弱碱性溶液中电极反应
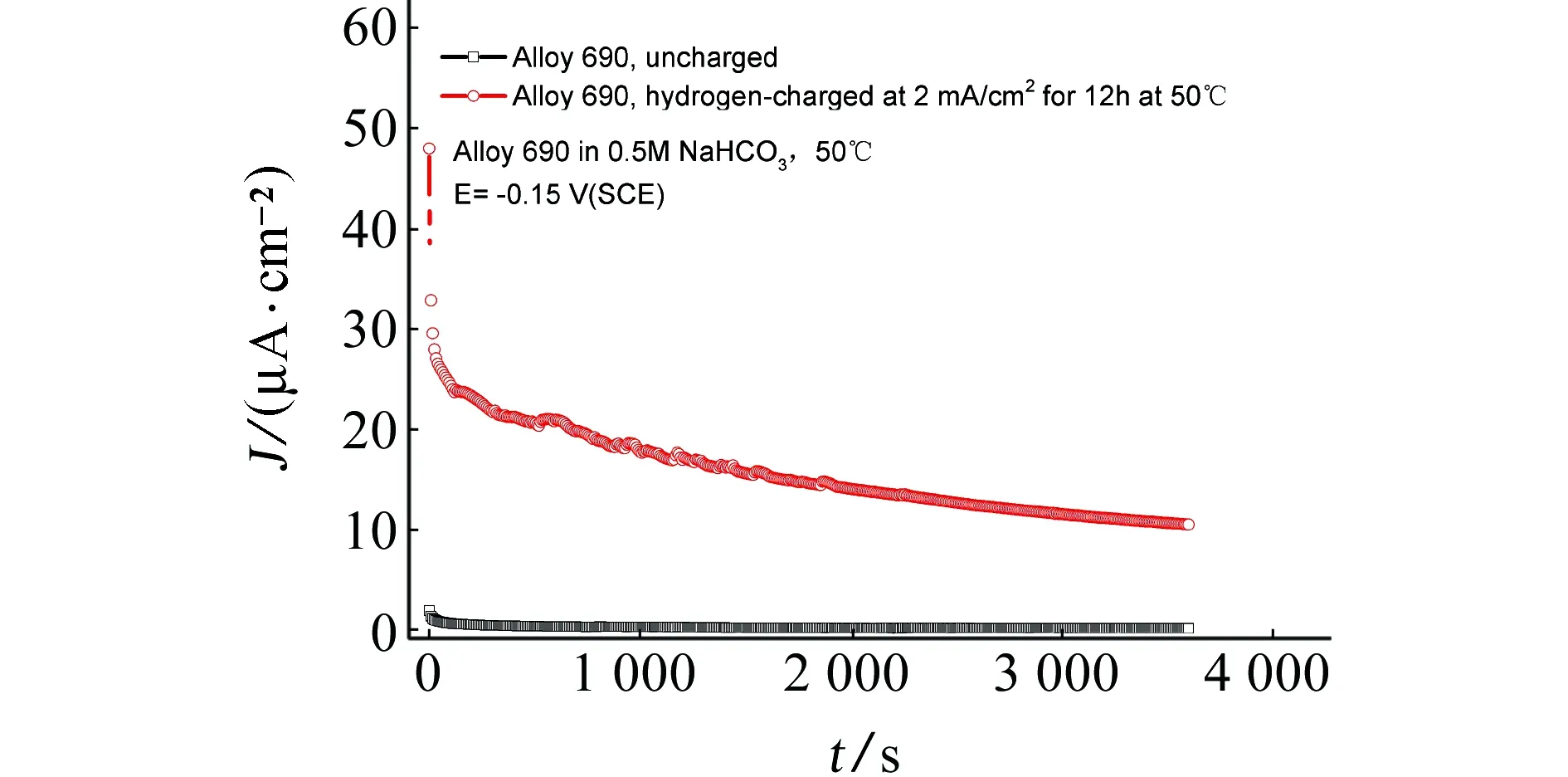
(a) E= -0.15 V
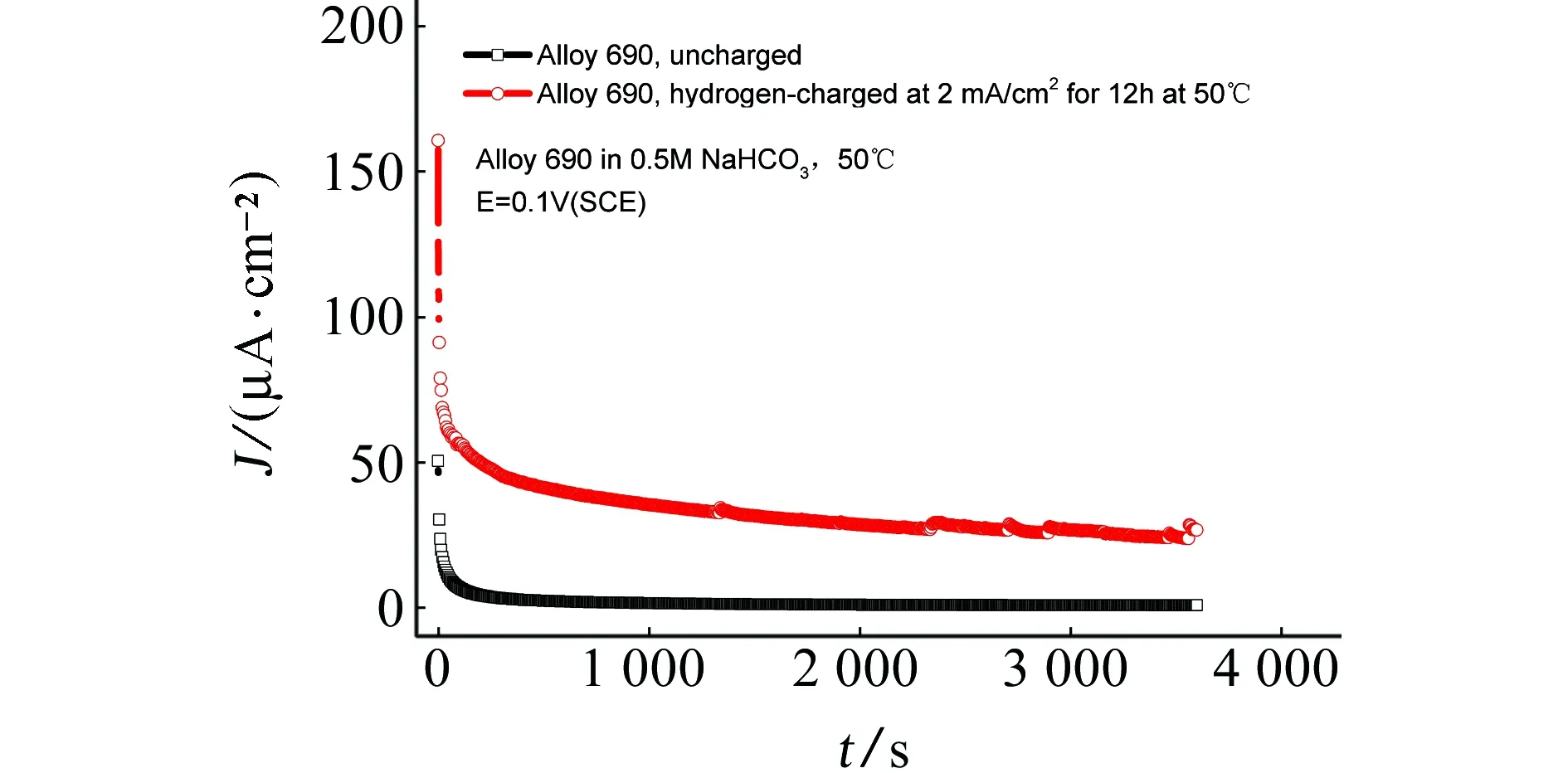
(b) E= 0.1 V图12 有、无充氢(充氢电流为2 mA/cm2)的690合金在50 ℃下0.5 mol/L NaHCO3溶液中不同恒电位极化下电流响应Fig. 12Current response in potentiostatic polarization for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 50 ℃
有关金属中的氢对金属电化学行为已有报道[6-21],曾一民等[10]曾发现预充氢会使镍在Na2B4O7溶液中的自腐蚀电位降低、阳极极化曲线出现明显的活化峰和高的维钝电流密度。本工作中发现预充氢对镍在NaHCO3溶液中的电化学行为有类似的作用。氢对合金电化学行为的作用相比对纯金属的作用更复杂。690合金中约30%的铬能抑制阳极溶解并提高钝化膜的稳定性。有、无预充氢时,690合金在NaHCO3溶液中的阳极溶解速率均显著低于纯镍,电化学阻抗也显著高于纯镍。
以镍为例,分析金属阳极反应以及金属中的氢的影响。参照金属溶液的电位-pH图[25],根据电位不同,镍在NaHCO3溶液中可能发生如下阳极反应:
(1)
(2)
(3)
(4)
690合金含有30%左右的铬。铬在水溶液中会发生如下反应中的一种或者几种:
(5)
(6)
(7)
(8)
(9)
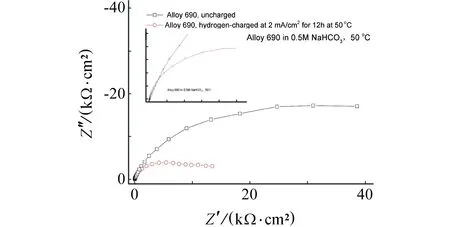
(a) Nyquist
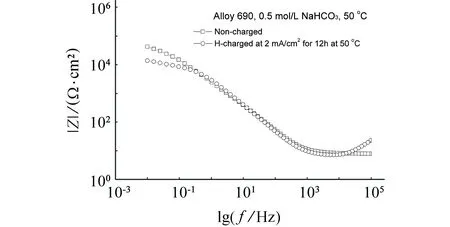
(b) Bode图13 有、无充氢(充氢电流为2 mA/cm2)的690合金在50 ℃下0.5 mol/L NaHCO3溶液中开路电位下电化学阻抗谱Fig. 13EIS results at open circuit potential for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 50 ℃

图14 有、无充氢(充氢电流为2 mA/cm2)的690合金在70 ℃下0.5 mol/L NaHCO3溶液中-0.15 V恒电位极化下电流响应Fig. 14Current response in potentiostatic polarization at -0.15 V for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) Alloy 690 in 0.5 mol/L NaHCO3 at 70 ℃
(10)
镍基高铬合金还有可能生成同时含有镍和铬的化合物:

(a) Nyquist
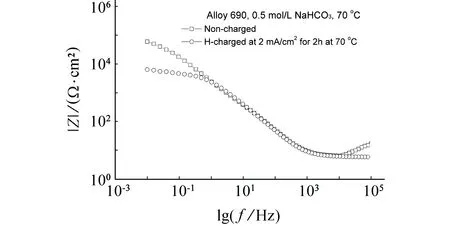
(b) Bode图15 有、无充氢(充氢电流为2 mA/cm2)的690合金在70 ℃下0.5 mol/L NaHCO3溶液中开路电位下电化学阻抗谱Fig. 15EIS results at open circuit potential for uncharged and hydrogen-charged (charged at current density of 2 mA/cm2) alloy 690 in 0.5 mol/L NaHCO3 at 70 ℃
(11)
高电位时会发生析氧反应:
(12)
2.4 固溶氢对镍和690合金电化学行为的影响
氢进入金属内部后,可以通过多种方式影响金属上的阳极反应。首先,金属中的氢可以失去电子被氧化而对外测阳极电流产生贡献。依据Nishith和Shoji[22]的第一性原理计算结果,金属中的氢与金属原子之间会发生电子再分布,导致金属和氢的电荷特性发生变化。假定p为金属中的氢所带的电荷,含有氢的金属所带的电荷为-p,则金属中氢的氧化反应与金属阳极反应特性均会发生变化。
Qiao和Mao[17-19]曾提出如下氢对金属活性阳极溶解的影响的理论分析。含有氢的金属活性溶解电流可以用下式表示:
(13)
式中:JAct(H)和JAct分别是含氢和不含氢金属的阳极溶解电流密度;αAct是阳极溶解反应电荷转移系数(此处假设αAct不受氢的影响),R是标准气体常数为8.31 J/(mol K),T是绝对温度(K);ΔGM(H)是由于金属中溶解氢引起的金属的Gibbs自由能变化。
当表面成膜反应也参与金属阳极反应速率控制时,参照有关的金属钝化理论[23-26],阳极电流可表示如下:
(14)
式中:Ee,act、Jact,0和βact分别是金属活性阳极溶解反应的平衡电位、交换电流密度和Tafel斜率(对应自然对数)。Ee,ff、Jff,0和βff分别是金属表面成膜反应的平衡电位、交换电流密度和Tafel斜率。C为电流密度与表面膜生成或溶解速率之间的转换系数,K是与H+浓度有关的金属表面膜溶解速率,B是与溶液中阴离子有关的金属表面膜溶解速率。用η表示金属表面膜的总溶解速率。

(15)
金属中的氢对金属在水溶液中电化学的影响可以通过如下方式:氢的氧化电极反应的叠加;氢引起的金属阳极溶解反应自由能的变化而导致真实阳极极化曲线的变化;氢及其反应产物导致的金属表面状态的变化特别是表面膜覆盖度或者保护性的变化等。预充氢对开路电位的影响可以是上述几种作用的综合结果。图3中阳极极化曲线出现明显的阳极电流密度峰并且初始部分阳极电流与预充氢时间的关系较小,提示预充氢引起的表面状态变化会对加速阳极溶解起重要作用,由于氢对电子转移过程控制的阳极活性溶解速率的影响较小。预充氢48 h镍的阳极电流峰值以及维钝电流密度均大于未充氢镍以及充氢2 h的镍,表明金属中的氢对稳定钝化膜的形成有阻碍作用并且降低钝化膜的保护性,即镍中的氢对反应(2)、(3) 或(4)成膜反应有阻碍作用并增大生成膜的反应活性。氢的作用方式与金属在水溶液中所处的状态以及表面膜的形成能力与保护性密切相关。在25 ℃、50 ℃和70 ℃下预充氢690合金的阳极极化曲线构形与未充氢试样相比没有显著变化,在开路电位附近不出现阳极电流峰,表明690合金中的氢对钝化膜生成的影响要小于镍中氢对钝化膜生成的影响,即对于690合金需要更长的充氢时间和更高的氢含量才能对反应(7)、(8)或者(11)起到明显的阻碍作用(图7),而同样的充氢时间下高温充氢有利于氢快速进入690合金,所以在70 ℃下充氢2 h也能对阳极极化曲线起到显著的影响。试验结果表明金属中氢对阳极反应的影响与电极反应类型有密切关系,即氢对690合金较高电位下的与低价态-高价态铬转换阳极反应和氧析出反应(参见式(9)、(10)和(12))的影响相对较小。
分析氢对阳极反应作用的动力学机理,还存在很多需要测试的定量数据,比如由金属中的氢对外测电流发生贡献的三项电流密度包括阳极溶解、氢的氧化和阴极电流的区分。乔利杰等人[8]测试了有、无充氢的不锈钢的阳极极化行为并用等离子光谱分析了相应试验后溶液中的离子,明确了氢对金属阳极溶解过程的加速作用。由于金属中氢的存在,金属表面的电化学位发生变化,影响表面膜的生成,特别是当H被氧化为H+后会影响金属表面局部环境[10]。金属中的氢可以通过影响与局部pH有关的金属表面膜的溶解速率K从而影响金属表面膜的总的溶解速率η,见式(14)和(15)。 式(13)表明金属中的氢会影响金属活性溶解反应速率[17-19],由此也会影响外测电流密度。量子化学计算的结果[22]表明金属中的氢会影响金属的电荷特性,而电荷特性的变化会直接影响金属溶解电化学动力学,参见式(1)、(5)、(6)和(11)。根据式(14)和(15), 增大K可以增大η使得在其他电子转移步骤动力学参数不变的情况下增大阳极电流密度以及氢导致的金属活性阳极溶解电流的提高均会引起外测电流密度的增大。已有报道金属中的氢会扩散进入钝化膜而改变钝化膜的组成、结构以及有关的界面反应动力学特性[9-16]。李成涛等[27-28]的试验结果表明690合金在NaOH溶液中的电化学阻抗谱表现为单一的容抗弧。本试验中没有充氢镍和690合金在弱碱性溶液中的电化学阻抗基本表现为单一的容抗弧。预充氢后镍和690合金阻抗谱形状会发生显著变化,数值显著降低,并会出现多个时间常数,表明镍或者690合金中的氢会改变反应速率控制机制、提高电化学反应活性或者是降低表面膜的保护性。有、无预充氢试样的电化学阻抗谱在不同频率范围内的异同,反映出氢对界面反应不同基元过程的作用。690合金在弱碱性溶液中的电化学行为涉及电子转移反应、传质过程和钝化膜特性,因此所研究温度区间温度对690合金阳极极化行为的影响表现出复杂性,比如没有充氢690合金的维钝电流与温度的关系没有表现为Arrhenius关系,与预充氢690合金在弱碱性溶液中的电化学行为与温度的相关性也有所不同。进一步分析预充氢条件、充氢试样中氢的分布和有关电极过程动力学过程将有助于定量分析氢影响电极反应动力学几种方式的交互作用方面。
3 结论
(1) 预充氢降低了纯镍NaHCO3溶液中的开路电位。预充氢使纯镍阳极极化曲线上出现明显的阳极电流峰并增大过钝化电位之前的阳极电流密度。预充氢后镍在自腐蚀电位下的电化学阻抗谱出现多个时间常数并显著低于没有充氢镍的数值。
(2) 预充氢降低了690合金在NaHCO3溶液中的开路电位但不显著改变其阳极极化曲线的形状。预充氢增大690合金阳极极化曲线中一次过钝化电位之前的阳极电流密度,而对电位高于一次过钝化区之后阳极电流密度的影响不大。预充氢后690合金在开路电位下的电化学阻抗降低,界面反应加速。在25~70 ℃之间,有、无预充氢690合金电化学行为与温度的相关性有差异,提示温度影响是对多种电极基元过程影响的综合结果。
(3) 氢对金属阳极过程的作用与电极反应类型、速率控制步骤以及表面膜的稳定性有关。结合电化学热力学与动力学分析了预充氢影响镍和690合金的机理和途径。
致谢:作者感谢日本东北大学庄子哲雄教授有益的讨论。
[1] SCOTT P M,BENHAMOU C. An overview of recent observation and interpretation of IGSCC in nickel base alloys in PWR primary water[C]//Proc.10th Inter.Conf.Environmental Degradation of Materials in Nuclear Power Systems-Water Reactors,NACE,2001,CDROM.
[2] BAMFORD W,PALMN A. Service experience with alloy 600 and associated welds in operating PWRs,including repair activities and regulatory and code actions[C]//Proc.13th Inter.Conf.Environmental Degradation of Materials in Nuclear Power Systems-Water Reactors,ANS,2009,CDROM.
[3] ANDRESEN P L,MORRA M M,AHLUWALIA K. SCC of Alloy 690 and its weld Metals[C]//Proc.5th Int.Conf.Environmental Degradation of Materials in Nuclear Power Systems-Water Reactors,TMS,2011,CDROM.
[4] SHOJI T,LU Z P,YAMAZAKI S. The effect of strain-hardening on PWSCC ofnickel-base Alloys 600 and 690[C]//Proc.14th Int.Conf.Environmental Degradation of Materials in Nuclear Power Systems-Water Reactors,ANS,2009,CDROM.
[5] 韩恩厚,王俭秋,吴欣强,等. 核电高温高压水中不锈钢和镍基合金的腐蚀机制[J]. 金属学报,2010,46(11):1379-1390.
[6] HASEGAWA M,OSAWA M. Anomalous corrosion of austenitic stainless steel exposed at high temperature and pressure[J]. Corrosion 1980,36(2):67-73.
[7] 胡小丽,黄震中,乔利杰,等. 氢和应力对阳极溶解的影响[J]. 中国腐蚀与防护学报,1996,16(3):187-194.
[8] QIAO L J,LUO J L. Hydrogen-facilitated anodic dissolution of austenitic stainless steels[J]. Corrosion,1998,54(4):281-288.
[9] 曾一民,乔利杰,褚武扬. 氢对310不锈钢钝化膜的影响[J]. 中国腐蚀与防护学报,1999,19(4):233-238.
[10] 曾一民,乔利杰,林昌健,等. 氢对纯镍钝化膜的影响[J]. 中国腐蚀与防护学报,1999,19(6):321-326.
[11] 曾一民,乔利,杨迈之,等. 氢对纯铁钝化膜电子性质的影响[J]. 中国腐蚀与防护学报,2000,20(2):74-80.
[12] YANG Q,LUO J L. Effects of hydrogen on disorder of passive films and pitting susceptibility of type 310 stainless steel[J]. J Electrochem Soc,2001,148(1):B29-B35.
[13] YU J G,ZHANG C S,LUO J L,et al. Investigation of the effect of hydrogen on the passive film on iron by surface analysis techniques[J]. J Electrochem Soc,2003,150(2):B68-B75.
[14] YU J G,ZHANG C S,LUO J L. NORTON P R. Photoelectrochemical study of hydrogen-loaded passive film[J]. J Electrochem Soc,2003,150(8):B405-B411.
[15] YU J G,LUO J L,NORTON P R. Electrochemical investigation of the effects of hydrogen on the stability of the passive film on iron[J]. Electrochimica Acta,2002,47(10):1527-1536.
[16] DANT C,LU Z P,SHOJI T,et al. Effects of hydrogen on the anodic behavior of Alloy 690 at 60 ℃[J]. Corros Sci,2010,52(4):228-1236.
[17] QIAO L J,MAO X. Thermodynamic analysis on the role of hydrogen in anodic stress corrosion cracking[J]. Acta Metall Mater,1995,43(1):4001-4006.
[18] MAO S X,GU B,WU N Q,et al. The mechanism of hydrogen facilitated anodic dissolution type stress corrosion cracking (theories and experiments)[J]. Philos Mag A,2001,81(7):1813-1831.
[19] 褚武扬,乔利杰,陈奇志,等. 断裂与环境断裂[M]. 北京:科学出版社,2000:178-189.
[20] LU B T,LUO J L,NORTONP R,et al. Effects of dissolved hydrogen and elastic and plastic deformation on active dissolution of pipeline steel in anaerobic ground water of near-neutral pH[J]. Acta Materialia,2009,57(1):41-49.
[21] LU B T,QIAO L J,LUO J L,et al. Role of hydrogen in stress corrosion cracking of austenitic stainless steels[J]. Philosophical Magazine,2011,91(2):208-228.
[22] DASN K,SHOJI T. An atomic study of hydrogen effect on the early stage oxidation of transition metal surfaces[J]. Int J Hydrogen Energy,2013,38(3):1644-1656.
[23] SHOJI T,LU Z,TAKEDA Y,et al. Quantification of mechano-chemical interactions at multi-scales and theoretical modeling of stress corrosion cracking initiation and short crack growth.Proc.the SCC Initiation Workshop[C]//Beaune,Burgundy,France,2008,EPRI,CDROM.
[24] LU Z P,HUANG C B,HUANG D L,et al. Effects of a magnetic field on the anodic dissolution, passivation and transpassivation behaviour of iron in weakly alkaline solutions with or without halides[J]. Corros Sci,2006,48(10):3049-3077.
[25] 杨熙珍,杨武. 金属腐蚀电化学热力学电位-pH图及其应用[M]. 北京:化学工业出版社,1991:78-137.
[26] 曹楚南. 腐蚀电化学原理[M]. 北京:化学工业出版社,第二版,2004.
[27] 李成涛,程学群,董超芳,等. pH值对690合金钝化膜电化学性能的影响[J]. 材料保护,2010,43(12):4-7.
[28] 张鉴清. 电化学测试技术[M]. 北京:化学工业出版社,2010.
Effects of Hydrogen on Electrochemical Behavior of Nickel and Alloy 690 in Weak Alkaline Solution
XIA Xiao-feng1, LU Zhan-peng1, CHEN Jun-jie1, XIAO Qian1, XIONG Ru2, XIA Shuang1, YAO Mei-yi1, ZHOU Bang-xin1
(1. Institute of Materials Science, School of Materials Science and Engineering, Shanghai University, Shanghai 200072, China; 2. National Key Laboratory of Reactor Fuel and Material, Nuclear Power Institute of China, Chengdu 610041, China)
The effects of pre-charged hydrogen on electrochemical behavior of Alloy 690 in a slightly alkaline solution at 25, 50 and 70 ℃ were investigated by electrochemical methods. The results showed that pre-charged hydrogen shifted the open circuit potential in the negative direction, decreased the electrochemical impedance, did not affect the shape of the anodic polarization curve, increased the current density in the anodic polarization curve at potentials before the first transpassivation potential for alloy 690 in a bicarbonate solution. Pre-charged hydrogen caused a new current peak, increased the current density at potentials before the transpassivation potential for nickel, and decreased the electrochemical impedance for alloy 690 in a bicarbonate solution. The effects of hydrogen on electrochemical behavior of metals or alloys were related to the types of electrode reactions, the rate-determining steps and the stability of surface films.
nickel-based alloy 690; hydrogen; weak alkaline solution; electrochemical corrosion
2014-02-19
教育部博士点基金项目(20123108110021); 核燃料与材料重点实验室基金项目; 上海市浦江人才计划(12PJ1403600)
吕战鹏(1967-),研究员,博士,从事材料腐蚀与防护研究,021-56336107,zplu@shu.edu.cn
TG174
A
1005-748X(2015)01-0036-09

