氢氧化钠-尿素-氧化锌体系制备抗油抗菌纸的研究
焦 丽 马金霞 戴红旗
(南京林业大学,江苏省制浆造纸重点实验室,江苏南京,210037)
氢氧化钠-尿素-氧化锌体系制备抗油抗菌纸的研究
焦丽马金霞*戴红旗
(南京林业大学,江苏省制浆造纸重点实验室,江苏南京,210037)
摘要:使用氢氧化钠-尿素-氧化锌水溶液选择性溶解滤纸纤维,以制备自增强的抗油抗菌纸。探讨了处理温度和时间对纸张强度性能和抗油性能的影响,同时评价了制备的抗油抗菌纸对大肠杆菌和金黄色葡萄杆菌的抗菌性能。使用扫描电子显微镜(SEM)、傅里叶红外光谱(FT-IR)、X射线衍射仪(XRD)对纸张结构进行表征,同时使用原子吸收分光光度计(AAS)和X射线光电子能谱(XPS)测定了纸张中氧化锌的含量。结果表明,滤纸经过处理后,纸张抗张指数和耐破指数均提高2倍,在24 h内能够完全阻止油脂渗透,对金黄色葡萄球菌具有明显的抗菌效果,同时纸张中氧化锌含量符合食品安全要求的范围,此法制备的抗油抗菌高强度纸张具有作为食品包装材料的潜力。
关键词:氢氧化钠-尿素-氧化锌溶解体系;抗油;抗菌
随着国家对可再生资源和可降解材料的日益关注和重视,越来越多的研究者将资源丰富的可再生资源作为研究对象,望以开发出环保价廉的材料。作为常用包装材料之一的纸和纸板具有优异的力学性能、价廉、环保等特点。但普通的纸和纸板因表面孔隙和内部毛细管作用,油脂易于渗透,且易受微生物腐蚀[1-2]。因此,改善纸和纸板的抗油抗菌性能,对于扩大其作为包装材料的应用范围具有重要意义。
通过表面涂布和高打浆度的方式改善纸张抗油的方法存在着环保、食品安全和成本问题[3- 6]。纸张抗油性能与其孔隙大小有关,通过减少纸张孔隙可有效改善纸张抗油性能[7- 8]。纤维素纤维细胞壁由多层结构组成,表面无序的低分子层易溶于纤维素溶剂[9]。溶解的纤维素填充在纤维孔隙间并吸附在未溶解且仍保留高结晶度和纤维长度的纤维素骨架上,从而降低纸张孔隙率,以改善纸张抗油性能和强度性能。
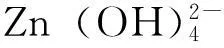
NaOH-尿素-ZnO体系不能完全溶解相对分子质量较高(M>14×104)的纤维素,本研究利用该体系选择性溶解滤纸纤维的无定形区(聚合度为860),溶解的纤维素填充于纤维孔隙间并吸附在保持纸张力学强度的未溶解纤维表面,从而形成良好界面和有效降低纸张孔隙率,以提高纸张抗油性能和强度性能;并通过NaOH-尿素-ZnO水溶液体系一步法制备自增强的抗油抗菌纸。
1实验
1.1原料与仪器
滤纸:飞世尔牌,中细孔慢速定性P4级(聚合度为860);NaOH、尿素、ZnO购于南京化学试剂有限公司,分析级。
WZL-300纸张力学强度测试仪,杭州轻通仪器开发公司;YQ-Z23A耐破度测定仪,中国杭州轻工检测仪器厂;UItima TV多功能组合式X射线衍射(XRD)仪,日本株式会社理学;JSM-7600F扫描电子显微镜(SEM),日本电子株式会社;ZX0101007 360傅里叶变换红外光谱仪(FT-IR),美国尼高力公司;TAS-990原子吸收分光光度计,北京普析通用仪器有限责任公司;AXIS Ultra DLD X射线光电子能谱,英国。
1.2实验方法
1.2.1抗油抗菌纸的制备
配制8%NaOH-12%尿素- 0.25%ZnO水溶液(均为质量分数,下同),将滤纸浸渍在该溶液中30 s吸收饱和后取出,在一定温度(25、0、-12、-18℃)下放置一定时间(30、60、120、180 min),使用去离子水清洗滤纸,以去除纸张表面残余的NaOH和尿素,最后在0.1 MPa、100℃下干燥15 min。在温度25℃、湿度50%下平衡24 h,然后测量纸张各项指标。
1.2.2纸张强度性能的测定
纸张抗张强度和耐破度分别按照TAPPI T 494 om— 01和TAPPI T 403 om— 02的方法进行测定。
1.2.3纸张抗油性能的测定
依据修订版的TAPPI T-507—99柔性包装材料的抗油性能测定方法进行测定。
1.2.4纸张孔隙率的测定
纸张孔隙率的测量采用介质饱和法测定,在相同预处理条件下,乙醇饱和处理不同纸样,8 h后取出纸样,两面附以滤纸并在一定压力下吸收30 s后,迅速称量质量W1,之后将纸样置于103℃恒温箱中干燥至绝干W2,根据式(1)得到纸张孔隙率。
(1)
式中,W1为试样饱和前的质量;W2为试样饱和后的质量;V为纸张体积;d为乙醇密度。
1.2.5纸张微观结构的分析
(1)利用SEM分析纸张微观结构的变化,将抗油抗菌纸在105℃下干燥8 h,经过切片和表面喷金后,在15.0 kV下观察纸张的表面和横截面形态。
(2)FT-IR分析,将制备的抗油抗菌纸放置在多功能反射头上,测定纸张的红外吸收光谱。
(3)采用UltimaIV型XRD仪分析滤纸纤维和经NaOH-尿素-ZnO体系处理后纸样纤维的结晶度变化,用镍片消除Cu Kα辐射(40 kV,30 mA),衍射角2θ为5°~50°,步宽为0.02°,扫描速度为2°/min。本研究中纤维素的结晶度以结晶指数来衡量,采用Segal法计算纤维的结晶指数(见式(2)):

(2)
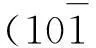
1.2.6纸张抗菌性能的测定
纸张抗菌性能的测定主要依据GB/T 20944.1—2007琼脂平皿扩散法,采用革兰氏染色阴性的大肠杆菌以及革兰氏染色阳性的金黄色葡萄球菌测定纸张的抗菌性能。
1.2.7纸样中ZnO含量和可释放Zn2+含量的测定
纸样中ZnO含量的测定依据HB 5219.1-21—1998中的原子吸收光谱分析法(AAS)测定锌含量。首先绘制标准曲线,分别制备0.2、0.4、0.8、1.6、3.2、4.8、6.0 mg/L Zn2+标准溶液。然后将2.000 g的纸样在高温炉575℃、4 h灰化后加入2 mL HCl和2 mL HNO3消解,过滤后在100 mL容量瓶中定容待测。
纸样中可释放Zn2+含量的测定过程为:将1 cm×1 cm的纸样浸渍在5 mL去离子水中,在37℃振荡器上放置20天,取出纸样,在上述溶液中加入1 mL HCl和1 mL HNO3消解,过滤后在100 mL容量瓶中定容待测。
纸样中Zn元素和O元素的化学结合价态通过XPS的测试结果进行确定。
2结果与讨论
2.1处理温度对纸张强度性能和抗油性能的影响
据文献[17]报道,纤维素能够快速溶解于在预冻(-12℃)的7%~10% NaOH-12%尿素- 0.25% ZnO溶液中,因其溶解过程是放热反应,若溶解体系不进行预冻处理,即使溶液的成分相同,纤维素也不能溶解。在-12℃,纤维素能够随时间的延长不断溶解,纸张性能随之不断变化。因此,本实验探讨不同处理温度对纸张性能的影响。
图1和图2分别为处理温度对纸张强度性能、孔隙率及紧度的影响。表2为处理温度对纸张抗油性能的影响。
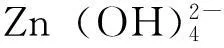

图1 处理温度对纸张强度性能的影响
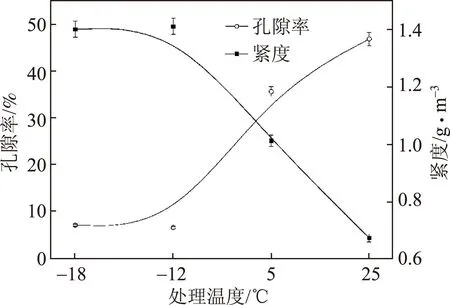
图2 处理温度对纸张孔隙率和紧度的影响
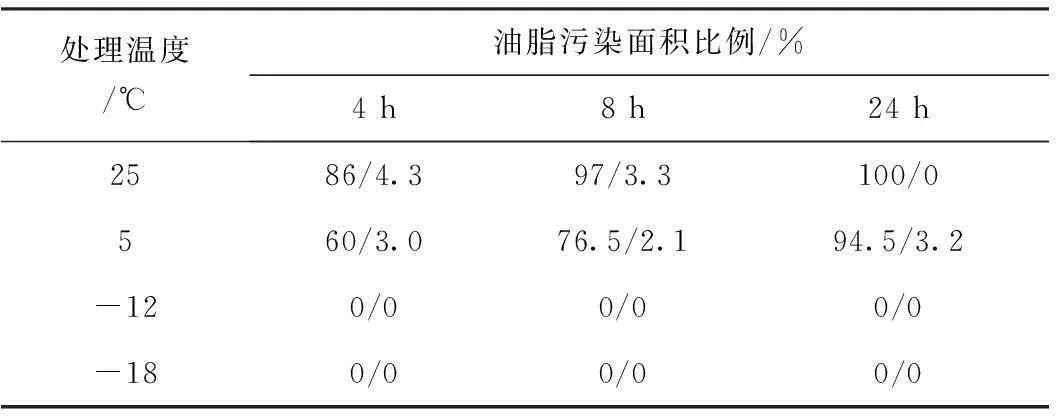
处理温度/℃油脂污染面积比例/%4h8h24h2586/4.397/3.3100/0560/3.076.5/2.194.5/3.2-120/00/00/0-180/00/00/0
2.2处理时间对纸张强度性能和抗油性能的影响
将滤纸置于预冻的NaOH-尿素-ZnO溶液中,随时间的延长,滤纸纤维逐渐溶解,首先溶解是在滤纸纤维中的无定形区,随溶解时间的延长,纤维素中的结晶区也逐渐溶解,纤维素中的结晶区对纸张强度性能起到重要作用。本实验探讨不同处理时间对纸张性能的影响。图3、图4和表2分别为处理时间对纸张强度性能、紧度、孔隙率以及纸张抗油性能的影响。
由图3、图4和表2可知,随处理时间的延长,纸张的抗张指数、耐破指数及紧度增大,孔隙率逐渐降低;处理时间120 min时,在24 h内油脂无法渗入纸张内部。首先,滤纸浸渍水溶液后,滤纸纤维中纤维素表面的无定形区低分子链不断润胀,无定形区氢键逐渐被破坏形成溶解纤维,随处理时间的延长,部分结晶区也被溶解[10,20]。溶解的纤维填充在滤纸纤维
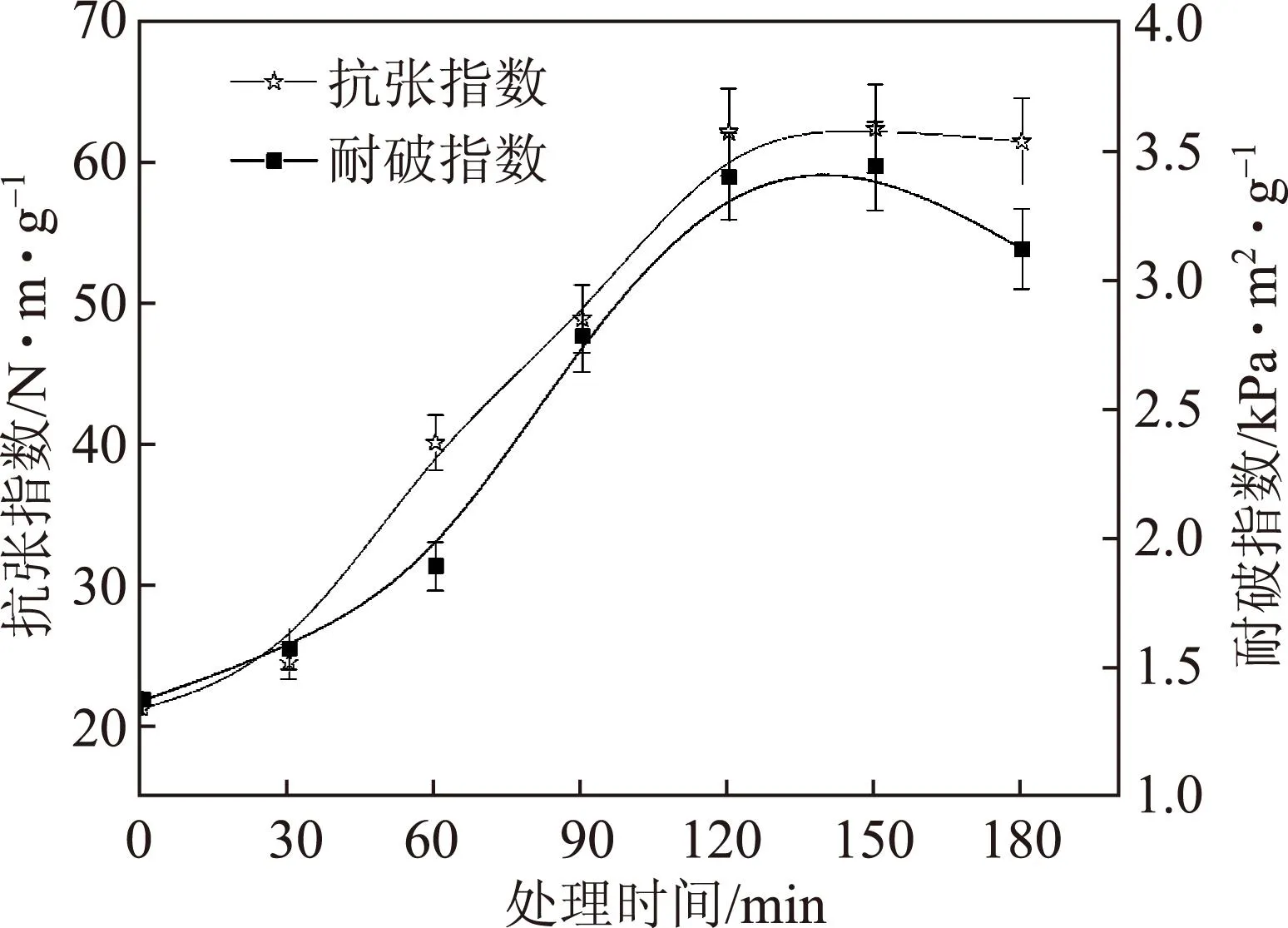
图3 处理时间对纸张强度性能的影响
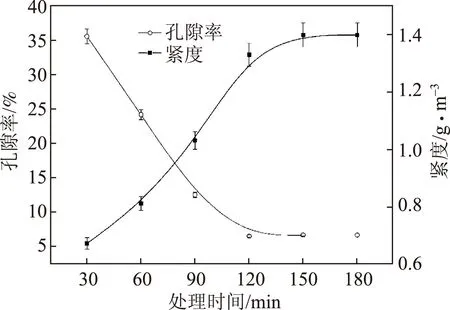
图4 处理时间对纸张紧度和孔隙率的影响

处理时间/min油脂污染面积比例/%4h8h24h3067/3.3589/2.1495/4.456032.5/1.6351/0.8976/3.289011.5/0.5816/0.6722/0.791200/00/00/01500/00/00/01800/00/00/0

图5 滤纸和抗油抗菌纸的SEM图像
孔隙间并吸附在未溶解的纤维表面,在水中凝固再生后,大量氢键重排从而形成良好的界面,有效减少了滤纸纤维间的孔隙和提高纸张强度[21]。由于滤纸纤维的强度性能主要取决于纤维素的结晶度,处理时间继续延长,结晶度降低,纸张的强度性能随之降低[22]。处理120~150 min的纸张表现出的强度是原纸强度的3倍,且在24 h内完全可以阻止油脂的渗透。
2.3纸张微观结构的分析
为了分析纸张在-12℃中处理120 min时强度性能和抗油性能增强的原因,对抗油抗菌纸微观结构进行了分析,结果如图5所示。从图5可看出,滤纸表面和横截面结构疏松,孔隙较大。但经过-12℃的8%NaOH-12%尿素- 0.25%ZnO水溶液处理120 min后,纸张表面和横截面结构致密、孔隙较少。这表明在8%NaOH-12%尿素- 0.25%ZnO水溶液中,滤纸纤维无定形区和部分结晶区溶解填充在滤纸纤维孔隙间和吸附在未溶解的纤维素骨架上,在水中再生后,形成大量氢键,减少了孔隙,使结构致密。此外,介质饱和法测定纸张的孔隙率由61.0%降到15.4%。
为分析经过8%NaOH-12%尿素- 0.25%ZnO水溶液处理后,纸张纤维素分子基团和结晶度的变化,对抗油抗菌纸和滤纸进行了FT-IR扫描,结果如图6所示。从图6可知,抗油抗菌纸在3400 cm-1处出现了分子内羟基伸缩振动特征峰,特征峰变宽和向低波数方向移动,表明纤维素分子键间氢键增多。滤纸纤维表面无定型区和部分结晶区溶解,分子间和分子内氢键被破坏,在水中再生时大量的分子间氢键重新生成。此外,经过8%NaOH-12%尿素- 0.25%ZnO水溶液处理后,滤纸纤维的一些特征峰出现偏移。如滤纸纤维特征峰从1430、1111和895 cm-1处偏移至1420、1007和893 cm-1处。这表明经过处理后,纤维素结晶区由Ⅰ向Ⅱ转变。吸收峰由1430 cm-1处偏移至1420 cm-1处表明纤维素Ⅱ和无定形区增多。吸收峰由895 cm-1处偏移至893 cm-1处表明纤维素晶体Ⅰ的减少[23-24]。因此,通过FT-IR谱图可知,滤纸纤维经8%NaOH-12%尿素- 0.25%ZnO水溶液处理后结晶区减少,无定形区增多,分子间氢键增多,有效减少了纸张孔隙,在溶解纤维和未溶解纤维之间形成良好界面,减少应力集中,进而提高纸张强度。
图7为滤纸和抗油抗菌纸的XRD图。由图7可知,滤纸纤维在14.7°、16.6°、22.7°处显示3个最强峰,是纤维素Ⅰ晶型的特征峰;抗油抗菌纸在12.3°、20.3°、22.0°处显示出3个最强峰,是纤维素Ⅱ晶型的特征峰[16]。由此可知,纤维素在8%NaOH-12%尿素- 0.25%ZnO水溶液中发生了纤维素晶型的转变,结晶度由80%下降到53%。滤纸纤维在8%NaOH-12%尿素- 0.25%ZnO水溶液中无定形区润胀溶解后,部分结晶区也被溶解,导致结晶指数降低。溶解纤维的无定形区增加、游离羟基增多和填充在未溶解纤维骨架中的结合面积增大,有利于纸张紧度、抗张指数和耐破指数的提高。
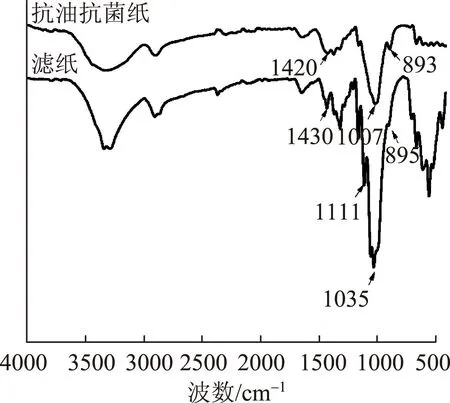
图6 滤纸和抗油抗菌纸的FT-IR图

图7 滤纸和抗油抗菌纸的XRD图

图8 滤纸和抗油抗菌纸对金黄色葡萄球菌和大肠杆菌的抗菌效果
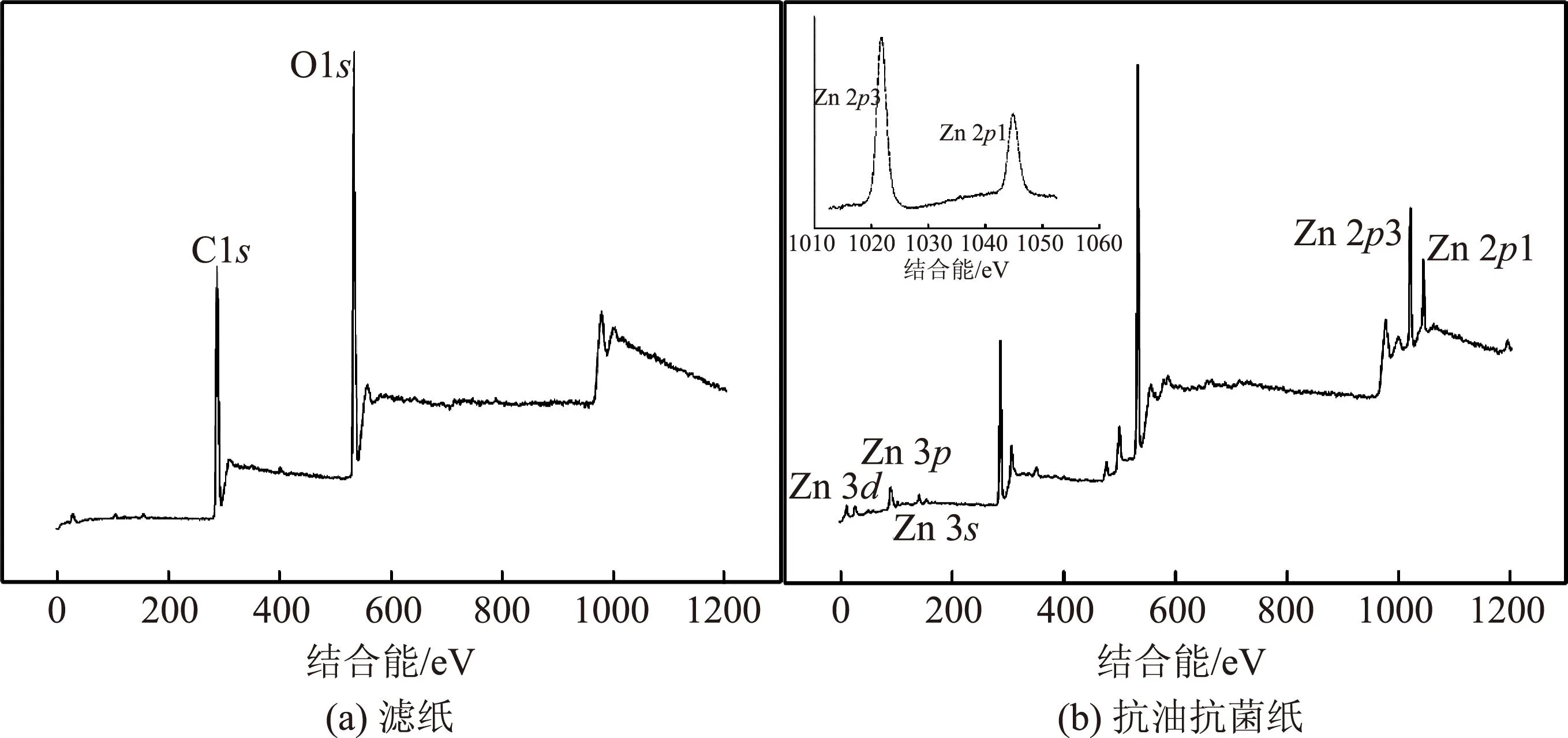
图9 滤纸和抗油抗菌纸的XPS图
2.4纸张抗菌性能评价
图8为滤纸和抗油抗菌纸对金黄色葡萄球菌和大肠杆菌的抗菌效果。如图8所示,经8%NaOH-12%尿素- 0.25%ZnO水溶液处理后的纸样在黑暗和光照下对金黄色葡萄球菌表现出相似大小的抑菌环,但对大肠杆菌的效果却不明显。A.Azam等[25]研究发现,ZnO颗粒对金黄色葡萄球菌表现出的抑菌环比对大肠杆菌表现出的抑菌环大,这可能是因为大肠杆菌比金黄色葡萄球菌具有更强的抗杀力。水溶液中含有4.45×10-5~1.25×10-3mmol/L ZnO颗粒在黑暗条件下才对大肠杆菌表现出明显的抑菌性。在本实验中,大肠杆菌周围没有出现明显的抑菌环,可能因为纸样中ZnO含量少和大肠杆菌具有较高的抗杀力。ZnO的抗菌机理目前还有争议。ZnO抗菌机理有以下几种情况:光催化ZnO释放活性氧(ROS)损坏DNA、细胞膜、细胞蛋白等导致细胞死亡;ZnO与水反应产生活性氧产物如H2O2、HO·等,也属于光催化产生的ROS;Zn2+溶出造成糖酵解跨膜质子转移和耐酸性;ZnO吸附在细菌细胞壁表面或在细胞质内累积造成细胞膜和内部细胞成分(如DNA)受损。为了研究纸样中Zn2+的溶出对抗菌效果的影响,测定了纸样中Zn2+的溶出量,但通过FAAS没有检测到从纸样中溶出Zn2+表现出的吸收峰,表明ZnO能够牢固在纸张纤维表面[15,26-30]。
Berdan等[31-32]认为,Zn2+对于金黄色葡萄球菌的最低抑菌浓度不低于80 mg/L。由FAAS结果可知,纸样中溶出的Zn2+含量低于Zn2+抑菌或杀菌的浓度(2 mg/L)。由此认为,纸样中ZnO产生抗菌效果可能是由ZnO产生了活性氧类物质,如ZnO和水反应产生HO·,当2个HO·相结合时产生H2O2而具有抗菌性。
图9为滤纸和抗油抗菌纸的XPS图。由图9可知,经过8%NaOH-12%尿素- 0.25%ZnO水溶液处理后,纸样的XPS图谱不仅出现了C1s和O1s峰,还出现了Zn 2p、Zn 3s、Zn 3p和Zn 3d峰,表明处理后纸样中不仅含有C、O元素,还含有Zn元素。其中,Zn 2p3和Zn 2p1峰的结合能分别为1022.3 eV和1045.4 eV,相差22.9 eV,意味着存在ZnO[31-33]。
此外,使用FAAS测试了处理纸样中保留的ZnO含量;每克纤维素中含有4.36 μg ZnO;由于ZnO含量较少,在FT-IR图和XRD图中没有出现ZnO的特征峰。ZnO对老鼠的半数致死量大于2000 mg/kg[34-36],因此,纸样中残留的ZnO在安全使用范围内,即制备的抗油抗菌纸具有作为食品包装材料的潜力。
3结论
实验采用NaOH-尿素-ZnO水溶液体系选择性溶解滤纸纤维,制备自增强的抗油抗菌纸;主要探讨了不同溶解条件对纸张抗油、抗菌、强度性能及其形态变化的影响。
(1)制备抗油抗菌纸的关键工艺是使用纤维素溶解体系在滤纸表面选择性溶解,形成均匀基质相吸附在未溶解纤维骨架上,溶解的纤维填充于纤维孔隙中增强纤维间的结合力和降低孔隙率,进而改善纸张的强度性能和抗油性能。
(2)使用8%NaOH-12%尿素- 0.25%ZnO水溶液体系在-12℃中处理滤纸120 min,制备得到的抗油抗菌纸具有最佳的强度性能、抗油及抗菌性能。该抗油抗菌纸的抗张指数和耐破指数是未处理纸张的3倍,在24 h内具有完全阻止油脂渗透的能力,且对金黄色葡萄球菌也具有明显的抗菌效果。
参考文献
[1]Khaoula khwaldia Elmira A-T, Stephane Desobry. Biopolymer coatings on paper packaging materials[J]. Comprehensive Reviews in Food Science and Food Safety, 2010(9): 82.
[2]Cha D S, Chinnan M S. Biopolymer-Based Antimicrobial Packaging: A Review[J]. Critical Reviews in Food Science and Nutrition, 2004, 44: 223.
[3]Ham-Pichavant F, Sèbe G, Pardon P, et al. Fat resistance properties of chitosan-based paper packaging for food applications[J]. Carbohydrate Polymers, 2005, 61: 259.
[4]Kjellgren H, Gällstedt M, Engström G, et al. Barrier and surface properties of chitosan-coated greaseproof paper[J]. Carbohydrate Polymers, 2006, 65: 453.
[5]HENRIK KJELLGREN G E. The relationship between energy requirement and barrier properties in the production of greaseproof paper[J]. TAPPI JOURNAL, 2005(4): 8.
[6]Raheem D. Application of plastics and paper as food packaging materials-an overview[J]. Emirates Journal of Food and Agriculture, 2012, 25: 177.
[7]Ma Jinxia, Zhou xiaofan, Xiao Huining. Effect of NaOH/urea solution on enhancing grease resistance and strength of paper[J]. Nordic Pulp & Paper Research Journal, 2014, 29: 246.
[8]Kjellgren H. Barrier properties of greaseproof paper[D]. Karlstad: Karlstad University, 2005.
[9]Bruno Medronho B L. Brief overview on cellulose dissolution/regeneration interactions and mechanisms[J]. Advance in Colloid and Interface Science, 2014(222): 502.
[10]Cai J, Zhang L, Chang C, et al. Hydrogen-bond-induced inclusion complex in aqueous cellulose/LiOH/urea solution at low temperature[J]. Chemphyschem, 2007(8): 1572.
[11]刘睿, 韩卿, 钱威威. 纤维在NaOH-尿素体系中的溶解性能[J]. 中国造纸, 2015, 34(7): 18.
[12]吴翠玲, 李新平, 秦胜利. 纤维素溶剂研究现状及应用前景[J]. 中国造纸学报, 2004, 19(2): 171.
[13]龙柱, 邓海波, 李中石, 等. 4种天然纤维素在氢氧化钠-尿素-水体系中的溶解差异[J]. 中国造纸学报, 2012, 27(3): 43.
[14]Yang Quanling, Qi Haisong, Lue Ang, et al. Role of sodium zincate on cellulose dissolution in NaOH/urea aqueous solution at low temperature[J]. Carbohydrate Polymers, 2011, 83: 1185.
[15]He L, Liu Y, Mustapha A, et al. Antifungal activity of zinc oxide nanoparticles againstBotrytiscinereaandPenicilliumexpansum[J]. Microbiol Res, 2011, 166: 207.
[16]Wang Y, Deng Y. The kinetics of cellulose dissolution in sodium hydroxide solution at low temperatures[J]. Biotechnol Bioeng, 2009, 102: 1398.
[17]Cai Jie, Zhang Lina, Liu Shilin, et al. Dynamic Self-Assembly Induced Rapid Dissolution of Cellulose at Low Temperatures[J]. Macromolecules, 2008, 41: 9345.
[18]Zhang S, Li F-X, Yu J-y, et al. Dissolution behaviour and solubility of cellulose in NaOH complex solution[J]. Carbohydrate Polymers, 2010, 81: 668.
[19]Wei Yuping, Cheng Fa, Hou Guili, et al. Amphiphilic cellulose-Surface activity and aqueous[J]. Reactive & Functional Polymers, 2008, 68: 981.
[20]王志杰, 王李. NaOH-尿素体系对棉纤维润胀性能的影响[J]. 中国造纸, 2015, 34(8): 24.
[21]Zhang Lina, Mao Yuan, Zhou Jinping, et al. Effects of Coagulation Conditions on the Properties of Regenerated Cellulose Films Prepared in NaOH/Urea Aqueous Solution[J]. Industrial & Engineering Chemistry Research, 2005, 44: 522.
[22]Brahim S B, Cheikh R B. Influence of fibre orientation and volume fraction on the tensile properties of unidirectional Alfa-polyester composite[J]. Composites Science and Technology, 2007, 67: 140.
[23]Oh S Y, Yoo D I, Shin Y, et al. FTIR analysis of cellulose treated with sodium hydroxide and carbon dioxide[J]. Carbohydrate Research, 2005, 340: 417.
[24]Carrillo F, Colom X, Suol J J, et al. Structural FTIR analysis and thermal characterisation of lyocell and viscose-type fibres[J]. European Polymer Journal, 2004, 40: 2229.
[25]Azam A, Ahmed A S, Oves M, et al. Antimicrobial activity of metal oxide nanoparticles against Gram-positive and Gram-negative bacteria: a comparative study[J]. Int J Nanomedicine, 2012, 7: 6003.
[26]ByGuy Applerot A L, Rachel Dror, Nina Perkas, et al. Enhanced Antibacterial Activity of Nanocrystalline ZnO[J]. Advance Functional Material, 2009, 19: 842.
[27]Espitia P J P, Soares N d F F, Coimbra J S d R, et al. Zinc Oxide Nanoparticles: Synthesis, Antimicrobial Activity and Food Packaging Applications[J]. Food and Bioprocess Technology, 2012, 5: 1447.
[28]Raghupathi K R, Koodali R T, Manna A C. Size-dependent bacterial growth inhibition and mechanism of antibacterial activity of zinc oxide nanoparticles[J]. Langmuir, 2011, 27: 4020.
[29]Xie Y, He Y, Irwin P L, et al. Antibacterial activity and mechanism of action of zinc oxide nanoparticles againstCampylobacterjejuni[J]. Appl Environ Microbiol, 2011, 77: 2325.
[30]Zhang L, Jiang Y, Ding Y, et al. Mechanistic investigation into antibacterial behaviour of suspensions of ZnO nanoparticles againstE.coli[J]. Journal of Nanoparticle Research, 2009, 12: 1625.
[31]Berdan Aydin Sevinc, Luke Hanley. Antibacterial activity of dental composites containing zinc oxide nanoparticles[J]. Journal of Biomedical Materials Research Part B: Applied Biomaterials, 2010, 94B: 22.
[32]Sawai J. Quantitative evaluation of antibacterial activities of metallic oxide powders(ZnO, MgO and CaO) by conductimetric assay[J]. Journal of Microbiological Methods, 2003, 54: 177.
[33]Chennakesavulu K, Reddy M M, Reddy G R, et al. Synthesis, characterization and photo catalytic studies of the composites by tantalum oxide and zinc oxide nanorods [J]. Journal of Molecular Structure, 2015, 1091: 49.
[34]Andre Nel, Tian Xia, Lutz Madler, et al. Toxic Potential of Materials at the Nanolevel [J]. Science, 2006, 311: 622.
[35]Lab S. Material Safety Data Sheet Zinc oxide MSDS[OL]. http://wwwsciencelabcom.2013.
[36]Stella W Y, Wong Priscilla. Toxicities of nano zinc oxide to five marine organisms: influences of aggregate size and ion solubility[J]. Anal Bioanal Chem, 2010, 396: 609.
(责任编辑:常青)
Preparation of Antibacterial and Oil-resistant Paper Using a NaOH-urea-ZnO Solution
JIAO LiMA Jin-xia*DAI Hong-qi
(DepartmentofPulpandPaperScienceandTechnology,NanjingForestryUniversity,Nanjing,JiangsuProvince, 210037) (*E-mail: jxma@njfu.edu.cn)
Abstract:The surface of filter paper was selective dissolved using NaOH-urea-ZnO (mass ratio of 8∶12∶0.25) aqueous solution. The effects of processing time and temperature on the mechanical properties of the paper were evaluated. The paper was characterized using Scanning Electron Microscopy (SEM), X-ray Diffraction (XRD), Fourier Transform Infrared Spectroscopy (FT-IR). The content of ZnO in sample was measured by Atomic Absorption Spectrophotometer (AAS) and X-ray photoelectron spectroscopy (XPS). The oil-resistance and antibacterial properties of the produced paper were also investigated. The results showed that the tensile and burst strengths of the paper were 2 times higher than that of the original at an optimum processing condition. Meanwhile, the treated paper was completely oil-resistant within 24 h and demonstrated good antibacterial properties when exposed to Staphylococcus aureus. The residual zinc oxide content in the paper could meet the safety regulation of food packaging. The prepared antibacterial and oil-resistant paper has good potential to be packaging material.
Keywords:NaOH-urea-ZnO solvent; oil-resistant; antibacterial
中图分类号:TS761
文献标识码:A
文章编号:1000- 6842(2016)01- 0013- 07
作者简介:焦丽,女,1987年生;在读博士研究生;主要研究方向:造纸化学品。*通信联系人:马金霞,E-mail:jxma@njfu.edu.cn。
收稿日期:2015-10-23
本课题得到国家自然科学基金(31470599)、江苏省优势学科(PAPD)、南京林业大学博士论文创新基金和江苏省创新工程(KYZZ15- 0254)的资助。

