高良姜素对哮喘小鼠气道炎症及肿瘤坏死因子-α表达的影响
谷奕诺 吴艳玲
(延边大学药学院,吉林 延吉 133002)
高良姜素对哮喘小鼠气道炎症及肿瘤坏死因子-α表达的影响
谷奕诺 吴艳玲
(延边大学药学院,吉林 延吉 133002)
目的 探讨高良姜素对哮喘小鼠气道炎症及肿瘤坏死因子(TNF)-α表达的影响。方法 40只小鼠随机分为正常对照组、哮喘组、地塞米松组、高良姜素组。卵白蛋白致敏并激发建立小鼠哮喘模型,计数支气管肺泡灌洗液(BALF)中嗜酸性粒细胞,观察支气管肺组织病理的改变,酶联免疫吸附(ELISA)法检测血清TNF-α的水平,Western印迹法检测肺组织TNF-α 蛋白的表达。结果 高良姜素组BALF中嗜酸粒细胞计数及肺内炎症细胞评分明显低于哮喘组(P<0.01);哮喘组血清TNF-α含量、肺组织TNF-α 蛋白表达均显著高于正常对照组,高良姜素组上述指标均低于哮喘组(P<0.01)。结论 高良姜素可降低哮喘小鼠TNF-α的表达,减轻哮喘小鼠气道炎症。
哮喘;高良姜素;肿瘤坏死因子-α
哮喘是一种以慢性气道炎症和气道高反应性为特征的变态反应性疾病为发病机制并未完全阐明,普遍认为炎症细胞在气道的浸润及其分泌的炎症介质介导了哮喘的炎症过程〔1〕。研究表明肿瘤坏死因子(TNF)-α是介导其炎症发生的重要因素〔2〕。目前,糖皮质激素仍是哮喘治疗的一线药物,但因长期应用存在的不良反应,开发新的抗哮喘药物十分必要。高良姜素(3,5,7-三羟基黄酮)是一种黄酮类化合物,广泛存在于高良姜和蜂胶中,具有多种药理学活性,如抗肿瘤、抗微生物、抗感染、抗氧化等〔3~5〕。研究表明,高良姜素可通过阻断组胺的释放及包括TNF在内的炎症介质表达而下调肥大细胞源性过敏性炎症〔6〕,但高良姜素对哮喘的治疗作用及机制并不很清楚。本研究应用高良姜素干预卵白蛋白(OVA)诱导的过敏性哮喘小鼠模型,探讨其对哮喘气道炎症的作用及可能机制。
1 材料与方法
1.1 材料 实验动物:清洁级8~10周龄(体重20~24 g)的雌性BALB/c小鼠40只,购自吉林大学白求恩医学部动物室。试剂:高良姜素(Sigma公司)、OVA(Sigma公司)、氢氧化铝凝胶(Sigma公司)、小鼠TNF-α酶联免疫吸附(ELISA)检测试剂盒(武汉博士德生物有限公司)、TNF-α抗体(Cell Signaling公司)。设备:超声雾化器(德国百瑞公司)、Olympus显微镜(日本Olympus公司)、电泳仪、转膜仪(Bio-rad公司)。
1.2 方法
1.2.1 哮喘模型的建立及分组 将小鼠随机分为4组:正常对照组、哮喘组、地塞米松组、高良姜素组,每组10只,适应性喂养1 w。哮喘组:于实验第0、7、14天致敏,腹腔注射1 mg氢氧化铝乳化的OVA 20 μg。在第21~23天激发,以超声雾化器雾化3% OVA盐水气溶胶吸入,1次/d,30 min/次。地塞米松组及高良姜素组:哮喘模型建立同哮喘组,但于每次激发前3 h,分别腹腔注射高良姜素(10 mg/kg)和地塞米松(2 mg/kg)。正常对照组:腹腔注射及雾化时均给予同体积生理盐水。于末次激发后24 h处死小鼠,取血、支气管肺泡灌洗液及肺组织。
1.2.2 支气管肺泡灌洗液(BALF)中嗜酸性粒细胞计数 各组小鼠BALF低速离心10 min,沉渣以1 ml的Hanks液重悬,取0.1 ml重悬液涂片做吉姆萨染色,计数至少200个细胞做嗜酸性粒细胞计数。
1.2.3 肺组织病理学检查 取小鼠左肺组织以10%甲醛溶液固定,常规脱水石蜡包埋切片,做苏木素-伊红(HE)染色,乙醇脱水,透明封片,镜检观察肺组织的炎性浸润情况。以Myou等〔7〕制定的5分评分系统为标准半定量评定支气管周围炎症细胞浸润程度,根据支气管周围炎性细胞的多少评分,评判标准:无炎性细胞环绕(0分);少量炎性细胞环绕(1分); 1个细胞层厚度的炎性细胞环绕(2分); 2~4个细胞层厚度炎性细胞环绕(3分);多于4个细胞层厚度的炎性细胞环绕(4分)。
1.2.4 ELISA法检测血清TNF-α 末次雾化激发24 h后麻醉小鼠,摘眼球取血约500 μl,2 000 r/min离心2~3 min,取上清即为血清。根据ELISA检测试剂盒的说明书操作,测定各组小鼠血清中TNF-α含量。
1.2.5 Western印迹法检测肺组织TNF-α的表达 提取各组小鼠肺组织的总蛋白,BCA 法测定蛋白浓度,行SDS-PAGE电泳,转膜1 h后洗涤,分别加1∶1 000稀释的兔抗TNF-α抗体、兔抗β-actin抗体(1∶500),4℃孵育过夜。将 PVDF 膜洗涤后,将其浸泡于二抗中,室温下摇床摇荡1 h。再次洗膜,ECL 试剂盒化学发光法显示蛋白条带,图像分析软件测定蛋白条带的吸光度(A) 值。
1.3 统计学方法 采用SPSS16.0软件进行t检验。
2 结 果
2.1 各组小鼠BALF中嗜酸性粒细胞计数及肺内炎症细胞评分比较 哮喘组BALF中嗜酸性粒细胞数目及炎症细胞评分较其他各组显著升高(P<0.01)。高良姜素组与地塞米松组比较差异无统计学意义。见表1。
2.2 各组小鼠肺组织HE染色的改变 镜下可见正常对照组肺泡结构清晰,肺泡间隔无水肿增厚及炎性细胞浸润;哮喘组肺泡结构破坏,支气管及血管周围可见大量炎性细胞浸润,肺泡间隔明显增宽;地塞米松组及高良姜素组较哮喘组支气管及血管周围炎性细胞浸润明显减少,肺泡壁未见明显增厚(见图1)。
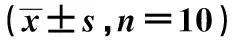
表1 各组小鼠BALF中嗜酸性粒细胞计数及 肺内炎症细胞评分
与正常对照组比较:1)P<0.01;与哮喘组比较:2)P<0.01
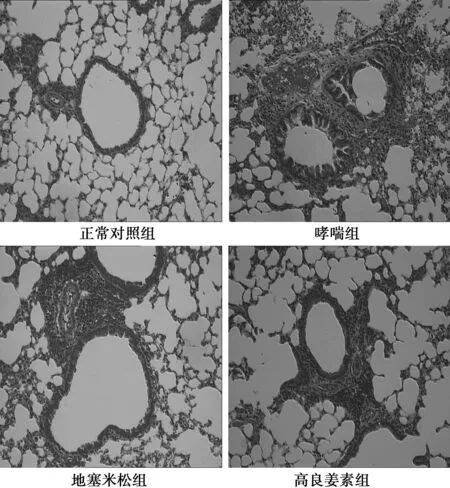
图1 高良姜素对哮喘小鼠肺组织HE染色的影响(×200)
2.3 各组小鼠血清TNF-α水平比较 哮喘组血清TNF-α水平(195.66±14.64)pg/ml明显高于正常对照组(117.67±15.82)pg/ml(P<0.01);高良姜素组(144.05±9.54)pg/ml低于哮喘组(P<0.01)。高良姜素组与地塞米松组(137.00±12.12)pg/ml差异无统计学意义。
2.4 各组小鼠肺组织TNF-α蛋白表达的变化 哮喘组肺组织TNF-α蛋白表达水平(1.85±0.39)明显高于正常对照组(1.0)(P<0.01);高良姜素组(1.49±0.31)低于哮喘组(P<0.01)。高良姜素组与地塞米松组(1.36±0.29)差异无统计学意义。见图2。
图2 各组小鼠肺组织TNF-α蛋白表达的变化
3 讨 论
哮喘是一种以气道高反应性为主要特征的气道慢性非特异性炎症性疾病,多种炎症细胞及炎症介质介导了哮喘的发生发展过程。嗜酸性粒细胞、淋巴细胞和肥大细胞等炎症细胞浸润是哮喘气道炎症的实质,而嗜酸性粒细胞反应又是其中的关键特征。嗜酸性粒细胞通过释放前炎症介质、细胞毒性介质和细胞因子而调节气道炎症和重塑过程的启动。本实验结果与之前的相关研究结果一致〔8〕,表明高良姜素具有减轻OVA诱导的哮喘小鼠气道炎症的作用。
TNF-α是一种具有多种生物学效应的前炎症细胞因子,主要由单核-巨噬细胞分泌,与机体的炎症、免疫反应有着十分密切的关系〔2〕。Farjadian等〔9〕报道哮喘患儿血清TNF-α水平明显高于正常对照组,经天然抗炎症药物如ω-3治疗后,哮喘患儿肺功能明显好转的同时血清TNF-α水平较治疗前下降,提示药物可能通过调节TNF-α的表达起到抗哮喘的作用。本研究结果表明TNF-α参与了哮喘的发病。
研究表明,高良姜素可以有效抑制臭氧所致慢性阻塞性肺疾病小鼠气道炎症的发生,降低血清中TNF-α等炎症因子的水平〔10〕。另有学者研究显示高良姜素可以减轻哮喘小鼠的气道高反应性,降低支气管肺泡灌洗液中白细胞介素(IL)-4、-5、-13的水平,其可能的作用机制是通过抑制核转录因子(NF)-κB通路〔9〕。本实验结果提示高良姜素减轻哮喘气道炎症的可能机制包括对TNF-α表达的影响。
1 Saglani S,Lloyd CM.Novel concepts in airway inflammation and remodeling in asthma〔J〕.Eur Respir J,2015;46(6):1796-804.
2 Tan HT,Sugita K,Akdis CA.Novel biologicals for the treatment of allergic diseases and asthma〔J〕.Curr Aller Asthma Rep,2016;16(10):70.
3 Benguedouar L,Lahouel M,Gangloff SC,etal.Ethanolic extract of algerian propolis and galangin decreased murine melanoma T〔J〕.Anticancer Agents Med Chem,2016;16(9):1172-83.
4 Navarro-Navarro M,Ruiz-Bustos P,Valencia D,etal.Antibacterial activity of Sonoran propolis and some of its constituents against clinically significant Vibrio species〔J〕.Foodborne Pathog Dis,2013;10(2):150-8.
5 Jung YC,Kim ME,Yoon JH,etal.Anti-inflammatory effects of galangin on lipopolysaccharide-activated macrophages via ERK and NF-κB pathway regulation〔J〕.Immunopharmacol Immunotoxicol,2014,36(6):426-32.
6 Kim HH,Bae Y,Kim SH.Galangin attenuates mast cell-mediated allergic inflammation〔J〕.Food Chem Toxicol,2013;57:209-16.
7 Myou S,Leff AR,Myo S,etal.Blockade of inflammation and airway hyperresponsiveness in immune-sensitized mice by dominant-negative phosphoinositide 3-kinase-TAT〔J〕.J Exp Med,2003;198(10):1573-82.
8 Zha WJ,Qian Y,Shen Y,etal.Galangin abrogates ovalbumin-induced airway inflammation via negative regulation of NF-κB〔J〕.Evid Based Complement Alternat Med,2013;767689.
9 Farjadian S,Moghtaderi M,Kalani M,etal.Effects of omega-3 fatty acids on serum levels of T-helper cytokines in children with asthma〔J〕.Cytokine,2016;85:61-6.
10 王晓月,葛 爱,孙培莉 等.高良姜素对臭氧所致COPD 气道炎症的影响〔J〕.南京医科大学学报:自然科学版,2016;36(6):700-4.
〔2016-10-25修回〕
(编辑 郭 菁/滕欣航)
吴艳玲(1977-),女,副教授,博士,硕士生导师,主要从事中药药理学研究。
谷奕诺(1995-),男,在读本科,主要从事呼吸药理学研究。
R562.2+5
A
1005-9202(2017)05-1096-02;
10.3969/j.issn.1005-9202.2017.05.025

