先天性Ⅶ缺乏症孕妇围产期凝血功能分析及治疗思路
梁晓浏 林正明 江建锋 杨园园
·论著·
先天性Ⅶ缺乏症孕妇围产期凝血功能分析及治疗思路
梁晓浏 林正明 江建锋 杨园园
目的 分析1例先天性Ⅶ缺乏症孕妇围产期凝血功能并讨论治疗策略。方法 对1例先天性Ⅶ缺乏孕妇围产期不同时间点的血液样本,采用凝固法测定患者血浆凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、血浆凝血酶时间(TT),采用Clauss凝固法测定血浆纤维蛋白原(Fbg)、采用胶乳免疫比浊法测定D-二聚体(DD)及抗凝血酶Ⅲ(ATⅢ)。结果 围产期替代治疗前患者凝血功能指标表现为PT延长,Fbg轻度上升,其余指标正常,术前给予重组VII生物活性制剂,1 h内患者出现PT缩短,呈现高凝状态;术中患者凝血功能未发生紊乱;手术分娩后患者凝血功能逐渐变为异常,表现为PT延长,DD增高,术后3 d PT水平基本恢复到术前状态。 结论 围产期动态检测凝血功能指标,特别是PT的变化情况,对本例先天性Ⅶ缺乏孕妇行剖宫产分娩极为重要,同时结合其他凝血、纤溶指标可有效实时判断患者体内凝血功能状况。
先天性Ⅶ缺乏 围产期 凝血功能 治疗策略
凝血因子Ⅶ(FⅦ)是1种由406个氨基酸残基构成的多肽链,相对分子量为6.0×104,属丝氨酸蛋白酶家族,由肝脏合成(依赖Vit K),在血液中含量少(约为2 mg/L)且半衰期短(4~6 h),主要参与激活机体外源性凝血途径。先天性FVII缺乏是1种较罕见的遗传性凝血功能缺陷疾病,个体发病率约为1:50万,研究证明其主要遗传规律为杂合子遗传,患者临床表现不一,从无异常症状到潜在的致命性皮肤、粘膜出血不等。而先天性FⅦ缺乏症孕妇更罕见,干预替代治疗主要是预防性应用重组Ⅶ生物活性制剂(rFⅦa),但给药时机和剂量较关键[1]。
本院于2016年收治1例先天性FⅦ缺乏症孕妇,在术前适当时机给予rFⅦa进行干预替代治疗,患者顺利行剖宫产分娩,通过对其围产期凝血功能的动态检测,为预防术中及产后出血等并发症的发生提供参考依据。
材料与方法
1 样本来源 1例来自本院收治的FⅦ缺乏孕妇,28岁,既往于2003年在上海瑞金医院确诊为遗传性凝血因子Ⅶ缺乏症并建议不宜妊娠,平素无皮肤、粘膜出血倾向。入院时体重67 kg,初步诊断:G1P0孕37+1周待产,分娩脐带绕颈2周,遗传性FVII缺乏症。采用枸橼酸钠抗凝真空采血试管(抗凝剂浓度0.109 mol/L,抗凝剂:血液=1∶9)按标准操作规程采集静脉血约2 ml,采血后轻轻颠倒混匀8次并立即由专人送检。
2 试剂与仪器 所用检测试剂和质控品均来源于德国西门子公司,具体名称及批号:P T(Thromborel☒ S 批号546910)、APTT(Dade☒Actin☒ Activated Cephalopplastin Reagent,批号557210)、Fbg(Dade☒ Thrombin Reagent,批号547283)、TT(Test Thrombin Reagent,批号4 6 1 6 6)、D-d i m e r(I N N O V A N C E☒D-Dimer,批号46428)、AT III.(Berichrom☒Antithrombin III(A),批号46343)、OVB(Dade☒ Owren’s Veronal Buffer ,批号547091)、CaCl2(Cacium Chloride Solution 0.025 mol/L,批号539776)、正常值质控血清(Dade☒ Ci-Trol☒ 1 ,批号548029)、高值质控血清(Dade☒ Ci-Trol☒ 2 ,批号548261)、低速离心机(科大中佳 型号KDC-40)、全自动血凝分析仪(日本希森美康,型号CS5100、CA7000)
3 检测方法
3.1 检测流程:检测前依据标准操作规程开机、清洗、预温,按试剂说明书准确配制检测用试剂及正常值质控血清、高值质控血清,所配试剂及质控品于室温平衡30 min再放入仪器检测,质控品所得数值对照说明书提供的靶值和参考范围,结合本实验室室内质控规则(源于Westgard规则),查看LIS质控系统中L-J曲线显示当日检测在控。接收样本,核对患者信息并观察标本量及抗凝效果(是否有血凝块),判定合格后立即以3 000 r/min(1 610 g离心力)速度离心15 min,小心取出试管(尽量垂直取放以免样本重悬)拔盖后上机检测。
3.2 检测结果判定:本实验室已建立凝血相关指标正常参考范围,分别为:PT(10~14 s)、INR(0.85~1.15)、APTT(20~40 s)、Fbg(2~4.75 g/L)、TT(14~21 s)、DD(0~0.55 mg/L)、AT-III(75%~125%),血凝分析仪检测所得数值同步上传LIS系统后自动判定,在多次送检样本中发现1次PT结果显示“未检出”,查看血凝仪反应曲线后作出判定。
结 果
针对该例FⅦ缺乏症孕妇围产期凝血功能相关指标的检测,结果显示术前除PT明显延长,INR值升高外,其余指标基本处于正常参考范围见表1。该患者于手术麻醉前静脉推注重组因子Ⅶ生物活性制剂(rFⅦa)4 mg,给药剂量主要依据患者体重及药品说明书提供的指导用药量。给药20 min后(术前约1 h)抽血检测显示PT为“未检出”,见表1。观察反应曲线,见图1。初步判定为高凝状态,电话告知临床。于50 min后(术前约0.5 h)再次抽血检测得出PT为7.1 s,INR为0.68,遂全麻下行子宫下段剖宫产术,成功分娩1名活男婴,术中出血约400 ml,无其他异常。术后动态检测凝血相关指标,显示PT逐渐延长,第3天PT基本恢复到术前水平,可能和rFⅦa在患者体内代谢率相关。此时患者虽PT明显延长,但并无皮肤、粘膜出血症状。其他指标除DD上升、AT-Ⅲ呈波动性变化(先轻度下降后恢复正常)外均无异常。

表1 围产期凝血指标结果
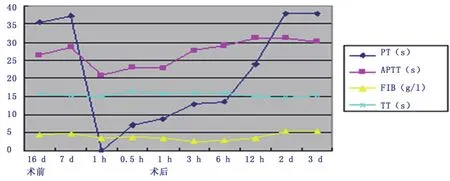
图1 围产期主要凝血指标变化趋势
讨 论
凝血因子Ⅶ(FⅦ)缺乏症依据病因可分为先天性和获得性两种,FⅦ是依赖于Vit K由肝脏合成,故肝脏疾病、Vit K缺乏或使用Vit K拮抗剂等均可导致获得性FⅦ缺乏,而部分原发性疾病(如系统性红斑狼疮、抗磷脂综合征等)患者体内可伴随出现凝血因子抑制物,且大部分以抗体形式存在,能部分或完全中和一种或多种凝血因子活性与功能,可引起PT或APTT延长[2]。先天性FVII缺乏症可由常染色体隐性遗传引起,发病率1∶(50万~200万),据数据库统计显示,FVII基因突变至少有124种,包括错义、无义、剪切位点、启动子、小的插入和缺失等6种。
2016年Napolitano[3]等统计分析449例遗传性FⅦ缺乏症(男215例,女234例),并评估女性患者临床体征及性别差异性,女性患者主要表现为粘膜出血、妇科出血。结论:长期预防性给予rFVIIa制剂替代治疗可有效降低月经过多、铁离子丧失甚至避免子宫切除。
先天性FⅦ缺乏症患者临床体征表现不一。研究发现[4]:出血等症状出现及严重程度和FVII活性水平并无必然关联,给长期预防性应用rFⅦa治疗带来挑战。实验室直接测定FⅦa水平是临床诊断的首选方法,相关检测包括基因测序等,但目前不能凭借单项实验结果可准确预测出血风险。而国外学者研究也发现[5]:在FⅦ缺乏患者需手术治疗时,用rFⅦa进行术前替代治疗,将患者FⅦ活性水平强制性提升到15 %以上并非必须,相对来说患者的出血病史更重要。
Baumann Kreuziger[6]等收集了1953~2011年FⅦ缺乏孕妇手术相关报道,涉及62名孕妇分娩94例活婴,FⅦa为5.5%,有32%的孕妇分娩前进行了预防性止血治疗。结果显示:rFⅦa可用于手术前干预治疗,但并非强制性预防措施。本次报道的先天性FⅦ缺乏症孕妇,住院期间曾外地送检FⅦa,结果仅为1.8%,但患者住院期间并无皮肤、粘膜出血症状,孕期内也未给予rFⅦa进行预防治疗。因条件限制在围手术期无法做到动态监测FⅦa水平,我们通过对患者凝血功能指标特别是PT的动态检测,在给予rFⅦa后适当时机(50 min)行剖宫产手术,获得较满意的结果。患者给药后短期内出现高凝状态,可能与孕妇自身存在的应激状态有关,且当体内FⅦa水平高于正常时,亦有可能发生血栓或弥散性血管内凝血(DIC)的潜在风险,特别对于FⅦa缺乏的孕妇。故给药后手术时机的选择尤为重要,须综合考虑患者凝血功能指标和临床体征。
目前对遗传性FⅦ缺乏症研究焦点主要集中在应用rFⅦa进行替代治疗的时机和剂量。针对不同临床症状、年龄、性别等因素,报道的结果也不相同,将来的治疗趋势可能发展为个性化治疗。但毫无争论的是,围手术期术前患者凝血功能检测出现异常必须引起高度重视。对有凝血功能障碍且无临床出血症状的病例,术前应进行多学科讨论,及时实施干预性治疗,可有效预防术中、术后致命性出血的发生。Jones[7]等报道1例患颅缝早闭婴儿,2个月时行选择性修复术,术前实验室检测确定为PT延长,患儿无任何临床出血史,麻醉、外科、血液科等会诊后确定为FⅦ缺乏症。最新报道[8]显示:对4例家族性FⅦ缺乏患儿给予rFⅦa治疗,在婴儿期每周给予2~3次、每次(15~30) μg/kg的治疗方案(最佳剂量、治疗间隔及疗效)安全有效。
本例报道患者剖宫产成功分娩1例男性活婴,新生儿初步诊断为“新生儿高胆红素血症、新生儿肺炎”,体格检查显示:患儿后背见少许出血点,双肺呼吸音粗。凝血功能检查:PT 16.7 s 、APTT 59 s 、Fbg 0.9 g/L,其他指标无明显异常。给予25 ml/次/天新鲜冰冻血浆输注治疗,2 d后体征好转。因患者要求自动出院,故未进一步作相关检测。
总之,国内目前受临床诊疗及实验室检测水平的诸多条件限制,加之患者经济条件的制约,对先天性FⅦa缺乏症孕妇制定精准的预防性治疗方案,且实施后达到满意的临床效果并不多见,本例报道为其诊疗提供了新思路。
1 Baumann Kreuziger LM,Morton CT,Reding MT. Is prophylaxis required for delivery in women with factor VII deficiency?[J] Haemophilia,2013,19(6):827-832.
2 Vanessa Afonso da Silva,Sheila Soares Silva,and Fabrício Frederico Mendes Martins.Acquired deficiency of coagulation factor VII[J].Rev Bras Hematol Hemoter,2015,37(4):269–271.
3 Napolitano M,Di Minno MN,Batorova A,et al. Women with congenital factor VII deficiency:clinical phenotype and treatment options from two international studies[J]. Haemophilia. 2016,22(5):752-759.
4 Sevenet PO,Kaczor DA,Depasse F. Factor VII Deficiency:From Basics to Clinical Laboratory Diagnosis and Patient Management[J]. Clin Appl Thromb Hemost,2016,1:1076029616670257.
5 Woehrle D,Martinez M,Bolliger D. Hereditary heterozygous factor VII deficiency in patients undergoing surgery :Clinical relevance[J]. Anaesthesist,2016,65(10):746-754.
6 Jones KL,Greenberg RS,Ahn ES,et al. Elevated prothrombin time on routine preoperative laboratory results in a healthy infant undergoing craniosynostosis repair:Diagnosis and perioperative management of congenital factor VII deficiency[J]. Int J Surg Case Rep,2016,24:77-79.
7 Kuperman AA,Barg AA,Fruchtman Y,et al. Primary prophylaxis for children with severe congenital factor VII deficiency-Clinical and laboratory assessment[J]. Blood Cells Mol Dis,2016 Dec 19. pii:S1079-9796(16)30204-2.
Analysis of the Coagulation Function of a Pregnant with Congenital Factor Ⅶ deficiency in Peripartum Period and Discussion of Treatment Strategy
LIANG Xiao-liu,LIN Zheng-min,JIANG Jian-feng,et al.
Department of Blood Transfusion,The First People's Hospital of Hefei,Hefei 230061
Objective Analysis the coagulation function of a perinatal pregnant with congenital VII deficiency and the discussion of the treatment strategy. Methods Blood samples from a pregnant with congenital factor VII deficiency at the different time points in peripartum period was collected,plasma clot formation is used to determine the prothrombin time (PT),activated partial thromboplastin time (APTT),thrombin time (TT),Clauss method is used to determine the fibrinogen (Fbg),partcle-enhance immunoturbidimeric assay is used to determine D-dimer (DD)and antithrombin-III. Results Before the prophylactic substitution treatment in peripartum period,PT was prolonged and Fbg was mild rised,the other index was normal,recombinant activated factor VII (rFVIIa)was given to patients within 1 hour in preoperative,the pregant is characterized by PT shorten and presented high coagulation state. Intraoperative coagulation function was normal and no bleeding complications; postoperation coagulation function became abnormal,characterized by PT extension,higher DD and after 3 days PT was recovered to preoperative levels. Conclusion It may be essential to deteced coagulation function in the perinatal pregnants with congenital factor VII deficiency dynamically,especially the change of PT,such this case of cesarean delivery. Other indexes of coagulation and fibrinolytic may be judge patient's coagulation function effectively.
Congenital factor Ⅶ deficiency Peripartum Coagulation function Treatment strategy
R457.1
A
1671-2587(2017)04-0400-04
2016-11-30)
(本文编辑:姚萍)
10.3969/j.issn.1671-2587.2017.04.026
230061 安徽省合肥市第一人民医院输血科
梁晓浏(1973–),男,安徽无为人,主管技师,硕士,主要从事临床输血工作,(E-mail)809508387@qq.com。

