骨盆Ⅰ区及Ⅰ+Ⅳ区肿瘤切除和重建术后内固定失败的预后因素分析
林鹏 林秾 潘伟波 黄鑫 叶招明
(浙江大学医学院附属第二医院骨科,杭州 310009)
手术切除治疗是目前治疗骨盆Ⅰ区及Ⅰ+Ⅳ区原发性肿瘤以及一些孤立性转移性肿瘤的主要方式[1,2]。与半骨盆截肢相比,尽管保肢手术后肿瘤局部复发的风险相对较高,但其可以更好地保留患肢功能[3,4]。骨盆肿瘤的保肢手术具有一定的挑战[5],但随着大量的临床实践以及影像学检查、辅助治疗手段、手术技术和重建材料的发展,此类手术的疗效有了很大进步[2,6-8]。
肿瘤切除术后重建的方法较多,有切除后旷置[9]、不同类型的钉棒系统固定[10-15]、植骨[16,17]、骨水泥联合接骨板或螺钉固定[18,19]、假体固定[20]等。重建手术的目的是恢复骨盆环的连续性和稳定性,允许患者早期活动,减少负重后骨盆残余部分的扭转和塌陷,更好地保留患者术后的肢体功能[2,5-7,21]。钉棒系统内固定重建已成为治疗骨盆Ⅰ区及Ⅰ+Ⅳ区肿瘤切除术后骨缺损的主要治疗方式之一,但固定方式尚无统一认识,文献报道不同固定方式的内固失败率也有所差异。本研究比较不同钉棒系统固定术后的结果和并发症,探讨术后内固定失败的危险因素。
1 资料与方法
1.1 临床资料
回顾性分析2003年5月至2017年2月我院收治的54例累及骨盆Ⅰ区或Ⅰ+Ⅳ区的肿瘤患者,其中12例患者因为随访资料不完善,予以排除。最终,共有42例患者纳入本研究,其中男23例,女19例;年龄15~69岁,平均(41.0±17.7)岁。所有病例均进行了骨盆肿瘤切除以及单棒双钉或双棒四钉的钉棒系统重建,部分患者同时予植骨或骨水泥强化;其中单棒双钉组12例,双棒四钉组30例。42例骨盆肿瘤患者中,原发性肿瘤35例,转移性肿瘤7例;原发性肿瘤中软骨肉瘤12例,骨肉瘤9例,尤文肉瘤2例,纤维肉瘤1例,恶性纤维组织细胞瘤1例,骨巨细胞瘤6例,动脉瘤样骨囊肿2例,孤立性纤维瘤1例,非骨化性纤维瘤1例。患者体重34~70 kg,平均(56.2±8.2)kg,身高149~177 cm,平均(166.1±7.3)cm,身体质量指数(body mass index,BMI)12.9~25.6,平均20.3±2.6。对患者的一般情况、手术及其他治疗情况、临床效果以及内固定失败率进行统计分析。
纳入标准:①诊断为骨盆Ⅰ区或Ⅰ+Ⅳ区的原发性或转移性肿瘤;②接受骨盆Ⅰ区或Ⅰ+Ⅳ区肿瘤切除及钉棒系统内固定重建手术;③资料完整,随访时间>1年。排除标准:①术后无法下地行走的患者;②肿瘤同时累及骨盆Ⅱ区或Ⅲ区;③因内固定周围肿瘤局部复发导致的内固定松动失败病例;④在外院接受手术的病例。
1.2 手术方法
参照Enneking报道的骨盆肿瘤分区方法及原则[22]进行肿瘤切除及机械重建。根据肿瘤的位置和累及的范围采取不同手术方式:33例接受骨盆Ⅰ区肿瘤切除,9例接受骨盆Ⅰ+Ⅳ区肿瘤切除。
9例接受EnnekingⅠ+Ⅳ区肿瘤切除的患者,在接受Ⅳ区切除时,1例为右侧半骶骨联合骶骨远端横形切除,右侧S1-5神经根及对侧S4-5神经根切除;1例为左侧半骶骨联合骶骨远端横形切除,左侧S1-5神经根及对侧S3-5神经根切除;3例为右侧半骶骨切除及右侧S1-3神经根切除;4例接受部分骶骨翼切除。
骨盆环缺损的重建选择腰-髂或骶-髂固定:在脊柱侧,经过椎弓根或椎体侧方向L4、L5或骶椎椎体中置入万向椎弓根螺钉;在骨盆近髋臼侧,根据残留骨质的情况,选择合适方向和角度置入椎弓根螺钉,再通过连接棒连接远近端螺钉[12,14](图1、2)。腰-髂固定为盆外固定,骶-髂固定为盆内固定。部分患者骨盆环缺损仅由钉棒系统进行重建;有的患者在钉棒系统周围及骨缺损处予抗生素骨水泥填充加强(图1);部分患者则接受骨缺损处自体骨植骨,如自体腓骨、自体髂骨块、钛网内填充自体骨块等(图2)。12例接受单棒双钉的钉棒系统重建(包括单棒三钉固定),30例接受双棒四钉的钉棒系统重建(包括单棒四钉固定)。

图1 患者,男,68岁,骨盆Ⅰ区软骨肉瘤,骨盆平片示肿瘤切除、骶骨-髂骨钉棒系统固定及骨水泥强化术后改变

图2 患者,女,63岁,骨盆Ⅰ区骨软骨肉瘤,行肿瘤切除、植骨及L5-S1椎弓根-髂骨双棒四钉固定术
1.3 术后处理
术后卧床1个月,1个月内进行床上髋关节及下肢主动活动;1个月后在拄拐情况下开始下地,患肢部分负重锻炼,逐渐强化至术后3个月;术后3个月开始患肢全部负重行走及功能锻炼。
1.4 随访计划及疗效评估
术后1年内要求患者第1、3、6、9、12个月定期门诊随访,复查骨盆X线片及骨盆CT。1年后每半年复查1次骨盆平片及骨盆CT,3年后每年复查1次X线片及CT。记录患者疼痛、功能及满意度等情况,并使用视觉模拟评分(visual analogue scale,VAS)评价患者疼痛程度,使用国际骨与软组织肿瘤协会(Muscu⁃loskeletal Tumor Society,MSTS)93功能评分系统[23]评价下肢功能情况。根据骨盆平片、骨盆CT及三维重建评估肿瘤复发、植骨块愈合、内固定松动、断裂等情况。并根据定期随访情况,记录患者存活或死亡等情况。
1.5 统计学分析
采用SPSS 22.0统计软件进行数据分析,计量资料以均数±标准差表示,组间比较采用t检验。根据患者年龄、性别、BMI、肿瘤部位、内固定方式以及治疗情况等因素行Kaplan-Meier单因素分析,Log Rank检验比较各组内固定生存率,对P<0.05的因素再进行多因素Cox比例风险模型分析。P<0.05为有统计学差异。
2 结果
2.1 随访情况
所有患者均获得随访,随访时间13~168个月,平均(36.1±32.3)个月。主要并发症包括:7例创口并发症及浅表感染,5例因骶神经根切除后神经功能障碍,1例深静脉血栓形成,4例肺部感染,1例术后骨不愈合,6例内固定失败。
6例内固定失败出现在术后3~61.9个月,平均(24.7±20.3)个月。末次随访时,6例出现内固定失败,15例死亡但无内固定失败,21例存活且无内固定失败。所有患者平均内固定无失败生存时间为(32.5±30.9)个月。2例内固定失败患者接受了翻修手术,其中1例接受了内固定拆除术,另1例接受了内固定翻修以及自体腓骨植骨重建。
末次随访时,所有患者VAS评分0~5分,平均(1.2±1.3)分,MSTS93功能评分16~29分,平均(24.7±2.9)分;内固定失败患者VAS评分1~5分,平均(3.0±1.1)分,MSTS93功能评分16~25分,平均(21.2±3.2)分;无内固定失败患者术后VAS评分0~3分,平均(0.9±1.0)分,MSTS93功能评分18~29分,平均(25.3±2.6)分。无内固定失败患者VAS评分显著优于内固定失败组(P=0.000),无内固定失败患者MSTS评分显著高于内固定失败组(P=0.001)。
2.2 Kaplan-Meier单因素生存分析
患者钉棒系统固定方式、年龄、肿瘤是否累及骨盆Ⅳ区对内固定预后的影响有统计学意义(P<0.05,表1)。单棒双钉组患者术后6~12个月、18个月、24个月和36~48个月的内固定累积失败率分别为8.3%、18.5%、32.1%和54.7%;双棒四钉组患者术后1年、2~5年和6~14年的内固定累积失败率分别为0%、4.3%和28.3%。双棒四钉组的内固定存活率明显高于单棒双钉组的存活率(P=0.003,图3);≤21岁年龄组的内固定失败率高于>21岁年龄组(P=0.009);骨盆Ⅰ、Ⅳ区肿瘤切除组内固定失败率高于骨盆Ⅰ区切除组(P=0.007)。
2.3 多因素Cox 比例风险模型分析
根据Kaplan-Meier单因素生存分析的结果,将钉棒系统固定方式、年龄、肿瘤是否累及骨盆Ⅳ区放入Cox比例风险模型,结果显示,钉棒系统固定方式为独立预后因素(P=0.021),行单棒双钉固定时内固定失败的相对危险度为13.2(95%CI:1.5~118.4)。

表1 42例患者内固定生存率单因素分析结果

图3 Kaplan-Meier单因素生存分析比较单棒双钉组和双棒四钉组内固定生存率的差异
3 讨论
内半骨盆切除术后,无论采用何种重建方式,内固定的失败都是一个常见的并发症[9,12,14,17]。钉棒系统内固定重建已成为治疗骨盆Ⅰ区及Ⅰ+Ⅳ区肿瘤切除术后骨盆环缺损的主要手术方式之一[10],其相对比较简单、有效,但也有一定的内固定失败率。目前,只有少数报道利用有限元分析比较不同钉棒系统的生物力学性能[24],本研究比较了不同钉棒系统重建骨盆Ⅰ区及Ⅰ+Ⅳ区肿瘤切除术后骨盆环缺损的内固定生存情况,发现固定强度不足是术后发生内固定失败的主要原因。
Nassif等[12]和Sabourin等[13]报道了单棒双钉固定骨盆环缺损,取得了满意的疗效。本研究中,也有病例采用了同样的固定方式,尽管部分患者取得了满意的效疗,但内固定的总体失败率显著高于双棒四钉组,主要原因是单棒双钉固定抗扭转能力较弱,内固定的总体固定强度不足(图4)。Aach等[15]介绍了双棒四钉的固定方法,认为其固定强度较好,如果联合骨水泥强化或植骨,其初始稳定性更佳,其结论与本研究相似。
因为椎体间存在微动(如L4/5、L5/S1),盆外固定时内固定应力较大,容易出现内固定的疲劳断裂或松动,其远期稳定性不如盆内固定[24]。因此,如果情况许可,我们建议进行盆内固定(图1)。但有些情况下,肿瘤累及骨盆Ⅳ区,行部分骶骨切除,骶骨上固定的位置非常有限,只能行盆内+盆外固定(图2)或盆外+盆外固定。骨盆Ⅰ+Ⅳ区切除组内固定失败率高于骨盆Ⅰ区切除组(P=0.007),部分原因与其术中骶骨固定的位置有限,患者接受盆外固定有关。与螺钉经椎弓根固定相比,经腰椎、骶椎侧方进钉的螺钉固定为前路支撑重建,更具生物力学优势[25]。
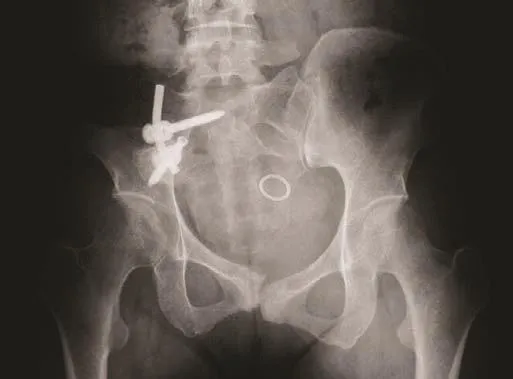
图4 患者,女,37岁,骨盆Ⅰ区软骨肉瘤,行肿瘤切除、植骨及骶骨-髂骨单棒双钉固定,骨盆平片示内固定断裂
生物学重建有骨不愈合、移植骨骨折[26]以及感染[27,28]等并发症,但其远期效果满意,为广大学者所推荐[12,16,29,30]。在肿瘤切除术后,首选取同侧残留髂骨进行植骨[12,17],其与自体腓骨移植相比,具有损伤小、容易获取等优势,其不足是对于较大的骨缺损无法进行重建。对于较大的骨缺损,游离或带血管腓骨是常用的移植材料[16,30],异体腓骨移植有相对较高的感染和骨不愈合发生率[28,31],目前较少应用;带血管自体腓骨移植可以获得满意的效果,但其相对复杂、耗时长,并有较大的供区损伤[32];尽管游离自体腓骨移植的成骨活性不如带血管腓骨[33],但其供区损伤小、操作便捷[29]。骶髂部位血供较丰富,并且有良好的软组织包盖,因此推荐游离腓骨移植治疗较大的骨盆环缺损。
术后放疗或化疗可降低植骨的活性,导致骨不愈合,进而影响重建的稳定性[13,16],因此术后接受放化疗的患者可选择钉棒系统联合骨水泥固定的机械性重建。
我们发现内固定的失败率与患者年龄有一定的相关性,≤21岁年龄组的内固定失败率高于>21岁年龄组。年轻患者更容易发生内固定失败,其原因可能是:年轻患者其总体活动量较大、对生活质量要求较高,因此对内固定强度也提出了更高的要求。
在选择重建的方式时,需要综合考虑患者年龄、肿瘤的性质及预后等因素。对于年龄较轻的患者,生物学重建比机械重建有更好的远期稳定性[12,29,30];对于一些年龄较大、无法长期卧床的患者,钉棒系统联合骨水泥固定可获得良好的初始稳定性,可以让患者术后早期下地活动,减少并发症[14]。良性肿瘤与一些预后差的恶性肿瘤患者的重建方式应有所区别。一些良性肿瘤以及软骨肉瘤等预后较好的恶性肿瘤切除后推荐行生物学重建,以获得良好的远期稳定性;对于一些预后差的肿瘤,可以选择钉棒系统联合骨水泥强化,以获得满意的初始机械稳定性。
综上,骨盆Ⅰ区及Ⅰ、Ⅳ区肿瘤切除术后双棒四钉固定可以提供良好的短期及长期稳定性,而单棒双钉固定的强度相对不足。对于年轻患者以及良性肿瘤患者,肿瘤切除后建议采用钉棒系统联合自体骨移植的生物学重建;对于老年患者、恶性肿瘤患者以及需要放化疗的患者,建议采用钉棒系统联合骨水泥的机械性重建。

