卡培他滨联合化疗治疗晚期胰腺癌的系统评价
郑家雷 苏方 方向 汪子书 郑荣生 孙国平
1平安徽医科大学第一附属医院肿瘤内科(合肥230022);2蚌埠医学院第一附属医院肿瘤内科(安徽蚌埠233003);3中国科技大学附属第一医院老年消化科(安徽省立医院)(合肥230001)
胰腺癌(pancreatic cancer,PC)是恶性程度最高的消化系统肿瘤;早期缺乏特异性的临床表现,大多患者出现症状就诊时肿瘤已经扩散或转移,确诊后5年生存率低于10%[1]。胰腺癌近年来全球范围内均呈快速上升趋势。2018年美国预计新发胰腺癌患者5.5万例,因胰腺癌死亡人数达4.4万例[2];预计到2030年胰腺癌将成为美国第2大癌症死亡原因[3]。我国国家癌症中心发布的最新数据也显示中国胰腺癌发病率上升到恶性肿瘤的第10位,癌症相关死亡率位于第6位[1]。即便人们体检意识不断增强以及诊断技术不断提高,大部分胰腺癌发现时已是不可切除的晚期。中国的《胰腺癌诊治指南(2014)》指出对于不可切除的局部进展期或转移性胰腺癌,积极的化学治疗有助于缓解症状、延长生存期及改善生活质量[4]。因此积极探索安全有效的化疗方案对晚期胰腺癌患者具有重要的意义。近年来循证医学证据[5-6]表明吉西他滨(gemcitabine,GEM)联合化疗优于标准的GEM单药化疗,认为GEM联合化疗是今后治疗胰腺癌的希望与方向。与长培他滨(CAP)相关的进展期胰腺癌化疗临床试验已于临床开展,然而各自的结论尚存在差异[7-8]。本研究旨在通过系统评价的方法研究CAP联合GEM化疗是否能在不增加毒副反应的前提下提高晚期胰腺癌的治疗效果,延长患者的生存期,为临床治疗胰腺癌提供参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型比较CAP联合化疗治疗晚期胰腺癌的随机对照试验。
1.1.2 研究对象(1)所有病例均是经病理学或细胞学检查证实的Ⅲ~Ⅳ期(进展期或转移)胰腺癌患者;(2)年龄 ≥ 18岁,性别不限;(3)ECOG评分为0~2分,或Kamofsky评分≥60分。
1.1.3 干预措施试验组采用CAP联合对照组方案治疗,对照组采用GEM单药或联合治疗。
1.1.4 结局指标(1)中位生存期;(2)疾病无进展生存期;(3)治疗总有效率(CR+PR);(4)1年生存率;(5)3/4期毒副反应。
1.1.5 排除标准(1)非中、英文文献;(2)同时患第2种恶性肿瘤者;(3)1个月内接受其他的抗癌治疗;(4)预计生存期小于3个月者。
1.2 文献检索计算机检索PubMed、The Cochrane Library(2017年 3期)、WanFang Data、CNKI数据库,搜集CAP联合化疗方案治疗晚期胰腺癌的随机对照试验(RCT),检索时限均从建库至2017年12月1日。此外,追溯纳入文献的参考文献,以补充获取相关文献。检索采取主题词和自由词相结合的方式。英文检索词包括gemcitabine,capecitabine,pancreatic cancer,pancreatic carcinoma;中文检索词包括吉西他滨、卡培他滨、胰腺癌。
1.3 文献筛选及资料提取由2位评价员独立筛选文献、提取资料并交叉核对,如遇分歧,则咨询第三方协助判断,缺乏的资料尽量与作者联系予以补充。文献筛选时首先阅读文题和摘要,在排除明显不相关的文献后,进一步阅读全文,以确定最终是否纳入。资料提取内容主要包括:(1)纳入研究的基本信息,包括研究题目、第一作者、发表杂志及时间等;(2)研究对象的基线特征,包括各组的样本数、患者的年龄、性别和疾病状况等。(3)干预措施的具体细节、随访时间等;(4)偏倚风险评价的关键要素;(5)所关注的结局指标和结果测量数据。有效性、安全性等。
1.4 统计学方法采用RevMan 5.3软件进行Meta分析。计数资料采用相对危险度为效应指标,计量资料采用均数差为效应指标,各效应量均给出其点估计值和95%CI。纳入研究结果间的异质性采用χ2检验进行分析(检验水准为α=0.1),同时结合I2定量判断异质性的大小。若各研究结果间无统计学异质性,则采用固定效应模型进行Meta分析;若各研究结果间存在统计学异质性,则进一步分析异质性来源,在排除明显临床异质性的影响后,采用随机效应模型进行Meta分析。
2 结果
2.1 文献筛选流程及结果初检出相关文献493篇,经逐层筛选后,最终纳入6篇随机对照试验[7-8,10-13]。其中 5 个英文研究[7-8,10-12],1 个研究为中文研究[11],共1 317例晚期胰腺癌。
2.2 纳入研究的基本特征纳入研究的基本特征见表1。

表1 纳入6项RCT研究的基本情况Tab.1 The basic information of 6 RCTstudies
2.3 Meta分析结果
2.3.1 中位生存期共纳入5个RCT[7-8,10-12]提供了CAP联合化疗方案对照组中位生存期情况。各研究间差异无统计学意义(P=0.87,I2=0),固定效应模型Meta分析结果显示CAP联合化疗方案较对照组延长了患者的中位生存期[HR=0.86,95%CI(0.77 ~ 0.96),P=0.006] (图1)。
2.3.2 疾病无进展生存期共纳入5个RCT[7-8,10-12]报道了疾病无进展生存期,各研究间差异无统计学意义(P=0.93,I2=0),固定效应模型Meta分析结果显示CAP联合化疗方案较对照组延长了患者的明显延长了患者疾病无进展生存期,差异有统计学意义[HR=0.83,95%CI(0.75 ~ 0.91),P=0.000 2] (图2)。
2.3.3 治疗总有效率共纳入6个RCT[7-8,10-13]报道了治疗的总有效率,各研究间无显著异质性(P=0.35,I2=10%),固定效应模型Meta分析结果显示CAP联合化疗方案的治疗有效率明显高于对照组,差异有统计学意义[OR=1.82,95%CI(1.34~ 2.46),P=0.000 1] (图3)。
2.3.4 1年生存率共纳入 3 个 RCT[10,12-13]报道了1年生存情况,各研究间差异无统计学意义(P=0.73,I2=0),固定效应模型Meta分析结果显示CAP联合化疗方案的1年总生存率与对照组差异无统计学意义[OR=1.10,95%CI(0.78~ 1.57),P=0.58] (图4)。

图1 卡培他滨联合化疗方案与对照组中位生存期的Meta分析Fig.1 Meta analysis of median survival time of capecitabine combined chemotherapy and control group

图2 卡培他滨联合化疗方案与对照组疾病无进展生存期的Meta分析Fig.2 Meta analysis of progression free survival of capecitabine combined chemotherapy and control group
2.3.5 3/4 级毒副作用共纳入 6 个 RCT[7-8,10-13]的3~4级毒副作用,固定效应模型Meta分析结果显示CAP联合化疗方案3~4级中性粒细胞减少、口腔炎及手足综合征的发生率高于对照组(P<0.05)。两方案的3~4级贫血、血小板减少、乏力、恶心呕吐及腹泻的差异没有统计学意义(P>0.05)(表2)。

图3 卡培他滨联合化疗方案与对照组总有效率的Meta分析Fig.3 Meta analysis of overall response rate of capecitabine combined chemotherapy and control group

图4 卡培他滨联合化疗方案与对照组1年生存率的Meta分析Fig.4 Meta analysis of 1 year overall survival rate of capecitabine combined chemotherapy and control group
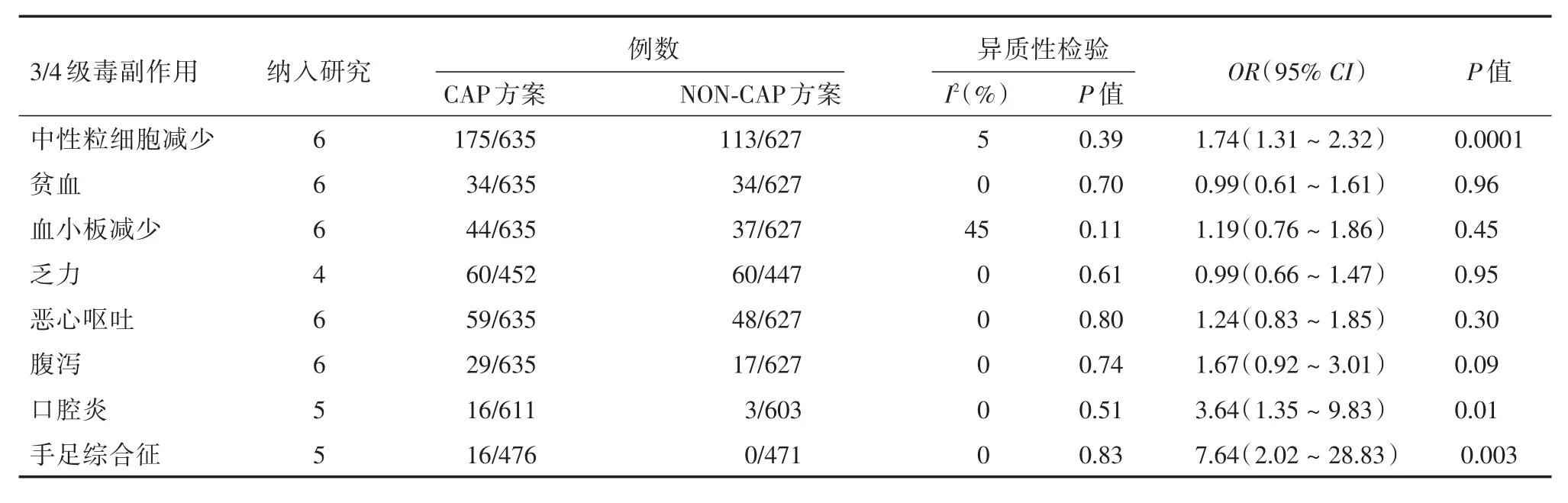
表2 卡培他滨联合化疗方案与对照组3~4级主要毒副作用比较Tab.2 Grade 3-4 toxicities of capecitabine combined chemotherapy and control group
3 讨论
晚期胰腺癌患者生存时间短,目前最适合的化疗方案仍不明确,所以寻找有效的化疗药物改善预后较为迫切。以GEM为基础的化疗药物治疗胰腺癌临床效果确切,并为美国国立综合癌症网络(NCCN)的胰腺癌诊疗指南及中国的《胰腺癌诊治指南(2014)》所推荐[4]。对于不可切除的局部进展期或转移性胰腺癌,在全身状况良好的情况下,采用以GEM或氟尿嘧啶类药物为基础的同步放化疗或诱导化疗后放疗可有效缓解症状及改善患者预后[4]。近年来有研究[8]报道CAP联合GEM化疗方案能够延长晚期胰腺癌患者的疾病无进展生存期,但部分研究[7-8]结果不一致;因此对于CAP联合GEM化疗方案治疗晚期胰腺癌的临床效果及安全性尚无确切结论,故本研究拟通过系统评价的方法得到CAP联合GEM化疗方案治疗晚期胰腺癌的循证医学证据。本研究共纳入6个研究1 317例晚期胰腺癌患者,分析结果显示:CAP联合化疗方案的中位生存期、疾病无进展生存期明显长于对照组,治疗总有效率明显高于对照组;但在1年生存率方面CAP联合化疗方案较对照组差异无统计学意义。在毒副作用方面,CAP联合化疗方案3~4级中性粒细胞减少、口腔炎及手足综合征的发生率高于对照组。
本研究结果显示在晚期胰腺癌的治疗中,CAP联合化疗方案较对照组延长了患者的中位生存期及疾病无进展生存期,提高了患者治疗的总有效率,但1年生存率无明显差异;提示CAP联合GEM方案在治疗晚期胰腺癌时短期内可能更有效控制病情、提高患者生活质量及延长患者生命,但对患者1年生存率无明显影响。近年来靶向治疗是肿瘤治疗的新希望,但近期关于晚期胰腺癌靶向治疗的临床试验均以失败告终。凡德他尼联合GEM未改善晚期胰腺癌生存情况[14];厄洛替尼虽被证实联合GEM可改善局部进展和(或)转移性胰腺癌患者预后,但生存获益有限[15];循证医学证据也表明不同靶向治疗联合GEM并未改善晚期胰腺癌生存状况[16]。本系统评价的一项Ⅱb期临床试验报道了厄洛替尼联合CAP、GEM与厄洛替尼联合GEM方案在治疗晚期胰腺癌患者中的疗效,结果显示厄洛替尼联合联合CAP、GEM并不能延长患者的总生存期及疾病无进展生存期[7]。在毒副作用方面,两方案均显示了常见的血液学及非血液毒性;但CAP联合化疗方案的中性粒细胞减少、口腔炎及手足综合征的发生率明显高于对照组;因此在使用CAP联合化疗中需注意监测患者血常规,及时了解中性粒细胞变化情况;注意预防口腔炎及手足综合征的发生。对于存在腹腔转移的胰腺癌患者,SATOI等[17]报道了静脉和腹腔注射紫杉醇联合S-1治疗胰腺癌腹腔转移的研究,结果显示患者的中位总生存期为16.3个月,1年生存率为62%,有效率与疾病控制率分别为36%和82%,因此该方案有望成为临床上控制腹膜转移的治疗方案。
经过严格筛选共入组6项RCT研究;其中5篇Jadad评分≥3分,属于高质量的临床研究。本系统评价仍然存在一定的不足及局限性:(1)部分研究未采用正确的随机分配和隐藏方法,可能造成选择性偏倚。(2)未纳入非中、英文文献,难免存在偏倚,故要想获得确凿的证据尚需要扩大样本,长期随访。
晚期胰腺癌的化疗效果仍不理想。综上所述,本研究结果显示CAP联合应用可能改善进展期胰腺癌患者的短期生存情况及生存质量;但会导致部分毒副反应增加,且1年以后的远期生存无明显改善。本研究受限于纳入研究对象数量较少,下一步尚需多中心、大样本随机对照试验进一步验证。

