4,6-二羟基嘧啶废水电化学处理技术研究
姜笔存,戴祖明,许 玲,曲艳南
(南京环保产业创新中心有限公司,南京 211102)
4,6-二羟基嘧啶是一种重要的有机合成中间体,用于医药工业生产磺胺类药磺胺莫托辛,也是维生素B4、抗肿瘤药及辅助药类的中间体。4,6-二羟基嘧啶是由丙二酸二乙酯(或丙二酸二丁酯)与甲酰胺经环合而得,其生产废水具有高盐、高氮、高COD和难生物降解等特征[1]。此类废水传统处理方法为混凝沉淀、Fenton氧化、H2O2氧化、臭氧氧化等一种或几种组合,但是普遍存在药剂耗用量大、处理效率低且易产生二次污染等缺点[2]。
电化学法具有无药剂投加、无污泥产生、功能灵活且易于控制的优势,是一种适应国家发展要求的环境友好废水处理技术。本文以4,6-二羟基嘧啶废水为研究对象,以废(盐)治废,研究新型电化学技术强化废水脱氮除碳性能效果,并与传统氧化工艺开展技术经济性比较。
1 试验与检测方法
1.1 废水来源与水质
4,6-二羟基嘧啶生产废水取自西南某化工有限公司,其主要水质指标如表1所示。
1.2 电极制备
锡锑钌DSA形稳阳极制备:五水合四氯化锡、三氯化锑与水合氯化钌按比例溶于异丙醇中,将配制的异丙醇溶液刷涂于钛板表面,所得钛板置于80℃干燥箱中5 min,之后移至500℃马弗炉中焙烧5 min,重复上述刷涂焙烧过程5次,最后1次置于500℃马弗炉中焙烧1 h[3]。
1.3 试验方法
电化学工艺条件:选用自制的锡锑钌DSA电极为阳极,钛电极作为阴极,电极板面积24 cm×50 cm×2,板间距5 mm。
氧化工艺条件:选用现有工程参数,3%双氧水(30%)和500 mg/L七水硫酸亚铁,空气搅拌,Fenton氧化24 h,H2O2氧化48 h。
1.4 测量方法
化学需氧量(COD)依据《水质化学需氧量的测定 重铬酸盐法》(HJ 828-2017)中的方法测定;总氮(TN)依据《水质总氮的测定碱性过硫酸钾消解紫外分光光度法》(HJ636-2012)中的方法测定;氨氮(NH3-N)依据《水质 氨氮的测定 纳氏试剂分光光度法》(HJ 535-2009)中的方法测定;pH值依据《水质pH值的测定 玻璃电极法》(GB6920-1986)中的方法测定。
2 结果与讨论
2.1 传统氧化工艺处理废水研究
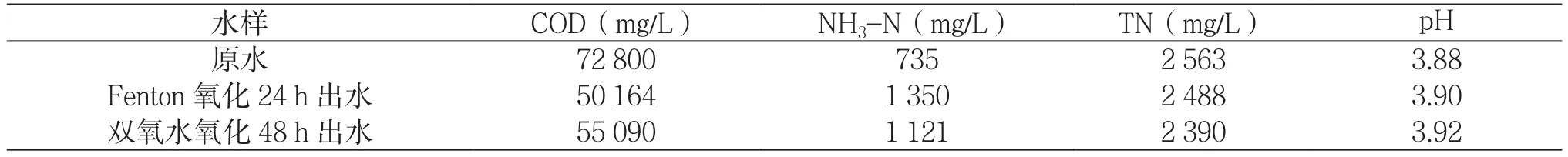
表1 Fenton与H2O2工艺处理效果
如表1所示,传统的Fenton氧化以及H2O2氧化工艺对4,6-二羟基嘧啶废水COD都有一定的去除能力,去除率分别达到31.09%和24.33%。
然而,两种氧化工艺对氨氮去除效果较差,废水经过Fenton和H2O2氧化之后氨氮浓度反而升高,这可能是由于4,6-二羟基嘧啶的含氮杂环被破坏而形成氨氮;H2O2的氧化能力弱于Fenton的氧化能力,致使H2O2处理工艺中氨氮增加量少于Fenton工艺。Fenton和H2O2氧化无总氮去除能力,测试总氮浓度略微降低,可能是由于溶液中氨氮部分挥发。
此外,Fenton氧化和H2O2氧化处理工艺处理前后的pH值变化不大,因而后续工艺需外加大量碱调节pH至中性。试验表明,Fenton氧化调碱还会形成大量铁泥沉淀。
2.2 电化学工艺电流密度对COD去除影响
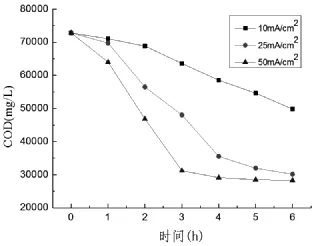
图1 不同电流密度下废水COD变化动力学曲线如图1所示,废水COD浓度随电氧化时间延长而
降低,呈现先快后慢的趋势,符合有机污染物降解一级反应动力学规律。随着电流密度增加,电化学COD去除效果持续增加。废水COD处理效率与电流密度呈正相关,因为电流密度决定了电化学氧化过程中活性氯的产率。电流密度分别为10 mA/cm2、25 mA/cm2和50 mA/cm2时,经6 h电氧化,COD去除率分别为31.59%、58.58%、61.12%。电流密度50 mA/cm2的6 h去除效果仅略微优于电流密度25 mA/cm2的,可能是因为大电流温升高加快了活性氯的分解。电流密度为25 mA/cm2时,整个反应过程温度控制在40℃以下,然而电流密度为50 mA/cm2时,3 h后废水温度在50~52℃,活性氯高温极易分解而失去氧化能力。综合技术经济性,25 mA/cm2电流密度是此研究电化学COD去除的理想条件。
2.3 电化学工艺电流密度对氨氮和总氮去除影响
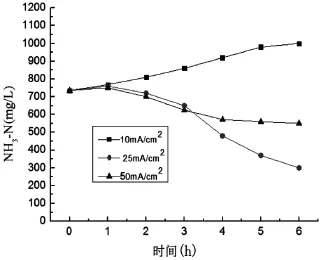
图2 不同电流密度下废水中氨氮动力学变化曲线
4,6-二羟基嘧啶废水中氮主要由氨氮和有机氮等组成。电化学总氮降解主要经过二种路径,一是羟基嘧啶的含氮杂环被氧化破坏,氮基团脱落转化为无机氮;二是电化学产生的活性氯与氨氮发生折点加氯反应生成氮气。氨氮折点加氯反应如下[4]:
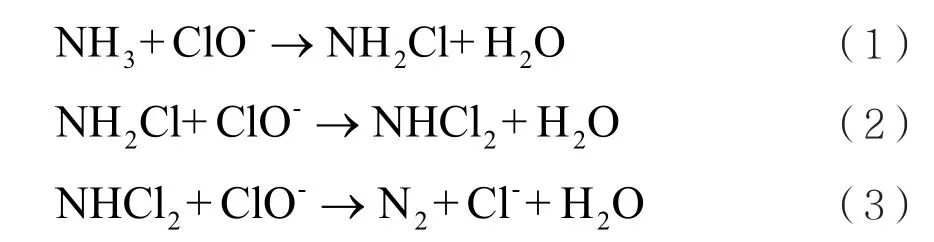
如图2所示,在10 mA/cm2的电流密度下,氨氮浓度随着反应时间增加反而增高,这是由于含氮杂环有机物氧化的氨氮产率大于折点加氯反应的氨氮去除率,使得氨氮在电化学反应过程中累积。
在25 mA/cm2和50 mA/cm2电流密度下,氨氮浓度先微微增加后显著降低。这可能是因为反应初期活性氯产生浓度较低,含氮杂环有机物氧化是主反应;随着反应时间延长,折点加氯氨氮去除速率加快,溶液中氨氮浓度开始降低。电流密度25 mA/cm2下电化学前3 h的氨氮去除效果略低于电流密度50 mA/cm2的,然而,电流密度25 mA/cm2下电化学后3 h的氨氮去除效果优于电流密度50 mA/cm2的,这也表明大电流下累积的温度升高导致活性氯分解,进而降低折点加氯反应的氨氮去除能力。

图3 不同电流密度下废水中总氮动力学变化曲线
如图3所示,虽然3种电流密度下氨氮均存在增加现象,3种电流密度下总氮浓度均随着电化学反应时间增加而降低,证实了折点加氯除氨氮反应的持续存在。电流密度10 mA/cm2总氮去除效果低于电流密度25 mA/cm2的,是因为活性氯生成量随着电流密度增加而增加。电流密度50 mA/cm2的6 h电化学总氮去除效果低于电流密度25 mA/cm2的,也表明大电流温升抑制了氨氮折点加氯转化为氮气的效果。
2.4 电化学工艺电流密度对pH影响

图4 不同电流密度下废水中pH变化曲线
如图4所示,在50 mA/cm2电流密度下,pH值在电催化氧化反应初期变化剧烈,1 h内由3.88升至8.00左右,随后5 h,pH值变化小于1;在25 mA/cm2电流密度下pH值在电氧化反应初期同样变化剧烈,2 h内由3.88升至7.54;在10 mA/cm2电流密度下pH值增加平缓。电流密度越大,pH值增加越快,是因为阴极析氢反应速率与电流密度成正相关。当pH达到7.00后,pH值变化趋于平缓,可能是因为溶液中氢氧根浓度升高,阳极析氧反应加快,大量消耗氢氧根导致pH变化缓慢。
2.5 传统氧化工艺与电化学工艺经济性比较

表2 新型电化学与传统氧化工艺经济性分析
从表2可以看出,电化学工艺每吨废水处理成本为30~40元,而Fenton氧化和H2O2氧化吨水处理成本分别高达120元和180元,因此电化学工艺经济性明显优于Fenton氧化和双氧水氧化工艺。从时效性来看,电化学平均每小时COD去除浓度为7107 mg/L,而Fenton氧化和H2O2氧化平均每小时COD去除量分别为943 mg/L和369 mg/L ,电化学工艺具有更好的动力学特性。此外,Fenton氧化和H2O2氧化引入大量无机离子增加了废水的盐分,使得后续工序处理负担加重。
3 结论
在电流密度为25 mA/cm2时,4,6-二羟基嘧啶废水电化学工艺6 h内COD去除率为58.58%,效果优于传统Fenton氧化(24 h COD去除率31.09%)和H2O2氧化(48 h COD去除率24.33%)。传统Fenton氧化和H2O2氧化的氨氮和总氮无显著去除效果,然而,在电流密度25 mA/cm2时,新型电化学工艺总氮去除率达68.78%。电化学工艺无药剂投加、无污泥产生、无盐分增加,是一种环境友好的4,6-二羟基嘧啶废水处理技术。

