羚黄宝儿丸包衣工艺的优化及制剂稳定性研究Δ
陈丽斯,曾利杰,彭红英,江 涛,陈晓坚
(广州白云山敬修堂药业股份有限公司,广州 510130)
羚黄宝儿丸由麝香、黄连、羚羊角、甘草、冰片、人参、人工牛黄、猪胆膏、丁香等9味中药制成;该药为银白色包衣微丸,味苦、性凉,具清热熄风、除痰定惊、开窍醒神之功效[1],可用于小儿发热、惊哭夜啼、痰热咳嗽、泄泻、脾胃虚弱及消化不良等的治疗[2]。该药含有麝香、冰片等成分,如贮存不当,易造成其中挥发性成分的流失而影响药品质量、降低药效,故原制剂采用铝箔包衣。虽然铝元素曾被认为是一种安全的元素,但随着医学的深入发展,人们逐渐意识到铝元素的毒性[3]。铝元素不会对人体产生急性毒性,但其摄入体内后长期蓄积会引发严重的慢性毒性,如阿尔茨海默病、慢性肾功能衰竭等[4]。该药作为儿童用药,更应避免使用铝箔包衣。另外,铝箔难溶于液体,只能采用传统的包衣锅滚转包衣,但包衣锅存在干燥效率低、能源浪费大、操作耗时长等缺点[5]。为此,本研究鉴于冰片的挥发性及铝箔包衣的种种弊端,改用流化床薄膜包衣,并对工艺进行优化,同时参考上述相关文献[6-11]采用气相色谱法考察了制剂的稳定性,旨在为该药的剂型完善提供参考。
1 材料
1.1 仪器
FLP-5型流化床包衣机(常州市佳发制粒干燥设备有限公司);BT-300型蠕动泵(重庆杰恒蠕动泵有限公司);BS400S-WE1型电子天平(德国Sartorius公司);6890型气相色谱仪,包括氢火焰离子化检测器等(美国Agilent公司);KQ-600DE型超声波清洗仪(昆山市超声仪器有限公司)。
1.2 药品与试剂
龙脑对照品(批号:110881-201508,纯度:96.8%)、水杨酸甲酯对照品(内标,批号:110707-201614,纯度:100%)均由中国食品药品检定研究院提供;包衣材料Opadry 290F690003(上海卡乐康包衣技术有限公司,批号:SH562240);羚黄宝儿丸(铝箔包衣,广州白云山敬修堂药业股份有限公司,批号:S07014、S07015、S07016,规格:60丸/瓶);羚黄宝儿丸(薄膜包衣,广州白云山敬修堂药业股份有限公司,批号:S07017、S07018、S07019,规格:60丸/瓶);羚黄宝儿未包衣素丸(广州白云山敬修堂药业股份有限公司,批号:S07011、S07012、S07013);其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 包衣工艺的优化
取Opadry中药薄膜包衣材料适量,加水制成浓度为12%的包衣液,采用流化床包衣机对羚黄宝儿未包衣素丸(投料量750 g)进行包衣。
2.1.1 包衣液喷入方式 流化床包衣机的包衣液喷入方式主要有顶喷、侧喷和底喷3种方式。选择进风温度为50℃、雾化压力为0.20 MPa、蠕动泵转速为5 r/min、引风频率为25 Hz、包衣理论增质量比例为4%,以包衣微丸色泽是否均匀、粘丸情况、包衣液粘壁情况及合格丸收率为指标,考察不同包衣液喷入方式的薄膜包衣效果。结果,包衣液喷入方式为底喷时,包衣微丸色泽均匀,基本无粘丸,未见包衣液粘壁,合格丸收率为96.0%,优于其他喷入方式。故确定包衣液喷入方式为底喷。
2.1.2 进风温度 流化床温度需通过调节进风温度来控制。流化床温度过低,易导致包衣液不能及时挥干而使物料过度润湿,部分物料黏附在器壁上不能流化,从而易造成微丸粘连而起团;流化床温度过高,除易导致包衣液被过早挥干而不能有效包衣外,还可能引起温度敏感型物料性质的变化。参照铝箔包衣样品的工艺干燥温度≤60℃,选择包衣液喷入方式为底喷、雾化压力为0.20 MPa、蠕动泵转速为5 r/min、引风频率为25 Hz、包衣理论增质量比例为4%,以包衣微丸色泽是否均匀、粘丸情况、包衣液粘壁情况及合格丸收率为指标,考察不同进风温度(40、45、50、60℃)的薄膜包衣效果。结果,进风温度为50℃时,包衣微丸色泽均匀,基本无粘丸,未见包衣液粘壁,合格丸收率为97.0%,优于其他温度条件。故确定进风温度为50℃。
2.1.3 雾化压力 雾化是通过气流将液体高度分散为液滴的过程,目的在于增加包衣液与物料的接触面积。雾化压力过小,会使包衣液的液滴太大,在微丸表面铺展时易发生衣膜不均匀,不能达到良好的包衣效果;雾化压力过大,则微丸易碰撞顶部筛网,导致丸体碎裂[12]。选择包衣液喷入方式为底喷、进风温度为50℃、蠕动泵转速为5 r/min、引风频率为25 Hz、包衣理论增质量比例为4%,以包衣微丸色泽是否均匀、粘丸情况、包衣液粘壁情况及合格丸收率为指标,考察不同雾化压力(0.10、0.15、0.20、0.25 MPa)的薄膜包衣效果。结果,雾化压力为0.20 MPa时,包衣微丸色泽均匀,基本无粘丸,未见包衣液粘壁,合格丸收率为97.8%,优于其他压力条件。故确定雾化压力为0.20 MPa。
2.1.4 蠕动泵转速 蠕动泵转速决定包衣液的加入速率。选择包衣液喷入方式为底喷、进风温度为50℃、雾化压力为0.20 MPa、引风频率为25 Hz、包衣理论增质量比例为4%,以包衣微丸色泽是否均匀、粘丸情况、包衣液粘壁情况及合格丸收率为指标,考察不同蠕动泵转速(2、3、4、5 r/min)的薄膜包衣效果。结果,蠕动泵转速为5 r/min时,包衣微丸色泽均匀,基本无粘丸,未见包衣液粘壁,合格丸收率为97.1%,优于其他转速条件。故确定蠕动泵转速为5 r/min。
2.1.5 引风频率 引风频率决定流化床内流化气体的强弱。流化气体是流化床内微丸流化、微丸干燥热源及带走水分的载体[13]。在流化包衣技术中,适当的流化气体可保证流化床层内物料始终保持良好的沸腾流化状态。选择包衣液喷入方式为底喷、进风温度为50℃、雾化压力为0.20 MPa、蠕动泵转速为5 r/min,包衣理论增质量比例为4%,以包衣微丸色泽是否均匀、粘丸情况、包衣液粘壁情况及合格丸收率为指标,考察不同引风频率(20、25、30、35 Hz)的薄膜包衣效果。结果,引风频率为25 Hz时,包衣微丸色泽均匀,基本无粘丸,未见包衣液粘壁,合格丸收率为98.0%,优于其他频率条件。故确定引风频率为25 Hz。
2.1.6 包衣理论增质量比例 选择包衣液喷入方式为底喷、进风温度为50℃、雾化压力为0.20 MPa、蠕动泵转速为5 r/min、引风频率为25 Hz,考察不同包衣理论增质量比例(2%、3%、4%)的合格丸收率及对微丸外观均匀度、引湿性、溶散时限、龙脑含量的影响。结果,合格丸收率分别为98.0%、97.1%、97.6%。当包衣理论增质量比例为2%时,包衣微丸外观均匀度最差;当包衣理论增质量比例为3%、4%时,包衣微丸外观均匀度基本一致。不同包衣理论增质量比例条件下所得微丸的引湿性及溶散时限无明显差异。通过烘箱法(60℃)考察不同包衣理论增质量比例对微丸中挥发性成分的影响,结果显示,烘9 h时取样测定,不同包衣理论增质量比例下所得微丸中龙脑含量接近;烘24 h时取样测定,包衣理论增质量比例为2%时所得微丸中龙脑含量降低明显,而包衣理论增质量比例为3%、4%时所得微丸中龙脑含量无明显差别。综合考虑,确定包衣理论增质量比例为3%。
2.1.7 最优包衣工艺 确定最优包衣工艺:包衣液浓度为12%,包衣液喷入方式为底喷,进风温度为50℃,雾化压力为0.20 MPa,蠕动泵转速为5 r/min,引风频率为25 Hz,包衣理论增质量比例为3%。按此包衣工艺条件所制得微丸的外观圆整、色泽均匀。
2.2 制剂稳定性研究
2.2.1 色谱条件 色谱柱:Technologies DB-WAX(30 m×0.25 mm,0.50 μm);升温程序:初始温度为130 ℃,保持20 min后,以9℃/min升温至200℃,保持8 min;进样口温度:220℃;检测器:氢火焰离子化检测器;检测器温度:250 ℃;进样量:1 μL。
2.2.2 混合对照品溶液的制备 精密称取龙脑对照品、水杨酸甲酯对照品各适量,加乙酸乙酯溶解,制成含龙脑、水杨酸甲酯质量浓度均为0.1 mg/mL的混合对照品溶液。
2.2.3 内标溶液的制备 精密称取水杨酸甲酯对照品适量,加乙酸乙酯溶解,制成质量浓度为2.5 mg/mL的内标溶液。
2.2.4 供试品溶液的制备 取样品1.0 g,研成细粉,过65目筛,精密称取0.5 g,置于25 mL量瓶中,加“2.2.3”项下内标溶液1 mL,加甲醇20 mL,超声(功率:600 W,频率:40 kHz)处理30 min,放冷,加甲醇定容,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.5 阴性对照溶液的制备 按处方比例制备不含冰片的阴性样品,再按“2.2.4”项下方法制备阴性对照溶液。
2.2.6 专属性考察 分别取上述混合对照品溶液、供试品溶液和阴性对照溶液各1 μL,按“2.2.1”项下色谱条件进样测定,记录色谱图,详见图1。由图1可知,各色谱峰分离良好,且阴性对照溶液在龙脑对照品出峰相应位置未见色谱峰出现,对测定无干扰。
2.2.7 线性关系考察 精密称取龙脑对照品10 mg,置于20 mL量瓶中,加乙酸乙酯溶解并定容,制成质量浓度为0.5 mg/mL的对照品溶液A;取水杨酸甲酯对照品适量,加乙酸乙酯溶解,制成质量浓度为1.0 mg/mL的内标溶液A。精密吸取上述对照品溶液A 0.5、1、2、3、4、5 mL,分别置于10 mL量瓶中,加上述内标溶液A 1 mL,加乙酸乙酯定容至刻度,摇匀,取1 μL,按“2.2.1”项下色谱条件进样测定,记录峰面积。以龙脑与内标物质量浓度比(x)为横坐标、峰面积比(y)为纵坐标进行线性回归,得回归方程为y=7.019 3x-0.004 5(r=0.999 9)。结果表明,龙脑检测质量浓度线性范围为0.026~0.26 mg/mL。
2.2.8 定量限与检测限考察 分别精密量取“2.2.2”项下混合对照品溶液适量,倍比稀释,按“2.2.1”项下色谱条件进样测定,以信噪比10∶1、3∶1分别计算定量限、检测限。结果,龙脑的定量限为3.9 ng,检测限为1.2 ng。
2.2.9 精密度试验 取“2.2.2”项下混合对照品溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,龙脑与内标物峰面积比的RSD为0.51%(n=6),表明仪器精密度良好。
2.2.10 稳定性试验 取“2.2.4”项下供试品溶液(批号:S07014)适量,分别于室温下放置0、3、6、9、12、24 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,龙脑与内标物峰面积比的RSD为1.07%(n=6),表明供试品溶液于室温下放置24 h内基本稳定。

图1 气相色谱图Fig 1 GC chromatograms
2.2.11 重复性试验 取样品细粉(批号:S07014)1.0 g,共6份,按“2.2.4”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并以内标法计算样品含量。结果,龙脑平均含量为5.04 mg/g,RSD为1.03%(n=6),表明本方法重复性良好。
2.2.12 加样回收率试验 取已知含量样品细粉(批号:S07014)0.50 g,共6份,分别精密加入一定量的混合对照品溶液,按“2.2.4”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并以内标法计算加样回收率,结果见表1。

表1 加样回收率试验结果(n=6)Tab 1Results of recovery tests(n=6)
2.2.13 样品含量测定 取3批薄膜包衣样品适量,按“2.2.4”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并以内标法计算样品含量,结果见表2。

表2 样品含量测定结果(n=3,mg/g)Tab 2 Results of content determination of samples(n=3,mg/g)
2.2.14 制剂加速稳定性试验 取3批羚黄宝儿未包衣素丸(批号:S07011、S07012、S07013),按薄膜包衣工艺制备薄膜包衣样品。取铝箔包衣样品与薄膜包衣样品各200瓶,置于(40±2)℃、相对湿度(75±5)%条件下,分别于放置第0、1、2、3、6个月时取样,按“2.2.4”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并以内标法计算样品含量,结果见表3。
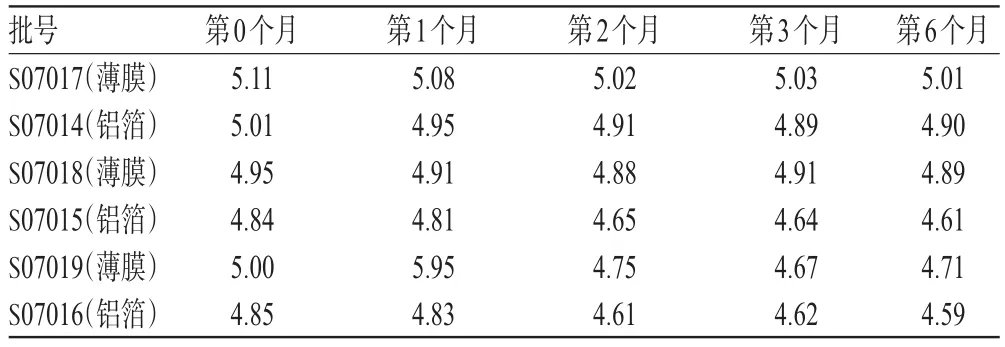
表3 制剂加速稳定性试验结果(n=5,mg/g)Tab 3 Results of accelerated stability tests of the preparation(n=5,mg/g)
根据表3,按公式[损失率=│(第n个月含量-第0个月含量)│/第0个月含量×100%]计算,铝箔包衣样品的平均损失率为4.10%,薄膜包衣样品的平均损失率为3.00%,两种包衣样品的平均损失率均小于5%,表明两种包衣样品在(40±2)℃、相对温度(75±5)%条件下放置6个月内基本稳定,但后者平均损失率更低。
2.2.15 制剂长期稳定性试验 取铝箔包衣样品与薄膜包衣样品各200瓶,置于(20±2)℃、相对温度(40±5)%条件下,分别于放置第 0、3、6、9、12个月时取样,按“2.2.4”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并以内标法计算样品含量,结果见表4。

表4 制剂长期稳定性试验结果(n=5,mg/g)Tab 4 Results of long-term stability tests of preparation(n=5,mg/g)
根据表4,按损失率公式计算,铝箔包衣样品的平均损失率为0.75%,薄膜包衣样品的平均损失率为0.66%,两种包衣样品的平均损失率均小于1%,表明两种包衣样品在(20±2)℃、相对温度(40±5)%条件下放置12个月内基本稳定,但后者平均损失率更低。
3 讨论
薄膜包衣是将高分子化合物溶于适当的溶剂,并在温和的加工条件下通过喷雾方法均匀地喷于丸芯表面,形成数微米厚的塑性高分子材料薄膜层。薄膜包衣技术具有包衣时间短、包衣理论增质量比例小、毒性小、防潮效果好等优点[14]。流化床包衣干燥效率高,尤其适用于干燥速率高的薄膜包衣液(如水分散体),且能使微丸薄膜包衣层的厚度更加均匀[15]。本研究采用流化床薄膜包衣,通过单因素试验分别考察并筛选包衣工艺的重要参数,优化后的包衣工艺稳定、可行,操作简便,节约成本的同时可防止药物中挥发性成分的流失,提高制剂质量的可控性。
加速稳定性试验可在短时间内考察制剂在极端条件下的含量变化情况,以初步预测其稳定性,同时也是对制剂在运输、贮存过程中可能遇到的短暂的超常条件下的稳定性进行模拟考察[16]。长期稳定性试验可明确制剂在常规条件下贮存的稳定性情况,以确定药品的有效期,是稳定性试验的核心[17]。本研究中,两种包衣样品的稳定性无明显差异,均较稳定;但各时间点的测定结果显示,两种包衣样品中薄膜包衣样品的龙脑含量均较高,提示薄膜包衣样品中挥发性成分损失较少。
综上所述,优化所得羚黄宝儿丸薄膜包衣工艺稳定、可行;所制微丸外观圆整、色泽均匀,且稳定性较好。

