体外生物测定法在食品接触材料安全性评价中的应用研究进展
王文娟,蔡小芳,唐 洁,张喜荣,封 棣*
(北京工商大学食品学院,北京市食品添加剂工程技术研究中心,食品质量与安全北京实验室,北京 100048)
食品接触材料(food contact materials,FCM)中的有意添加物(intentionally added substance,IAS)(如单体添加剂、聚合物生产助剂等)以及非有意添加物(non intentionally added substance,NIAS)(如反应产物、分解产物等)可能会在与食品接触过程中迁移至食品,从而对人体健康造成潜在风险[1]。化学分析测试是FCM化学迁移安全性评价中的重要组成部分,主要有2 种方式:一种是常规的符合性测试,是对IAS迁移物进行有目标地分析,产品除了要求使用成分必须列于欧盟相关法规的肯定清单中,还必须证明产品符合总迁移、特定迁移以及残留限量的要求;另一种是对NIAS的无预期目标物的测试[2]。一直以来,对NIAS的识别和量化非常困难,且耗时长,是FCM化学迁移的安全评价所面临的一大挑战。近年来,随着高灵敏、高分辨质谱与高效分离色谱联用技术的发展,以及高效多样的样品前处理技术的应用,使得FCM中的化学迁移物(挥发性、中等挥发性以及难挥发性物质)可以得到较全面地分析[3-9]。Bengtström等[3]利用气相色谱-四极杆飞行时间串联质谱和超高效液相色谱-四极杆飞行时间串联质谱对显示出芳香烃受体活性的回收比萨盒的提取液进行了全面地非靶标物质初步鉴定;本实验室使用吹扫捕集[4-5]、固相微萃取[4,6-7]、超声萃取技术[7]等前处理技术与气相色谱-质谱联用对食品接触硅橡胶制品中的挥发性和半挥发性物质进行了分析。但是由于FCM组成复杂,其对迁移物的分析不可能是完整详尽的,也无法评价FCM化学迁移的整体安全性。
体外生物测定法是利用酵母、细菌或细胞等进行的生物体外短期毒性实验,可有效针对生物体某一特异性效应,评价测试物的危害性以及探索其毒性作用机制,符合动物福利指导准则3R原则(减少(reduce)、优化(refine)和代替(replace)),是动物实验的传统替代技术[10-11],具有成本低、时间短等优点。欧洲议会发表在2016年10月的2015/2259/(INI)[12]报告提出:应鼓励将生物测试作为一种可选的预警措施,以确保化学成分复杂FCM的安全性,并用于开发FCM化学分析和毒理测试的研究。体外生物测定法可以检测出不能通过化学分析或定量结构-活性关系(quantitative structure-activity relationship,QSAR)预测的FCM的潜在毒性,能够提供FCM化学迁移(混合物)的实际危险和质量评估的综合信息[13]。目前,对FCM的体外生物测定主要集中在细胞毒性[14-15]、遗传毒性[16-17]和内分泌干扰[18-20]这3 类毒性终点,近年来已被应用于塑料[14]、纸质[21-23]、罐头涂层[24]、纳米材料[16]等FCM中化学迁移物的毒性评价。
1 细胞毒性
细胞毒性物质通过干扰细胞稳态,破坏细胞完整性或细胞基础功能,导致细胞坏死或凋亡[13]。细胞毒性实验采用体外方法,以生物学性状基本相同的细胞系(或株)为对象,避免了活体动物的使用及其个体差异,操作简单;检测终点灵敏度高,可以在细胞存活状态下,观察细胞毒性物质对细胞内结构和功能的影响,分析作用机理和剂量-效应关系。依据不同的检测终点,细胞毒性检测有多种方法。
1.1 细胞通透性的改变
细胞通透性的改变是常见的细胞毒性终点之一[13]。它的原理是将细胞暴露于待测物中,向其中加入实验所用染料并进行培养,根据染料对细胞的作用或者染料进入细胞的情况,检测细胞活力或者间接判断细胞膜通透性的改变情况,获得关于细胞通透性损伤的信息。最常用的检测方法是中性红摄入(neutral red uptake,NRU)实验。NRU实验是基于细胞对中性红的摄入能力来检测细胞增殖或细胞毒性的方法。活细胞可以摄入中性红,并在溶酶体中积累;当细胞增殖加快,数量增多时,中性红摄入量增加;当细胞受到损伤时,中性红摄入量下降,通过检测中性红摄入量可以确定其对细胞的影响情况。
1.2 细胞增殖的破坏
细胞增殖的破坏也是常见的细胞毒性终点之一,它的原理是毒性物质发挥作用杀死细胞或阻断细胞周期,从而减少整个群体的增殖。检测方法除了生化方法,如细胞中总蛋白质含量(total protein content,TPC)测定实验和5-溴脱氧尿嘧啶核苷(5-bromodeoxyuridine,BrdU)掺入实验[25]之外,还有细胞计数法和噻唑蓝(3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide,MTT)或衍生物(MTS(3-(4,5-dimethylthiazol-2-yl)-5-(3-carboxymethoxyphenyl)-2-(4-sulfophenyl)-2H-tetrazolium salt)、WST-1(4-[3-(4-iodophenyl)-2-(4-nitrophenyl)-2H-5-tetrazolio]-1,3-benzene disulfonate tetrazolium salt))实验。MTT实验是利用显色剂MTT检测细胞存活和生长的方法。MTT能被活细胞线粒体中琥珀酸脱氢酶还原,成为不溶性的蓝紫色结晶物甲臜,并沉积在细胞内;而死细胞则没有这种功能。
1.3 RNA合成的抑制
RNA合成抑制实验是将氚标记的尿苷加入处理后的细胞RNA中,测量RNA合成动力学,如果与阴性对照相比RNA合成的动力降低30%或更多,则认为待测物具有细胞毒性。RNA合成抑制实验可靠、灵敏、重现性好。Riquet等[14]采用RNA合成抑制实验研究分别由抗氧化剂Irgafos 168、抗氧化剂Irganox 1076和紫外线吸收剂Tinuvin 326制备的聚丙烯(polypropylene,PP)薄膜的细胞毒性,结果表明,在薄膜的模拟使用环境(微波和电子束)下,只有Irgafos 168制备的PP薄膜提取物在RNA合成抑制实验中显示出强细胞毒性。
1.4 测试方法的联用
近20 年来用于评估FCM提取物细胞毒性的测定方法、原理及应用总结如表1所示。

表1 近20 年来FCM提取物的细胞毒性生物测定方法Table 1 Cytotoxic bioassays for FCM extracts published in the literature in the last 20 years
由于每种测试方法指示的毒性途径不同,研究人员将几种测试方法联用从而获得更多的毒性信息。Maisanaba等[15]采用NRU、MTS实验对2 种用于FCM的硅烷改性黏土矿物进行体外细胞毒性评价,结果显示,在选择的质量浓度范围(0~250 μg/mL)内,一种样品在NRU和MTS实验中均无细胞毒性;而另一种样品在2 种实验中均表现出显著的细胞毒性。Mittag等[24]采用4 种测定方法(BrdU-酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)、WST-1、NRU、RNA合成抑制实验)以及4 种细胞系(人宫颈癌细胞Hela-S3、人结肠癌细胞Caco-2、人结肠癌细胞HT-29、人肝癌细胞HepG2),评估2 种罐涂料(聚酯树脂和环氧树脂)95%乙醇迁移液的细胞毒性,最终不同方法显示的细胞毒性结果也不同。相同的是,2 种罐涂料均对Caco-2细胞显示出细胞毒性作用,但仅有环氧树脂涂料对HepG2细胞显示出显著的细胞毒性。Maisanaba等[16]采用MTS、NRU、TPC方法分别研究了含有2 种改性黏土的聚乳酸(polylactic acid,PLA)纳米复合材料的提取物对Caco-2和HepG2细胞系的细胞毒性。在不同的细胞和暴露时间(24、48 h)条件下,3 种测试方法的结果均为阴性。Bradley等[21]用NRU、TPC和RNA合成抑制实验,在人喉癌上皮细胞系Hep-2、小鼠肝癌细胞系Hepa1c1c7、HepG2和HeLa细胞系中研究了19 份食品接触纸或纸板的热水、冷水、95%乙醇和Tenax提取物的细胞毒性。结果显示水或Tenax提取物呈阴性,4 份样品的95%乙醇提取液呈阳性。Maisanaba等[26]使用Caco-2细胞系对暴露24 h和48 h后的2 种硅烷改性黏土进行NRU和MTS实验,结果显示暴露24 h和48 h后2 种样本均呈阴性。
2 遗传毒性
遗传毒性是指DNA在染色体水平、分子水平和碱基水平上受到各种损伤,从而造成基因突变、染色体结构和数量改变的毒性作用,可能引起癌症、遗传疾病和先天性缺陷。
2.1 致突变
致突变最常用的是鼠伤寒沙门氏菌/组氨酸回复突变实验(Ames实验)。Ames实验需要在4 种标准实验菌株(鼠伤寒沙门菌TA98、TA97、TA100、TA102)上进行,并分别进行不加及加代谢活化系统(S9混合物)的检测,是应用最广泛的检测基因突变的体外实验。其原理是检测待测物诱发鼠伤寒沙门氏菌/组氨酸营养缺陷型突变株(his-)回复突变成野生型(his+)的能力。根据选择性培养基上生长的细菌菌落数目,与对照组自发回复突变菌落数目相比较,来测定化学物质诱导微生物基因突变的能力。该方法具有灵敏度高、检出率高、操作简便等优点。Ames II实验作为Ames实验的一种有效替代方法,使用2 种菌株(TA98和混合菌株TA7001-7006)即可进行检验,其对诱变剂敏感性更强,实验结果可重复性更好,实验室间差异小[27]。
Maisanaba等[16]用Ames实验评估了2 种PLA纳米复合材料提取物的致突变性,结果为阴性。Mittag等[24]使用Ames II实验检测了2 种罐涂料(聚酯纤维和环氧树脂)的95%乙醇提取液,结果均为阴性,但是该研究没有添加外源代谢系统(S9混合物),因此可能产生假阴性数据。徐峰等[28]对二氧化碳基塑料进行了Ames实验,结果为阴性,表明该材料没有致突变性。
2.2 DNA原始损伤
2.2.1 彗星实验(Comet实验)
Comet实验是检测单个细胞DNA损伤和修复的实验。它可以检测到DNA单、双链断裂,碱基活性损伤以及DNA修复期间产生的DNA链断裂。在Comet实验中,细胞DNA受到损伤产生链断裂,其碎片进入凝胶中,在凝胶电泳时碎片离开核DNA形成尾状带,未损伤的DNA部分保持球形。Comet实验具有快速、简单、灵敏的特点,少量细胞就可以分析,无需放射性标记,适用于任何可制成单细胞悬液的真核细胞,而且适用范围广、敏感性高。
Ozaki等[22]利用人早幼粒急性白血病细胞系HL-60进行了Comet实验,结果发现8 份纸板样品中有6 份呈显著阳性。蔡亚云等[29]用Comet实验研究了不同粒径(10 nm~1 μm)的聚苯乙烯(polystyrene,PS)塑料颗粒对斑马鱼腮细胞的毒性影响,结果呈阳性。Riquet等[14]使用Comet实验研究分别由抗氧化剂Irgafos 168、Irganox 1076和紫外线吸收剂Tinuvin 326制备的PP薄膜的遗传毒性,12 种提取物的测试结果全部为阴性。Maisanaba等[26]使用Caco-2细胞系对暴露24 h和48 h后的2 种硅烷改性黏土进行Comet实验以评估其遗传毒性,结果均呈阴性。
2.2.2 BlueScreen HC测定法
BlueScreen HC测定法是基于人体细胞报告基因的一种检测方法,专为高通量筛选化学物质遗传毒性而设计。其原理是利用Gaussia荧光素酶,检测经基因修饰的包含GADD-45a启动子的人类淋巴母细胞TK6。目前已经在药物制剂和香精香料等领域验证了该方法的可行性[30]。Koster等[31]利用该法(加或不加S9混合物)检测了3 种纸板提取物的遗传毒性,结果为阴性。
2.3 染色体和染色体组畸变
2.3.1 微核实验
微核(micronuclei,MN)实验可以检测位于人类或啮齿动物细胞系间期细胞细胞质中的MN,从而有效检测致癌物和致敏物。可用于MN实验的哺乳类动物细胞有骨髓细胞、肝细胞、淋巴细胞等。
2.3.2 姐妹染色单体交换实验
姐妹染色单体交换(sister chromatid exchange,SCE)实验是用于检测双染色体姐妹染色单体之间DNA相互交换的生物测定法。SCE实验的检测核心是差异地标记姊妹染色单体,即利用BrdU掺入DNA分子中观察姐妹染色单体,观察不同数量胸腺嘧啶核苷组成的染色体区域[32]。Ergene等[33]在人类血液淋巴细胞上进行SCE实验来评估多种聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)瓶装饮用水的遗传毒性,结果均为阴性。
2.3.3 染色体畸变实验
染色体畸变(chromosome aberration,CA)实验是检测化学物质影响染色体数量和结构的基本方法,其原理是将哺乳动物细胞暴露于待测物中,在暴露后的预定时间间隔内,用中期停滞物质(秋水仙碱)处理细胞,收集细胞并染色,用显微镜分析以检查CA情况。
2.4 测试方法的联用
由于每种测试方法指示的毒性途径不同,研究人员将几种测试方法联用从而获得更多的遗传毒性信息。Nakai等[34]利用Ames实验和CA实验(中国仓鼠肺细胞CHL/IU)评估了与食品接触PS材料中丙酮提取物的遗传毒性,测试结果均为阴性。Bach等[17]采用Ames实验和MN实验(HepG2细胞)测试暴露在阳光或高温条件下PET瓶装饮用水提取物的遗传毒性,结果均为阴性。Maisanaba等[15]采用Ames和Comet实验对2 种用于FCM的硅烷改性黏土矿物进行评价,一种样品在2 种实验中均为阴性,另一种样品则在2 种实验中均表现出显著的DNA氧化损伤。Bradley等[21]用Ames实验和Comet实验对用不同提取物(热水、冷水、95%乙醇、Tenax)提取的19 份食品接触纸或纸板以及1 份非食品接触纸板进行研究。Ames实验结果表明,20 份样品的乙醇提取物中有1 份呈阳性,Comet实验中水或Tenax提取物呈阴性。Lionti等[35]用Ames实验和MN实验研究3 种用于合成食品接触涂料常见前体的遗传毒性,包括原硅酸四乙酯(tetraethylorthosilicate,TEOS)、甲基三乙氧基硅烷(methyltriethoxysilane,MTES)和3-缩水甘油氧基丙基三乙氧基硅烷(3-glycidyloxypropyltriethoxysilane,GPTES)。Ames实验结果显示,加或不加S9混合物的情况下,TEOS和MTES均无致突变性,GPTES在TA100和TA1535菌株中观察到阳性反应;MN实验中,3 种样本全部呈阴性。Séverin等[36]采用Ames实验和MN实验评估聚碳酸酯上2 种溶胶-凝胶涂料的体外遗传毒性,结果均为阴性。Souton等[37]通过Comet实验和MN实验研究回收纸板起始和最终产品的迁移物在人肝癌细胞(HepG2/HepaRG)上诱导的遗传毒性,结果呈阳性,此外,FCM起始物表现出的DNA损伤可能会得到进一步的修复,而最终产品可能会将DNA损伤转化为染色体突变,从而证实了评价最终产品提取物危害的重要性。
近20 年来用于评估FCM提取物遗传毒性的生物测定方法、原理总结见表2。
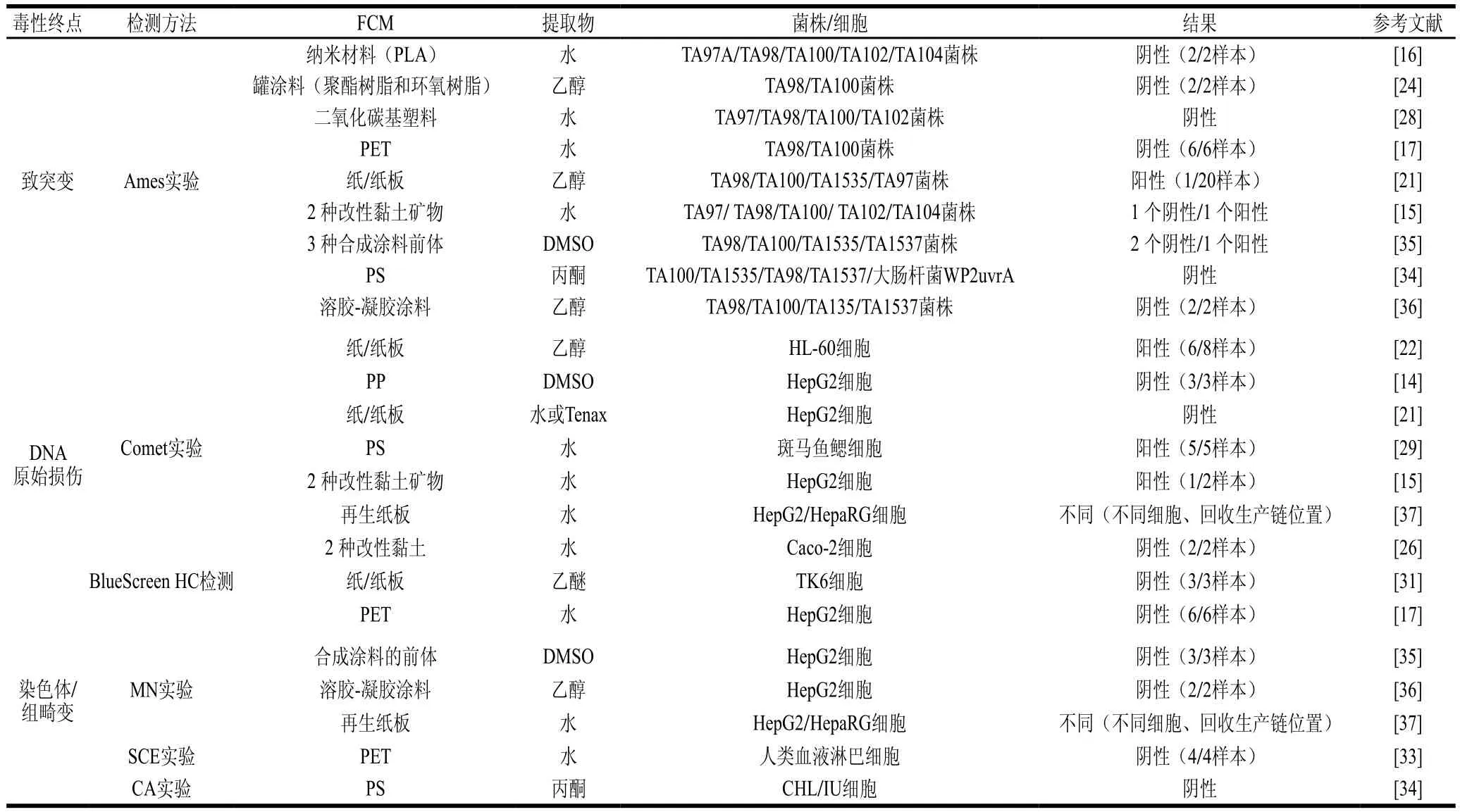
表2 近20 年来FCM提取物遗传毒性的生物测定方法Table 2 Genetic toxicity bioassays for FCM extracts published in the literature in the past 20 years
3 内分泌干扰效应
内分泌干扰物(endocrine disrupting chemicals,EDCs)主要包括性激素(雌/雄/孕激素)干扰物、肾上腺皮质激素(糖/盐皮质激素)干扰物等,可通过干扰人体内天然激素的活动过程从而对生殖、神经和免疫系统等功能产生影响。EDCs可以与人体和动物体内特定的激素受体结合,从而干扰内分泌系统的正常功能。研究发现从食品包装迁移到食品中的化学物质(如双酚A(bisphenol A,BPA)、邻苯二甲酸盐)会导致EDCs对人体的入口暴露[38-39],因此内分泌干扰逐渐成为国内外研究人员高度关注的问题,也是评估FCM安全性的一个重要毒性终点。FCM内分泌干扰效应的测试方法主要有人乳腺癌MCF-7细胞增殖实验(E-Screen实验)和报告基因测试法。
3.1 E-Screen实验
E-Screen实验的原理是雌激素活性物质可以与雌激素受体(estrogen receptor,ERs)结合并刺激ER+细胞增殖,因其简单易行而被广泛应用于雌激素活性物质的筛选。实验比较在不存在雌激素(阴性对照)、存在17β-雌二醇(阳性对照)、存在待测物的情况下,接种MCF-7细胞所获得的细胞数量。Wagner等[18]利用E-Screen实验分析18 种包装在玻璃瓶或PET瓶中的矿泉水,结果18 份样品中的11 份样品检测到雌激素活性。武宗高等[40]利用该法检测3 种增塑剂邻苯二甲酸二丁酯(dibutyl phthalate,DBP)、BPA和壬基酚(nonyl phenol,NP)的雌激素活性及其联合效应,结果表明DBP、BPA和NP均能够促使细胞进入S期(DNA合成期),显著促进MCF-7细胞增殖,具有雌激素活性。Lopez-Espinosa等[23]检测40 种纸或纸板乙醇提取物的雌激素活性,结果90%样品的提取物呈阳性。
3.2 报告基因测试
3.2.1 酵母菌雌(雄)激素筛选实验
在酵母菌雌(雄)激素筛选(yeast estrogen screen,YES)/(yeast androgen screen,YAS)测定中,酵母菌株含有稳定整合的人类雌(雄)激素受体(hERα/hAR)基因和受雌(雄)激素反应元件(ERE/ARE)控制的含有lacZ报告基因(编码β-半乳糖苷酶)的表达质粒。酵母中的雌(雄)激素受体基因被雌(雄)激素活性物质激活,在蛋白质转录和合成过程中,报告基因也同时被激活,编码β-半乳糖苷酶的基因表达并转录生成β-半乳糖苷酶,通过测定其活性来定量出待测物的类雌(雄)激素活性。它可以检测雌(雄)激素活性(YES/YAS)及抗雌(雄)激素(YAES/YAAS)活性。该实验的优点是原理简单、易于操作、费用低廉,且酵母不具有内源性受体,不存在核受体干扰现象。
G u a r t等[19]使用YA E S/YA A S分析方法研究Tritan™ BPA替代树脂和聚碳酸酯的迁移。在40 ℃水中放置10 d后,检测结果为阴性。Wagner等[41]使用YES检测法分析20 种包装在玻璃瓶或PET瓶中的矿泉水,结果60%的样品检测出雌激素活性。此后,Wagner等[42]又用YAES和YAAS分析18 种瓶装水的抗雌激素活性和抗雄激素活性,结果表明,13 种样品有抗雌激素活性,16 种样品有抗雄激素活性。Kirchnawy等[43]对不同食品包装用塑料的提取物进行研究,首先使用YES实验分析了PET、PP、聚乙烯(polyethylene,PE)、PS和复合薄膜提取物的雌激素效应,结果显示42 个样品中有7 个样品出现雌激素受体阳性,11 种PET样品的雌激素活性均为阴性;然后使用YES、YAS并结合化学分析(气相色谱-质谱联用和高效液相色谱-质谱联用)对样品中的雌激素和雄激素活性物质进行了表征,结果表明,18 个样品中的4 个样品在YES测定中显示雌激素活性。Mertl等[44]研究3 种食物接触纸板的提取物,其中2 种在YAAS中显示出抗雄性激素活性。
3.2.2 荧光素酶报告基因实验
荧光素酶是生物体内催化荧光素或脂肪醛氧化发光的一类酶的总称,可分为萤火虫荧光素酶和细菌荧光素酶。荧光素酶报告基因实验是以荧光素为底物,靠酶和底物的相互反应发光,通过荧光测定仪也称化学发光仪或液闪测定仪检测萤火虫荧光素酶活性的实验。这一实验具有特异性强、灵敏度高、信噪比高等优点。
Bach等[17,45]使用HepG2细胞系和人乳腺癌细胞株MDA-MB453-kb2研究了暴露于阳光(2、6、10 d)和高温(40、50、60 ℃)下PET瓶装水及玻璃瓶装水的雌激素活性和抗雄激素活性,结果均为阴性。Plotan等[20]利用报告基因检测结合固相萃取技术,研究了14 个品牌(共42 份样品)瓶装矿泉水的内分泌干扰能力,结果在78%的样本中发现雌激素受体(ER)、雄激素受体(androgen receptor,AR)、孕激素受体(progesterone receptor,PR)和糖皮质激素受体(glucocorticoid receptor,GR)活性。Maggioni等[46]使用Hela细胞分析了在意大利市场购买的5 种PET瓶装矿泉水的雌激素受体活性,结果为阴性。Chevolleau等[47]使用Hela细胞系研究7 种PET瓶装水和4 种玻璃瓶装水的多种激素活性(ER、AR、PR、GR、甲状腺激素受体(thyroid hormone receptor,TR)),结果为阴性。Séverin等[36]使用HepG2细胞系通过转录激活检测评估聚碳酸酯上2 种溶胶-凝胶涂料的雌激素活性,结果为阴性。Veyrand等[48]使用人骨肉瘤细胞系U2OS对PS/PE塑料杯中抗氧化剂亚磷酸三壬基酚酯(tris(nonylphenyl) phosphite,TNPP)的降解产物4-壬基酚(4-nonyl phenol,4-NP)进行雌激素活性和抗雄激素活性,结果均为阳性。Rosenmai等[49]在人卵巢腺癌细胞系BG1Luc4E2、中国仓鼠卵巢细胞系ATCC、小鼠胚胎成纤维细胞系NIH-3T3、大鼠肝癌细胞H4IIE和U2OS细胞系中,对20 个食品接触类纸和纸板进行8 种报告基因(AR、ER、芳香烃受体(aryl hydrocarbon receptor,AhR)、过氧化酶增殖激活受体γ(peroxisome proliferator-activated receptor γ,PPARγ)、GR、视黄酸受体(retinoic acid receptor,RAR)、核转录因子2(nuclear factor (erythroid-derived 2)-like 2,Nrf2)和肿瘤抑制基因53(transformation-related protein 53,p53))测定,结果显示,20 种样本中11 种具有AR活性和抗AhR活性,9 种具有ER活性,12 种具有PPARγ活性,16 种具有Nrf2活性,6 种具有p53活性,但是20 种样本对RAR和GR受体均为阴性。
3.3 测试方法的联用
表3 FCM内分泌干扰性的生物测定Table 3 ndocrine disruption bioassays for FCM extracts

表3 FCM内分泌干扰性的生物测定Table 3 ndocrine disruption bioassays for FCM extracts
检测方法 FCM 提取物 菌株/细胞 结果 参考文献PET/玻璃 水 MCF-7细胞阳性(23/29样本雌激素活性)阳性(11/29样本抗雌激素活性)阳性(8/29样本雄激素活性)阳性(12/29样本抗雄激素活性)[50]E-Screen PET/玻璃 水 MCF-7细胞 阳性(11/18样本雌激素活性) [18]BPA替代树脂(PS/TritanTM) 乙醇 MCF-7细胞 不同(不同聚合物、包装和过程) [51]DBP/BPA/NP DMSO MCF-7细胞 阳性(雌激素活性) [40]纸/纸板 乙醇 MCF-7细胞 阳性(36/40样本雌激素活性) [23]PET/PP/PE/PS/复合薄膜/纸板 DMSO 重组酵母菌株阳性(4/18样本雌激素活性)阴性(雄激素活性)阳性(大多数样本拮抗活性)[43]报告基因检测酵母YAES/YAAS奶制品纸盒 DMSO 重组酵母菌株 阳性(2/3样本抗雄激素活性) [44]PET/PP/PE/PS/复合薄膜 乙醇 重组酵母菌株 阳性(7/42样本雌激素活性) [43]Tritan TM/聚碳酸酯 水 重组酵母菌株 阴性(2/2样本(抗)雌激素和(抗)雄激素活性) [19]PET/玻璃(YES) 水 重组酵母菌株 阳性(12/20样本雌激素活性) [41]PET(YAES/YAAS) 水 重组酵母菌株 阳性(13/18样本抗雌激素活性)阳性(16/18样本抗雄激素活性) [42]PET/玻璃 水 PALM细胞 阳性(8/29样本雄激素活性)阳性(12/29样本抗雄激素活性) [50](PS/TritanTM) 乙醇 大鼠肝癌细胞(H4IIE) 阳性(雌激素活性) [51]BPA替代树脂PET 水 MDA-kb2/HepG2细胞 阴性(抗雄激素和雌激素活性) [17, 45]PET 水 MCF-7/T47D细胞[20]荧光素酶报告基因实验阳性(16/42样本雌激素活性)阳性(16/42样本雄激素活性)阳性(12/42样本抗雄激素活性)阳性(15/42样本孕激素活性)阳性(23/42样本糖皮质激素活性)PET 水 HeLa细胞 阴性(5/5样本雌激素活性) [46]PET/玻璃 水 HeLa细胞 阴性(11/11样本类雌(雄)激素活性) [47]PS/PE DMSO U2OS细胞 阳性 [48]食品接触纸/纸板 DMSO ATCC细胞(AR)H4IIE细胞(AhR)BG1Luc4E2细胞(ER)NIH-3T3细胞(PPARγ)U2OS细胞(GR/RAR/Nrf2/p53)11/20样本AR阳性;11/20样本抗AhR阳性;9/20样本ER阳性;12/20样本PPARγ阳性;16/20样本Nrf2阳性;6/20样本p53阳性)20/20样本RAR和GR阴性[49]溶胶-凝胶涂料 乙醇 HepG2细胞 阴性(2/2样本雌激素活性) [36]
Real等[50]应用E-Screen实验和人前列腺癌细胞PALM的萤光素酶测定法调查了西班牙南部市售的29 种饮用水(PET及玻璃瓶包装)的激素活性(雌激素、雄激素激动剂和拮抗剂作用)。E-Screen实验证明了所有样品中都含有至少一种激素活性;PALM细胞萤光素酶实验中,29 个样品中8 个显示雄激素受体活性,12 个样品为抗雄激素受体活性。Bittner等[51]采用E-Screen实验和报告基因测试对14 种热塑性树脂的提取物(10%、50%、100%乙醇和盐水)进行研究,结果表明,3 种TritanTM树脂在盐水提取后表现出显著的ER活性。近年来用于评估FCM内分泌干扰性的生物测定方法、原理及应用总结见表3。
4 结 语
体外生物测定法可以针对特定的毒理学终点进行研究,具有敏感、快速等优点。目前针对FCM危害的体外生物测定的研究主要集中在FCM提取物的细胞毒性、遗传毒性和内分泌干扰性方面。体外生物测定法可以检测出不能通过化学分析或QSAR预测的潜在毒性(特别是NIAS),由于包含了“鸡尾酒效应”(由于累加效果甚至协同效应,使得混合化学品的毒性超过各自单独效应的总和),它能够提供FCM提取物的实际危险和质量评估的综合信息,还可与化学分析结合,共同应用于FCM的风险评估。
目前国内有关FCM安全性评价的体外生物测定的相关研究极少。鉴于体外生物分析方法的独特优点与快速筛选能力,建议深入研究并推广其在FCM安全性评价中的应用,并探索评价方法的标准化,积极推进通用、快速、有效的FCM安全性评估生物测定方法体系的建立。

