煤表面活性特征结构对3个氧分子的吸附研究
王晓波
(太原理工大学 院士工作办公室,山西 太原 030024)
煤自燃是煤矿安全生产的重大灾害之一,对矿区周围的生态环境也造成了破坏。煤自燃是一个复杂的物理、化学反应过程。经过多年的发展历程,已形成许多相关煤自燃的学说[1-2].早可追溯到 17世纪,Dr.Plott 提出煤炭自燃是其中的黄铁矿导致的,后来又有研究认为是细菌诱导或者酚基诱导的等。随着科学技术的发展,关于煤炭自燃机理研究越来越深入,目前被大家广泛接受的煤炭自燃理论是煤氧复合作用学说。煤与氧相互作用发生氧化自燃反应的过程包括物理吸附、化学吸附和化学反应3个阶段。其中,煤物理吸附氧气的阶段是引起煤与氧发生反应的开端[3-5].
煤是一种由多种有机小分子和大分子混合组成的孔隙结构丰富、比表面积大的有机岩。它能够自发在煤表面吸附气体,并释放大量吸附热为煤炭自燃提供能量。
以简化的芳香环作为煤的芳香环骨架,并适当添加侧链构建煤活性特征结构简化模型,用于分析煤吸附氧气的作用机理[6].应用量子化学密度泛函理论和方法,深入探究煤活性特征结构吸附3个氧分子的吸附机理和吸附过程,为进一步揭示煤自燃的本质提供基础理论。
1 吸附几何构型
煤活性特征结构模型是只保留苯环和侧链的简化结构,见图1,氧分子在苯环或者在侧链上吸附,吸附的位置不同导致煤自燃的程度不同。由量子化学计算软件Gaussian03程序,采用密度泛函理论(DFT),基准采用B3LYP/6-311G计算得到煤活性特征结构吸附与3个氧分子的吸附平衡几何构型,见图2.
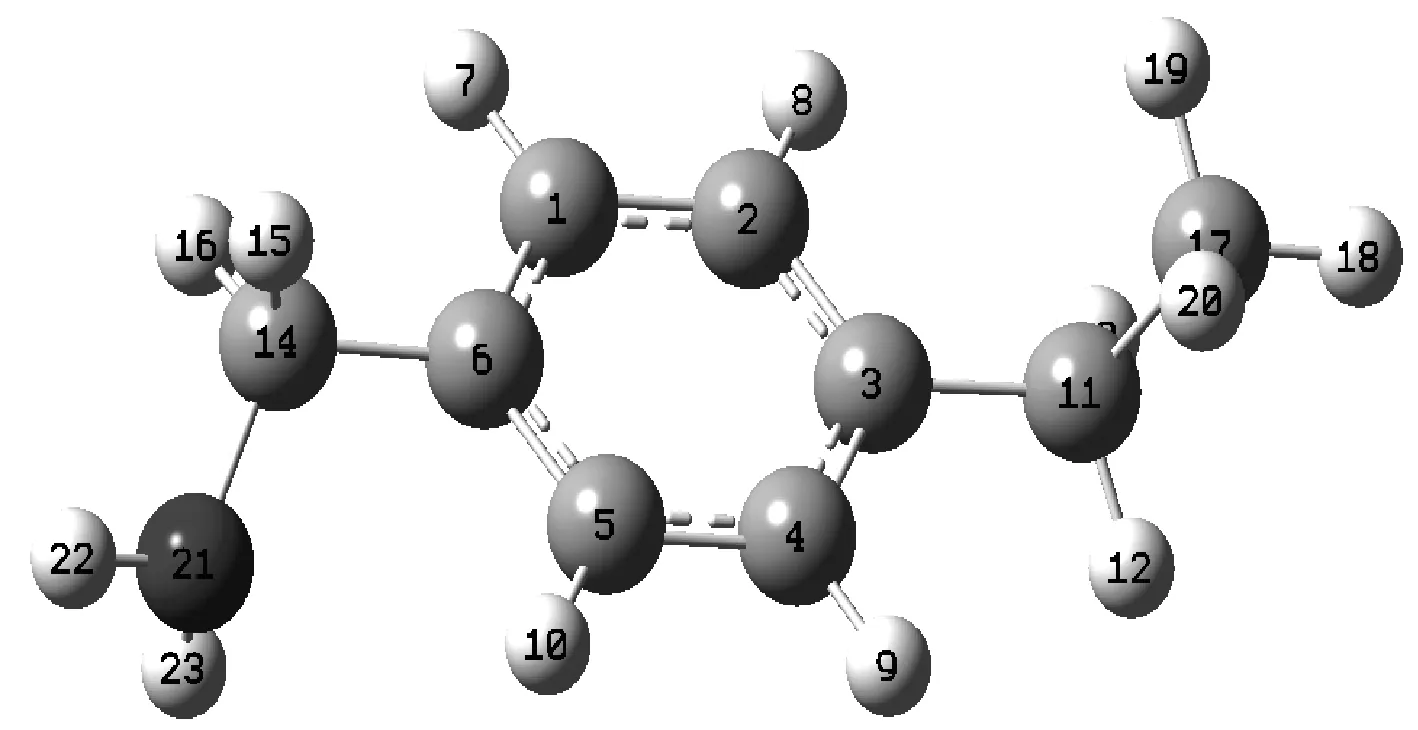
图1 煤活性特征结构模型图
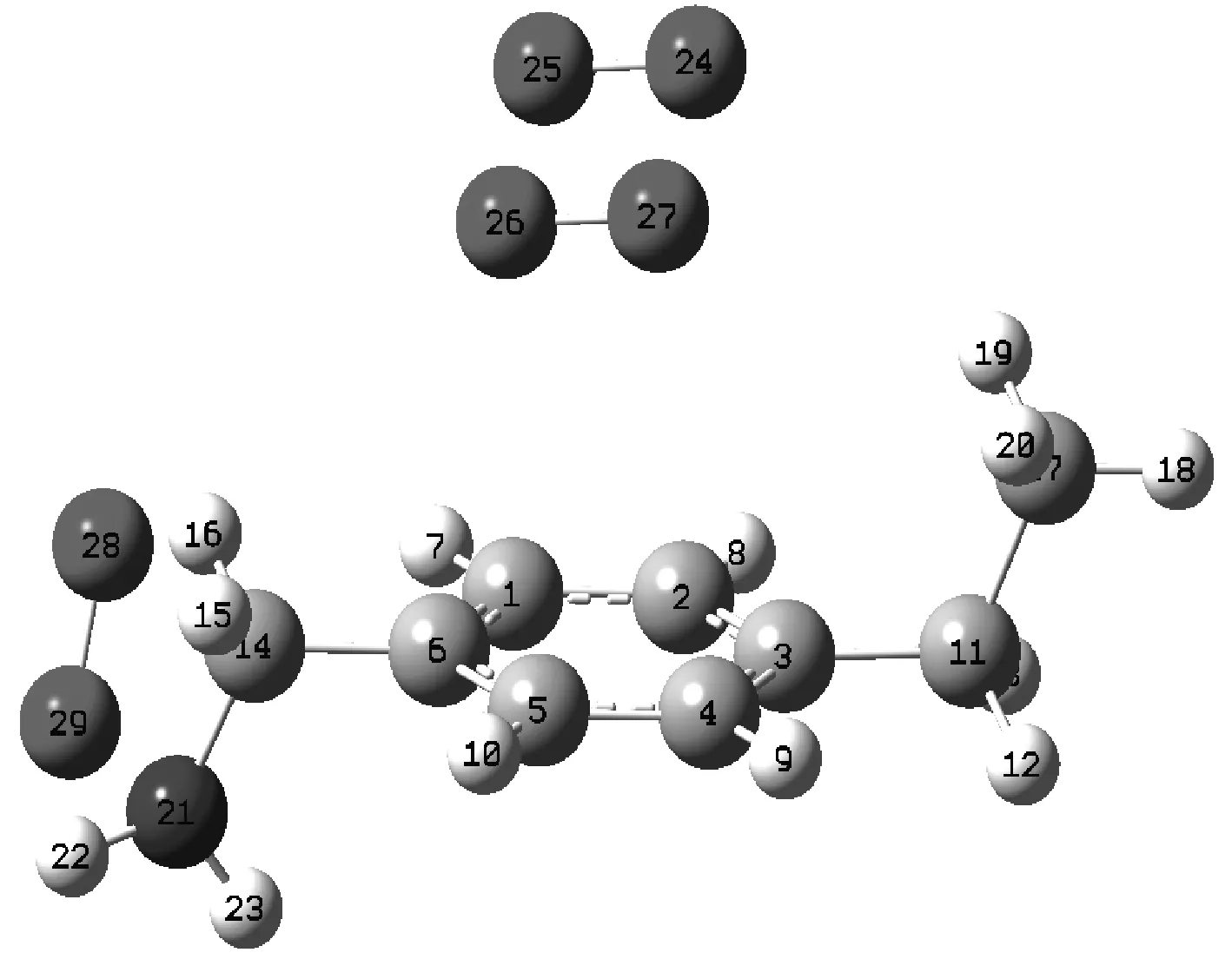
图2 活性特征结构与氧吸附平衡几何构型图
通过对比图1,2以及构型数据表明,煤与3个氧分子的吸附是物理吸附。通过计算键长、键角可以描述氧分子在煤表面的位置。煤活性特征结构与氧吸附平衡几何构型化学键键长见表1.

表1 煤活性特征结构与氧吸附平衡几何构型化学键键长表
由表1计算分析得出,吸附在煤活性特征结构苯环上的氧分子在吸附前的键长为125.82 pm,吸附后各氧分子的键长都有变化,O24-O25变为126.37 pm,O26-O27变为126.54 pm.吸附在煤表面侧链上O28-O29的键长变为132.14 pm.氧分子被煤表面吸附后由于煤表面与氧分子的相互作用,O-O键被拉长变大。键长增加则氧分子活性增强,增加煤活性特征结构与氧发生化学反应的可能性,且侧链吸附的氧分子变化最大,说明侧链上的氧分子比苯环上的氧分子更活跃。
2 平衡吸附位置及距离
应用量子化学密度泛函理论计算优化后的吸附模型,可以看出,煤表面对3个氧分子吸附组成的吸附态中,2个氧分子的位置位于苯环所在平面的上方,1个位于煤表面的含氨基侧链上。
由吸附平衡构型可看出,O24原子距苯环C原子的距离分别为:R(O24,C1)=349.422 pm,R(O24,C2)=350.273 pm,R(O24,C3)=331.321 pm,R(O24,C4)=296.643 pm,R(O24,C5)=299.299 pm,R(O24,C6)=315.351 pm.O25原子距苯环C原子的距离分别为:R(O25,C1)=247.935 pm,R(O25,C2)=350.274 pm,R(O25,C3)=311.031 pm,R(O25,C4)=313.709 pm,R(O25,C5)=320.496 pm,R(O25,C6)=313.899 pm.
O26原子距苯环C原子的距离分别为:R(O26,C1)=331.428 pm,R(O26,C2)=397.354 pm,R(O26,C3)=453.431 pm,R(O26,C4)=448.996 pm,R(O26,C5)=391.227 pm,R(O26,C6)=317.902 pm.O27原子距苯环C原子的距离分别为:R(O27,C1)=365.724 pm,R(O27,C2)=443.641 pm,R(O27,C3)=450.019 pm,R(O27,C4)=410.860 pm,R(O27,C5)=350.742 pm,R(O27,C6)=317.760 pm.
O28、O29原子距侧链C原子的距离分别为:R(O28,C14)=267.381 pm,R(O29,C14)=272.032 pm.
O原子与含氨基侧链N原子的距离分别为:R(O28,N21)=273.173 pm,R(O29, N21)=204.436 pm.
从以上数据分析得到,煤活性特征结构苯环对氧分子的吸附位置位于苯环的平面上方。含氨基侧链对氧的吸附位于C-N键的正上方,且氧原子与N原子的距离较近。
3 电荷集居数与振动频率
通过分析电荷集居数与振动频率,可以得到煤活性特征结构与氧分子吸附前后各轨道电子布居数。
煤活性特征结构苯环上的C原子有电荷转移到氧分子上,电荷增加少说明侧链吸附氧之后会造成苯环对氧吸附的减弱。电子转移使氧分子的O-O键强度减弱,键拉长拉大。
当氧分子吸附在侧链上时,H16、H22、H23全部失去电子,则氢原子的净电荷增加,增强了C-H键、N-H键。
吸附在含氨基侧链上的氧分子的净电荷发生了较大的改变,O26、O27的4P轨道分别得到电子。证明侧链对氧的吸附是一种比较强的相互作用,而且其得到的电子主要由C14和N21来提供,由于吸附在侧链的氧分子的最高占据轨道得到了大量的电子,削弱了O-O键的作用,导致O-O键的键长拉长的作用比较明显。
煤活性特征结构吸附氧前后的C-C键、O-O键和C-H键的红外伸缩振动频率对比见表2.
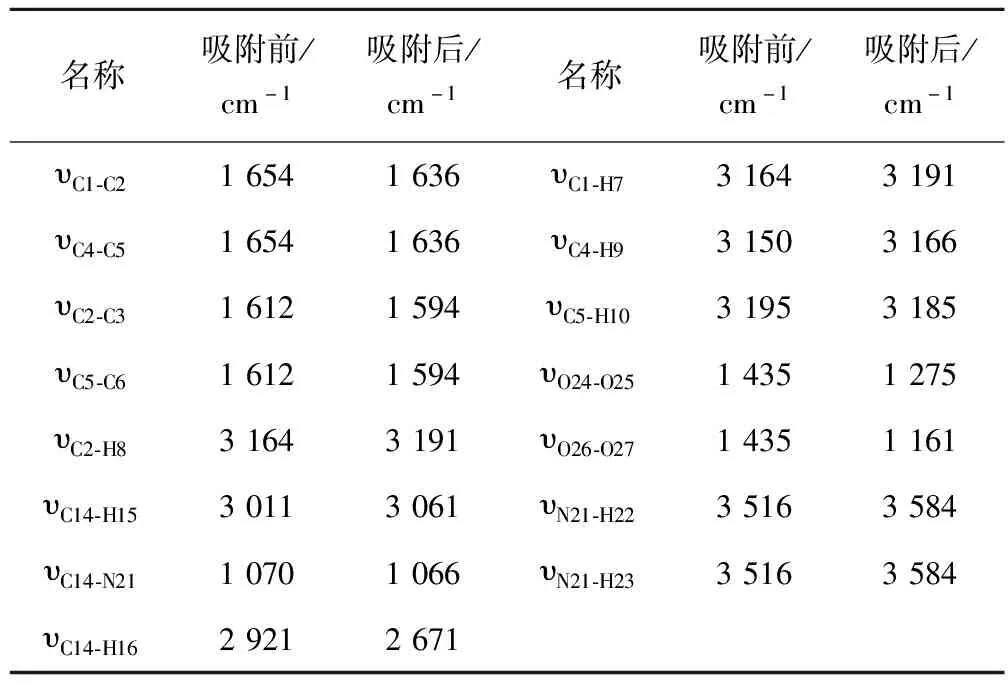
表2 煤活性特征结构与氧分子吸附前后红外振动频率比较表
吸附前O-O键的振动频率为1 435 cm-1,吸附后苯环上的O-O键的振动频率为1 275 cm-1,侧链上的O-O键的振动频率为1 161 cm-1,吸附后振动频率均减少,同时说明氧原子之间的化学键减弱。C-H键与N-H键的振动频率变化较小,而且它们的频率都具有增大的趋势,说明在吸附态中它们的化学键得到了不同程度地加强;但是在吸附态中,C-C键的振动频率并没有增大,反而有不同程度地减小,这是由于苯环碳原子上的电子向氧分子转移,导致了苯环C-C键的减弱。
4 吸附能
吸附能计算公式为:
ΔE=EM+EO2-Ecomplex
(1)
式中:
ΔE—煤活性特征结构与氧分子的吸附能,kJ/mol;
EM—吸附前煤活性特征结构的能量,kJ/mol;
EO2—吸附前氧分子的能量,kJ/mol;
Ecomplex—煤活性特征结构吸附氧分子的平衡几何构型的能量,kJ/mol.
煤表面与氧分子发生吸附放出能量,使煤体温度升高,在蓄热环境好的条件下,随着能量的积聚,煤体温度的不断升高导致煤氧化自燃。吸附前的氧气分子的能量为-150.26 Hartee,煤表面的能量为-405.33 Hartee,3个氧分子与煤表面吸附后组成的吸附态的能量为-856.17 Hartee.由式(1)计算得到氧分子与煤活性特征结构的吸附能为202.11 kJ/mol,由此可知,氧分子易与煤活性特征结构发生物理吸附。
5 结 论
1)氧分子与煤活性特征结构的吸附能为202.111 kJ/mol,氧分子易与煤活性特征结构发生物理吸附。
2)键长增加则氧分子活性增强,增强与煤表面发生化学反应的可能性,且侧链上的氧分子比苯环上的氧分子更活跃。
3)煤活性特征结构苯环上的C原子有电荷转移到氧分子上,电荷增加少说明侧链吸附氧之后会造成苯环对氧吸附的减弱。电子转移使氧分子的O-O键强度减弱,键拉长拉大。
4)吸附在含氨基侧链上的氧分子的净电荷发生了较大的改变,证明侧链对氧的吸附是一种比较强的相互作用,而且其得到的电子主要由C14和N21来提供,由于吸附在侧链的氧分子的最高占据轨道得到了大量的电子,削弱了O-O键的作用,导致O-O键的键长拉长的作用比较明显。

