肝细胞生长因子对大鼠大脑中动脉梗塞后凋亡变化的实验分析
许璐璐,汤 宏,高 宁,沈 倩,陈 杰,吴海波
脑卒中是人类致残及致死率较高的疾病之一,随着中国社会老龄化、居民不健康生活,脑卒中的发生率每年增长约8.3%,其中以缺血性卒中占比最多[1]。由于脑梗塞发生后出现急性局部血流中断,从而发展为缺血缺氧、脑组织软化坏死,甚至出现相应的神经系统症状,严重的会导致昏迷和死亡[2]。随着医疗环境及技术的发展,缺血性脑卒中治疗已经飞速发展,如阿司匹林等一系列抗血小板药物的临床应用,以及近些年兴起的溶栓取栓操作,均使缺血性脑卒中的治疗有了明显改善,但缺血性脑卒中引起的致残率及带给患者家庭的经济负担是无法估计的。
肝细胞生长因子(hepatocyte growth factor, HGF)是一种能调节血管和神经再生、组织重建及抗凋亡信号的细胞因子,HGF与其受体c-Met结合激活信号通路从而产生生物学效应[3]。研究表明,HGF与激活的c-Met结合能保护心脏避免心肌缺血引起的损伤,以及有助于缺血后的心室重塑等[4],HGF在Alzheimer疾病和脊髓轴索损伤中能起到神经保护作用[5-6],但其在颅内卒中的研究报道较少。本实验将探究大鼠大脑中动脉栓塞(middle cerebral artery occlusion, MCAO)模型建立后HGF对脑组织凋亡的影响。
1 材料与方法
1.1 实验动物及分组雄性SD大鼠62只,每只重250~300 g,由美国罗马琳达大学动物实验中心提供,随机分为Sham组、MCAO组及HGF组,实验组按不同取材时间点分为模型后6、24、72 h。具体分组如下:实验1组:将大鼠随机分为Sham组、MCAO组(6、24、72 h),每组6只大鼠,Western blot检测取材使用的脑组织为大鼠受伤侧/右侧大脑半球脑组织;实验2组:将大鼠随机分为Sham组、MCAO组(24 h),每组4只大鼠,用于免疫荧光共染定位c-Met与神经元;实验3组:将大鼠随机分为Sham组、MCAO组(24 h)、HGF组,每组6只大鼠,在模型制作成功后24 h进行行为学评定,并处死大鼠,行TTC染色;实验4组:将大鼠随机分为Sham组、MCAO组(24 h)、HGF组,每组4只大鼠,用于TUNEL染色评估细胞死亡。
1.2 主要试剂及仪器重组人HGF(美国Abcam公司),兔抗c-Met抗体(美国Aabcam公司),德国徕卡荧光显微镜,TUNEL试剂盒(美国Roche公司),TTC试剂(美国Sigma Aldrich公司)。
1.3 模型制作MCAO模型制作参照文献[7],氯胺酮(80 mg/kg)/甲苯噻嗪(20 mg/kg)腹腔注射麻醉成功后,仰卧位平躺暴露颈部,正中切开皮肤分离皮下组织及肌肉,显露右侧颈总动脉、颈内动脉及颈外动脉,结扎颈外动脉远端,用显微动脉阻断夹临时阻断颈总动脉血流,并在颈外动脉近端剪一小口,将线栓经小口逐步放入颈内动脉至右侧大脑中动脉处,感觉到阻力或线栓进入长度达1.8~2 cm即为达到大脑中动脉处,此时结扎固定线栓,缝合皮肤,放置37 ℃温箱复苏。Sham组仅将线栓放入大脑中动脉位置后立即拔出[8]。HGF组大鼠在MCAO造模成功后1 h经鼻腔内给药,每只大鼠10 μg/kg。
1.4 神经行为学评分修定的Garcia评分和平衡木测试用于大鼠的神经行为学评分,Garcia评分共有6组(自发运动、四肢对称性运动、前肢外伸、爬行、身体本体感觉及胡须触觉反应),每组评分范围0~3分。平衡木为测试大鼠在狭长的木棍上行走1 min的能力,评分范围0~5分[9]。
1.5 梗塞面积评估模型制作成功后24 h处死大鼠,断头取脑,切片放入TTC中浸泡,待脑组织颜色改变后取出拍照,梗塞区面积使用Image J软件统计。
1.6 免疫荧光、TUNEL染色大鼠在模型制作成功后24 h再次麻醉大鼠,断头取脑,经10%中性福尔马林、30%蔗糖浸泡,冷冻切片机10 μm厚切片,分别经过兔抗c-Met抗体过夜及相应二抗,最后在荧光显微镜下拍照。TUNEL染色同样取10 μm厚切片,按照试剂盒说明书步骤进行操作,最后在显微镜下拍照[10]。
1.7 Western blot法模型制作成功后在相应的时间点断头处死大鼠,取右侧梗塞大脑半球脑组织快速放入液氮并转移至-80 ℃低温冰箱保存。待所有时间点准备完成后按说明书操作提取蛋白,制备10%分离胶+4%积层胶,待电泳转膜后,加入一抗孵育过夜,次日孵育二抗,再曝光显影,曝光条带使用Image J软件分析。
1.8 统计学分析采用Prism 6.0软件进行统计学分析,不同组间数据分析采用Student-test或One-way ANOVA,以P<0.05为差异有统计学意义。
2 结果
2.1 大鼠MCAO模型建立后脑组织中c-Met的表达Western blot结果显示,大鼠MCAO模型建立后脑组织中c-Met表达逐渐增多,并在24 h达峰值,与Sham组相比,差异有统计学意义(P<0.05,图1)。
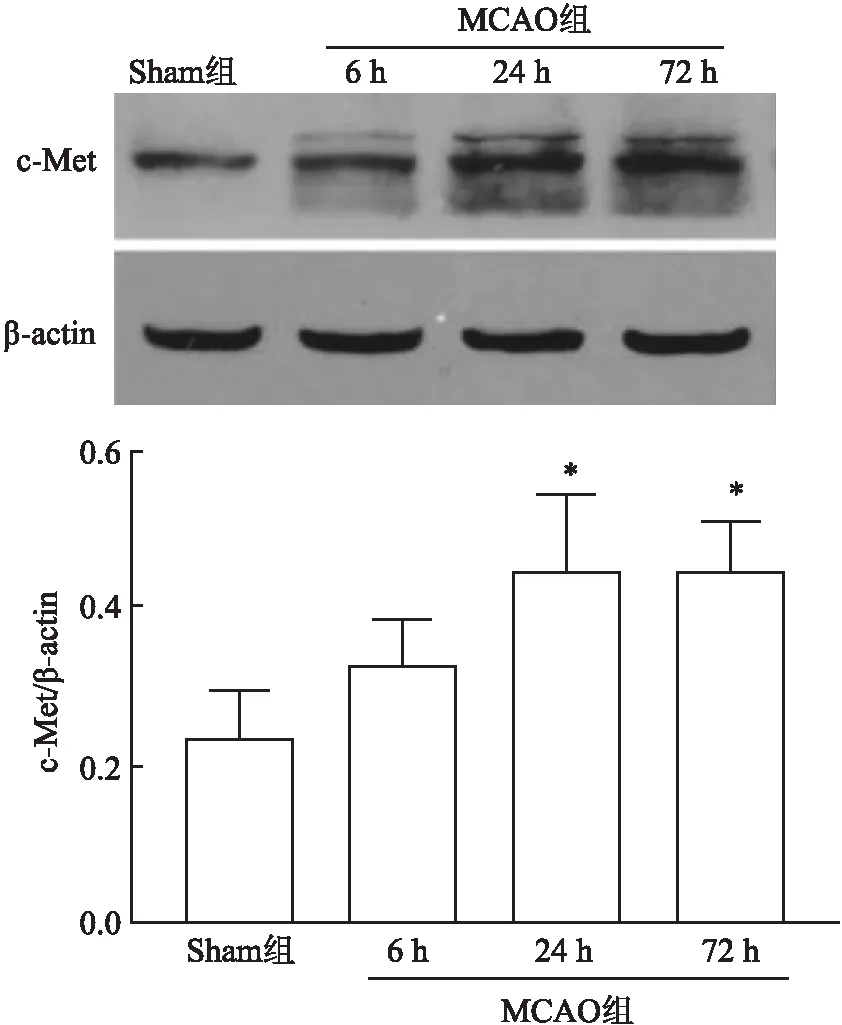
图1 MCAO模型建立后脑组织中c-Met的表达:与Sham组比较,*P<0.05
2.2 大鼠MCAO模型建立后24 h脑组织神经元中c-Met的表达免疫荧光双标显示,c-Met在大鼠脑组织神经元中表达,且MCAO组的表达明显多于Sham组(图2)。
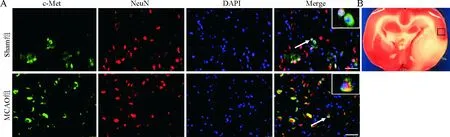
图2 A.c-Met与神经元标志物(NeuN)定位:绿色为c-Met,红色为NeuN,蓝色为DAPI;B.从缺血半暗带区域选取的图片
2.3 HGF给药对大鼠行为学评分和梗塞面积的影响HGF给药组Garcia和平衡木评分较Sham组和MCAO组有明显改善,差异有显著性(P<0.05),同时TTC染色显示HGF组梗塞面积小于MCAO组,差异有显著性(P<0.05,图3)。

图3 大鼠在MCAO模型后的行为学评分和TTC染色:A、B.分别是Modified Garcia和平衡评分;C、D.分别是大鼠脑组织TTC染色和梗塞面积统计;与Sham组比较,*P<0.05,与MCAO组比较,#P<0.05
2.4 HGF给药对神经元凋亡的影响TUNEL染色示,HGF给药组TUNEL阳性细胞明显少于MCAO组,差异有显著性(P<0.05),取材点为梗塞区附近的半暗带(图4)。

图4 HGF给药对神经元凋亡的影响:A.TUNEL与神经元免疫荧光染色,红色为TUNEL,绿色为神经元,蓝色为DAPI核;B.三组TUNEL阳性神经元的百分比,与Sham组相比,*P<0.05;与MCAO组相比,#P<0.05;C.从缺血半暗带区选取的图片
3 讨论
本实验发现,大鼠脑梗塞后给予HGF治疗能明显减轻梗塞面积及提高大鼠行为学评分,而且能使TUNEL阳性的凋亡细胞减少。首先实验通过大鼠MCAO模型建立后不同时间点确定HGF的受体c-Met在24 h达峰值。其次实验用免疫荧光法证明c-Met在大鼠脑组织神经元中表达。实验再次证明HGF给药后大鼠的梗塞面积减少且行为学评分升高,可能是通过抗凋亡减轻TUNEL阳性细胞产生作用。
目前卒中是全球第二大主要致死疾病,仅次于缺血性心脏疾病。据WHO统计,每年约有1 500万人发生卒中[11]。缺血性卒中很大比例是由动脉粥样硬化所致,随着知识的普及,人们逐渐认识到高血压、糖尿病、吸烟等均与缺血性卒中的发生密切相关[12]。目前对于缺血性卒中,全国各大医院成立了卒中中心,争取在发病6 h以内进行干预治疗,挽救缺血坏死脑组织,然而对于中国这样发展中国家,各个地域发展不均衡,尤其是偏远地区患者很难及时送诊,因此积极探讨药物对卒中影响的研究有着至关重要的作用。
HGF是一种能调节血管再生、神经再生、组织重建的细胞因子,同时也发现HGF能通过AKT调节抗凋亡信号[13]。c-Met是一种络氨酸激酶受体,其主要表达于上皮细胞、内皮细胞、肝细胞以及神经元[14],HGF是c-Met的特异性配体,并且与c-Met结合后能导致一系列生物反应,如增殖、迁移、血管再生等。Nakamura等[15]在对心脏的研究发现,缺血发生后使用HGF的特殊抗体使内源性HGF失效,则导致心肌细胞死亡明显升高,梗塞面积扩大,从而证明HGF对缺血心脏有明显保护作用。蒋晨雪等[16]在肿瘤的研究中发现HGF/c-Met通路可通过PI3K/Akt促进肿瘤血管生成,抑制肿瘤细胞凋亡以及促进肿瘤细胞转移。然而HGF与c-Met结合在脑细胞产生作用的机制尚未明确。因此本实验从大鼠MCAO模型建立后脑组织神经元中c-Met的表达,证明HGF/c-Met信号存在于神经细胞中,并可能产生一系列的作用。
凋亡是缺血性脑卒中后常见的病理现象,脑组织的缺氧损伤诱发细胞凋亡,凋亡发生能直接影响缺血半暗带区脑组织的存活,是脑梗进一步加重的机制之一[17]。在心肌梗塞和肿瘤的研究中均发现HGF/c-Met信号通路存在抗凋亡功能,本实验重点探究缺血性脑卒中后调节凋亡细胞能否改善半暗带区脑组织的功能。Hong等[18]的研究证实内源性HGF通过血液再通进入脑组织产生抗凋亡功能。本实验结果显示c-Met在大鼠MCAO模型建立后表达升高,且在24 h达峰值,3天时表达仍偏高,说明大鼠在脑梗塞发生后脑组织可能出现自我保护机制,促进c-Met受体增多,在此时给予外源性HGF使之与c-Met结合,产生级联生物学反应,调控凋亡细胞挽救缺血半暗带区的脑组织,从而减轻大鼠脑组织梗塞面积,并改善大鼠的行为学评分。
卒中发生后脑组织会出现一系列的病理反应过程,如氧化应激、炎症、凋亡、血脑屏障的破坏及自噬的发生等,本文仅从凋亡角度探讨HGF对脑组织缺血性卒中发生的作用,存在局限性,后续实验可以进一步探究HGF对其他作用的影响。综上所述,HGF可以减轻大鼠脑梗塞后的凋亡,也许能成为研究治疗梗塞的机制之一。

