利用肝脏剪切波速度评估肝豆状核变性患者合并脾亢的可行性
王 瑞,王金萍,韩 辉,李 燕,王佳佳
肝豆状核变性 ( hepatolenticular degeneration, HLD)是一种罕见的常染色体隐性遗传性铜代谢障碍,以肝脏和神经系统疾病为特征,在我国发病率高于欧美国家。多数患者在儿童时期即发病,且具有发病隐匿、临床表现形式多样、病程进展快的特点,如不及时治疗后果严重。肝脏是最早也是最易铜沉积的脏器,随着病程的进展,肝脏的代偿能力不能维持时,会出现肝细胞的变性坏死,导致肝纤维化、肝硬化,继发门静脉高压引起脾功能亢进。对于HLD合并脾亢的患者,临床医师选择驱铜治疗时会有所顾虑,且当病情严重时不得不采取手术切除脾脏来延缓病情发展恶化。既往的超声研究多集中在弹性成像技术评估肝豆状核变性患者肝纤维化程度等方面,对肝脾相关性的研究少见。本研究旨在探索利用肝脏剪切波速度(shear wave velocity,SWV)能否评估脾功能亢进,为临床调整治疗方案提供依据。
1 资料与方法
1.1 一般资料 选取2018-10至2020-07在我院接受超声检查的42例肝豆状核变性患者,其中男31例,女11例,年龄8~50岁,平均(28.02±11.02)岁。所有患者均依据指南临床明确诊断为肝豆状核变性。
1.2 诊断标准 肝豆状核变性:(1)精神和(或)神经症状;(2)不明原因的肝损害;(3)24 h尿铜增高和(或)血清铜蓝蛋白减低;(4)角膜色素环(K-F环)阳性;(5)2条染色体均携带ATP7B基因突变。符合(1或2)+(3和4)或(1或2)+5时可诊断。
脾功能亢进:(1)存在脾脏肿大;(2)白细胞、红细胞、血小板可单独或同时减少;(3)骨髓呈造血细胞增生象;(4)脾切除后可使血细胞接近正常;(5)放射性核素扫描发现脾区Cr量大于肝脏2~3倍。诊断以前三项最重要,需结合临床综合分析。
1.3 方法 采用Siemens OXANA 3、S2000型彩色多普勒超声诊断仪,配备声脉冲辐射力成像(acoustic radiation force impulse imaging, ARFI)软件,选用凸阵探头(频率2.5~6.0 MHz)。空腹状态下先行常规二维腹部超声检查,观察肝脏及脾脏大小、形态、内部回声及血流等情况,并记录相关数据。嘱患者左侧卧位,右上肢抬至头部,将ARFI感兴趣区置于肝右叶包膜下2~3 cm,最深不超过6 cm,避开肝内大血管、胆管等非目标结构,嘱患者屏住呼吸3~5 s,待图像稳定后测量肝右叶SWV值并记录。所有HLD患者均于空腹状态下采集静脉血。采用希森美康系列全自动血液分析仪检测血常规指标:白细胞(WBC)、红细胞(RBC)及血小板(PLT)。
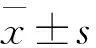
2 结 果
2.1 基本情况 纳入研究的42例肝豆状核变性患者,按照脾脏是否亢进分为A组(HLD不合并脾亢)32例和B组(HLD合并脾亢)10例。A组中男24例,女8例,年龄8~50岁,平均(27.63±11.05)岁;B组中男7例,女3例,年龄11~44岁,平均(29.30±11.43)岁。两组性别、年龄比较,差异无统计学意义,具有可比性(>0.05,表1)。
2.2 单因素分析 B组WBC、RBC、PLT均低于A组,差异有统计学意义;B组SWV高于A组,差异有统计学意义(<0.05,表1、图1)。

表1 两组肝豆状核变性患者单因素资料比较
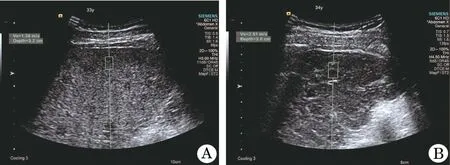
图1 肝豆状核变性患者SWV值
2.3 相关性分析 将肝脏SWV值与WBC、RBC、PLT进行相关性分析, SWV与WBC、PLT呈显著负相关,与 RBC呈弱负相关(表2)。

表2 两组肝豆状核变性患者肝脏SWV值与WBC、RBC、PLT的相关性分析
2.4 ROC曲线 绘制评估脾亢SWV的ROC曲线,曲线下面积:0.850,95%:0.702~0.998,最佳截断值为2.0,敏感度及特异度分别为90%、84.4%(图2)。

图2 SWV评估脾亢的ROC曲线
3 讨 论
HLD是一种常染色体隐性遗传性铜代谢障碍疾病,其致病机制在于ATP7B突变导致铜蓝蛋白合成障碍以及铜在胆汁中的排泄障碍,使得过量的铜沉积于脏器。铜的沉积首发于肝脏,随着铜在肝脏内的沉积超出肝脏的代偿能力,便会出现肝细胞的变性坏死,进而向肝纤维化、肝硬化演变。HLD患者随着肝脏病理损伤的加重,继发门静脉高压,致使脾静脉回流受阻,脾脏病理性淤血直至诱发脾功能亢进。对于合并脾亢的患者是否需要接受临床治疗一直都存在争议。Boyer等认为,大部分脾亢仅是实验室指标异常,不需要特殊的干预且解决脾亢是否会对患者预后产生影响目前并不确定。Kurokawa等则认为,脾亢可能会促进肝纤维化向肝硬化演变,加剧病情的进展,所以针对脾亢的治疗对肝硬化病情的缓解至关重要。值得注意的是,HLD不同于其他类型的肝脏疾病,患者需要终身驱铜治疗,但部分驱铜药物会降低血细胞水平,所以一旦HLD患者合并脾亢,临床医师不得不限制驱铜药物的应用甚至停药以避免血细胞进一步减低。但也有HLD合并脾亢的患者,药物治疗无效,不得不采取脾脏切除术。文献[8]对232例脾切除术后的患者进行追踪发现术后并发症的发生率高达36.2%。徐余兴等发现门静脉血栓是肝豆状核变性脾切除术最严重并发症,严重影响患者的预后。所以,如果能在脾亢出现前即进行临床干预调整治疗方案,对控制病情的进展至关重要。
脾功能亢进没有单一指标可以进行诊断,临床一般认为脾脏的肿大结合血细胞减少可作为脾亢的主要诊断依据。目前,对于脾脏大小的评估主要依靠超声检查,但患者的体型、体位、腹部气体及操作者经验等均会对测量产生一定的偏差。实验室的指标虽然敏感,可一旦出现明显下降,往往提示脾功能亢进进入较为严重的阶段。此外,国外相关研究也提出脾功能亢进的严重程度与脾脏是否增大并不呈正相关,脾大的患者可能不存在脾亢,而脾脏大小正常的患者亦有可能存在脾亢。所以,临床需要一种新的检查方法来帮助评估HLD患者是否存在脾功能亢进以便及时调整治疗方案。
3.1 肝脏SWV值与肝脏损伤 既往研究显示,超声弹性成像技术ARFI可以帮助评估肝脏的受损程度,该技术主要通过测量肝脏剪切波速度SWV值来反映肝组织的硬度,肝脏损伤越严重,组织质地越硬,SWV值越高,反之亦然。陈敏等对373例慢性肝炎患者进行研究认为肝脏SWV值与肝纤维化分期存在显著的正相关。王晓静等对肝豆状核变性患者肝脏硬度进行测量,认为SWV值可以反映HLD肝脏病理变化过程。
3.2 肝脏损伤与脾功能亢进 HLD患者诱发脾亢的发病机制在于铜过量沉积造成肝组织损伤,继发门静脉高压,脾静脉回流受阻,脾脏被动性充血,长期以往除脾脏储血过多外,网状内皮系统增生使得血细胞破坏增多,形成脾亢,可见肝脏的损伤是导致脾亢的直接原因,二者的因果关系正是本研究的病理基础。本研究结果显示,HLD合并脾亢患者的肝脏SWV值明显高于不合并脾亢者,这说明随着脾脏功能亢进的出现使HLD患者肝脏硬度增加,这也与文献[15]认为肝脾存在相关性,脾脏的增大会加重肝脏损伤及硬度的结果相符。
3.3 肝脏SWV值与脾功能亢进 为了进一步验证肝脏SWV值与脾功能亢进的相关性,本研究选用临床最常用于评估脾功能亢进的实验室指标进行相关性分析,即白细胞、红细胞、血小板。这三个指标可直接反映了脾功能亢进对血细胞的破坏作用:脾功能亢进时脾的阻留及破坏能力增加,致使血细胞减少,由于正常脾脏无储存红细胞功能,所以早期白细胞和血小板减低明显,中晚期全血细胞减低。本研究单因素分析也证实这三个指标与脾功能亢进相关,与既往研究结果一致。本研究将肝脏SWV值与这三个指标进行相关性分析,结果显示SWV值与WBC、RBC、PLT均存在相关性,其中与WBC、PLT相关性最为显著,而这两个指标也正是早期脾亢时最敏感的参数,这进一步证实了肝脏SWV值可以评估早期脾功能亢进。最后我们绘制肝脏SWV的ROC曲线检验其评估脾亢的效能,结果显示曲线下面积为0.850,当最佳截断值为2.0时,敏感度及特异度高达90.0%、84.8%。说明以肝脏SWV为2.0 m/s来评估HLD患者是否存在脾亢,具有较高的敏感度及特异度。本研究的不足之处在于并未对脾亢的严重程度进行分组,未来我们会加大样本量研究需要外科手术干预脾功能亢进时的肝脏SWV值。
总之,利用ARFI技术测量肝脏SWV值对评估脾亢具有较高的敏感度和特异度,值得临床推广使用。

