负载在泡沫镍基底上的Fe-Ni-Mo氧化物的超快速制备及其析氧催化性能研究
吴帅炜,高涛涛,唐相民,虞淑敏,刘 荣
(1.成都大学 机械工程学院,四川 成都 610106; 2.成都大学 高等研究院,四川 成都 610106;3.成都大学 基础医学院,四川 成都 610106)
0 引 言
随着经济的快速发展,社会对能源的需求呈不断增长的态势.研究表明,传统化石燃料的大量消耗会导致环境污染并影响社会经济的可持续发展,而通过开发高效且可再生的清洁能源具有极为重要的现实意义[1-2].研究发现,氢气因具有能量效率高、可再生及无碳排放等特点,而被认为是理想的能源和化石燃料的替代品之一[3-6].目前,利用电化学水分解制氢工艺被认为是一种高效、环保及绿色可持续的制氢技术.电化学水解制氢过程中的化学反应包括析氢反应(hydrogen evolution reaction,HER)和析氧反应(oxygen evolution reaction,OER)[7-9].其中,OER是一个复杂的4电子转移过程,通常需要较高的过电势才能驱动OER的发生.对此,科研人员一直致力开发具有高活性的阳极电催化剂以此来提高OER的效率,从而实现整体能量消耗的降低.研究表明,作为催化剂材料之一的贵金属虽表现出较高活性,但其昂贵的价格和稀缺性限制了它的广泛应用;而过渡金属材料,例如Ni、Co、Fe及Mo等,因为具有多价态并且储量丰富、价格低廉,不失为一类极具开发前景的催化材料[10-13].基于此,本研究利用纳米金属界面的微波焦耳热效应和水溶液微波吸收热效应制备了Fe-Ni-Mo/NF复合材料,并将其作为催化电极,分析了其在碱性条件下的OER催化性能,并使用多种物理表征方法对其形貌与组成进行了测试,同时利用三电极体系分析了将其作为催化电极的OER催化活性和稳定性,拟为通过超快速方式构建高活性催化材料提供重要参考依据.
1 实 验
1.1 材料与仪器
1.1.1 材 料
实验所用材料包括:九水合硝酸铁(Fe (NO3)3·9H2O)、六水合硝酸镍(Ni (NO3)2·6H2O)、十二钼磷酸(H3PO4·12MoO3) 、浓盐酸(HCl),氢氧化钾(KOH),以上试剂均为分析纯,购于成都市科隆化学品有限公司;泡沫镍(Nickel Foam,NF),购于昆山广嘉源新材料有限公司;实验所用蒸馏水由本实验室自制.
1.1.2 仪 器
实验所用仪器包括:M1-L213B型微波炉(广东格兰仕微波生活电器制造有限公司),SB-5200DTD型超声波清洗机(宁波新艺超声设备有限公司),BSA124S-CW型电子天平(赛多利斯科学仪器(北京)有限公司),MULTI AUTOLAB-M204型电化学工作站(瑞士万通(中国)有限公司),DX-1000型X射线粉末衍射仪(丹东方圆仪器有限公司),JIB-4700F型扫描电子显微镜(日本电子株式会社),K-Alpha+型X射线光电子能谱仪(上海禹重实业有限公司).
1.2 Fe-Ni-Mo/NF与单金属及双金属试样制备
1)在实验中,首先,用1 mol/L HCl对NF(0.50 cm×3.00 cm×0.16 cm)进行浸泡并超声处理30 min,以去除NF表面的杂质和氧化物,然后用蒸馏水再对其进行多次冲洗,最后将冲洗干净的NF放置于真空干燥箱中60 ℃温度下干燥6 h,处理后得到的NF记作Deal NF;其次,利用电子天平精确称取0.282 8 g 硝酸铁(九水)、0.002 9 g硝酸镍(六水)、0.001 5 g 十二钼磷酸,再取2 mL的蒸馏水与称量好的试剂在4 mL的离心管中进行均匀混合,再超声处理2 min以形成混合的Fe-Ni-Mo前驱液,并将处理好的Deal NF放入混合均匀的前驱体溶液中,使之完全浸没后,一并放入超声清洗机中超声处理30 s;最后,取出处理好的Deal NF,立刻放入微波炉中进行加热处理,在800 W的功率下加热3 min,冷却后取出,最终制得Fe-Ni-Mo/NF复合材料试样.
2)在上述相同的制备条件下,基于单金属和双金属材料,本实验分别制备Mo/NF、Ni/NF、Fe/NF 、Fe-Mo/NF、Fe-Ni/NF和Ni-Mo/NF等复合材料试样作为对照品.
1.3 材料表征
对实验制备的Fe-Ni-Mo/NF和Deal NF试样分别采用扫描电镜(scanning electron microscope, SEM)对其微观形貌进行观察;采用X射线衍射仪(X-ray diffraction,XRD)对其进行物相分析,测试条件为:Cu靶,管电压为40 kV,管电流为30 mA.2θ的取值范围为10 °~ 90 °,步进角度为0.06 °/s,采样时间为1 s;采用X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)对其表面元素的化学价态进行分析,测试条件为,单色化AIKa源(Mono AlKa),电压15 kV,束流15 Ma,分析仪器的扫描模式为CAE,仪器功函数为4.2.
1.4 电化学性能测试
在室温下,本研究采用标准的三电极体系利用电化学工作站将实验制备的试样作为电极进行电化学性能测试.在该体系中,制备的试样作为工作电极,汞/氧化汞(Hg/HgO)电极作为参比电极,石墨电极作为对电极,电解液浓度为1 mol/L的KOH溶液.
在电化学性能测试中,分别测试了Deal NF、Fe-Ni-Mo/NF、Fe-Mo/NF、Fe-Ni/NF、Fe/NF、Ni-Mo/NF、Mo/NF和Ni/NF等试样的过电位(η),并采用线性扫描伏安法(linear sweep voltammetry,LSV )、循环伏安法(cyclic voltammetry,CV)和电化学阻抗谱(electrochemical impedance spectroscopy,EIS)等技术手段对作为电极材料试样的催化活性进行了测试.
在试样的LSV测试时,电压范围为0 ~ 0.8 V,扫描速度为0.1 V/s.所有测量的电位值均基于可逆氢(reversible hydrogen electrode,RHE )电极进行转换[14],其公式为,
ERHE=EHg/HgO+0.059 1×pH+0.098V
(1)
η=Ei-Et
(2)
式中,0.098 V为Hg/HgO电极在室温下的标准电极电势,Ei为实际电压值,Et为理论电压值,Et为1.23 V vs.RHE.
同时,在1 mol/L的KOH溶液中对Deal NF、Fe-Ni-Mo/NF、Fe-Mo/NF、Fe-Ni/NF、Fe/NF、Ni-Mo/NF、Mo/NF和Ni/NF等试样作为电极材料进行了CV和EIS测试,以此计算不同电极的双电层电容和电化学阻抗.CV测试电压范围为0~0.1 V,扫速为 0.02~0.01 V/s,EIS测试电压为0.65 V,频率为0.01 Hz~105Hz.此外,为了分析作为电极材料试样的电化学稳定性能,还对其进行了1 000圈的LSV测试.
2 结果与讨论
2.1 XRD分析
实验制备的Fe-Ni-Mo/NF与Deal NF试样的XRD图谱如图1所示.
由图1可知,Deal NF图谱中,在2θ=44.8 °、52.2 °、76.6 °出现了3个明显的特征衍射峰(JCPDF card No.04-0850),分别归属于镍的(111)、 (200)及 (220)晶面;Fe-Ni-Mo/NF图谱中,除了出现归属于镍的3个特征峰外,没有发现可归属于复合氧化物的特征峰.此表明,生长在NF表面的复合氧化物结晶度较低,其微弱的衍射峰被结晶度较高的镍基底的衍射峰所掩盖.

图1 Fe-Ni-Mo/NF和Deal NF的XRD图谱
2.2 微观形貌分析
实验制备的Fe-Ni-Mo/NF与Deal NF试样的低倍和高倍SEM图像如图2所示.

图2 Fe-Ni-Mo/NF和Deal NF试样的SEM图像
由图2可知,实验制备的Fe-Ni-Mo/NF试样呈相互交织的珊瑚状附着在Deal NF表面(见图2(a)、(b)、(c)和(d))且具有较高的粗糙度,结合图2(e)、(f)来看,制备的试样的这种结构有利于其电化学活性面积的提升和催化活性的改善.
2.3 化学价态分析
实验制备的Fe-Ni-Mo/NF试样的Fe、Ni、Mo和O的XPS谱图如图3所示.
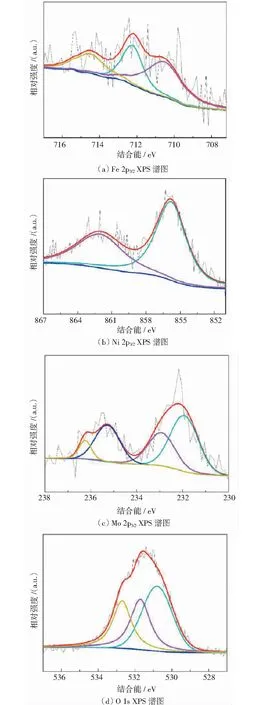
图3 Fe-Ni-Mo/NF试样的XPS谱图
图3中,图3(a)为Fe 2p3/2的XPS谱图,位于712.35 eV、714.55 eV和710.35 eV的XPS峰表明Fe3+的存在;图3(b)为Ni 2p3/2的XPS谱图,位于855.8 eV的XPS 峰可以归属Ni2+,另一个峰是对应的卫星峰;图3(c)为Mo 3d的XPS谱图,位于231.92 eV和235.27 eV的峰归属于Mo5+,位于232.92 eV和236.24 eV可归属于Mo6+;图3(d)为O 1s的XPS谱图,位于531.71 eV和532.70 eV的峰可归属于-OH和吸附水的存在,位于530.80 eV的特征峰归属于金属氧化物.实验证实了Fe-Ni-Mo复合氧化物的形成.
2.4 电化学性能分析
2.4.1 析氧性能分析
实验制备的试样的析氧性能如图4所示.

图4 试样的LSV曲线
从图4中可以看到,Deal NF的极化电流密度较小,此表明,Deal NF催化活性较低;Fe-Ni-Mo/NF相对于单金属和双金属试样作为催化电极表现出了最高的极化电流密度,此表明,Fe-Ni-Mo/NF具有最优的析氧催化活性.同时,与单金属和双金属试样相比,Fe-Ni-Mo/NF的催化电极活性最优,充分体现了Fe-Ni-Mo 3种金属复合获得的协同效应对提升电极的催化活性具有重要作用.实验显示,Fe-Ni-Mo/NF作为催化电极仅需要258 mV的过电位就可以达到100 mA/cm2的电流密度.
2.4.2 ECSA分析
由于双电层电容与电化学活性面积呈正相关,高的双电层电容意味着高的电化学活性面积.对此,本研究基于不同扫描速度下的循环伏安曲线获得了制备的试样作为电极材料的双电层电容数据,结果图5所示.
在图5中,图5(a)显示,实验制备的试样作为电极的双电层电容分别为Deal NF (1 030 μF/cm2)、Fe-Ni-Mo/NF (884.93 μF/cm2)、Fe-Mo/NF(822.27 μF/cm2)、Fe-Ni/NF(856.26 μF/cm2)、Fe/NF(588.82 μF/cm2)、Ni-Mo/NF(889.14 μF/cm2)、Mo/NF(1 180 μF/cm2)和Ni/NF(799.47 μF/cm2).据此可知,Fe-Ni-Mo/NF相比于单金属与双金属材料具有更高的电化学活性面积,这有利于催化活性的提升.此外,为了进一步衡量催化电极的本征活性,本研究将LSV曲线归一化于双电层电容,结果如图5(b)所示.其中,Fe-Ni-Mo/NF作为催化电极仍具有最高的电流密度,故其具有最高的本征活性,这主要源于Fe-Ni-Mo 3种金属间的协同效应.
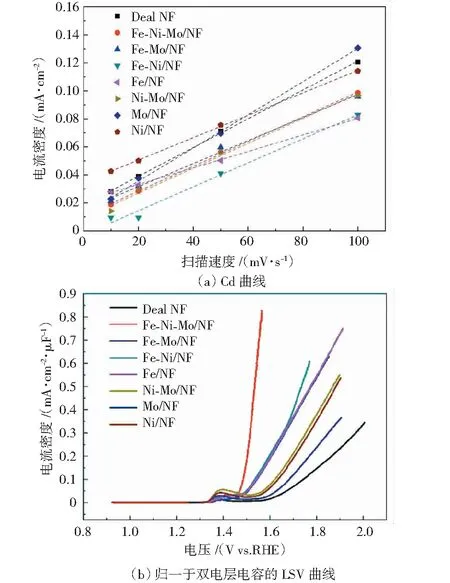
图5 试样的双电层电流密度图
2.4.3 Tafel斜率分析
实验制备的试样的Tafel斜率测试结果如图6所示.
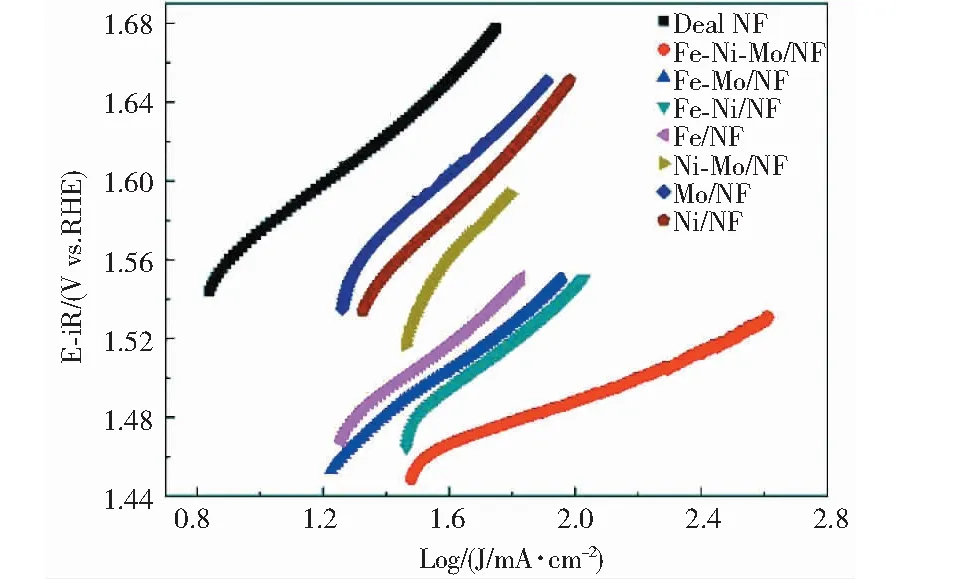
图6 试样的Tafel斜率曲线
图6中,Deal NF、Fe-Ni-Mo/NF、Fe-Mo/NF、Fe-Ni/NF、Fe、Ni-Mo/NF、Mo/NF和Ni的Tafel斜率分别为134 mV/dec、63 mV/dec、124 mV/dec、132 mV/dec、131 mV/dec、212 mV/dec、157 mV/dec和166 mV/dec.其中,Fe-Ni-Mo/NF展现出了最小的Tafel斜率,并且远小于其他单金属以及双金属.事实上,较小的Tafel斜率说明在催化反应过程中增加相同的过电势可以获得更大程度的极化电流密度的增加,此对于实际电解水过程十分有利,特别是在采用大电流密度电解水分解制氢过程时.
2.4.4 电化学阻抗分析
实验制备的试样的电化学交流阻抗图和基于等效电路图(内插图)的拟合图谱如图7所示.

图7 试样的电化学交流阻抗图谱(内插图为等效电路图)
由图7可知,Fe-Ni-Mo/NF表现出最小的电阻.此表明,Fe-Ni-Mo/NF作为催化电极在催化反应过程中具有最高的电子转移效率.
2.4.5 催化稳定性分析
研究证实,优异的催化电极除了具有高效的催化活性,还应具备良好的稳定性[14].为了分析作为催化电极的试样稳定性,在实验中对Fe-Ni-Mo/NF进行了多次LSV扫描,其结果如图8所示.
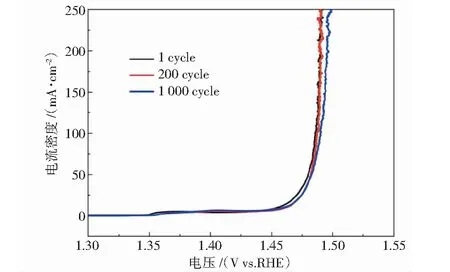
图8 Fe-Ni-Mo/NF稳定性测试曲线
由图8可知,即使1 000圈后,Fe-Ni-Mo/NF作为催化电极的极化电流并没有出现明显降低,这充分展现出该复合材料所具有的优异析氧催化稳定性.这主要是在实验中多金属复合氧化物是通过快速微波加热的工艺使其原位生长在Deal NF基底上,避免了黏结剂的使用和氧化物颗粒在反应过程中的团聚,并据此获得了优异的催化稳定性.
3 结 论
本研究通过快速、便捷和低成本的微波加热法工艺成功制备了在Deal NF基底上原位生长的Fe-Ni-Mo/NF金属复合氧化物纳米颗粒.同时,通过XRD、SEM和XPS等技术方法对制备的试样的结晶度、微观形貌、元素组成、催化性能以及电化学性能进行了分析测试.结果表明,Fe-Ni-Mo/NF 具有极高的析氧催化活性,其达到100 mA/cm2电流密度所需的过电位仅为258 mV,远低于贵金属材料.同时,Fe-Ni-Mo/NF还具有最小的Tafel斜率(63 mV/dec).此外,更为重要的是将其作为电极材料表现出了极优异的催化稳定性.本制备方法工艺简单、快速,且成本较低,此对下一步实现低成本制备其他多金属复合催化电极材料具有实际的参考价值.

