1例信迪利单抗注射液导致严重皮肤免疫毒性的病例及文献回顾分析
田雪梅,卢立山,李俊义,史存发,罗昆,刘敏,殷波
鄂尔多斯市中心医院药剂科,鄂尔多斯 017020
信迪利单抗注射液是一种免疫检查点抑制剂(immune checkpoint inhibitors,ICIs),于2018年底获批上市。信迪利单抗对T细胞表面的程序性死亡蛋白1(programmed cell death 1,PD-1)分子具有较强的亲和力,通过阻断体内PD-1与程序性死亡分子配体1(programmed cell death ligand 1,PD-L1)的结合,阻断肿瘤免疫耐受的 PD-1/PDL1 信号,重新激活淋巴细胞,使免疫系统进入激活的抗肿瘤状态,从而达到治疗肿瘤的目的[1-2]。与一些引起皮疹的靶向药物类似,免疫相关的皮肤毒性和药物的疗效也存在一定相关性。一项帕博利珠单抗治疗肺癌、黑色素瘤和前列腺癌的研究发现[3],出现皮肤毒性的患者无进展生存期优于未出现皮肤毒性的患者,提示发生皮疹可以作为免疫治疗临床预后的良好指标。
1 病历资料
患者1例,男性,53岁,主因“直肠癌2年多,化疗5周期,免疫治疗联合靶向治疗11周期”入院。患者于2019年12月无明显诱因出现腹痛,以上腹部和下腹部为主,就诊于本院,腹部计算机断层扫描术(computer tomography,CT)示:腹膜及网膜多发病变、右侧心隔角区淋巴结增大,考虑转移。随后患者就诊于北京大学肿瘤医院,正电子发射断层扫描(positron emission tomography,PET)/CT示:腹膜及网膜弥漫增厚、腹盆腔积液伴高代谢,符合恶性表现,考虑为原发性,膈区多淋巴结,疑为转移。静脉滴注注射用紫杉醇[白蛋白结合型,齐鲁制药(海南)有限公司,国药准字H20193309,规格100mg]200mg,qd+口服卡培他滨片(上海罗氏制药有限公司,国药准字H20073024,规格0.5g)1.5g,bid+静脉滴注贝伐珠单抗注射液[罗氏制药(瑞士)有限公司,国药准字SJ20170035,规格100mg(4ml)/瓶]350mg,qd,化疗3周期。2020年4月21日于西安大兴医院就诊,行全麻下腹腔镜探查+腹腔转移瘤切除术+大网膜切除术+肠黏连松解术,术后给予静脉滴注信迪利单抗注射液[信达生物制药(苏州)有限公司,国药准字S20180016,规格100mg(10ml)/瓶]200mg,qd+静脉滴注贝伐珠单抗注射液350mg,qd治疗11周期。2022年3月11日患者颈部出现大面积红疹,考虑药疹,给予口服醋酸泼尼松片(天津力生制药股份有限公司,国药准字H12020123,规格5mg)20mg,qd,对症治疗后好转,继续给予信迪利单抗注射液200mg+贝伐珠单抗注射液350mg治疗。2022年4月19日患者右肩部、右前臂出现密集水疱,伴有皮肤破溃渗血,局部瘙痒(见图1)。患者使用信迪利单抗注射液免疫治疗导致严重的皮肤不良反应为3度,静脉滴注给予注射用甲泼尼龙琥珀酸钠(PFIZER SA,国药准字HJ20170197,规格40mg)40mg,q12h,牛痘疫苗接种家兔炎症皮肤提取物注射液(Nippon Zok: pharmaceutical Co., Ltd., 注 册 证号S20140085,规格3.6 Neurotropin单位/3ml/支)7.2U,qd,维生素C注射液(天方药业有限公司,国药准字H41020284,规格2ml∶0.25g)0.25g,q12h,口服盐酸西替利嗪片(UCB-Pharma AG,H20171304,规格10mg)10mg,qn,皮肤破溃处每日清创换药。4月25日,颈部皮肤无渗血,颜色较前加深,结痂(见图2),无瘙痒症状,次日停用注射用甲泼尼龙琥珀酸钠,给予口服醋酸泼尼松片25mg,qd。经过2周的治疗,静脉滴注注射用甲泼尼龙琥珀酸钠40mg,q12h由静脉滴注转为口服,逐渐减量,患者皮肤好转(见图3)。考虑患者使用信迪利单抗注射液后出现严重的皮肤免疫相关不良反应(immune-related adverse,irAE),停用免疫治疗,更换化疗方案:静脉滴注贝伐珠单抗注射液350mg,qd+静脉滴注盐酸伊立替康注射液[Pfizer Australia Pty Ltd,国药准字HJ20160576,规格 2ml∶40mg(按 C33H38N4O6·HCl·3H2O 计)]300mg,qd+静脉滴注注射用雷替曲塞(南京正大天晴制药有限公司,国药准字H20090325,规格2mg)3mg,qd后多次随访,患者皮肤恢复良好,残留褐色斑点(见图4和图5)。
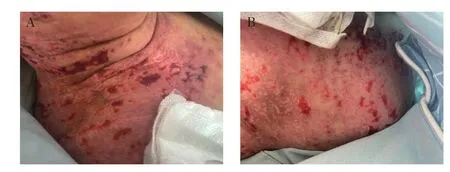
图1 入院时(2022-04-19)皮疹情况
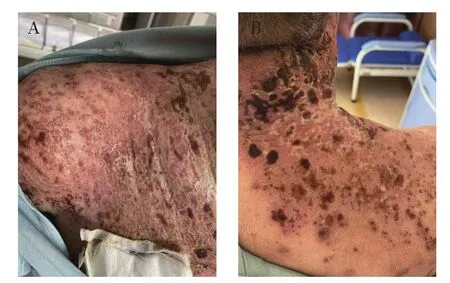
图2 治疗6天后(2022-04-25)皮疹情况
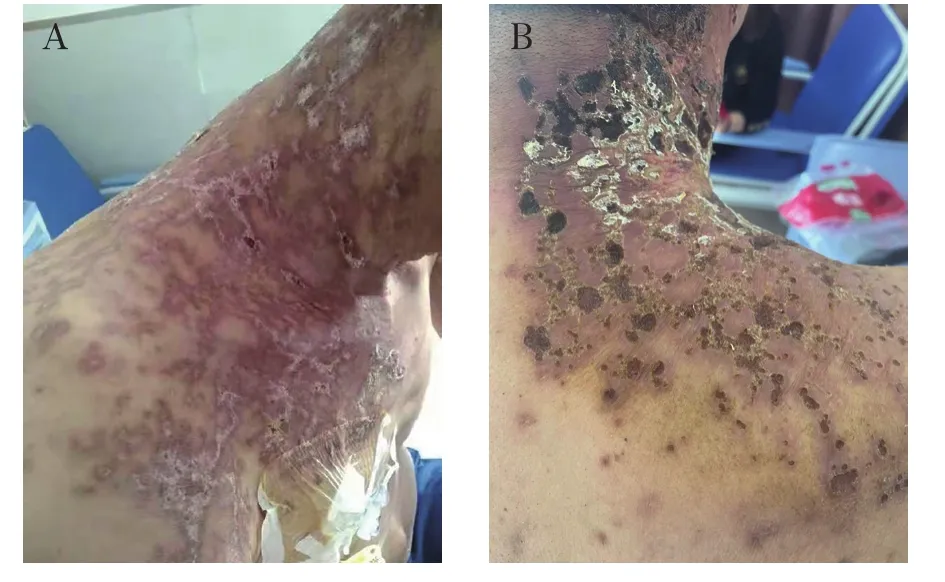
图3 治疗2周后(2022-05-04)皮疹情况
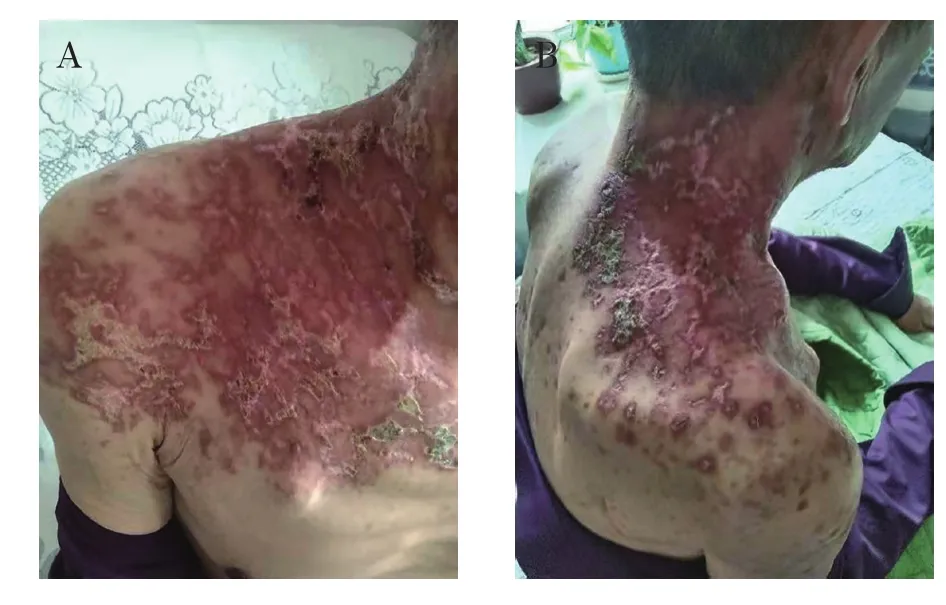
图4 出院2周后随访皮疹情况
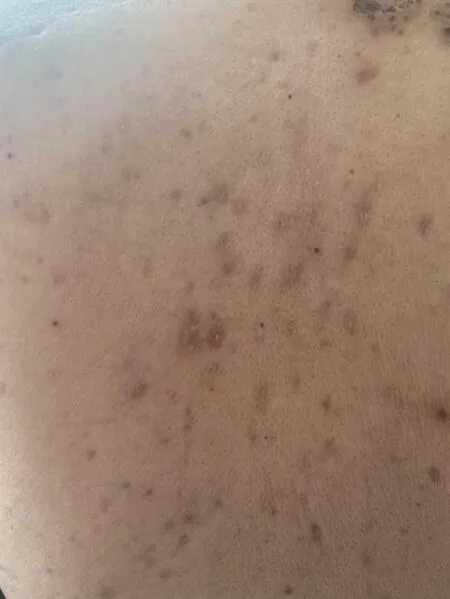
图5 出院1个月后随访皮肤情况
2 用药分析
信迪利单抗注射液属于PD-1抑制剂,2018年底在我国获批用于治疗复发性以及难治性霍奇金淋巴瘤,目前其被广泛用于治疗多种实体瘤,包括非小细胞肺癌(non-small cell lung cancer,NSCLC)以及食管癌等[1-2]。ICIs在进展性肿瘤中被广泛使用,PD-1(也被称为CD279)是最主要的ICIs之一,主要表达于T细胞、B细胞、活化的单核粒细胞、树突细胞(dendritic cell,DC)以及自然杀伤细胞(natural killer cell,NK)。PD-1的配体PD-L1(B7-H1、CD274),主要表达于抗原提呈细胞[4]、巨噬细胞、非造血细胞以及实体器官(如心脏、肺、胎盘、肝脏)。ICIs能够增加抗肿瘤效应,但同时也增加了免疫损伤的发生风险[4-5]。相关研究表明[4-8],ICIs导致的irAE覆盖全身各个系统器官疾病,包括皮肤疾病(46%~62%)、胃肠道疾病(22%~48%)、自身免疫系统疾病(7%~33%)、内分泌系统疾病(12%~34%)、呼吸系统疾病(3%~8%)以及泌尿道系统疾病(1%~7%)。PD-1/PD-L1抑制剂皮肤irAE较为常见,多数较轻,严重的不良反应较为罕见,包括皮肤炎症(斑丘疹、苔藓样、湿疹)、免疫大疱性疾病、白癜风、斑秃、罕见的严重的皮肤药物反应[如重症多形红斑型药疹(Stevens-Johnson syndrome, SJS) 和中毒性表皮坏死松解症 (toxic epidermal necrolysis, TEN)]、嗜酸性粒细胞增多和系统症状的药疹(drug reaction with eosinophilia and systemic symptoms,DRESS)等[9]。
临床药师以ICIs、PD-1/PD-L1、信迪利单抗、免疫相关不良反应等为关键词,从中文数据库(中国知网、万方数据库、维普数据库)和英文数据库(PubMed、UpToDate)检索,共收集2019~2022年期间相关文献47篇,排除非皮肤不良反应、非信迪利单抗导致的药品不良反应,共剩余文献8篇,汇总免疫检查点导致皮肤irAE的特点[10-17]。见表 1。
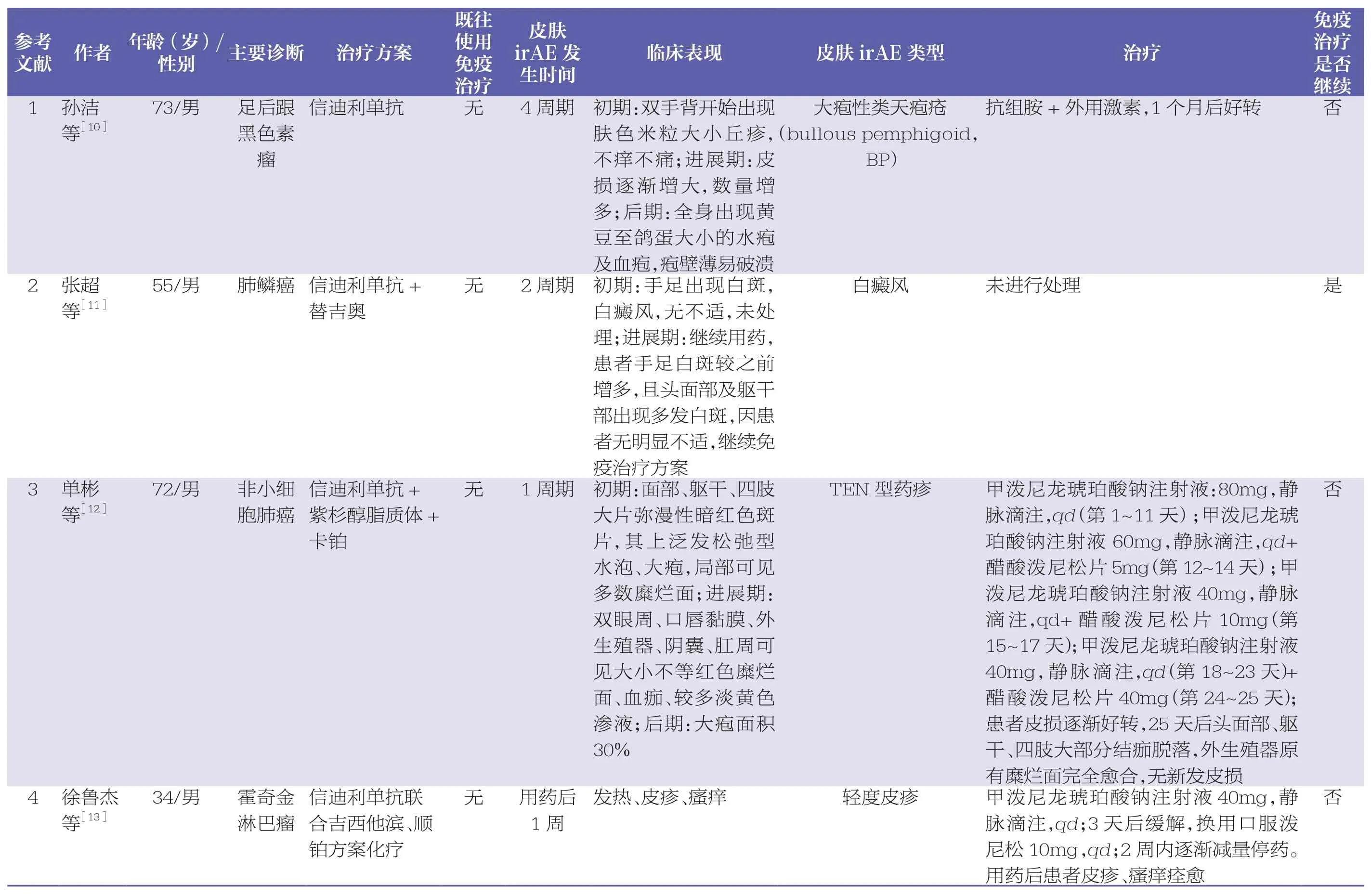
表1 信迪利单抗导致的皮肤irAE的个案报道
3 病例分析
本例患者因直肠癌给予信迪利单抗注射液免疫治疗联合贝伐珠单抗。前11周期治疗顺利未出现皮肤irAE;11周期后出现红疹,未重视,仅对症处理;病情好转,继续使用后,皮肤出现大面积破溃渗出,较前显著加重。患者出现皮肤损伤的时间及特征与药物使用存在明确的时间相关性,临床症状与皮肤irAE相符。同时,由于信迪利单抗注射液皮肤不良反应远高于贝伐珠单抗,临床药师查阅药物相关说明书及文献,信迪利单抗注射液皮肤irAE的发生十分常见,1级发生率为5.5%、2级为2.3%,3级为0.9%,而贝伐珠单抗皮肤与皮下组织类相关的药品不良反应主要有手足综合征,未提及皮疹、斑丘疹等严重皮肤不良反应。患者期间未使用其他药物,根据《不良反应关联性判断Naranjo评分法》[18]得分与药物因果关系强度,评价患者严重皮肤不良反应相关性,该患者最终得分为7分(总分≥9分,肯定相关;5~8分,很可能;1~4分,可能有关;≤0分,可疑)。因此,综合考虑本患者病例的严重皮肤反应为信迪利单抗注射液导致的药品不良反应。
4 讨论
4.1 皮肤irAE与性别相关性分析
本文献研究收集的案例报告中,主要集中于男性患者(6/8,75%),而本研究病例患者也为男性。这与2022年Zheng等[19]发表的一项真实世界的研究结果相似(男性发生率为83.70%)相符,提示可能与患者本身所患肿瘤类型相关。信迪利单抗注射液目前批准的临床适应症主要有:经典型霍奇金淋巴瘤、非小细胞肺癌(非鳞状非小细胞肺癌、鳞状非小细胞肺癌)、肝细胞癌、食管鳞癌以及胃/胃食管交界处腺癌。可能原因在于这些肿瘤在男性中的发病率高于女性,信迪利单抗用药概率高,导致皮肤irAE发生率高。本研究文献检索的8篇个案报道中,肺癌3例(肺腺癌、非小细胞肺癌、肺鳞癌),均为男性,这与肺癌流行病学相符,即肺癌发病率男性高于女性,且是男性癌症死亡的原因之一,但是目前相关研究表明这种差异已缩小[19-20]。检索的8篇文献中,有1例食管鳞癌(女性)和1例食管胃连接处癌(男性),而目前食管鳞癌流行病学研究结果表明该癌种无性别特异性。其他3例报道患者肿瘤类型为黑色素瘤(男性)、霍奇金淋巴瘤(男性,结节性淋巴细胞为主的霍奇金淋巴瘤流行病学中,表明男性患病率达75%)、宫颈癌(女性)。本研究收集的8个病例中虽然没有肝细胞癌患者,但是查阅肝细胞癌流行病学发现该病多发于男性,男女比例约3∶1[21-23]。通过分析各种肿瘤的男女发病例,可以发现男性皮肤irAE发生率较高。
4.2 皮肤irAE发生时间
皮肤毒性最常表现为斑丘疹和瘙痒。严重的皮肤不良反应包括Stevens-Johnson综合征、中毒性表皮坏死松解症等。需要注意的是,斑丘疹可能是其他皮肤irAE的早期表现。皮肤毒性发生率约为3.5%,其中1级1.5%,2级1.1%,3级0.7%,4级 0.2%。中位发生时间为用药后0.8个月(范围:0.1~16.5个月),好转中位持续时间为1.1个月(范围:0.1~15.1个月)[24-29]。本研究报道的患者用药11周期后出现皮疹,未处理,继续使用后逐渐加重皮肤出现疱疹,破溃渗出,经过治疗,1个月左右逐渐恢复。收集的8个病例中,不良事件均发生在用药4周期内,经过积极治疗仅有1例患者死亡,其他7例患者均恢复。皮肤不良事件是PD-L1/PD-1最常见的irAEs,发生率高达46%~62%[26]。皮肤毒性可以在治疗早期出现(治疗开始后的前几个星期),也有患者在治疗结束后出现皮肤irAE的报道。irAE发生的病理生理学机制目前尚不完全明确,但可能与 PD-1/PD-L1 阻断介导的 T 细胞活化,引起免疫系统过度激活相关。
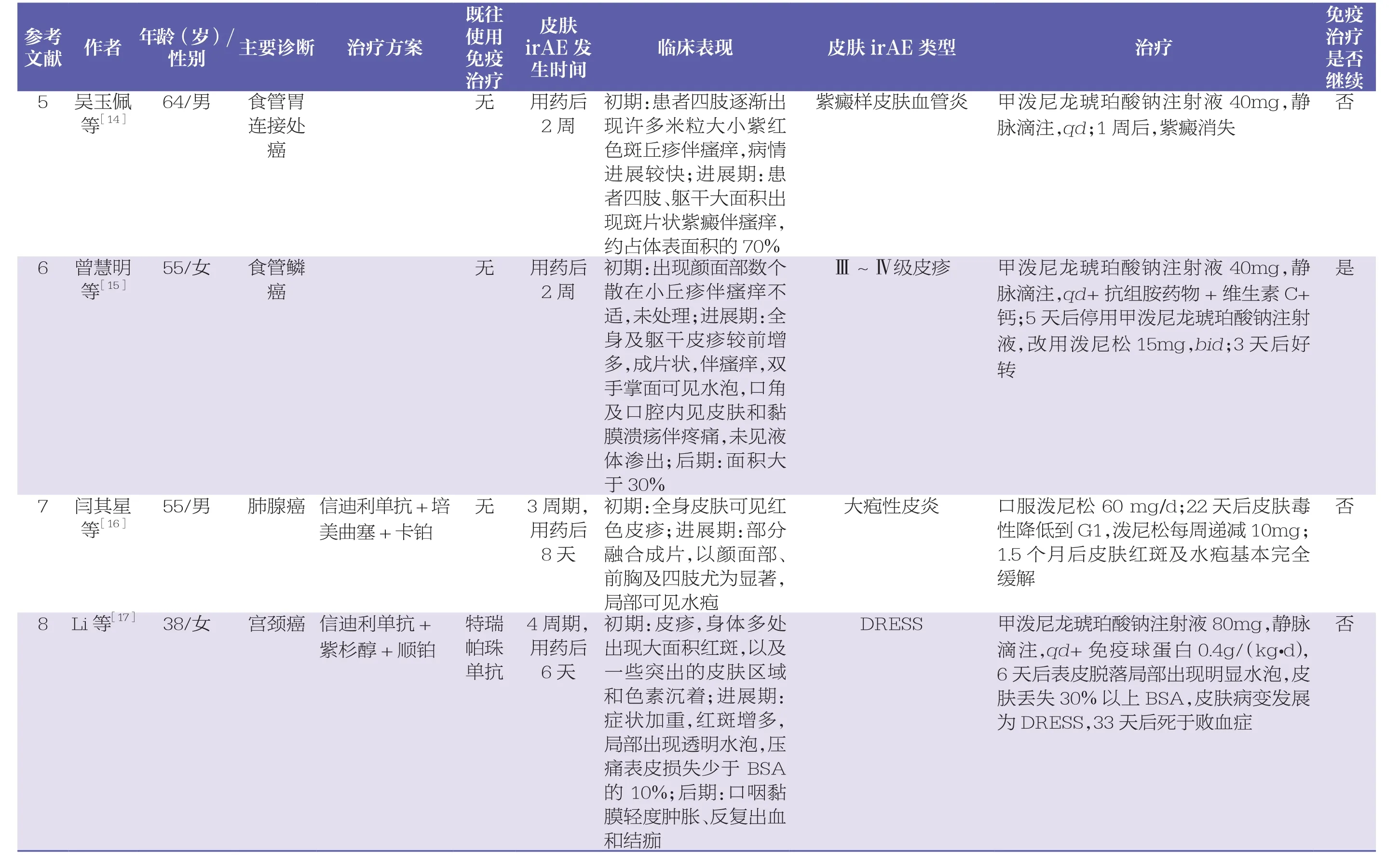
续表
4.3 皮肤irAE治疗措施
美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)、 欧 洲 肿 瘤 内 科 学 会(European Society for Medical Oncology,ESMO)和中国临床肿瘤协会(Chinese Society of Clinical Oncology,CSCO)均有irAE管理的临床指南。各指南对于皮损分级存在差异,但是整体治疗原则一致[26,30]。对于轻度皮疹/斑丘疹,推荐短期外用激素治疗,大疱性皮炎/SJS/TEN严重皮肤毒性,推荐甲基泼尼松龙/泼尼松0.5~1mg/(kg·d),根据皮肤损伤程度可以加大剂量至1~2mg/(kg·d),永久性停用PD-L1/PD-1抑制剂治疗。根据相关指南推荐[26,30],当发生3级皮肤反应时,建议暂停免疫治疗,口服抗组胺药,局部和/或全身使用强效糖皮质激素。同时说明书也指出,当发生3级皮肤反应时,需要暂停用药,待皮肤反应恢复为1~2级时才能考虑继续治疗。本研究患者经过皮肤科会诊皮损已经达到3级,积极给予静脉滴注激素治疗,逐渐过渡到口服醋酸泼尼松片联合盐酸西替利嗪片,以及给予维生素C注射液、葡萄糖酸钙注射液等治疗约1个月逐渐恢复,停用后更换化疗方案。汇总收集的8例个案报道中,5例初始治疗措施均采取静脉滴注激素治疗,逐渐减量,序贯口服。其中1例白癜风患者未采取治疗措施,1例初始即口服激素治疗,1例患者拒绝使用激素,给予抗组胺联合外用激素治疗。
5 小结
综上所述,本文通过报道一例严重皮肤免疫毒性病例,同时检索相关个案报道进行分析总结。与传统的化疗相比,irAE发生率较低且多为轻中度,具有可逆性,但严重者可致死。因此,医生和临床药师应给予更多关注。在患者免疫治疗前对患者做基线皮肤检查,已知有免疫相关性皮肤病史的患者应该到皮肤科就诊,进行基线皮肤检查,如大疱性类天疱疮、银屑病、扁平苔藓、红斑狼疮。发生皮肤不良反应时应详细询问病史,包括皮疹严重程度、合并症、伴随用药;查体需要包括全身皮肤检查,皮疹形态(特别是水疱)、皮疹的面积,黏膜是否受累。皮肤irAE属于排除性诊断,前提是排除既往皮肤相关性疾病、其他药物因素以及疾病并发症等,如感染、其他药物作用、其他系统性疾病、原发皮肤疾病。本研究的局限性是在使用前后,没有对患者自身免疫抗体、基因[如人类白细胞抗原(HLA)基因型]等的监测化验结果,未进行再激发试验。检索的文献数量有限,需要更加深入扩大检索范围。目前,信迪利单抗单独或联合治疗用于各种恶性肿瘤,临床药师应认识到其潜在的irAE,重视其irAE、风险因素、特殊人群的识别、治疗药物不良反应监测,可以建立相关药品不良反应数据库,对每一位使用PD-1/PD-L1抑制剂的患者进行充分评估和全面仔细的管理,提高临床疗效。同时应尽可能地降低药品不良反应风险,降低肿瘤患者的不良反应预后风险,延长患者生存期。

