壮药山芝麻的化学成分和药理研究进展
莫小林 陈 玲
广西中医药大学第一附属医院,广西 南宁 530023
山芝麻为梧桐科植物山芝麻(HelicteresangustifoliaL.)的干燥根或全株,《壮药学》谓其能调气道、谷道,清热毒,除湿毒,祛风毒[1]。临床上用于治疗感冒、麻疹、腮腺炎、痈疮、风湿骨痛、泄泻、痢疾、毒蛇咬伤,为广西民间常用的壮药。同时山芝麻是多种壮药制剂如三味板蓝根颗粒、三效微型灌肠剂的主要原料,也是多种中成药如莲芝消炎胶囊、感冒清片的主要原料。山芝麻为小灌木,高达1 m,根长而横走,黑褐色小枝有灰色短柔毛。叶互生,长圆形或椭圆形,先端钝或急尖,基部圆形,边全缘;上面近无毛或疏被星状柔毛;背面被灰白色或淡黄色星状短柔毛[2],实物如图1[3]所示。山芝麻喜温暖湿润的环境,以较肥沃而排水良好的砂质壤土生长为好。本文通过整理、归纳十年来国内外文献对山芝麻的化学成分和药理研究进展,为山芝麻的临床应用提供理论依据。

图1 山芝麻原植物实拍图
1 化学成分
至今,山芝麻中已报道鉴定了三萜类、甾体、倍半萜内酯类、香豆素类、有机酸及挥发油等化学成分,山芝麻中的三萜类成分如山芝麻甲酯、山芝麻宁酸甲酯和山芝麻宁酸具有降低转氨酶作用。山芝麻中咖啡酚奎尼酸类化合物具有广泛的抗菌、抗炎、抗氧化等活性,是山芝麻水提取液的药效物质基础[4]。研究均来自于山芝麻根,暂时无地上部分的化学成分研究报道。
1.1 三萜类化合物 山芝麻的三萜类成分具有抗炎镇痛、抗菌、抗病毒、抗肿瘤等活性[5]。苏丹等[6-7]建立了高速逆流色谱(HSCCC)法分离制备山芝麻中三萜类成分的方法,并测定了6种三萜类成分和总三萜的含量。从山芝麻乙酸乙酯萃取部位分离制备得到6个化合物,各化合物经鉴定分别为山芝麻宁酸甲酯、山芝麻酸甲酯、山芝麻宁酸、山芝麻酸、白桦脂酸、齐墩果酸。采用RP-HPLC同时测定山芝麻药材的6个主要三萜类成分,建立了紫外可见分光光度法测定山芝麻药材中总三萜的含量,用甲醇做为提取溶剂,使用乙酸乙酯进行超声萃取,既可以保证三萜类成分的提取效率,又可以达到较好的色谱分离,可以作为山芝麻药材的指标成分,用于山芝麻药材及其制剂的质量控制。
1.2 挥发油成分 苏丹等[8]将山芝麻药材粉碎至50目左右,用挥发油提取器水蒸气蒸馏法提取山芝麻的挥发性成分,用气相色谱-质谱(GC-MS)联用法对化学成分进行鉴定,采用峰面积归一法测定其含量。分离出109个化合物,鉴定了81个成分,占挥发油总成分的76.52%,主要为单萜烯类、倍半萜烯类及其含氧衍生物和脂肪族化合物等。萜类化合物是存在于植物界的一类化合物,其生物活性是多方面的,并且是某些中药的主要有效成分。山芝麻挥发成分中的主要萜类化合物有茴香烯、桉叶油烯、荜澄茄油、杜松萜烯、红没药烯、佛术烯、愈创木烯、香橙烯、紫罗兰烯等,分别具有镇痉、平喘、祛痰、止咳、抗菌、抗病 毒、抗癌、驱虫等作用。
1.3 有机酸类 宋伟峰等[9]采用水为溶剂加热回流提取法提取山芝麻药材,提取液采用高效液相色谱法串联质谱法研究了其水溶性化学成分。山芝麻药材水提取液的HPLC-MSn分析总离子流色谱图上有10个明显的色谱峰(如图2所示),表明山芝麻水提取液中含有10个主要的化学成分。对每个化学成分进行多级质谱分析,其中8个化学成分通过对照品得到了确证,分别为奎尼酸、柠檬酸、新绿原酸、绿原酸、隐绿原酸、异绿原酸C、异绿原酸A和异绿原酸B,详见表1。
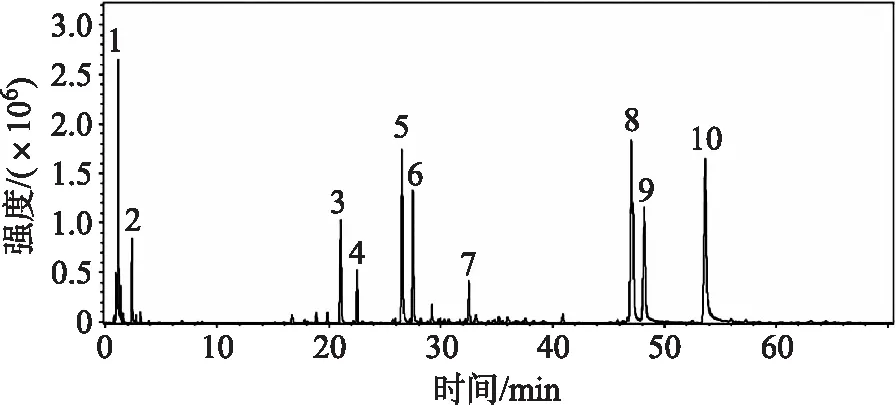
图2 山芝麻水提取液的总离子流图

表1 山芝麻水提取液的化学成分分析表
1.4 其他成分 金孝勤和庞素秋[10]采用硅胶柱层析、制备薄层层析等色谱方法,对山芝麻乙醇提取物分离纯化,用波谱和薄层方法进行化合物结构鉴定分离出的9种化合物,包括三萜类化合物、酚酸类化合物、木脂素、甾体类化合物等,分别是葫芦素B、葫芦素E、迷迭香酸、十二硫醇、β-谷甾醇、乌苏酸、细辛脂素、麦角甾醇、2,6-二甲氧基对醌。山芝麻的乙醇提取物在高剂量组抑瘤率为54.73%,表现出较好的抗肿瘤活性。经过四甲基偶氮唑蓝(MTT)分析,细辛脂素的IC50值显示对人结肠癌细胞(HT-29)显著抗增殖作用,对卵巢癌细胞(OVCA429)表现出微弱的抑制活性。
2 药理作用
山芝麻具有清热解毒之功效,临床用于治疗感冒高热、扁桃体炎、咽喉炎、腮腺炎、痢疾肠炎等疾病。药理学中上述功效与抗炎和镇痛作用相关。此外,也有抗肝、肺纤维化、抗氧化及清除自由基、免疫调节和抗肿瘤等作用。
2.1 抗炎镇痛作用 范文昌等[11]在对12种广东地产清热解毒药的抗炎作用实验研究中,灌胃给药山芝麻水提物生药16 g/kg对二甲苯所致小鼠耳廓肿胀有显著的抑制作用,还对醋酸所致小鼠腹腔毛细血管通透性增高有显著的抑制作用(P<0.05)。细胞因子失衡是溃疡性结肠炎(UC)产生肠道非特异性炎性反应的关键环节。与UC关系密切的促炎细胞因子主要有IL-1、IL-6、IL-8、TNF-α等,抗炎细胞因子主要有 IL-4、IL-10 等,它们可同时或相继、直接或间接作用于靶细胞,形成细胞因子网络,在UC的组织破坏及炎性反应中起着重要作用。灌胃给药山芝麻高剂量组(生药21.6 g/kg)、中剂量组(生药10.8 g/kg)、低剂量组(生药5.4 g/kg),采用三硝基本磺酸/乙醇法造模,双抗体夹ABC-ELISA法测定血清中IL-6、IL-10、TNF-α水平。与模型组比较,山芝麻高、中、低剂量组能显著降低大鼠促炎因子IL-6、TNF-α水平(P<0.05),山芝麻高剂量组能显著升高溃疡性结肠炎大鼠血清中抑炎因子IL-10水平(P<0.05),提示山芝麻水提物能平衡溃疡性结肠炎大鼠血清中炎症因子水平,并改善其病理组织损伤和症状[12]。范文昌等[13]在对12种广东地产清热解毒药的镇痛作用实验研究中,山芝麻能明显延长小鼠舔足时间,并能显著降低醋酸所致小鼠扭体反应次数(P<0.01),提示山芝麻不仅对外周性疼痛有镇痛作用,而且对中枢性疼痛有镇痛作用。
2.2 抗肝纤维化 天然产物具有结构多样、毒性较低、来源广泛等特点,在抗肝纤维化方面有着独特的优势和巨大的潜力,其作用机制包括抑制肝脏炎症反应,抗脂质过氧化损伤,抑制肝星状细胞(HSC)的活化和增殖,影响促纤维化因子的合成与分泌,以及调节细胞外基质合成与降解等[14-15]。α-平滑肌肌动蛋白(α-SMA)是HSC激活的标志,活化的HSC是导致肝纤维化的主要细胞,抑制活化的HSC增殖是抗肝纤维化的重要策略之一,阻断HSC活化增殖、促进其凋亡可有效抑制肝纤维化的形成[16-17]。黄莎等[18]将山芝麻等23种临床常用岭南中药分别先用95%乙醇提取,再用石油醚、乙酸乙酯、水饱和正丁醇和水依次萃取,制成115种中草药干浸膏,采用活化的大鼠肝星状细胞(HSC-T6)建立高通量筛选的肝纤维化体外模型,并应用模型初步筛选天然药物,结果显示用95%乙醇提取山芝麻,乙酸乙酯萃取提取物能使HSC-T6细胞的增殖率下降。林兴等[19]将75只肝纤维化模型大鼠随机分为5 组,每组各15只,山芝麻高、中、低剂量组分别予山芝麻水提物30 g/kg、15 g/kg、7.5 g/kg灌胃,秋水仙碱组予秋水仙碱1 mg/kg灌胃,模型组不用药。灌胃6周末采用免疫组化法检测各组肝组织中α-SMA、金属蛋白酶组织抑制因子(TIMP-1)蛋白表达情况并与15只正常大鼠(对照组)比较。结果山芝麻中、高剂量组α-SMA及TIMP-1表达明显低于秋水仙碱组和模型组(P<0.05、P<0.01),亦明显低于低剂量组(P<0.05)。山芝麻提取物高、中剂量还可显著降低肝纤维化大鼠肝组织ColⅠmRNA和ColⅠ蛋白的表达(P<0.05,P<0.01),且随着药物浓度的增加,其作用逐渐增强,呈现量效反应关系。显示山芝麻提取物能显著改善肝纤维化大鼠的肝脏组织结构,减轻肝纤维化[20]。
2.3 抗肺纤维化 周媛媛等[21]探讨山芝麻水提取物对百草枯致大鼠肺纤维化干预研究,将60只雄性大鼠随机分为3组,每组20只。百草枯(PQ)组予PQ农药40 mg/kg一次性灌胃;生理盐水对照组(NS 组)予注射用生理盐水40 mL/kg一次性灌胃;PQ联用山芝麻(RH)组予PQ农药 40 mg/kg 一次性灌胃后给予RH水提取物15 g/kg灌胃,1次/d,连续3 d。21 d后处死大鼠,开胸取左肺组织,观察3组大鼠肺组织外观后,石蜡切片,HE染色,在光学显微镜(光镜)下观察肺组织病理学改变,部分肺组织行免疫组化检测。研究发现,PQ灌胃后大鼠肺脏呈明显肺纤维化的病理改变,而用RH水提取物对PQ中毒治疗后比较:大鼠肺组织外观损伤范围较小,结节样改变数量较少,硬化程度较轻,光镜下PQ组及PQ联用RH组均有不同程度范围的慢性炎性灶,但PQ联用RH组肺组织胶原纤维、成纤维细胞增生程度较轻。免疫组化法及 Westernblot 法检测PQ大鼠肺组织均提示:PQ组Smo和Gli1蛋白表达明显增强,PQ联用RH 组 Smo及Gli1表达明显减弱,组间比较具有显著性差异(P<0.05)。结果表明RH水提取物显著减低SHH信号途径Smo和Gli1蛋白表达,减轻PQ诱发的大鼠肺纤维化,对肺纤维化有一定的干预作用。
2.4 抗氧化活性 活性氧(ROS)包括超氧阴离子自由基(O2-)、过氧化氢(H2O2)和羟基自由基(HO-),在心血管疾病、炎症、神经退行性疾病、动脉硬化和癌症等严重疾病的退化或病理过程中起着重要作用,过量的自由基是引起机体衰老和疾病的主要因素[22]。因此从天然产物中寻找高效、低毒的清除体内自由基的抗氧化剂已成为现代医药、保健行业研究的热点[23]。李克娟等[24]分别用水和乙醇提取山芝麻根,获得山芝麻水提取物(ARE)和山芝麻乙醇提取物(ERE)。在体外抗氧化活性实验中通过自由基清除试验、亚铁螯合试验和还原力试验来评估ARE和ERE的抗氧化活性。结果表明,两种提取物对DPPH自由基、ABTS自由基、羟基自由基表现出相似的清除能力和亚铁螯合能力,与ERE相比,ARE具有更强的自由基清除活性和还原能力,而螯合活性较低。
在山芝麻愈伤组织悬浮培养物(CE)的提取物的体外抗氧化实验[25]中,CE对DPPH自由基、羟基自由基、ABTS自由基的清除能力在0.08~2.50 mg/mL之间呈剂量依赖性增长,CE的DPPH清除率在2.50 mg/ mL的剂量下达到最大值。亚铁离子的螯合能力检测是筛选天然抗氧化剂的一个必要方法。CE是一种有效的亚铁离子螯合剂,显示出了剂量依赖性的螯合活性,其IC50值达到(4.65±0.08)mg/ mL。
刘倩薇等[26]采用超声波辅助水提取、乙醇沉淀,DEAE-52阴离子交换色谱法和Sephadex S-300凝胶色谱法,从山芝麻中分离和纯化了HALP1-1和HALP2-1成分。根据物理化学性质、紫外光谱、红外光谱分析,这些多糖被鉴定为酸性吡喃糖。特别是HALPs1-1被发现是分子量为151.7 kDa的葡聚糖,而HALPs2-1是由葡萄糖醛酸组成,分子量为114.81 kDa。体外抗氧化活性测定的结果显示,HALPs1-1和HALP2-1对DPPH、ABTS和羟基自由基都表现出浓度依赖性的清除作用。HALPs2-1在各馏分中具有最高的DPPH自由基、ABTS自由基和羟基自由基清除活性。
2.5 免疫调节作用 巨噬细胞几乎广泛地分布在人体的所有组织中,参与吞噬和消化外来物质的免疫反应,因此它们在保护人体免受各种疾病侵害方面起着至关重要的作用。在山芝麻愈伤组织悬浮培养物免疫调节活性研究[25]中,山芝麻愈伤组织悬浮培养物(CE)在0.78~400.00 μg/mL的剂量范围内对巨噬细胞的增殖表现出促进作用。剂量为6.25 μg/mL时,细胞存活率达到最高值(121.93±1.76)%。CE可以在0.78~400.00 μg/mL的剂量范围内激活巨噬细胞的增殖,且细胞毒性很小。还研究了CE对巨噬细胞吞噬能力的影响。结果表明,CE在1.56~12.50 μg/mL的浓度下能明显增强巨噬细胞的吞噬能力。CE在6.25 μg/mL浓度时,巨噬细胞的吞噬能力增加到最大值。DOX作为一种抗癌药物,可以诱导肿瘤和正常细胞的凋亡,导致细胞死亡。巨噬细胞的存活率因DOX处理而明显下降。用DOX(0.5 μm或1.0 μm)处理24 h后,细胞活力比分别下降到(41.53±1.72)%和(27.93±1.14)%。在CE(1.56~12.50 μg/mL)存在的情况下,细胞活力比的下降在一定程度上被抑制。对于用0.5 μm DOX处理的细胞,在CE的12.50 μg/mL下,存活率下降到(54.28±1.93)%。用1.0 μm DOX处理的细胞,接触12.50 μg/mL的CE,存活率下降到(37.73±0.88)%。提示CE对DOX引起的巨噬细胞损伤有保护作用。
孙霜[27]用DEAE Sepharose Fast Flow阴离子交换色谱法和Sephacry S-400色谱法从山芝麻中纯化了多糖部分(SPF3-1)。SPF3-1是一种酸性杂多糖,分子量约为13.36 kDa;体外免疫调节试验表明,SPF3-1能明显增强巨噬细胞的增殖,刺激巨噬细胞的吞噬能力,并能诱导NO和免疫调节细胞因子的产生。提示来自山芝麻的SPF3-1具有强大的免疫调节活性。
2.6 抗糖尿病 糖尿病的病情发展与血糖浓度的变化密切相关。在机体的血糖浓度调节机制中减缓小肠对淀粉等多糖的消化与葡萄糖的吸收是一个重要的机制。小肠二糖酶(蔗糖酶、麦芽糖酶、乳糖酶等)在肠道葡萄糖的生成中具有重要意义。在糖尿病病理状态下肠道的二糖酶的活性升高导致葡萄糖的生成加快进而导致葡萄糖的吸收加快,血糖升高加剧[28]。因此,二糖酶的抑制剂可以延缓可吸收单糖的释放过程,它们被广泛用于治疗餐后高血糖症。在山芝麻愈伤组织悬浮培养物抗糖尿病研究[24]中,山芝麻的培养物可以用来生产麦芽糖酶和蔗糖酶抑制剂。CE对麦芽糖酶和蔗糖酶的抑制作用在0.50~32.00 mg/mL范围内。以阿卡波糖为阳性对照,结果表明,阿卡波糖对麦芽糖酶和蔗糖酶有明显的抑制作用,IC50值小于0.50 mg/mL。此外,CE对大鼠的麦芽糖酶和蔗糖酶表现出剂量依赖性的抑制作用。在32.00 mg/mL的高浓度下,CE的麦芽糖酶抑制率达到约(73.97±0.11)%,其蔗糖酶抑制率约为(67.88±5.28)%。CE对麦芽糖酶和蔗糖酶的抑制IC50值分别约为13.29 mg/mL和13.76 mg/mL。
2.7 抗肿瘤 作为抗癌治疗的可能潜在来源,有学者将三种人类癌细胞系(肝癌HepG2、结肠癌DLD-1和肺癌A549)分别与不同浓度的山芝麻根提取物培养24 h和48 h[24]。使用WST-8试验评估它们的细胞毒性效果。ARE和ERE对癌细胞都表现出明显的细胞毒性作用,而且ARE对三种测试的癌细胞系都表现出时间和剂量依赖的抑制作用,并显示出高于ERE的增殖抑制作用。对于正常细胞系,与对照组相比,当其浓度≤50 μg/mL时,TIG3的存活率没有显示出明显的差异(P<0.001),表明在低浓度下没有细胞毒性作用。此外将ARE进行体内抗肿瘤实验BALB/c裸鼠通过口服ARE(200 mg/kg/d)或载体(PBS)进行预处理,为期14 d。在第15天,皮下接种HT1080纤维肉瘤细胞,每组连续口服4周。在实验过程中,对照组小鼠的肿瘤体积由于肿瘤的发展而逐渐增大,ARE处理的小鼠的平均肿瘤体积则被明显抑制(P<0.05)。在第42天,对照组的平均肿瘤体积为(497.30±144.12) mm3,远远大于ARE治疗组的(153.75±55.65)mm3(P<0.05)。将处死小鼠肿瘤组织进行称重,结果显示,200 mg/(kg·d)的ARE给药明显抑制了HT1080细胞肿瘤的生长(P<0.01)。对照组小鼠的平均肿瘤重量为(0.40±0.18)g,而200 mg/(kg·d)的ARE治疗小鼠的肿瘤重量为(0.19±0.07)g,肿瘤抑制率为(49.83±14.38)%(P<0.05)。通过比较对照组和治疗组动物在实验期间的体重变化,没有发现治疗组动物有明显的毒性。
苏丹等[29]研究了山芝麻(HT)的三种三萜类化合物螺旋藻酸(HA)、油酸(OA)和白桦脂酸(BA),对抑制结直肠癌(CRC)进展的作用。结果表明,HT提取物可以减少增殖并诱导HT-29结直肠癌细胞的凋亡。此外,HT提取物可以抑制LPS触发的IKK、IκB和NF-κB的磷酸化,减弱IL-6诱导的JAK2和STAT3的磷酸化,并抑制NF-κB和STAT3的下游基因靶点c-Myc、cyclin-D1、BCL-xL的表达。因此,HT提取物通过抑制NF-κB和STAT3信号传导,减少炎症、抑制细胞增殖和促进HT-29细胞的凋亡对CRC显示出有效的治疗和抗肿瘤作用。
3 小结与展望
山芝麻为广西民间常用壮药,主要分布于广西﹑广东﹑福建、江西、云南、海南、台湾等西南地区。味辛﹑微苦,性凉,有小毒[30]。山芝麻具有多种化学成分,部分具有较好的药理活性。山芝麻除了具有抗炎镇痛、抗肝、肺纤维化、抗氧化、免疫调节和抗肿瘤等药理作用外,有报道[31]山芝麻具有肾损害、中毒性休克、急性肾功能衰竭毒等副作用,但其有毒成分研究和毒理作用尚未见文献资料报道,值得进一步研究以保证山芝麻临床用药的安全。
山芝麻为广西传统特色优势壮药外感风痧颗粒的主要组成药材[32]。同时也是玉叶解毒颗粒等多种中成药的主要原料。虽为《广西壮族自治区壮药质量标准》(第三卷)收载品种,但缺少相应的质量评价研究。目前山芝麻的主要研究对象以根为主,针对全草的研究较少。随着山芝麻临床应用的增加及作为壮药制剂等的生产原料,增加了药材消耗量,应该加强山芝麻根及地上部分的质量标准研究,同时开展体内药效和药理评价,以阐明山芝麻的药效物质,从山芝麻悬浮培养物的提取物研究中发现,与同等野生山芝麻根相比,培养物可以产生更多活性成分和呈现出各种功能,能为开发山芝麻的功能产品及其临床治疗中的应用提供更有价值的信息。

