废弃金属制备矾类产品
——一个大学化学改进实验*
景学敏,卢绘洁,马雨萱,崔兴垚,魏 磊,马麦霞
(廊坊师范学院化学与材料科学学院,河北 廊坊 065000)
现阶段大学化学实验教学目标多数仍然只要求学生掌握基本原理、基本知识和基本操作,并通过操作规范得到准确的数据和结论,导致实验内容脱离生活,缺乏创新性[1];实验之间缺乏联系,知识不系统。联系生活实际、改进实验内容、归纳总结各实验之间联系具有重要的意义[2]。
生活中废弃金属制品来源广泛,包括废弃的家具、汽车交通用品、饮料罐、建筑材料和电器等,它们所产生的垃圾如果处理不当会造成资源的浪费,同时给社会造成不小的压力。将废弃金属回收并循环利用,变废为宝,有着巨大的经济效益和社会效益。将这种理念引入大学实验课堂中,既能激发学生“学以致用”的积极性、锻炼其主动探索精神和动手实践能力,又能将“循环经济和可持续发展”的理念融入教学,实现实验课程教学的思政。
结合我们教学团队长期的一线实验教学实践与需求,我们对金属成盐实验进行了改进,改进后的实验由单一金属变成三个金属分别通过溶解、蒸发结晶来制备相应盐类产物。改进后的实验项目适用于化学、应用化学、材料化学等相关专业大一学生。通过该实验不仅使学生巩固和运用所学理论知识,熟练掌握金属单质制备盐的相关操作,深化认识金属活泼性规律的本质;同时培养学生动手实践能力,激发同学们对于科研的兴趣与灵感,亲自体验“变废为宝”乐趣。
1 实验目的
(1)深入认识金属铝、铁和铜的性质及其成盐方法差异。
(2)从氧化还原角度认识金属活泼性规律的本质,了解明矾、绿矾和胆矾的制备方法。
(3)掌握溶解、蒸发结晶、过滤,以及沉淀的转移和洗涤等无机化合物制备的基本操作。
2 实 验
2.1 明矾的制备原理

2Al+2KOH+2H2O=2KAlO2+3H2↑
2KAlO2+H2SO4+2H2O=2Al(OH)3↓+K2SO4
2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
Al2(SO4)3+K2SO4+24H2O=K2SO4·Al2(SO4)3·24H2O ↓
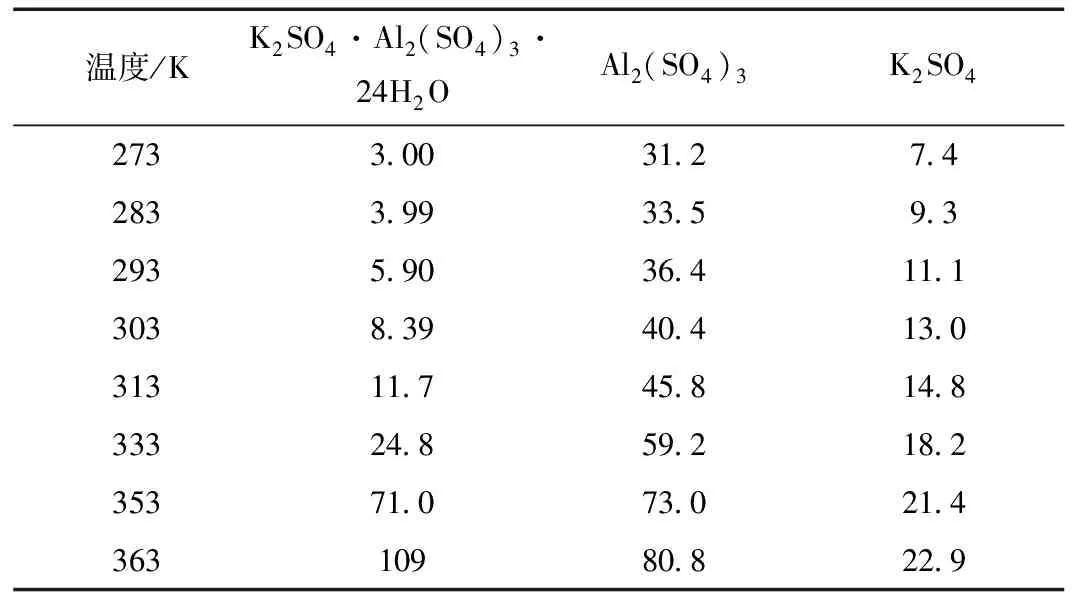
表1 不同温度下各物质的溶解度
2.2 绿矾的制备原理
将金属铁溶于稀硫酸中,得到硫酸亚铁溶液,溶液变为浅绿色,并且不断有气泡逸出[7-8]。将制的得的硫酸亚铁溶液蒸发浓缩结晶,即可析出绿矾晶体(七水硫酸亚铁,FeSO4·7H2O)。上述过程的化学反应方程式为:
Fe+H2SO4=FeSO4+H2↑
FeSO4+7H2O=FeSO4·7H2O ↓
2.3 胆矾的制备原理
金属铜是不活泼金属,不能直接和稀硫酸反应来制备硫酸铜,因而需要先将金属铜灼烧,灼烧之后得到氧化铜,然后将氧化铜溶于适当浓度的硫酸中[9-10]得到硫酸铜溶液。溶液经蒸发浓缩后即可析出胆矾晶体(五水硫酸铜,CuSO4·5H2O)。其主要化学反应方程式为:
2Cu+O2=2CuO
CuO+H2SO4=CuSO4+H2O
CuSO4+5H2O=CuSO4·5H2O ↓
2.4 主要试剂与仪器
仪器:电子台秤、分析天平、酒精灯、显微镜、精密鼓风干燥箱。
药品:铝、铁和铜金属制品、KOH、9M H2SO4、H2O2、Na2CO3、无水乙醇。
2.5 实验步骤
分别以易拉罐、废铁丝和废铜丝为原料来制备明矾、绿矾和胆矾,制备过程可分为三步:金属表面的预处理、金属的溶解和蒸发结晶析出产物。
2.5.1 明矾的制备
2.5.1.1 由易拉罐制备偏铝酸钾溶液
(1)预处理:用砂纸打磨易拉罐外皮至表面光亮,打磨好的易拉罐剪碎备用。
(2)将1.100 0 g KOH固体溶于盛有20.0 mL水的烧杯中得到氢氧化钾溶液,在通风橱内分多次向氢氧化钾溶液中加入0.500 0 g处理过的易拉罐细屑(烘箱70~80 ℃,也可用恒温水浴锅),盖上表面皿,待反应完全(不再有气泡产生),趁热过滤,滤液保留,取出未反应铁屑,自然干燥,称重并记录质量。
2.5.1.2 制备硫酸铝钾溶液
(1)Al(OH)3沉淀的生成与洗涤
在不断搅拌下,向制得的偏铝酸钾滤液中先加入9 M H2SO4溶液,后改为3 M H2SO4来调节溶液的pH值为8~9(不溶性絮状沉淀Al(OH)3不再产生),将所得混合物置于烘箱中煮沸10 min,自然冷却、过滤、水洗沉淀2~3次。
(2)Al(OH)3沉淀的溶解
将Al(OH)3沉淀转移至蒸发皿中,边搅拌边滴加3 M H2SO4硫酸溶液(5~10 mL)至生成的白色沉淀大部分溶解,呈现浑浊状态。继续加热至溶液澄清。如果溶液仍浑浊,可适当补加数滴3 M H2SO4溶液,使液体变澄清,得到硫酸铝溶液。向上述溶液中加入30.0 mL 3 mol/L KOH溶液,得到硫酸铝钾的混合溶液。
2.5.1.3 硫酸铝钾溶液蒸发浓缩制备明矾
在水浴条件下,将硫酸铝钾混合溶液蒸发,浓缩至液面有晶膜出现,室温自然冷却,减压抽滤,自然干燥后,称量晶体质量。
2.5.2 绿矾的制备
2.5.2.1 由废铁丝制备硫酸亚铁溶液
(1)预处理:称取1.000 0 g铁丝剪碎备用,再称取1.250 0 g Na2CO3于50 mL烧杯中,加入10.0 mL蒸馏水,稍加搅拌,配置成溶液。将铁屑放入Na2CO3溶液中,稍加搅拌,使铁屑没入碱液,放入烘箱,控制温度80 ℃,加热10 min,以除去表面有机物杂质。抽滤,取出铁屑,干燥,称量并记录未溶铁屑质量。
2.5.2.2 制备硫酸亚铁溶液
量取10.0 mL蒸馏水及15.0 mL 3 mol/L H2SO4,倒入50 mL烧杯中,放入处理好的铁屑,使铁屑完全没入溶液,盖上表面皿,置于80 ℃烘箱中反应,当溶液中气泡冒出较少时停止加热,加热过程中要及时观察溶液量的变化,适当补加酸和水。
2.5.2.3 硫酸亚铁溶液蒸发浓缩制备绿矾
用少量热水洗涤抽滤装置,将溶液趁热过滤,少量热水洗涤烧杯,洗涤液倒入抽滤漏斗,称取滤饼质量并记录(未反应的铁屑),将滤液转移至蒸发皿中,蒸发浓缩,注意观察溶液变化,出现晶膜时停止加热。将溶液转移至锥形瓶中,盖上瓶塞,室温静置冷却。抽滤,用少量冷的蒸馏水洗涤两次,再用少量无水乙醇洗涤晶体,收集滤饼,称量并记录。
2.5.3 胆矾的制备
(1)由废铜丝制备氧化铜
称量0.500 0 g废铜丝并剪碎,将其于酒精灯上充分灼烧,得到氧化铜。
(2)由氧化铜制备硫酸铜溶液
向装有灼烧样品的蒸发皿中加入3.0 mL 3 mol/L H2SO4,搅拌使大部分固体溶解,得到硫酸铜溶液,过滤,取出铜屑,自然干燥,称量并记录铜屑质量。
(3)硫酸铜溶液蒸发浓缩制备胆矾
将硫酸铜溶液倒入蒸发皿中,加热蒸发浓缩溶液,至表面有晶膜出现,撤掉酒精灯,自然冷却结晶。抽滤,收集晶体,称量并记录。
3 结果与讨论
3.1 产品形貌
由2.5.1~2.5.3步骤操作可分别得到三种矾类产品。在显微镜下观察产品形貌,如图1所示:三种产品均为透明晶体,其中明矾为无色正六面体形状晶体,颗粒较大,未发生聚集;绿矾为淡绿色块状晶体,部分发生聚集;胆矾为蓝色的透明块状晶体,大小均匀。

图1 明矾、绿矾和胆矾产品的照片
3.2 产率计算
产率可根据以下公式计算得到:
m/[(m1-m2)/M1×M2]
式中:m、m1和m2分别为产品质量、金属质量和未溶残渣质量,M1和M2分别对应金属单质和产物的分子量。
以前面的数据为例,可分别计算三种产品的产率:
如2.5.1步骤操作中:m1=0.500 0 g,m2=0.143 8 g,m=4.982 6 g,从而得到产率为78.84%。
如2.5.2步骤操作中:m1=1.000 0 g,m2=0.230 0 g,m=2.140 0 g,从而得到产率为55.98%。
如2.5.3步骤操作中:m1=0.500 0 g,m2=0.221 5 g,m=1.044 3 g,从而得到产率为95.99%。
至此,实验操作基本结束,后续同学们通过实验报告的撰写可再现其操作过程、数据处理情况、及对实验的思考和总结。教师再针对报告所呈现的问题,统一反馈给学生,让学生深刻体验和反思整个实验过程。通过本次实验方案的优化改进,可以收到三个方面的效果:
首先,在学生专业知识和综合素质培养方面。(1)改进后的实验方案可以从氧化还原角度,使学生更加深入地认识金属活泼性规律的本质。铝是两性金属,既可溶于酸又可溶于碱,实验中使用碱溶是为了减少易拉罐中其他金属的溶解带来的杂质影响。铁和铜为过渡金属,前者可用酸直接溶解,后者为不活泼金属,不能直接溶解,需要氧化后再酸溶。三种金属溶解方式的差异,可从电极电势的角度进行解释,如表2所示,酸性条件下,三种金属的标准电极电势分别为:-1.662 V、-0.447 V和0.341 9 V,与标准氢电极电势相比,铝和铁电极电势均小于氢的标准电极电势,因而均可与稀酸发生还原反应放出氢气,而铜电极电势大于氢的标准电极电势,无法与稀酸发生还原反应。在碱性条件下,铝的标准电极电势小于氢的标准电极电势,可以与稀碱发生还原反应。通过三个金属电极电势的比较,同学们可对金属活泼性规律的本质,即电极电势有更深入的认识,同时对氧化还原反应的理解更深刻。(2)改进后的实验方案,可以使学生熟练掌握溶解、蒸发结晶、过滤,以及沉淀的转移和洗涤等无机化合物制备过程的基本操作。实验产品的制备过程中,每一步操作都会影响最终产物的质量和品质:溶解和蒸发是否充分、过滤是否完全、沉淀洗涤方法是否正确、沉淀转移是否有损失,而每一步操作都凝聚着化学原理和规范,熟练地掌握这些操作,对于同学们化学专业综合素养的养成和实践能力的提升至关重要。

表2 三种金属的标准电极电势
其次,在学生思想和兴趣培养方面。(1)改进后的实验,金属原料来源于生活中的废弃金属制品,将生活实际与实验教学内容联系起来,使学生在把握实验目的和内容的同时也兼顾到环境保护的必要性,明确化学和环境密不可分的关系,逐步培养学生们的绿色环保意识。(2)对实验方案的改进优化,实现了多个实验的同步进行。面对多样化的原料,同学们的积极性和自主选择性被充分调动,他们通过相互比较原料、操作过程和产品的差异,更好地体验了“变废为宝”的过程快乐,同时进一步培养学生对于科研的兴趣与灵感。
最后,从教师的角度来看,优化改进后的实验,教师可以在讲授专业知识的同时,更好地将“绿色化学和环境保护”这一理念融于实验教学过程中,实现实验课程教学的思政。
4 结 语
本实验经过优化改进可作为化学及相关专业一年级学生的基础化学实验项目,计划学时4~6学时,建议每名学生单独选择其中1个项目完成。改进后的实验将原本孤立的三个实验有机地结合在一起,紧贴生活实际,以废弃金属铝、铁和铜制品为原料,以酸、碱或氧化还原溶解后,运用蒸发结晶的方法制备明矾、绿矾和胆矾;同时由于原料的多样化而带来的产品的多样性和差异性,会增加教学过程的灵活性和实验本身的趣味性;最后,改进后实验原料为同学们动手收集的生活中废弃金属制品,是一个“变废为宝”的实验过程,既激发了学生对废物再生利用的热情,又锻炼了学生的动手能力,对学生绿色环保意识的培养和科研兴趣的提升都有重要作用,同时教师可更好地将“绿色化学和环境保护”这一理念应用于实验教学过程中,实现实验课程教学的思政。

