基于化学反应原理的系统模型建构
吴健华 谭琪 王怀文


摘要:化学反应原理是对化学变化本质与规律的概括化认识,是调控化学反应的依据,包括化学反应与能量、化学反应的方向、速率、限度及调控等基本问题,对科研、生产等有着重要的指导作用。本单元主题教学课例以火箭推进剂的研究为真实情境,开展火箭推进剂的“发展与效能研究”“废气确定及处理”“工业制备的定量分析”等任务环节;引领学生基于多角度、多变量关系建构化学反应规律的问题解决思维系统模型,培养学生理解概括、迁移应用反应规律的学科能力。
关键词:化学反应原理;单元主题教学;火箭推进剂;真实情境;系统模型
文章编号:1008-0546(2023)09-0002-06
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2023.09.001
一、单元教学背景分析
1.课标教材分析
关于化学反应原理主题内容,不同版本教材均侧重于化学反应能量、方向、限度与速率等基本规律的研究,开展合成氨工业反应条件选择与优化的讨论,充分调动化学反应原理知识的理解、迁移与应用。新课程标准[1]建议创设真实情境,如开展火箭推进剂燃料的研究,形成合理利用化学反应中能量转化与物质变化的意识与思路;结合具体实例,认识化学反应的微观历程,能从限度、速率等多角度对化工生产条件进行综合分析,建构基于化学反应原理的系统模型,体会问题解决的思维演绎过程。
2.学情分析
通过本单元主题教学课例的实施,预期学生学业质量达到3、4水平(高阶水平):能结合问题情境,从定性与定量角度分析化学变化中能量转化,理解其在生产、生活中的重要应用;能从宏观与微观的认识角度,结合数据、图象、符号等多种方式对化学问题进行描述表征;能对反应速率、化学平衡等理论规律进行概括关联,基于多角度、多变量关系对真实情境中的化学反应原理进行预测推理、说明论证及迁移应用,进一步提出化学问题的解决方案。
二、单元主题教学目标
根据单元主题的结构性、进阶性,本教学课例安排为3课时,单元主题教学目标与课时目标设计见图1。
三、单元主题教学思维框架
课时一:基于化学反应原理的系统模型建构——火箭推进剂的发展与效能研究,见图2。
课时二:基于化学反应原理的系统模型建构——火箭推进剂废气确定及处理,见图3。
课时三:基于化学反应原理的系统模型建构——火箭推进剂工业制备的定量分析,见图4。
四、单元主题教学实施过程
元主题教学的3个课时项目活动已顺利实施。课时一重点发展学生结合宏观外界条件及微观反应机理的认知角度,运用化学反应速率的原理对真实情境下火箭推进剂反应条件的选择及优化问题进行讨论分析、推理论证,其課时一的教学实录如下:
环节一:多角度分析火箭推进剂的选择因素
【任务】利用热力学知识,解决火箭推进剂的选择问题。
【情境】2021年我国神舟十三号载人飞船运载火箭成功发射,标志着我国航天事业的高速发展。随着科技发展,液体推进剂的种类与性能在不断改良。
【问题】书写热化学方程式,计算热值,判断反应进行方向,归纳火箭推进剂的选择依据。
【师生活动】
教师:播放神州十三号载人飞船等爱国情境视频,简述火箭推进剂的作用原理,列举常见的液态推进剂(见表1)。
学生:观看视频,感受我国航天事业的伟大发展,了解火箭推进剂的作用原理。
教师:展示资料卡片(见表2),引导学生结合化学热力学知识进行思考,提出问题:
①N2H4(1)与N2O4(g)二者反应产生N2(g) .H2O(g),写出热化学方程式,并说明反应可自发进行的原因;
②结合燃烧热数据,说明液氢、液氧推进剂的优势;
③综合多角度因素归纳火箭推进剂的选择凶素。
学生:独立思考,小组交流讨论,得出结论:
解答①:根据盖斯定律,N2H4(1)与N2O4(g)反应的热化学方程式为2N2H4(1)+N204(g)===3N2 (g)+4H2O(g)△H=-1310.4 kJ.mol-1;分析该反应的特点:△H<0,AS>0,正方向为焓减且熵增的反应,在任何条件下可自发进行。
解答②:从物质的燃烧热考虑,丙烷、乙醇等的燃烧热数值较大,但考虑火箭的运载质量,应选择单位质量燃料可释放出较多能量(热值较高)的推进剂。经过计算比较可知,液氢的热值较高,其燃烧性能高。
解答③:结合不同推进剂的性能特点及热值数据,从多角度思考火箭推进剂的选择因素。液氢具有热值较高、产物无污染、原料来源丰富等优势,备受航天工业的青睐。
设计意图:对火箭推进剂的发展进行简要介绍,为后续问题解决作知识铺垫。通过组织对火箭推进剂燃料的选择判断,形成合理利用化学反应中能量转化与物质变化解决问题的思路,同时增强爱国情怀。
环节二:氢氧燃烧条件的初认识
【任务】结合化学反应规律,初步判断氢氧推进剂的燃烧条件。
【情境】假如你是火箭工程师,根据化学反应原理知识,该如何提高液氢和液氧的燃烧效率?
【师生活动】
教师:对于液氢、液氧推进剂,可以考虑从哪些角度提高其燃烧反应效率?
学生:发生的反应为2H2(g)+O2(g) =2H2O(g),可从速率角度出发,改变外界条件加快燃烧速率;或从平衡角度考虑,提高氢氧燃烧的反应限度。
教师组织评价:氢氧燃烧反应的平衡常数K的数量级高达10 83,表明反应正向进行的趋势极大;但在不同的反应条件下,其反应速率有快有慢。因此,应从速率的角度对反应进行调控。教师进一步提出问题,思考提高氢氧燃烧速率的外界条件的选择与调控。
学生:依据反应速率理论,从浓度、温度、压强及催化剂等因素进行分析。
教师:展示文献中推进剂燃烧速率的关系图象[3](图5),引导学生阅读图表资料获取信息,并完成表3的填写。
学生:阅读图象信息,交流并填写氢氧燃烧条件的实际选择,与理论分析进行比较。根据理论分析,按化学反应计量数比(2:1)成倍增大氢氧浓度、增大压强等条件均可加快燃烧反应速率;但根据图象分析判断,氢氧燃料当量比约为1.5时(适度增大H2浓度,氢氧浓度比为3:1)、反应保持相对低压,有利于燃烧反应的进行。实际的条件选择与理论分析产生问题冲突,小组交流讨论产生冲突的原因,提出猜想。
设计意图:组织学生基于外界条件对反应速率的影响,开展氢氧燃烧反应条件选择的初判断;结合文献资料中燃烧条件的选择,形成问题认知冲突,发展学生归纳论证、演绎推理、系统假设的思维能力。
环节三:氢氧燃烧条件的再认识
项目1:燃烧反应的微观机理研究
【任务】绘制反应历程与能量变化图,认识理解氢氧燃烧的反应机理。
【情境】氢氧推进剂燃烧条件的选择与理论分析存在冲突与差异,从微观反应机理认识氢氧燃烧的反应历程,解决实际条件的选择问题。
【师生活动】
教师:展示氢氧推进剂燃烧的简化反应机理[3](见表4),分析该自由基反应的特点,画出其反应历程与能量变化图。
学生:依据盖斯定律,结合各步反应的活化能Ea及反应热△H,绘制反应历程与能量变化图,将链引发、链传递及链终止三个阶段的基元反应表示在图中(见图6)。
依据学生绘制的图象,教师进一步提出问题:该反应历程分为几步进行?其中哪一步的活化能最大?解释链引发、链终止反应对温度条件敏感、不敏感的原因。
学生:从反应历程及活化能可知,链引发反应H2 (g)+M ===2H.g+M的活化能Ea最大,该步骤的发生是氢氧燃烧反应的先决条件,且为总反应的速控步,受温度影响较大;其他阶段的反应活化能较小,受其它凶素影响较大,需维持活性较高的H·、.OH、O.等自由基粒子(属于中间产物)的持续产生,保证燃烧反应的进行。
设计意图:通过对氢氧燃烧的微观机理进行研究,发展学生对化学反应历程的深层认识,强化微观探析、变化观念等学科素养的培养。学生通过动手绘制反应历程与能量变化图,化抽象概念为具体图象,加深对基元反应与活化能、速控步等概念的认识,有利于从不同维度深入理解化学反应规律。
项目2:氢氧燃烧条件的选择调控
【任务】多角度综合解决氢氧燃烧条件的调控问题。
【情境】结合资料信息及氢氧燃烧反应机理,分析氢氧燃烧反应所選择的实际条件。
【师生活动】
教师:引导学生结合反应特点及微观反应机理,多角度、多变量分析增大氢氧燃烧速率的实际条件选择。
该燃烧反应释放大量热,能维持反应高温进行。查阅资料可知,灌装火箭推进剂时无需加入催化剂。请分析氢氧推进剂燃烧需保持高温条件且不需要加入催化剂的原因。
学生:根据反应机理,链引发步骤产生H.自由基,引发后续反应持续进行;第一步反应H2(g)+M===2H.(g)+M的活化能很大,高温有利于促进H2解离产生H.,使反应快速进行。
催化剂在适宜温度范围内保持较高的催化活性;但温度过高时,催化剂的结构发生改变导致失活,因此不需加入催化剂,或可考虑研发更耐高温的催化剂。
教师:高效且适用范围广的催化剂是科技前沿的研究方向,相信未来会研发出有效的催化剂。结合宏观条件与微观反应机理,进一步对压强及浓度的选择调控作山分析。
学生:根据图象可知,实际选择的氢氧燃料当量比为1.5,燃料当量比大于1,说明提高氢气的相对浓度,有利于增大链引发的反应速率,提高燃烧效率。但氢气的相对浓度不宜过大,避免造成氢气的利用率较低;同时过多的液氢会造成火箭承载质量过重,凶此需要选择合适的燃料当量比。
教师:为提高储存容量,火箭灌装液态的氢氧燃料,在喷射点燃时维持一定压力。从文献图象资料分析,氢氧燃烧时保持相对低压。组织学生结合化学反应原理分析原因。
师生交流讨论:从氢氧燃烧的总反应考虑,提高压强有利于加快反应速率;但结合图象分析,高压与实际的压强选择不符,因此需考虑微观机理中各基元反应特点作出判断。理解自由基反应机理,链终止反应时H.与.OH相互碰撞形成惰性物质H2O,自由基发生湮灭,不利于链传递的进行,使得反应停止。链终止反应活化能最小,对温度不敏感,但受压强等外界因素的影响较大,因而需通过维持较低压强抑制该链终止反应的进行。
项目3:化学反应原理问题解决模型的建构
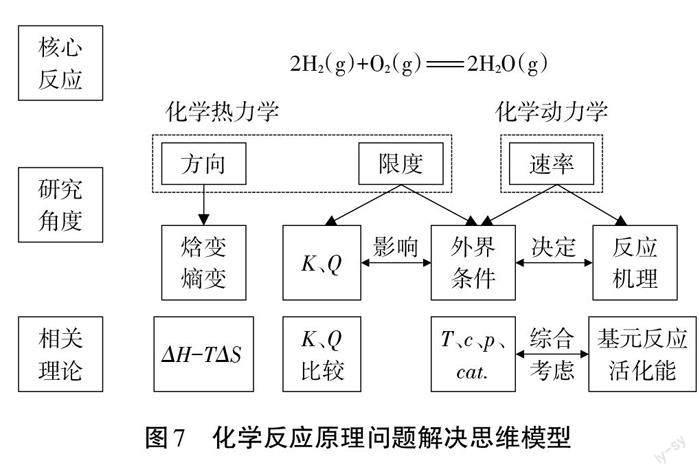
师生小结:结合火箭推进剂的综合选择凶素及氢氧燃烧反应条件的优化选择,化学反应原理的问题解决需要关注核心反应的特点,从化学热力学、动力学的角度对化学反应与能量、化学反应的方向、限度、速率及调控等研究角度进行问题剖析。运用相关理论,宏微结合,建构陌生情境下化学反应原理问题解决的思维模型(见图7),解决核心反应的真实情境问题。
设计意图:依据化学反应规律,结合微观反应历程与宏观外界条件,通过对氢氧燃烧条件的调控进行深度讨论,发展学生基于多角度、多变量关系对化学原理问题进行预测、推理、论证、迁移的学科能力,构建问题解决思维模型。
六、单元教学反思
元主题教学案例以火箭推进剂的研究为真实情境,旨在引领学生基于多角度、多变量关系,运用反应规律解决陌生情境下的化学反应原理问题,建构系统思维模型。单元主题教学的设计需要兼顾学情特点及知识发展的逻辑规律,考虑单元整体与分课时教学目标的整体性、关联性及递进性,避免出现知识内容重复或遗漏,难度层次欠缺梯度等情况。在课堂教学过程中尝试设置具有挑战性的活动环节,对于陌生情境、难度较高的问题任务,教师应及时搭建知识方法的脚手架,培养问题解决的思维方式,注重认知模型的建构,发展学习迁移能力.实现教学的“授之以渔”。通过前测后测、师生对话、书面表达、练习检测等多种形式进行教学评价,及时反馈学生情况、优化教学策略,提升课堂效益。通过本单元主题教学的实施,学生体会结合定性与定量、宏观与微观的学科视角,运用多重表征方式,对化学反应原理的本质与规律进行预测推理、说明论证及迁移应用,促进学科核心素养的培养,提高学业质量水平。
参考文献
[1] 中华人民共和国教育部.普通高中化学课程标准(2017年版2020年修订)[S].北京:人民教育出版社,2020.5.
[2] 宋天佑,程鹏,徐家宁,张丽荣.无机化学(第四版)上册[M].北京:高等教育出版社,2019.
[3] 李象远,申屠江涛,李宜蔚,李娟琴,王静波.燃烧反应机理构建的极小反应网络方法——氢氧燃烧[J].高等学校化学学报,2020,41(04):772-779.

